颗粒活性炭固定床精制F-90果葡糖浆的工艺*
2015-12-25周彦斌叶晓蕾罗建勇郭峰连晓东程世杰
周彦斌,叶晓蕾,罗建勇,郭峰,连晓东,程世杰
(广州双桥股份有限公司,广东广州,510280)
果葡糖浆也称高果糖浆(high fructose syrup)或异构糖浆,它是以酶法糖化淀粉所得的糖化液经葡萄糖异构酶的异构作用,将其中一部分葡萄糖异构成果糖,以果糖和葡萄糖为主要成分组成的一种混合型淀粉糖浆[1]。根据糖浆中果糖含量的多少,可将果葡糖浆分成果糖含量约为42%、55%、90%三大类产品,简称F-42、F-55、F-90。F-42是异构化葡萄糖得到的初级产品,同时也是生产F-90的原料;而F-90则是由F-42经过色谱分离技术纯化而得的产品,一般不直接销售,主要用于与F-42混合生产F-55[2];F-55是目前市场上销售量最大的果葡糖浆品种。
5-羟甲基糠醛又名5-羟甲基-2糠醛或5-羟甲基呋喃甲醛,英文简称为HMF,其分子中含有1个醛基和1个羟基,可以发生加氢、氧化脱氢、酯化、卤化、聚合、水解等多种化学反应[3]。HMF是美拉德反应的中间产物,由己糖生成,其含量主要受pH值、温度和糖液组成等影响。在酸性条件下,HMF生成量较多[4],而且酮糖(果糖)比醛糖(葡萄糖)更容易发生脱水反应生成HMF[5]。热处理时间延长,HMF含量升高,并且上升速率随热处理温度的升高而加快。F-90果葡糖浆含有90%以上的果糖,容易脱水产生大量HMF[6],HMF性质不稳定,进一步脱水分解成小分子物质,并最终经过缩合、聚合反应生成类黑色素,导致果葡糖浆变色,品质下降。因此,必须对F-90中的HMF含量进行控制,目前工艺中主要采用粉末活性炭去除糖浆中的HMF,但粉末活性炭回收难,消耗大,容易流失,容易导致浪费和污染,而颗粒活性炭(简称颗粒炭)在拥有发达的孔隙结构和巨大的比表面积[7]的同时,还兼具了吸附容量大、可再生、抗污染性能强、对液体流通阻力小、不易流失等优点,在淀粉糖工业中的应用潜力正越来越被重视。
目前对使用颗粒炭去除F-90中HMF的报道还相对较少,本文通过单因素和响应面分析的方法,对颗粒活性炭固定床(简称颗粒炭固定床)用于去除F-90中HMF的工艺条件进行了初步探讨。
1 材料与方法
1.1 材料
LF颗粒活性炭,卡尔冈炭素公司提供;F-90果葡糖浆,取自广州双桥股份有限公司色谱分离系统。
1.2 试剂与仪器
KH2PO4、甲醇、乙酸、NaOH、NaHCO3等均为分析纯;洗涤、配制及检测用水均为超纯水。
层析柱(上海沪西);恒温水浴箱(天津比朗);蠕动泵(保定兰格);高效液相色谱仪(Waters);紫外-可见分光光度计(Perkin-Elmer);密度仪(Anton Parr);pH计(Thermo ORION 3 STAR);数显折光仪(ATAGO,配有20℃恒温水浴);数显鼓风干燥箱(上海博迅);超声波清洗机(AUTOSCIENCE)。
1.3 实验方法
1.3.1 颗粒炭的预处理
用水洗涤颗粒炭至洗涤水电导率低于5 μS/cm,沥干水后放入60℃干燥箱中烘干至恒重,用80目筛除去细屑和小颗粒,密封后备用。
1.3.2 颗粒炭固定床的装填
向每组层析柱中分别装填86 g干燥的颗粒炭,用水下进上出缓慢灌满后排空颗粒炭内气体,将层析柱置于65℃的恒温水浴中浸泡30 min,用水第2次下进上出排尽颗粒炭床残留气体,轻轻敲打层析柱,使所有层析柱内的颗粒炭床体积均为180 mL,试验1.0 BV按180 mL计算。
1.3.3 F-90果葡糖浆的预处理
取色谱分离F-90果葡糖浆,用0.45 μm滤膜除去悬浮物及细菌,冷却至室温。
1.3.4 颗粒炭固定床精制F-90果葡糖浆的工艺研究
将层析柱放入恒温水浴中,启动蠕动泵,按设定流速由上至下进水通过颗粒炭固定床30 min后,切换成输送F-90果葡糖浆由上至下通过颗粒炭固定床,进糖体积达到3.0 BV后开始收集精制液,收集体积达3.0 BV后结束实验,将收集液混合均匀并冷却至室温,检测精制前后HMF含量。每组各进行3次平行实验。
1.3.4.1 温度对精制效果的影响
将层析柱分别置于65、70、75、80、85 ℃恒温水浴中,调节F-90果葡糖浆的pH值至4.9,以1.5 BV/h的速度通过颗粒炭固定床。
1.3.4.2 流速对精制效果的影响
将层析柱置于一定温度条件下,调节F-90果葡糖浆的 pH 值至 4.9,分别以 0.5、1.0、1.5、2.0、2.5 BV/h的速度通过颗粒炭固定床。
1.3.4.3 pH值对精制效果的影响
将层析柱置于一定温度条件下,控制一定的流速,分别调节 F-90果葡糖浆的 pH值至4.6、4.9、5.2、5.5、5.8,以 1.0 BV/h 的速度通过颗粒炭固定床。
1.3.4.4 精制工艺的优化试验
采用响应面分析法建立回归模型并进行优化[8],确定颗粒炭固定床精制F-90果葡糖浆的最佳工艺。
1.3.5 分析方法[9]
称取10 g样品,加入蒸馏水至30 g,用0.45 μm滤膜过滤并超声波消泡3 min,用高效液相色谱测定所得溶液的HMF含量,换算成每kg糖干基的HMF含量,计算出HMF的去除率。
高效液相色谱流动相的配制:称取4.49 g KH2PO4溶解于1 000 mL超纯水中,添加250 mL甲醇和25 mL乙酸并混合均匀,用1 mol/L NaOH溶液调节至pH 3.5,经过0.45 μm滤膜过滤、超声波脱气30 min后备用,密封良好可在1~4℃的冰箱中储存3个月。
色谱分析条件:Waters Bondapak C18柱,紫外检测器,检测波长283 nm,柱温为常温,流速0.8 mL/min,进样体积35 μL,运行时间10 min。

1.3.6 数据分析
所有结果均取平均值,数据采用Excel 2010和Design-Expert 8.0.6.1软件进行统计分析。
2 结果与讨论
2.1 单因素试验结果
2.1.1 温度对精制效果的影响
控制pH值为4.9,流速1.5 BV/h,对不同温度下的HMF去除效果进行考察,结果如图1所示。随着温度上升,HMF的去除率先增大后减小,温度为70℃时的HMF去除率最高。温度的上升能使F-90果葡糖浆的黏度下降,有利于HMF在颗粒炭表面扩散,促进吸附效率,但同时也会增加HMF生成量,且生成速率随温度升高而加快。温度从65℃到70℃,HMF的生成速率与颗粒炭的吸附效率的差值增加,HMF的去除率升高;70℃之后,HMF的生成速率与颗粒炭的吸附效率的差值逐步缩小,因此HMF去除率下降。
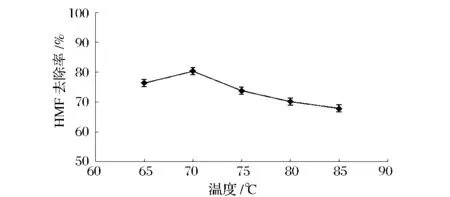
图1 温度对HMF去除率的影响Fig.1 Removal ratios of HMF at different temperatures
2.1.2 流速对精制效果的影响
控制pH值为4.9,温度为70℃,对不同流速下的HMF去除率进行考察,结果如图2所示。随着流速增大,HMF去除率呈先增大后减小的趋势。流速为1.0 BV/h时去除率最高,之后明显下降,流速>2.0 BV/h后下降速度减缓。由此可知,颗粒炭与F-90果葡糖浆的接触存在临界时间,遵循活性炭的吸附等温线。当流速较快时,接触时间低于临界时间,颗粒炭的吸附量较小,HMF的去除率较低;当流速较慢时,接触时间高于临界时间,颗粒炭吸附量增加,但同时由于在高温中停留使糖浆的HMF生成量也增加,当生成速率与颗粒炭吸附效率差值缩小时,HMF去除率下降。
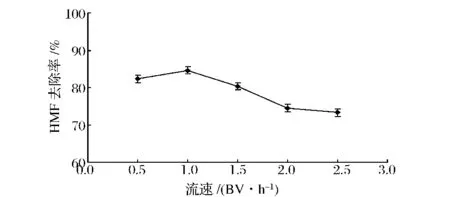
图2 流速对HMF去除率的影响Fig.2 Removal ratios of HMF at different flow velocities
2.1.3 pH值对精制效果的影响
控制温度为70℃,流速为1.0 BV/h,对不同初始pH值下的HMF去除率进行考察,结果如图3所示。当初始pH值从4.6升至5.2,HMF的去除率迅速升高;当初始pH值从5.2升至5.8,HMF的去除率则缓慢下降;pH值为5.2时,HMF的去除率最高。果糖在高温和pH值较低环境下均容易脱水生成HMF,HMF可进一步分解成甲酸、乙酰丙酸等小分子酸性物质[10],导致糖浆精制后pH值下降,因此同时考察了pH的初始值和出料值的下降幅度,结果如图4所示。当初始pH值从4.6增加到5.2时,pH下降值逐步减小,5.2时最低,而当初始pH值从5.2升高到5.8时,pH下降值迅速上升。综合上述结果可知,初始pH值5.2以下时酸性物质生成量较少,HMF生成量较多,去除率较低;pH值5.2以上,酸性物质生成量增多,催化果糖分解生成HMF;糖浆初始pH值为5.2时,HMF的去除率最高,同时也降低了HMF酸化分解的底物浓度,所以pH下降值最小。
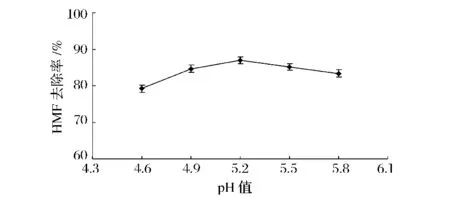
图3 pH值对HMF去除率的影响Fig.3 Removal ratios of HMF at different feeding pH values
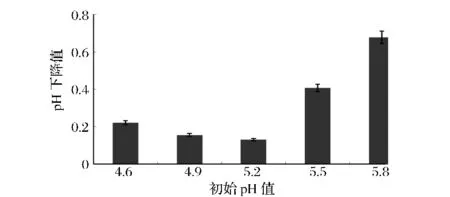
图4 不同初始pH值F-90果葡糖浆的pH值变化Fig.4 Reduction of pH at different feeding pH values
2.2 响应面优化试验
综合单因素试验结果,以温度(A)、流速(B)、pH值(C)为主要因素,以HMF去除率(Y)为响应值,采用3因素3水平响应面法优化工艺。因素编码及水平如表1所示,响应面试验设计及结果如表2所示。
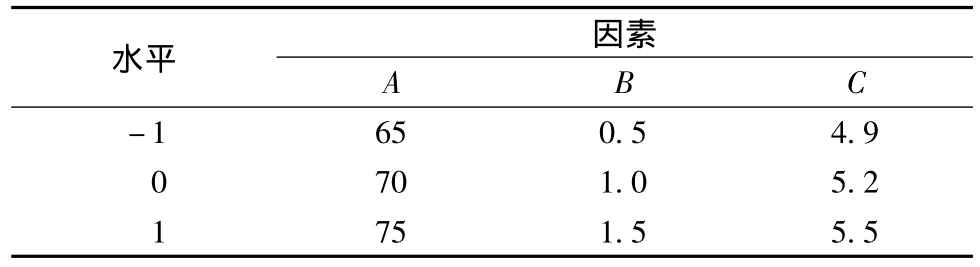
表1 响应面试验的因素水平表Table 1 Factors and their levels of response surface design

表2 响应面试验设计及结果Table 2 Response surface design arrangement and corresponding experimental data
对响应面试验结果进行多元回归拟合,得到二次多项回归方程为:Y=86.90-1.31 A-1.08 B-2.27 C+0.18 BC-5.30 A2-3.19 B2-4.53 C2。回归模型的方差分析结果如表3所示。
从表3可知,该回归模型极显著(P<0.000 1),R2=0.999 0,Radj2=0.997 8,失拟项不显著(P >0.05),说明模型与实际值拟合程度较好,可用该回归模型对颗粒炭精制F-90果葡糖浆的工艺进行分析和预测。其中一次项 A、B、C及二次项 A2、B2、C2极显著(P<0.01)。根据F值分析,各因素对HMF去除率的影响依次为:pH值>进料温度>流速。由此可知,pH值对HMF去除率的影响最大,其次为温度,流速影响最小。根据拟合模型绘制颗粒炭固定床精制F-90果葡糖浆工艺的三维响应面如图5所示。
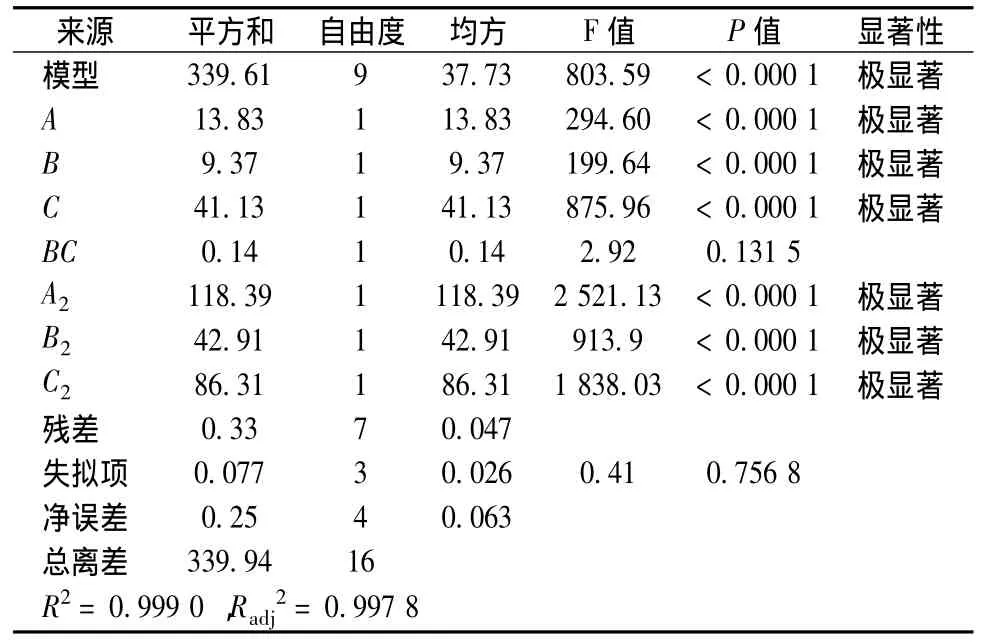
表3 回归模型的方差分析结果Table 3 Analysis of variance for the proposed regression model
由图5可知,温度为69~71℃、流速为0.9~1.1 BV/h、pH值为5.1~5.3时,HMF的去除率可以达到最大值。其余条件下HMF的去除率较低,呈逐步递减的趋势。
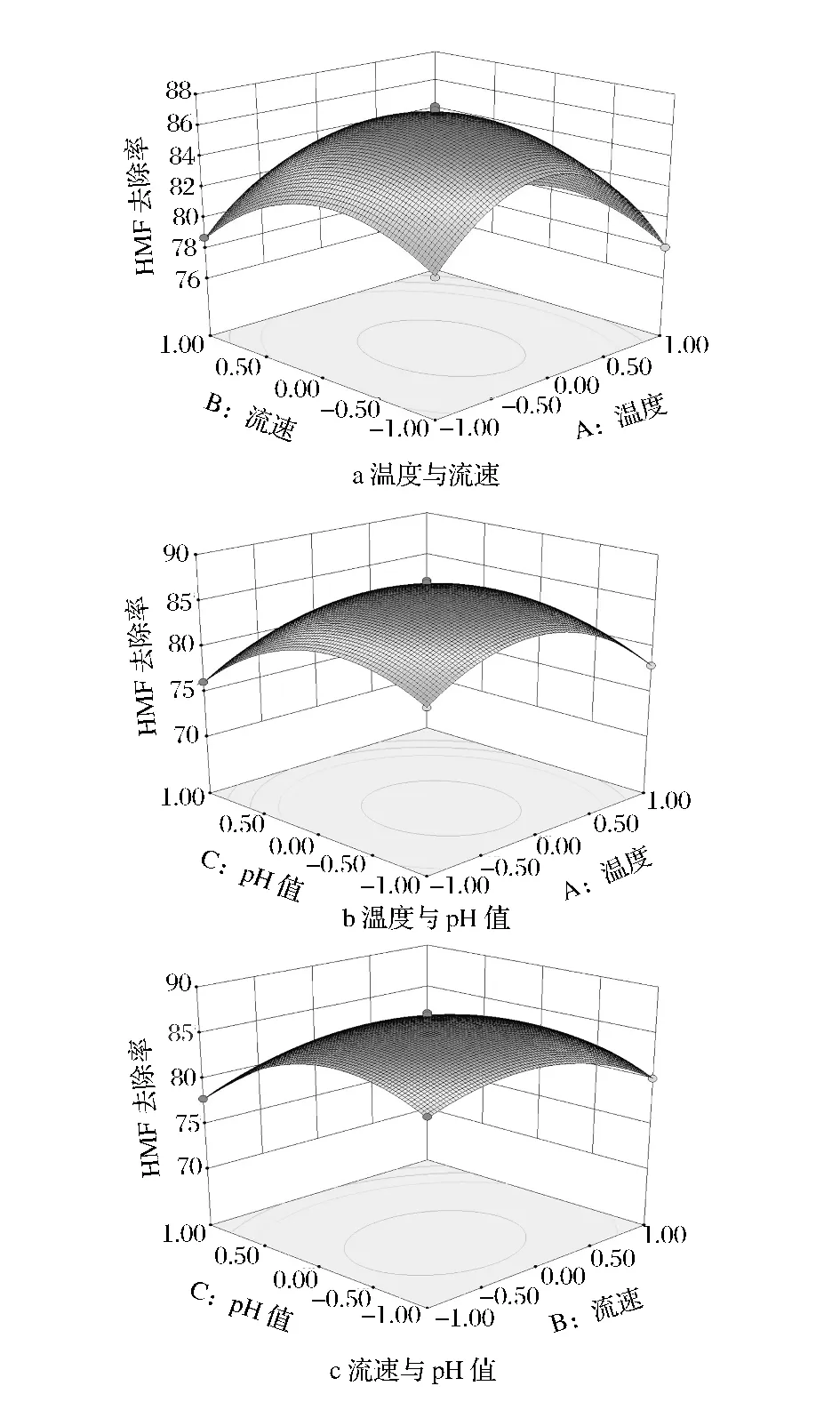
图5 颗粒炭固定床精制F-90果葡糖浆工艺的响应面图Fig.5 Response surface graphs of HFS 90 refining by fixed GAC bed
为进一步确定精制F-90果葡糖浆的最佳工艺,用Design Expert对试验参数进行优化,得到最优的颗粒炭固定床精制F-90果葡糖浆的工艺条件为:温度69.38℃,流速0.91 BV/h,pH 5.12,HMF去除率能够达到87.37%。
2.3 验证试验
根据上述优化出的参数,稍作调整后作为验证试验的条件,即:温度69.5℃,流速0.9 BV/h,pH 5.1。进行3次平行试验,实际得到的HMF去除率平均值为87.05%。与理论预测值比较,其相对误差为0.37%,可见HMF的去除率与预测值基本吻合,说明预测模型与实际情况拟合较好。
3 结论
在颗粒炭固定床精制F-90果葡糖浆的过程中,同时存在着颗粒炭吸附HMF和果糖分解生成HMF的反应,由于吸附量大于生成量,所以能够起到去除HMF的效果。但在实际生产应用中,颗粒炭的吸附效率较容易受到温度、糖浆初始pH值和流速等因素的影响。本文通过单因素试验与响应面分析的方法对以上几个主要影响因素进行了初步的分析,优选出颗粒炭固定床精制F-90果葡糖浆的最优工艺条件,具体结论如下:
(1)在使用颗粒活性炭固定床去除F-90果葡糖浆中HMF的体系中,存在着一定的吸附平衡关系,其中温度、糖浆初始pH值和流速都对HMF去除率有显著的影响作用;
(2)各因素对HMF去除率影响的显著性大小依次为:初始pH值>温度>流速;
(3)对回归模型作方差分析,得到颗粒炭固定床精制F-90果葡糖浆的最佳工艺参数为:温度69.5℃,流速0.9 BV/h,pH 5.1。经验证,HMF的去除率为87.05%,与预测值87.37%基本吻合,回归模型拟合度较好。
因此,本工艺能有效去除F-90果葡糖浆中的HMF,进而实现果葡糖浆产品的质量提升,为果葡糖浆制造企业提供一定的借鉴和参考。
[1] Helmut Uhlig.Industrial Enzymes and their Applications[M].New York:Wiley-Interscience,1998:200-201.
[2] Ramos J E T,Duarte T C,Rodrigues A K O,et al.On the production of glucose and fructose syrups from cashew apple juice derivatives[J].Journal of Food Engineering,2011,102(4):355-360.
[3] 董喜恩,蒋锋,罗根祥.糖类脱水生成5-羟甲基糠醛的研究进展[J].化工中间体,2010(2):17-22.
[4] 吴泰钢,黄才欢,白卫滨,等.绿原酸对糖酸反应体系中5-羟甲基糠醛形成的影响[J].现代食品科技,2014,30(10):74-79.
[5] Gökmen V,Morales F J.Processing contaminants:Hydroxymethylfurfural[J].Encyclopedia of Food Safety,2014,2:404-408.
[6] Jaewon Jeong,Churchil A Antonyraj,Seunghan Shin,et al.Commercially attractive process for production of 5-hydroxymethyl-2-furfural from high fructose corn syrup[J].Journal of Industrial and Engineering Chemistry,2013,19(4):1 106-1 111.
[7] Shashi Kumar,Mohd.Zafar,Jitendra K Prajapati,et al.Modeling sudies on simultaneous adsorption of phenol and resorcinol onto granular activated carbon from simulated aqueous solution [J].Journal of Hazardous Materials,2011,185(1):287-294.
[8] Mohd Hafizuddin Muhamad,Siti Rozaimah Sheikh Abdullah,Abu Bakar Mohamad,et al.Application of response surface methodology(RSM)for optimisation of COD,NH3-N and 2,4-DCP removalfrom recycled paper wastewater in a pilot-scale granular activated carbon sequencing batch biofilm reactor(GAC-SBBR)[J].Journal of Environmental Management,2013,121:179-190.
[9] ISBT 13.0-2006.Hydroxymethyl Fur-fural(HMF)and Furfural(FFA)[S].
[10] 蔡磊,吕秀阳,何龙,等.高温液态水中果糖无催化分解反应动力学[J].化工学报,2005,56(4):677-680.
