水杨醛亚胺类[O- NS]三齿钛配合物的合成及催化乙烯聚合
2015-12-24蓝芝刘公毅雷禄李永生宋文张爱清谢光勇
蓝芝,刘公毅,雷禄,李永生,宋文,张爱清,谢光勇
(1.中南民族大学 化学与材料科学学院 催化材料科学国家民委-教育部共建重点实验室,湖北 武汉 430074;2.百色学院 大学预科教育学院,广西 白色 533000)
水杨醛亚胺是一类非常重要的配体。Fujita 小组报道的水杨醛亚胺配位的第四族金属配合物(I),在助催化剂作用下可以高活性催化乙烯聚合[1]。由于该类催化剂是双配体结构,金属中心配位环境拥挤,导致大位阻的α-烯烃很难与其配位,难以催化乙烯与α-烯烃的共聚。
唐勇课题组在配合物(I)基础上引入一个边臂杂原子X (X=P、O、S、Se),得到三齿[ONX]配合物(II),在MMAO 作用下,对乙烯均聚和乙烯与α-烯烃共聚都有很高的活性,实现了过渡金属催化剂高活性地催化乙烯与极性单体共聚[2]。由于配合物存在边臂效应,能够起到更好的保护中心金属原子的作用,拥有更好的热稳定性;尤其是亚胺键还原后的配合物(III),在较高温度下仍然有不错的活性[3]。
配合物II、III 的边臂均为苯胺类,刚性较强,空间位阻较大。为了进一步简化配合物的合成,减小边臂的位阻,进而利于α-烯烃的配位,我们用2-丙硫基乙胺代替苯胺类边臂,使催化剂的刚性大大减小,得到了一类新型的水杨醛亚胺[O-NS]三齿钛的配合物(Ti1)。对配体的亚胺键还原,得到催化活性、热稳定性更好的催化剂Ti2。
1 实验部分
1.1 试剂与仪器
配体(1)和(2)均为自制[4];乙烯(99.99%),为分析纯或化学纯。
AM-400 型核磁共振仪;DF-101S 型集热式恒温加热磁力搅拌器;RE-52A 旋转蒸发器;SHZ-D 型循环水式真空泵;X-5 型熔点测定仪。
1.2 配合物的合成
配合物Ti1和Ti2的合成路线如下:

1.2.1 配合物Ti1的合成 在氮气气氛下,TiCl40.7 g(3.7 mmol)溶于10 mL 甲苯中,置于-78 ℃下,慢慢滴加溶于10 mL 甲苯溶液的配体(1)0.963 g(3.0 mmol),滴加时间超过15 min,升温至室温,并搅拌3 h。减压去除溶剂,收集红褐色固体,真空干燥,得到配合物Ti1。1H NMR (400 MHz,CDCl3):8.31(s,1H, HN C ),7. 34 (d,1H,Ar-H),7.14 (d,1H,Ar-H),3.41(t,2H,CH2),2.95(t,2H,CH2),2.35(t,2H,CH2),1.95(m,2H,CH2),1.44(s,9H),1.42(s,9H),1.12(t,3H,CH3)。元素分析(C20H32Cl3NOSTi)实测值(计算值),%:C 49.15(49.32);H 6.60 (6.43);N 2.87 (2.66)。1.2.2 配合物Ti2的合成 Ti2合成方法与Ti1类似。1H NMR (400 MHz,CDCl3):7.32(Ar-H,1H),7. 03(Ar-H,1H),10(2H,CH2-Ar),2. 90(2H,CH2),2.38(2H,CH2),1.95(—NH—),1.55(2H,CH2),1.45(9H),1.38(9H),1.08(3H)。元素分析(C20H34Cl3NOSTi)实测值(计算值),%:C 48.95(48.58);H 6.98 (6.65);N 2.85 (2.99)。
1.3 乙烯聚合
100 mL 聚合瓶用高纯氮气置换2 次,第三次用乙烯气体置换,加入30 mL 甲苯,升至反应温度,搅拌下加入助催化剂MMAO,搅拌5 min 后加入催化剂反应30 min后,用5%稀盐酸终止反应。过滤,得到聚乙烯,先后用蒸馏水和乙醇洗涤,烘干至恒重,计算催化剂的活性。
2 结果与讨论
2.1 配合物的合成与表征
文献报道[3]制备水杨醛亚胺类配合物通常是用氢化钠、钾或正丁基锂等强碱将酚羟基上的H 脱去,然后再与TiCl4配位反应。反应完成后过滤,去除产生的盐得到目标配合物。为了简化实验过程,我们采用一步法,即配体不经强碱脱氢,直接与TiCl4配位反应,配位完成后,减压去除溶剂,在40 ℃下加热抽真空以确保HCl 除尽。从核磁氢谱可以看出,与配体(1)和(2)相比,配合物Ti1和Ti2的羟基上的H 峰均消失;亚胺和仲胺键上的氢的位移(对比其各自的配体)均有不同程度的向低场移动。
2.2 乙烯聚合
乙烯压力0.1 MPa,催化剂用量4 μmol,溶剂甲苯30 mL。配合物Ti1和Ti2催化乙烯聚合的结果见表1。
由表1 可知,配合物Ti1表现出中等活性,而亚胺键还原后,配合物Ti2的催化活性明显提高,表现出高的催化活性。
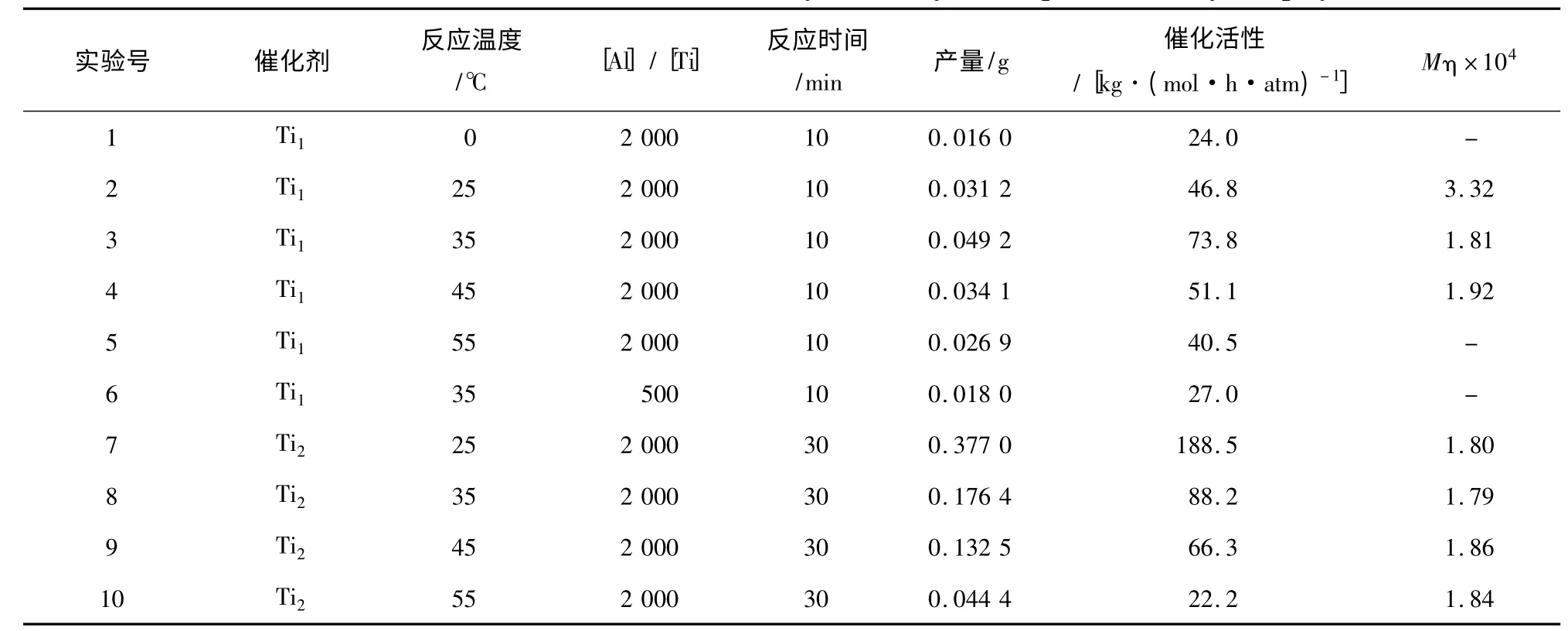
表1 聚合条件对配合物催化乙烯聚合的影响Table 1 The influences of reaction conditions on catalytic activity of complexes for ethylene polymerization
配合物Ti1与含苯环类边臂结构的配合物II 相比较[2-3]活性有所下降,说明苯环在边臂中可以增强催化剂的催化活性,原因可能是苯环能够与相连的S 共轭作用,稳定催化剂的金属活性中心。
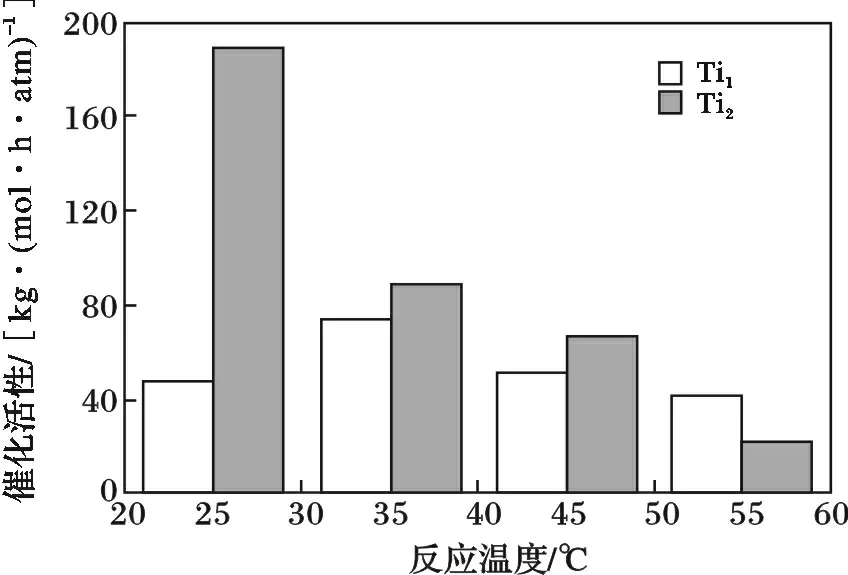
图1 反应温度对配合物Ti1、Ti2 催化活性的影响Fig.1 The effects of reaction temperature on catalytic activity of complexes Ti1 and Ti2
由图1 可知,配合物Ti1在35 ℃时到达最高活性73.8 kg/(mol·h·atm),温度升高或降低活性均下降。一般认为,在较低的温度下,乙烯的配位和插入速率慢,影响了活性。当温度升高时,这两个过程速率加快,活性也随之提高;但是,高温下催化剂容易分解,使催化剂失活;另外,高温下溶液中的乙烯的溶解度降低,这都是导致高温下活性降低的原因。
配合物Ti2随着温度的升高活性逐渐降低,在25 ℃时达到最高活性188.5 kg/(mol·h·atm);与配合物Ti1相比较,最高活性提高了2 倍多。原因可能是将配体(1)的亚胺键( CH N )还原成(2)的仲胺键(CNH)后,N 原子由sp2杂化变为了sp3杂化,使N 原子与金属中心的配位能力减弱,中心金属上的正电性增强,有利于金属与乙烯的配位[5-6]。
3 结论
合成了两种新型的[O-NS]三齿配体配位的钛配合物Ti1、Ti2。在助催化剂MMAO 作用下,配合物Ti1和Ti2均能催化乙烯聚合,配合物Ti1表现出了中等催化活性,最高可达73.8 kg/(mol·h·atm);当亚胺键还原后,配合物Ti2的催化活性明显提高,最高可达188.5 kg/(mol·h·atm)。
[1] Matsui S,Mitani M,Saito J,et al. A family of Zirconium complexes having two phenoxy-imine chelate ligands for olefin polymerization[J]. J Am Chem Soc,2001,123:6847-6856.
[2] Yang X H,Liu C R,Wang C,et al.[O-NSR]TiCl3-Catalyzed copolymerization of ethylene with functionalized olefins[J].Angew Chem Int Ed,2009,48:8099-8102.
[3] Hu W Q,Sun X L,Wang Cong,et al.Synthesis and characterization of novel tridentate[NOP]titanium complexes and their application to copolymerization and polymerization of ethylene[J]. Organometallics,2004,23:1684-1688.
[4] 刘公毅,李龙,徐晓航,等. 新型水杨醛亚胺及其胺衍生物的合成[J].应用化工,2013,42(10):1769-1771.
[5] Wan L,Zhang D,Wang Q,et al.Trans-1,2-diphenylethylene bridged salicylaldiminato-isoindoline titanium(IV)chloride complexes:Synthesis,characterization and catalytic polymerization[J].J Organometal Chem,2013,724:155-162.
[6] Hu P,Qiao Y L,Wang J Q,et al.Synthesis,characterization,and ethylene polymerization of titanium complexes with double-duty tridentate [ONN]ligands[J]. Organometallics,2012,31:3241-3247.
