不同吸附剂在沼气脱碳提纯中的分离性能
2015-12-21王志祥易红宏唐晓龙赵顺征左嫣然高凤雨张波文
王志祥,易红宏,唐晓龙,赵顺征,左嫣然,高凤雨,张波文
不同吸附剂在沼气脱碳提纯中的分离性能
王志祥,易红宏,唐晓龙,赵顺征,左嫣然,高凤雨,张波文
(北京科技大学土木与环境工程学院,北京,100083)
采用椰壳活性炭、5A和13X分子筛作为吸附剂,动态配气CO2/CH4混合气体作为模拟沼气,研究不用吸附剂及不用原料气配比条件下的CO2/CH4混合气的吸附分离性能,对吸附饱和的13X分子筛分别进行真空(4.5 kPa)脱附再生和热力(300 ℃)脱附再生。研究结果表明:在常温常压下,13X分子筛对混合气中CO2的穿透吸附容量为3.21 mmol/g,对CO2/CH4混合气体的分离系数可达10,明显高于5A分子筛和椰壳活性炭的分离系数;减小混合气中CO2的分压,其穿透时间也随着减小,且吸附容量的减小幅度大于分压的减小幅度;真空脱附再生后的13X分子筛吸附分离性能只能恢复到原来的40%左右,而热力脱附再生后分离性能效果较好。
活性炭;分子筛;吸附;穿透曲线;再生
沼气是一种生物质能源,具有清洁、高效、安全、可再生等特征。沼气制备及利用过程不仅能有效处理有机废弃物污染,减少温室气体排放总量,而且能缓解能源危机:因此,合理开发利用沼气对于缓解环境问题与能源问题具有重要的战略意义[1]。由于沼气中CH4体积分数为55%~65%,CO2体积分数为30%~ 40%,共存的CO2不仅影响CH4的燃烧效果,同时对贮存或运输管路造成腐蚀:因此,沼气脱碳提纯是沼气高效高值利用的重要环节。吸附法分离提纯技术具有污染小、脱碳脱水可同时完成、吸附剂可再生重复使用、工艺简单、投资少、CO2和CH4易回收等优 点[2−3],受到人们越来越多的关注与研究。吸附剂是吸附法分离的核心,研究较多的吸附剂有活性炭、硅胶、分子筛、金属−有机骨架等,与其他吸附剂相对比,活性炭和分子筛具有廉价易得、稳定性好、吸附性能好、吸附剂易再生等优点,成为人们研究的热点[4]。其中,活性炭是应用最广泛的吸附剂,它的比表面积是所有传统吸附剂中最大的[4−5],椰壳活性炭又是活性炭中比表面积较大的一种。分子筛以其具有规整的孔道结构、均匀一致的孔分布、较高的比表面积和吸附容量以及可调变的表面性质同样得到了广泛的应用[6−7],分子筛的突出特点是微孔孔容远远比其他传统吸附剂的高。5A和13X分子筛分别是A型分子筛和X型分子筛的典型代表。李通等[8]考察了不同材质活性炭及不同方法改性活性炭对CO2/CH4混合气体的吸附分离性能,结果发现煤质活性炭的吸附分离效果最好,5%(质量分数)的双氧水、5%(质量分数)的氨水及5%(质量分数)的盐酸改性对活性炭的吸附容量均有较大的提高。Remy等[9]发现低硅Li-KFI沸石在压力为 4 MPa,温度为303 K时CO2吸附容量达4.8 mmol/g,低硅Na-KFI沸石的最大分离因子可达18。Shang等[10]对菱沸石进行了研究,发现离子交换菱沸石在CO2/CH4混合气体吸附分离体系中存在“分子活板门”机理,钾离子交换菱沸石(KCHA)在273 K和100 kPa下,分离因子高达93。然而,将活性炭和分子筛作为对比分析其对CO2/CH4混合气体的吸附分离及分子筛再生方面的研究较少。本文作者选用椰壳活性炭、5A和13X分子筛作为吸附剂,对比分析其对沼气模拟气(CH4和CO2体积比(CH4):(CO2)=3:2)的吸附穿透行为,用吸附容量、分离系数及再生性能对吸附剂进行评价,选出性能优良的吸附剂。此外,还对真空脱附和热力脱附对其再生性能的影响进行研究。
1 材料与方法
1.1 实验材料
实验所用椰壳活性炭为北京惟事美环保科技有限公司,颗粒粒度为250~380 μm;5A和13X 分子筛购于国药集团化学试剂有限公司(球形,颗粒直径为3~ 5 mm研磨至粒度为250~380 μm)。用去离子水清洗3次,在110 ℃干燥箱中干燥12 h,然后在马弗炉中活化12 h,活化温度为300 ℃。降至室温之后放入干燥器中储存备用。CH4,CO2和N2均购于北京兆格气体科技有限公司(纯度分别为99.990%,99.999%和99.999%)。
1.2 实验仪器
配备有热导检测器(TCD)的气相色谱仪(GC−4000A型)、质量流量计(D08−4E型)、循环水多用真空泵(SHB−Ⅳ双A)、数显恒温水浴锅(AL204)、电热鼓风干燥箱(101−3AB型)、马弗炉(SX−G07123)、电子天平(AL204)、微型压力传感器(NS−Ⅰ1)、数字显示仪(NS−YB05C)和固定床反应器(自制)。
1.3 吸附剂性能评价
采用动态吸附实验装置所得的吸附穿透曲线来评价吸附剂的吸附分离性能。性能指标吸附容量、分离系数和再生性能均可通过实验求得。实验装置流程如图1所示。

图1 动态吸附实验装置流程图
实验所用反应装置固定床反应器(fix bed)直径×高为10 mm×200 mm,实验所需CH4和CO2的流量及混合气各组分浓度(体积分数)由质量流量计控制,经混合罐充分混合之后进入填充了吸附剂的固定床反应器,最后运用配备有热导检测器(TCD)的气相色谱仪(GC)测试出口的气体体积分数。一般来说,当吸附床出口开始有某气体检出时,表明该气体开始穿透(气体检测的体积分数达到原料气的5%),当各个气体检出体积分数等于初始体积分数时称为完全穿透[11]。绘制各组分的检出体积分数随时间的变化曲线,即得吸附穿透曲线。
穿透吸附容量由质量守恒定律求得[8]。
吸附分离系数是考察吸附剂对混合气体分离能力的一个标准。混合气体吸附分离系数()为

式中:A和B分别为某组分吸附相与气相摩尔分数;和分别为组分CO2和CH4。
2 结果与讨论
2.1 不同吸附剂的吸附分离性能
控制CH4与CO2的体积比为3:2,分别用1 g椰壳活性炭、5A分子筛和13X分子筛作为吸附剂,填充在固定床反应器中,在20 ℃下测定动态吸附穿透曲线。3种吸附剂的吸附穿透曲线如图2所示。

总流量:12 mL/min,(CH4)/(CO2)=3:2
1—CH4, 13X;2—CH4, 5A;3—CH4, YAC;4—CO2, 13X;5—CO2, 5A;6—CO2, YAC
图2 CO2/CH4混合气在椰壳活性炭(YAC),5A和13X分子筛上的吸附穿透曲线
Fig. 2 Breakthrough curves of CH4/CO2gas mixture on coconut shell activated carbon, 5A molecular sieve and 13X molecular sieve
从图2可以看出:3条CO2体积分数在初始阶段都几乎为0,然后逐渐恢复到原来的体积分数;对CO2的吸附容量明显大于对CH4的吸附容量,说明分离效果较好;3条CH4体积分数曲线在短时间内很低,然后迅速升至100%。这表明无论是椰壳活性炭(YAC),还是5A和13X分子筛,其对CO2和CH4的吸附速度都很快,直至吸附达到一定量。从穿透时间来看,混合气在椰壳活性炭和5A分子筛的穿透时间相差不大,相比之下,13X分子筛的穿透时间明显高于YAC和5A分子筛的穿透时间。
3种吸附剂对CO2的穿透吸附容量及对混合气体的分离系数如表1所示。

表1 不同吸附剂对CO2的穿透吸附容量及对混合气体的分离系数
从表1可知:13X分子筛对CO2的吸附容量和对CO2/CH4混合气体的分离系数方面都有明显优越性。导致椰壳活性炭、5A和13X分子筛对CO2/CH4吸附分离效果不同的原因有2个方面。1) 孔结构不同。椰壳活性炭虽然比表面积最大,但是其孔径大多集中在2~3 nm之间,小于1 nm的孔径非常少,而CO2分子与CH4的分子动力学直径分别为0.33 nm和 0.38 nm[12−13],因此,椰壳活性炭会因孔径过大而对CO2分子的吸附力小,吸附容量也小,对CO2分子与CH4的分子筛分效应也远不如分子筛筛分效果好[14]。5A和13X分子筛的孔径非常均一,5A分子筛的孔径在0.4~0.5 nm之间,13X分子筛的孔径在0.9~1.0 nm之间,比CO2和CH4分子的直径略大,分子筛分效应明显。2) 表面结构不同。活性炭的表面由疏水性石墨层和亲水性官能团构成,其中石墨层吸附疏水性化合物,而亲水性官能团主要吸附极性化合物。虽然CO2和CH4均为非极性的,但因CO2分子具有四极矩而使其具有一定的极性。然而,相比之下,分子筛由于具有骨架平衡阳离子而对拥有四极矩的CO2分子产生极化作用[15],使其具有更为强烈的极性,这样就明显增强了对CO2分子的吸附能力和对CO2/CH4混合气的分离能力。
2.2 不同原料气组成在13X分子筛上的吸附分离 性能
CH4与CO2的体积比分别控制为3:2和9:1,称取1 g对CO2/CH4混合气吸附分离效果较好的13X分子筛,填充在固定床反应器中,在20 ℃下测定动态吸附穿透曲线。所得结果如图3所示。
从图3可以看出:随着CH4与CO2体积比的增加,CO2的穿透时间减小,说明随着混合气中CO2分压的减小,13X分子筛对其饱和吸附容量变小,而且吸附容量减小幅度比分压减小幅度大。这一特点与CO2的吸附容量随压力的变化方面的特点一致[16−17]。一般来说,压力越大,吸附容量也越大,可能是因为压力变大后吸附剂就会扩容它的吸收孔[18],提高吸附能力。
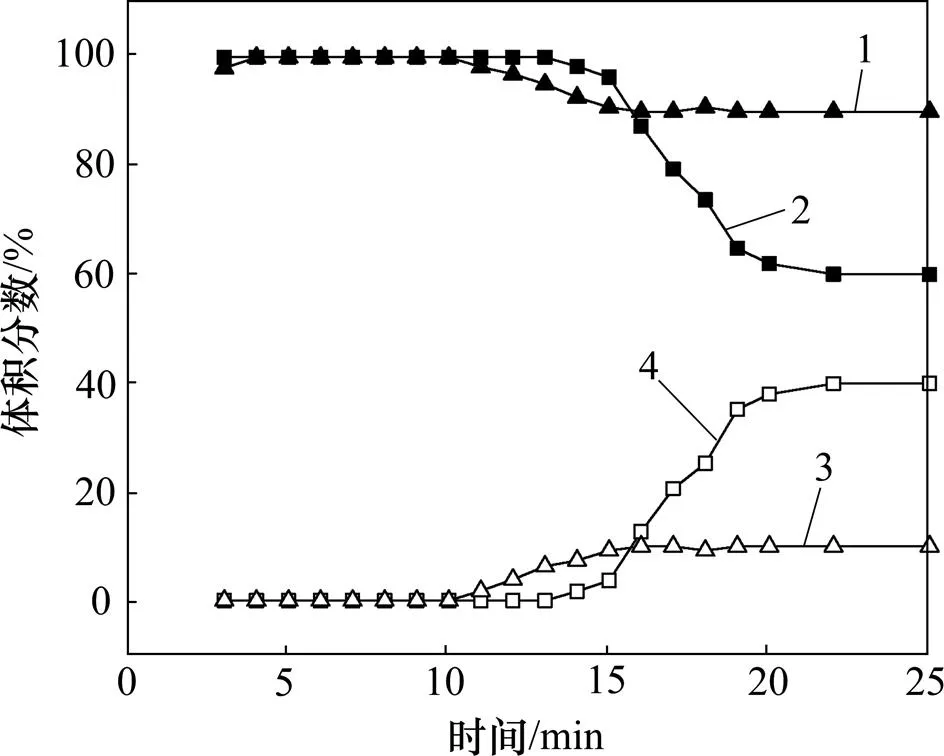
总流量:12 mL/min
1—吸附CH4,(CH4):(CO2)=3:2;2—吸附CH4,(CH4):(CO2)=9:1;3—吸附CO2,(CH4):(CO2)=3:2;4—吸附CO2,(CH4):(CO2)=9:1
图3 CO2/CH4混合气在13X分子筛上的吸附穿透曲线
Fig. 3 Breakthrough curves of CO2/CH4gas mixture on 13X molecular sieve
2.3 不同脱附方法对13X分子筛的性能影响
称取2份质量均为1 g的13X分子筛,分别填充在固定床反应器中,在CH4与CO2混合气的总流量为12 mL/min,体积比为3:2的气氛下充分吸附,直至吸附饱和。然后,将其中一份放入配有数显压力传感器的密封装置中,用循环水多用真空泵抽真空至 4.5 kPa,反复抽真空,直至数显压力传感器示数稳定,真空脱附完成,用这种方法脱附所得的13X分子筛样品记为13X-VD;取另一份13X分子筛放入马弗炉中,温度从室温以5 ℃/min速度升高到300 ℃后,保持 3 h,然后样品在马弗炉中自然降至室温,完成热力脱附。所得样品记为13X-TD。
控制CH4与CO2的体积比为3:2,分别取质量为 1 g真空(4.5 kPa)脱附之后的13X分子筛13X-VD及热力(300 ℃)脱附之后的13X分子筛13X-TD作为吸附剂,所得吸附穿透曲线如图4所示。
从图4可以看出:真空脱附再生之后的13X分子筛的吸附穿透时间与空白实验吸附穿透时间相比,相差非常明显,穿透时间降至不足原来的一半,而热力脱附再生之后的13X分子筛能完全恢复原来的吸附分离性能。这种现象可以用吸附势理论[10, 19]解释:吸附饱和的13X分子筛在压力很小的环境下,对CO2和CH4分子的吸附力减小,部分脱附出来,但是仍然存在一部分CO2和CH4分子被吸附,剩下的CO2和CH4分子的吸附容量比4.5 kPa 时13X分子筛对CO2和CH4分子的吸附容量要大;在300 ℃热力脱附时,由于温度的升高,CO2和CH4分子的热运动变得更加激烈,分子筛的骨架结构对其产生的吸附力已不足以束缚CO2和CH4分子,致使完全脱附出来。

1—吸附CH4,13X;2—吸附CH4,13X-TD;3—吸附CH4,13X-VD;4—吸附CO2,13X;5—吸附CO2,13X-TD;6—吸附CO2,13X-VD
3 结论
1) 在相同实验条件下,3种吸附剂对CO2的吸附容量及对CO2/CH4混合气体的分离系数从大至小均为13X,5A和YAC。其中,效果最好的13X分子筛对CO2的吸附容量为3.21 mmol/g,对CO2/CH4混合气体的分离系数可达10。
2) 在总流量和总压力不变的条件下,减小CO2的分压,其穿透时间也随之减小,表明CO2吸附容量与其组分分压有密切的关系,而且吸附容量的减小幅度大于分压的减小幅度。
3) 在真空(4.5 kPa)脱附及热力(300 ℃)脱附2种再生方法的对比实验中发现,热力(300 ℃)脱附是13X分子筛恢复吸附分离性能的良好方法,这为扩大其在沼气吸附分离提纯领域的工业应用奠定了基础。
[1] 国家能源局. 生物质能发展“十二五”规划[EB/OL]. [2012−12−28]. http://www.gov.cn/zwgk/2012-12/28/content_ 2301176.htm . The National Energy of Bureau. Biomass energy development in the twelfth five year plan[EB/OL]. [2012−12−28]. http://www.gov.cn/zwgk/2012-12/28/content_2301176.htm .
[2] 李喜. 甲烷/二氧化碳吸附剂研究[D]. 天津: 天津大学化工学院, 2005: 5−6. LI Xi. Experimental study on the adsorbents for the CO2/CH4mixture[D]. Tianjin: Tianjin University. School of Chemical Engineering and Technology, 2005: 5−6.
[3] Morishige K. Adsorption and separation of CO2/CH4on amorphous silica molecular sieve[J].The Journal of Physical Chemistry C, 2011, 115(19): 9713−9718.
[4] 刘培生. 多孔材料引论[M]. 北京: 清华大学出版社, 2012: 6−10. LIU Peisheng. The introduction of porous materials[M]. Beijing: Tsinghua University Press, 2012: 6−10.
[5] MU Bin, Walton K S. High-pressure adsorption equilibrium of CO2, CH4, and CO on an impregnated activated carbon[J].Journal of Chemical & Engineering Data. 2011, 56(3): 390−397.
[6] Silva J A C, Schumann K, Rodrigues A E. Sorption and kinetics of CO2and CH4in binderless beads of 13X zeolite[J]. Microporous and Mesoporous Materials, 2012, 158: 219−228.
[7] Alonso-Vicario A,Ochoa-Gómez J R, Gil-Río S. et al. Purification and upgrading of biogas by pressure swing adsorption on synthetic and natural zeolites[J]. Microporous and Mesoporous Materials, 2010, 134(1): 100−107.
[8] 李通, 罗仕忠, 吴永永, 等. 活性炭改性及其对CO2/CH4吸附性能的研究[J]. 煤炭学报, 2011, 36(12): 2012−2017. LI Tong, LUO Shizhong, WU Yongyong, et al. Study of the modifying of activated carbon and its adsorption properties of CO2/CH4mixture[J]. Journal of China Coal Society, 2011, 36(12): 2012−2017.
[9] Remy T,Peter S A,Denayer J F M, et al. Adsorption and separation of CO2on KFI zeolites: Effect of cation type and Si/Al ratio on equilibrium and kinetic properties[J]. Langmuir, 2013, 29(16): 4998−5012.
[10] Shang J, Li G,Webley P A, et al. Discriminative separation of gases by a “Molecular Trapdoor” mechanism in chabazite zeolites[J]. Journal of the American Chemical Society, 2012, 134(46): 19246−19253.
[11] 杨海燕, 李文哲, 高海云.碳基吸附剂提纯CH4/CO2混合气中CH4的研究[J].农业机械学报, 2013, 44(5): 154−157.YANG Haiyan, LI Wenzhe, GAO Haiyun. Purification of CH4from CH4/CO2mixture using carbon-based adsorbents[J]. Journal of China Agricultural Machinery, 2013, 44(5): 154−157.
[12] Yang R T. Adsorbents: Fundamentals and applications[M]. Hoboken: John Wiley and Sons, 2003: 8−16.
[13] 李云东, 易红宏, 唐晓龙, 等.吸附剂特性对CO2/CH4吸附分离的影响分析[J]. 化工进展, 2012, 31(5): 974−980. LI Yundong, YI Honghong, TANG Xiaolong, et al. Impact of the characteristics of adsorbents on the adsorption and separation of CO2/CH4binary system[J]. Chemical Industry and Engineering Progress, 2012, 31(5): 974−980.
[14] Huang Q L, Eić M. Commercial adsorbents as benchmark materials for separation of carbon dioxide and nitrogen by vacuum swing adsorption process[J]. Separation and Purification Technology, 2013, 103: 203−215.
[15] Seung-Tae Y, Kim J, Wha-Seung A. CO2adsorption over ion-exchanged zeolite beta with alkali and alkaline earth metal ions[J]. Microporous and Mesoporous Materials, 2010, 135(1): 90−94.
[16] Walton K S, Abney M B, LeVan M D.CO2adsorption in Y and X zeolites modified by alkali metal cation exchange[J].Microporous and Mesoporous Materials, 2006, 91(1): 78−84.
[17] Liang Z, Marshall M, Chaffee A L. CO2adsorption-based separation by metal organic framework (Cu-BTC) versus zeolite (13X)[J]. Energy & Fuels, 2009, 23(5): 2785−2789.
[18] Remy T, Peter S A, van der Perre S, et al. Selective dynamic CO2separations on Mg-MOF-74 at low pressures: a detailed comparison with 13X[J]. The Journal of Physical Chemistry C, 2013, 117(18): 9301−9310.
[19] Pham T D, Liu Q L, Lobo R F. Carbon dioxide and nitrogen adsorption on cation-exchanged SSZ-13 zeolites[J]. Langmuir, 2013, 29(2): 832−839.
(编辑 罗金花)
Adsorption separation performance of different absorbents for biogas decarbonization upgrading
WANG Zhixiang, YI Honghong, TANG Xiaolong, ZHAO Shunzheng, ZUO Yanran, GAO Fengyu, ZHANG Bowen
(School of Civil and Environmental Engineering, University of Science and Technology Beijing, Beijing 100083, China)
Dynamic adsorption experiments were carried out using coconut shell activated carbon, with 5A and 13X molecular sieves as adsorbents and gas mixtures with different CO2/CH4volume ratios as methane simulation. Vacuum (4.5 kPa) desorption and thermal desorption (300 ℃) on fully adsorbed 13X molecular sieve were carried out. The results show that the breakthrough adsorption amount of CO2on 13X molecular sieve is 3.21 mmol/g, and the separation factor of CO2/CH4gas mixtures is up to 10, significantly higher than those of the 5A molecular sieve and coconut shell activated carbon at room temperature and pressure. The breakthrough time becomes smaller, which accompanies the decrease of CO2partial pressure, and the decrease rate of adsorption amount is larger than that of partial pressure. The adsorption separation performance of vacuum desorption regeneration of 13X molecular sieve can only be restored to about 40% of the original one, while thermal desorption regeneration can achieve better results.
activated carbon; molecular sieve; adsorption; breakthrough curve; regeneration
10.11817/j.issn.1672-7207.2015.09.050
X511,O643.32+2
A
1672−7207(2015)09−3535−05
2014−11−22;
2015−01−30
教育部新世纪优秀人才支持计划项目(00022402);中央高校基本科研业务费专项资金资助项目(06101046) (Project(00022402) supported by the Program for New Century Excellent Talents in Chinese University; Project(06101046) supported by the Fundamental Research Funds for the Central Universities)
易红宏,教授,博士生导师,从事大气污染控制、环境功能材料等研究;E-mail: yhhtxl@126.com
