实验室制乙炔及性质检验的一体化微型实验设计
2015-12-18姚玉琴,衷明华
实验室制乙炔及性质检验的一体化微型实验设计
姚玉琴衷明华
(韩山师范学院化学系,广东 潮州 521041)
摘要:微型一体化实验可以使气体的制取与性质的实验同时进行,其优势在于缩短反应时间,实验效果明显。既能满足实验所要获取化学性质的要求,又大幅度地降低原料试剂的用量,减少化学反应对环境的污染,体现了绿色化学的理念。
关键词:乙炔微型化实验
在人教版高中化学教科书选修5中,实验室制取乙炔是中学化学教材中一个非常重要的实验。此实验常用饱和食盐水代替蒸馏水与碳化钙反应,但是实际操作过程中容易出现以下问题:
1.虽然用饱和食盐水来代替水,但电石和饱和食盐水的反应速率仍然相当快,速率难以控制。同时产生大量泡沫,容易堵塞导管,影响实验效果。
2.直接用点燃处理尾气产生大量浓烟,污染教室空气,影响师生健康。
3.乙炔制备和性质实验采用多次进行,没有连续性,既浪费药品又消耗时间。
因此,笔者为了克服上述不足,使用微型化改造,通过对乙炔的制取实验进行多次研究和操作验证,提出了本实验方案,希望能达到更好的教学效果。
一、实验原理
CaC2+2H2O→C2H2↑+Ca(OH)2
2MnO4-+6H++C2H2→2Mn2++2CO2+4H2O
CH≡CH+Br2→CHBr=CBr
CHBr=CHBr+Br2→CHBr2—CHBr2
二、实验用品
仪器:微型实验仪器一盒、注射器一个。
药品:25%乙醇水溶液、电石、硫酸铜溶液、酸性高锰酸钾溶液、溴水。
三、实验装置示意图(略去微型操作台装置部分)
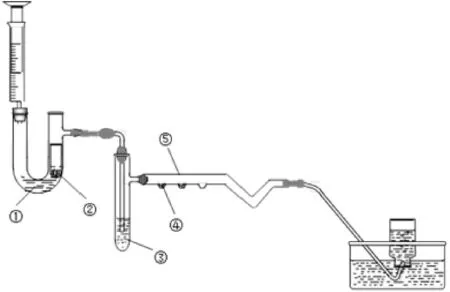
图 实验装置 (注:①25%乙醇水溶液;②电石;③硫酸铜溶液;④酸性高锰酸钾溶液;⑤溴水。)
四、实验步骤与现象
1.按照上图组装好仪器,并检查装置的气密性。
2.添加药品:在具支U形试管右侧内套管中加入少量电石,同时在U形管底部加入适量25%乙醇水溶液,液面要保持内套管底部以下,在U形具支试管的胶塞上开一个小孔,利用小孔插入注射器;在具支试管中加入硫酸铜溶液;在V形侧泡反应管的第一个凹槽加入酸性高锰酸钾溶液,在第二个凹槽中加入溴的四氯化碳溶液。
3.开始实验并观察实验结果:慢慢推动注射器的推手,以增大U形具支试管中的压强,从而使其内的25%乙醇水溶液与电石接触。反应比较温和、适中,有少量泡沫产生,但不影响对实验现象的观察,有气体产生。通过硫酸铜溶液以除去反应产生的杂质,继而通过酸性高锰酸钾溶液、溴水来检验乙炔的性质。此时观察到酸性高锰酸钾溶液、溴水均褪色,而剩余的乙炔则用排水法收集,实验结束后再用燃着的木条伸到集气瓶口,使少量乙炔在空气燃烧,燃烧时火焰明亮、伴有浓烈的黑烟。因此,乙炔可以再空气中燃烧,也易被酸性高锰酸钾溶液所氧化,也能与溴水发生加成反应。
五、改进实验后的优点
1.利用微型实验装置进行实验,装置组装简单、方便,实验药品用量减少,成本降低,乙炔的制取及性质检验一次性完成,简化了实验操作过程以及实验装置。
2.采用推动注射器手柄来改变U形具支试管中的压强,能较好的控制反应的发生与停止,也能较好的控制反应速率。
3.实验中将饱和食盐水用25%乙醇水溶液代替,使反应程度适中,泡沫产生较少,能清晰的观察到有气体产生。减少了实验的危险性,实验的可靠性、安全性增强。
4.利用V形侧泡反应管,可以方便、快速地检验出乙炔的性质。
5.实验过程中收集的乙炔气体,减少乙炔排放到空气中,污染环境,影响师生的身体健康,体现了绿色化学的理念。
