艾塞那肽对2型糖尿病患者血糖控制达标率的效果评价
2015-12-05余宏伟姜美君宋俊红董砚虎
余宏伟,姜美君,宋俊红,张 磊,董砚虎
1.潍坊医学院 临床学系(潍坊 261042);2.青岛内分泌糖尿病医院 内分泌科(青岛 266001)
糖尿病是一种以慢性高血糖为特征的代谢综合征[1],其主要病理生理特征是胰岛素分泌不足或作用不足引起的糖脂代谢紊乱,并继发水电解质代谢失衡。预计到2030年,全球糖尿病人数将突破4亿[2],其中2型糖尿病占绝大多数。ADA糖尿病医学诊断标准[3]推荐大部分2型糖尿病糖化血红蛋白(HbA1C)水平应小于7%。目前市场上治疗2型糖尿病的药物多存在体质量增加、低血糖或随着糖尿病病程延长继发性失效等问题。艾塞那肽作为一种胰升血糖素样肽-1(GLP-1)受体激动剂,是第1个被批准上市的用于治疗2型糖尿病血糖控制不理想患者的药物。随机对照试验已经证实艾塞那肽在2型糖尿病患者中血糖控制和体质量减轻方面的安全性,然而其对亚洲人群血糖控制目标实现的研究数据非常有限。本研究回顾性观察艾塞那肽对血糖控制不佳的2型糖尿病患者血糖控制目标达标率的影响和用药安全性。
1 资料与方法
1.1 临床资料
选取2010年1月至2014年11月于青岛内分泌糖尿病医院就诊并用艾塞那肽治疗3~32个月的2型糖尿病患者202例作为观察组,其中,男122例,女80例,平均年龄(58.45±10.11)岁,平均病程(12.87±4.35)年;另选同期于该院住院或门诊治疗的2型糖尿病非艾塞那肽治疗患者202例作为对照组,其中,男114例,女88例,平均年龄(52.61±11.37)岁,平均病程(15.02±6.58)年。所有患者均符合1999年WHO糖尿病诊断标准。排除标准:合并糖尿病急性并发症、感染、应激、严重心脑血管疾病、器官衰竭、使用免疫抑制剂及糖皮质激素、甲亢、甲减、妊娠等可能会影响血糖、血压、血脂监测的疾病。研究对象均知情同意。
1.2 治疗方法和观察指标
两组患者入院初期均接受糖尿病健康知识教育,强调饮食管理,运动时间控制在3餐后0.5~1h,运动强度相对稳定。两组均接受降压、调脂治疗,并根据血压、血脂水平及时调整治疗方案。观察组加用艾塞那肽(美国阿斯利康公司生产),2次/d,5μg/次,餐前30~40min皮下注射,若耐受良好,4周后改为2次/d,10μg/次皮下注射。以美国糖尿病协会推荐的大部分2型糖尿病HbA1C水平应小于7%为最优管理目标。出现饥饿感、心悸、出汗、头晕、视物模糊等低血糖症状,伴或不伴自我血糖监测结果≤3.9mmol/L,均认为出现低血糖。研究对象均于晚10:00后禁食,12:00后禁水,次日晨6:00抽取静脉血测HbA1C(高效液相色谱法,爱科来HbA1C分析仪)、TG(酶法,日立全自动生化分析仪)、TCHO(终点法,日立全自动生化分析仪)、LDL(免疫比浊法,日立全自动生化分析仪)。研究对象分别在基线和治疗结束时由经过专业培训的内科护士测量身高、体质量、腰围、臀围、血压,测量2次取其平均值,并计算 WSR、WHR、BMI。
1.3 统计学方法
采用SPSS 16.0统计软件进行数据处理,符合正态分布的计量资料以均数±标准差(±s)表示,组间比较采用独立样本t检验,每组治疗前后比较采用配对t检验。计数资料以百分比表示,率的比较采用四格表χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗前后一般临床资料和实验室指标比较
与治疗前比较,两组治疗后HbA1C均下降(P<0.01),观察组治疗后BMI、WSR、SBP、DBP下降(P<0.01);观察组与对照组比较,治疗前后BMI、WSR、SBP、DBP差异有统计学意义(P<0.05)(表1)。
表1 两组治疗前后临床资料和实验室指标比较(n=202,±s)
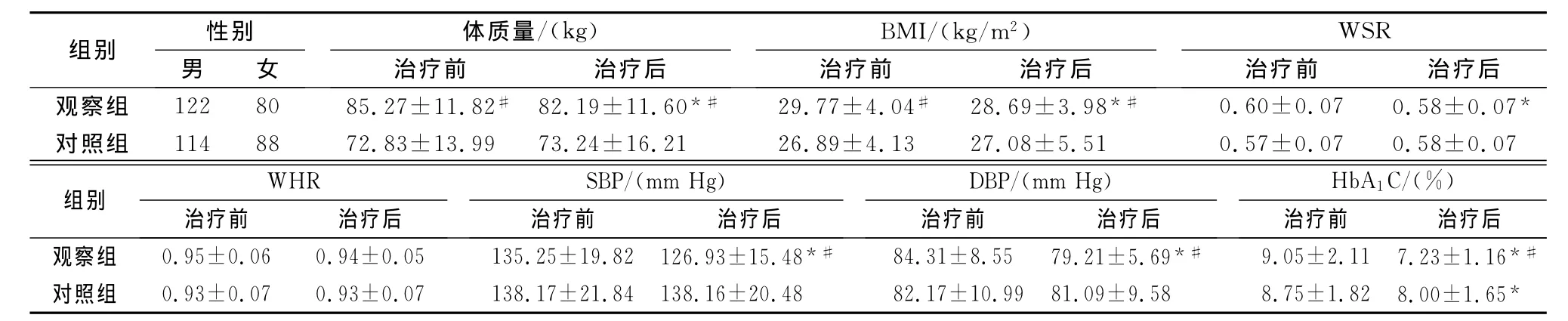
表1 两组治疗前后临床资料和实验室指标比较(n=202,±s)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05
组别 性别 体质量/(kg)BMI/(kg/m2)WSR治疗前 治疗后观察组 122 80 85.27±11.82# 82.19±11.60*# 29.77±4.04# 28.69±3.98*# 0.60±0.07 0.58±0.07男 女 治疗前 治疗后 治疗前 治疗后*SBP/(mm Hg)对照组 114 88 72.83±13.99 73.24±16.21 26.89±4.13 27.08±5.51 0.57±0.07 0.58±0.07组别 WHR DBP/(mm Hg)HbA1C/(%)治疗前 治疗后观察组 0.95±0.06 0.94±0.05 135.25±19.82 126.93±15.48*# 84.31±8.55 79.21±5.69*# 9.05±2.11 7.23±1.16*#治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 0.93±0.07 0.93±0.07 138.17±21.84 138.16±20.48 82.17±10.99 81.09±9.58 8.75±1.82 8.00±1.65*
2.2 两组治疗前后HbA1C达标率比较
治疗前两组HbA1C达标率比较差异无统计学意义(P>0.05),治疗后观察组HbA1C达标率显著高于对照组(P<0.05)(图1)。
2.3 两组不良反应发生情况比较
观察组和对照组低血糖发生例数分别为30例和34例,两组低血糖发生率(14.85%及16.83%)比较,差异无统计学意义(P>0.05)。观察组和对照组出现恶心、呕吐例数分别为40例和15例,观察组恶心、呕吐发生率较对照组明显升高(21.40%及7.50%),差异有统计学意义(P<0.05)。两组均无严重不良反应发生。
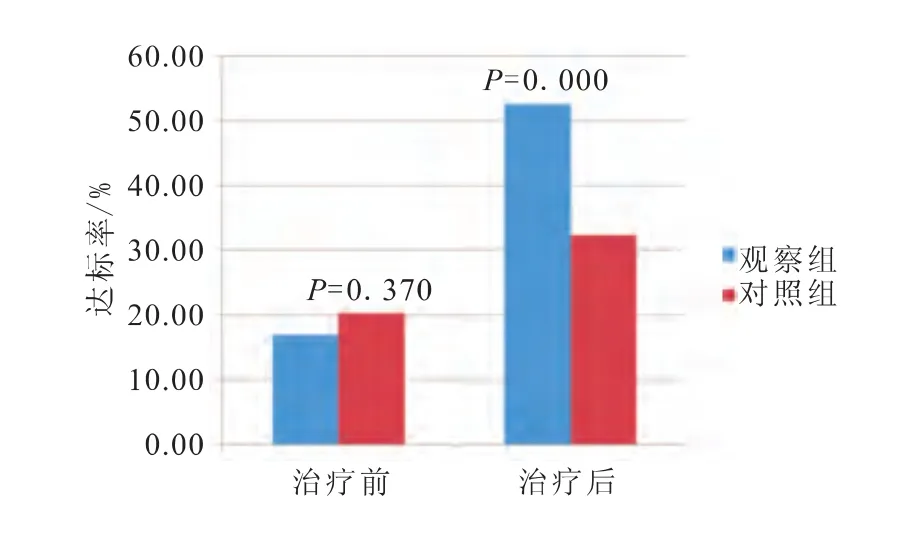
图1 两组治疗前后HbA1C达标率比较
3 讨论
2型糖尿病往往伴有脂代谢紊乱及胰岛素抵抗。据统计,60%~80%的成年2型糖尿病患者在发病前均有肥胖[4]。GLP-1主要由肠道L细胞合成和分泌,其特异性受体广泛表达于各种类型的细胞和组织上,包括胰腺α、β细胞、胃小凹、小肠黏膜、心肺和中枢神经系统等。相关研究[5]表明,GLP-1分泌不足与2型糖尿病发病有关。
GLP-1受体激动剂艾塞那肽具有葡萄糖浓度依赖性的特点,能显著改善HbA1C水平。观察组治疗后HbA1C水平较治疗前下降约1.8%,这与Bergenstal等[6-8]的研究结果基本一致。治疗前HbA1C的达标率为16.80%,治疗后达标率为52.48%,略高于叶林秀等[9]的研究结果,可能与样本量差异有关。一项多中心的随机双盲、安慰剂对照的临床研究[10]表明,艾塞那肽治疗24周后SBP和DBP分别平均下降了3.7mm Hg和2.3mm Hg,Klonoff等[11]证实,给予艾塞那肽治疗超过3年,患者SBP平均下降2.0mm Hg,DBP平均下降4.0 mm Hg。本研究观察组SBP平均下降8.3mm Hg,DBP平均下降5.1mm Hg,均高于既往研究,可能与降压药的应用有关。艾塞那肽使血压下降的机制一方面可能与血糖、血脂等代谢指标的控制、血管内皮细胞功能的改善有关,另一方面可能与GLP-1具有促进尿、钠排泄有关。关于艾塞那肽的降压作用是否独立于体质量的减轻及内脏脂肪含量的降低目前尚存争议[12-14]。无论是观察组治疗前后比较,还是观察组与对照组治疗后比较,结果均显示艾塞那肽可降低体质量、BMI、HbA1C、SBP及DBP水平。两组治疗后HbA1C达标率比较,观察组较对照组明显升高(P<0.05)。
本研究显示,观察组与对照组低血糖发生率差异无统计学意义,这与Cohen等[15]的研究结果一致。整个治疗过程中,两组均无严重不良反应发生。
综上所述,艾塞那肽可明显改善2型糖尿病HbA1C水平,降低血压,提高HbA1C达标率,且无严重不良反应发生,是2型糖尿病血糖控制不达标患者联合用药的理想选择。然而,由于艾塞那肽价格昂贵,限制了其在临床中的使用。目前关于艾塞那肽的临床资料有限,其对HbA1C、血压及血脂的远期治疗效果及长期用药安全性尚有待进一步研究。
[1]潘长玉.Joslin糖尿病学[M].北京:人民卫生出版社,2007:338.
[2]Shaw JE,Sicree RA,Zimmet PZ.Global estimates of the prevalence of diabetes for 2010and 2030[J].Diabetes Research and Clinical Practice,2010,87(1):4-14.
[3]American Diabetes Association.Standards of medical care in diabetes-2013[J].Diabetes Care,2013,36(1):11.
[4]黄立嵩,王立秋,林朱森,等.胰高血糖素样肽-1对胰岛素抵抗肌细胞脂代谢相关基因表达的干预作用[J].中国新药杂志,2010,19(6):526-536.
[5]Hare KJ,Vilsboll T,Asmar M,etal.The glucagonostatic and insulinotropic effects of glucagon-like peptide 1contribute equally to its glucose-lowering action[J].Diabetes,2010,59(7):1765-1770.
[6]Bergenstal RM,Wysham C,Macconell L,etal.Efficacy and safety of exenatide once weekly versus sitagliptin or pioglitazone as an adjunct to metformin for treatment of type 2diabetes(DURATION-2):a randomised trial[J].Lancet,2010,376(9739):431-439.
[7]Blonde L,Klein EJ,Han J,etal.Interim analysis of the effects of exenatide treatment on A1C,weight and cardiovascular risk factors over 82weeks in 314overweight patients with type 2diabetes[J].Diabetes,Obesity and Metabolism,2006,8(4):436-447.
[8]Amori RE,Lau J,Pittas AG.Efficacy and safety of incretin therapy in type 2diabetes:systematic review and metaanalysis[J].Jama,2007,298(2):194-206.
[9]叶林秀,郭昆全,朱梅,等.胰高血糖素样肽-1类似物对2型糖尿病患者体质量及胰岛β细胞的影响[J].湖北医药学院学报,2013,32(3):213-216.
[10]Moretto TJ,Milton DR,Ridge TD,etal.Efficacy and tolerability of exenatide monotherapy over 24weeks in antidiabetic drug-naive patients with type 2diabetes:A randomized,double-blind,placebo-controlled,parallel-group study[J].Clinical Therapeutics,2008,30(8):1448-1460.
[11]Klonoff DC,Buse JB,Nielsen LL,etal.Exenatide effects on diabetes,obesity,cardiovascular risk factors and hepatic biomarkers in patients with type 2diabetes treated for at least 3years[J].Current Medical Research and Opinion,2007,24(1):275-286.
[12]Monami M,Cremasco F,Lamanna C,etal.Glucagon-like peptide-1receptor agonists and cardiovascular events:ameta-analysis of randomized clinical trials[J].Exp Diabetes Res,2011,2011:215764.
[13]Okerson T,Yan P,Stonehouse A,etal.Effects of exenatide on systolic blood pressure in subjects with type 2diabetes[J].American Journal of Hypertension,2010,23(3):334-339.
[14]Paul S,Best J,Klein K,etal.Effects of HbA1C and weight reduction on blood pressure in patients with type 2diabetes mellitus treated with exenatide[J].Diabetes,Obesity and Metabolism,2012,14(9):826-834.
[15]Cohen ND,Audehm R,Pretorius E,etal.The rationale for combining GLP-1receptor agonists with basal insulin[J].Med J Aust,2013,199(4):246-249.
