Sysmex XN-9000血液分析仪检测低值血小板的性能评价
2015-12-03刘爱胜
吴 敏 文 艳 刘爱胜
Sysmex XN-9000血液分析仪检测低值血小板的性能评价
吴 敏①文 艳②刘爱胜①
目的:评价Sysmex XN-9000全自动血液分析仪检测全血中低值血小板(PLT)的性能。方法:随机收集XN-9000检测全血PLT计数<70×109/L的临床标本48份,分别用XN-9000和显微镜计数,通过对两种方法所测得的结果进行相关性分析,评价XN-9000检测全血中低值PLT的精密度、相关性、准确度、携带污染率、线性范围以及临床可报告范围。结果:XN-9000检测全血中低值PLT的批内和批间CV%分别为1.13%和1.29%;XN-9000与显微镜PLT计数结果具有高度相关性,回归方程为Y=0.917X+3.217,相关系数r=0.964;XN-9000检测全血中低值PLT的携带污染率为0.12%;检测PLT的正确度(Bias%)为-1.25%~1.80%;线性范围为(0~1206)×109/L;临床可报告范围为(0~6030)×109/L。结论:XN-9000血液分析仪检测全血中低值PLT具有很高的精密度和准确度,携带污染率极低,结果具有可靠性,可直接应用于临床。
XN-9000血液分析仪;低值血小板;显微镜检查;性能评价
DOI∶ 10.3969/J.ISSN.1672-8270.2015.08.016
[First-author’s address] Clinical Laboratory, Shenzhen Longhua New District People's Hospital, Guangdong 518109, China.
Sysmex XN-9000全自动血液分析仪是Sysmex公司最新推出的XN系列产品最高端一款血细胞分析仪,其在检测通道和试剂方面有所改变,其中增加了低值血小板(blood platelet,PLT)检测。PLT计数专用检测通道,主要用于低值血小板的检测。为了解XN-9000检测全血中低值PLT的性能,本研究对其性能进行评价。
1 材料与方法
1.1 仪器与试剂
Sysmex XN-9000全自动血液分析仪及配套试剂、校准品及质控品均购自日本Sysmex公司;CX21显微镜、BX50显微镜购自日本Olympus公司;血小板稀释液购于上海江莱生物科技有限公司;德国Brand改良Neubauer计数板购于上海正慧工贸有限公司。
1.2 标本来源
随机收集2014年1-8月深圳市龙华新区人民医院门诊患者标本48份,其中男性标本21份,女性标本27份;患者年龄5月~82岁,平均26.5岁。其血液常规检测PLT计数<70×109/L者视为低值PLT-F(按国际血液学复查规则41条定义),真空采集静脉血于EDTA-K2抗凝管内充分混匀送检,确保血标本无凝集现象。同一份标本上机和显微镜检测均于1 h内完成[1]。
1.3 精密度
参照(美国)全国委员会临床实验室(NCCLS)/ CLSI EP5-A文件[2]提供的方法,对XN-9000全自动血液分析仪检测全血中低值PLT的精密度进行评价。待室内高、中和低值质控物检测结果在控后,用XN-9000对低值PLT室内质控物连续检测20次,求出低值PLT的批内精密度;同时连续测定低值PLT室内质控物20 d,求出检测低值PLT批间精密度。
1.4 相关性分析
分别用XN-9000(X)参照NCCLS/CLSI EP15-P[3]、EP9-A[4]和显微镜(Y)参照《临床检验操作规程》第3版[5]检测120例低值PLT新鲜全血标本中的PLT,待室内高、中和低值质控物检测结果在控后,操作均由经验丰富的工作人员进行检测,各测3次,取均值,求回归方程及相关系数。
1.5 携带污染率
根据NCCLS/CLSI EP10-A文件[6]提供的方法,选取高、低值PLT新鲜全血标本,先连续测定高值标本3次(H1、H2、H3),后连续测定低值标本3次(L1、L2、L3)。携带污染率(%)=[(L1-L3)/(H3-L3)]×100[7-8]。
1.6 正确度
用XN-9000分析仪连续检测2014年卫生部第一批室间血液质控物3次,取平均值,与卫生部回报的结果靶值比较,并计算出相对偏倚(Bias),其计算公式1:
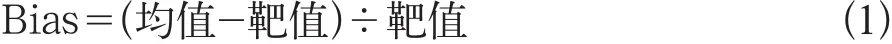
以评价XN-9000分析仪检测低值PLT结果的准确性。
1.7 线性范围
参考EP6-A2文件选取1份接近仪器检测上限的高值PLT(1256×109/L)标本和接近仪器检测下限的低值PLT(15×109/L),按等比例稀释成100%、50%、25%、6.25%、3.125%和0%。混匀后用XN-9000分析仪从低浓度到高浓度测定不同稀释度标本,各重复测定3次,取均值与理论值比较,并进行相关性分析,评价XN-9000分析仪检测PLT的线性范围[9]。
1.8 临床可报告范围
选取PLT浓度高于检测范围高限的临床标本2份(1317×109/L和1536×109/L),用9 g/L生理盐水对所选取样本按1∶2,1∶3,1∶4,1∶5及1∶9的5个比例稀释,分别为批号201411,201412,201413,201414,201415,混匀后各样本分别测定3次,取均值计算稀释回收率,其计算公式2:

以重复性CV值<5.0%,回收率在90%~l10%以内为可接受,确定最大稀释倍数,结合最大稀释倍数确定临床可报告范围。
1.9 统计学方法
采用SPSS 19.0软件进行统计处理,计量资料以均数±标准差(x-±s)表示,组间比较采用t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 精密度
XN-9000分析仪检测新鲜低值PLT全血标本批内精密度为1.17%,检测低值PLT室内质控物批内和批间精密度(CV%)分别为1.13%和1.29%,均低于仪器设定的要求(<5.00%)。
2.2 相关性
XN-9000分析仪检测全血中、低值PLT与显微镜检测结果具有良好的相关性(r=0.964),回归方程为Y=0.917X+3.217,经t检验,XN-9000分析仪与镜检检测低值PLT结果之间差异无统计意义(t=1.07,P>0.05)。
2.3 携带污染率
XN-9000分析仪检测低值PLT的携带污染率为0.12%(<1.00%),小于仪器设定的要求。
2.4 正确度
XN-9000分析仪连续检测卫生部血液室间质评PLT标本3次,取平均值与卫生部回报的靶值作比较,并计算Bias(%)值,Bias值均<5.0%,见表1。

表1 XN-9000分析仪检测PLT正确度(×109/L)
2.5 线性范围
XN-9000分析仪对高、低值PLT标本的不同稀释度样品分别进行测定,各稀释度的实测值和理论值之间相关性良好,相关系数r=0.9993,回归方程为Y=0.9996+2.4573,检测线性范围为(0.00~1206)×109/L。
2.6 临床可报告范围
XN-9000分析仪检测不同稀释倍数的标本中的PLT,在1∶5时,CV均在5%以内,当稀释倍数延伸至1∶9时,回收率超出实验设定范围,所以其最大稀释倍数为9倍。因此,本实验室XN-9000分析仪检测PLT临床可报告范围为(0~6030)×109/L,见表2。

表2 PLT回收率(%)
3 讨论
XN-9000分析仪是Sysmex公司最新推出最高端一款血细胞分析仪,其在检测通道和试剂方面有所改变,增加了低值PLT计数专用检测通道,主要用于低值血小板的检测。
良好的精密度是验证其他各项指标的基础,其大小应小于仪器规定的要求才能保证临床标本检测的重现性[10]。本研究结果显示,XN-9000分析仪检测低值PLT批内和批间精密度分别为1.13%和1.29%,均低于仪器设定的要求(5%),并且XN-9000分析仪检测低值PLT与显微镜人工PLT计数具有很高的相关性(r=0.981),两者结果差异无统计学意义,其原因为Sysmex XN-9000全自动血液分析仪采用液压聚焦法(DC检测法)和半导体激光器的流式细胞计数法对细胞计数,可以防止区域的血细胞回流,并可防止产生假性血小板脉冲,且计数细胞数量是其他系列的3~5倍之多,改善了血细胞计数的精确度和重现性。
携带污染率是判断高值标本是否影响低值标本检测结果的指标,其大小应符合仪器制造商的要求。本研究结果显示,XN-9000分析仪检测PLT标本携带污染率极低(0.12%),这主要与XN-9000分析仪血细胞计数时由于血细胞通过在一条直线上的小孔,可减少对贯流池的污染,降低细胞计数标本之间的携带污染率等有关。
XN-9000分析仪检测卫生部室间低值血小板质控物(PLT-F)的Bias%值为-1.25~1.80,均<5.0%,XN-9000分析仪检测低值PLT的正确度极高,这主要与其采用最新的荧光染色技术(PLT-O)。荧光染色技术(PLT-O)使用专用的荧光染液,该染液选择性染色血小板,网织红细胞难以染色,且不易受到红细胞碎片的影响及仪器增加了低值WBC及低值PLT专用检测通道,进一步确保了低值PLT检测结果的准确性等因素有关。
线性范围的验证是确定临床可报告范围的基础,当仪器检测超出线性范围的结果时,应视为不准确的测定值[11-15]。本研究结果显示,XN-9000分析仪检测血小板的线性范围广(0.00~1206)×109/L及临床可报告范围宽(0~6030)×109/L,有利于高值PLT检出的准确性,这主要与PLT-F通道中的PLT计数是XE系列产品的3~5倍之多,极大地提高了PLT检测的精密度和准确性等因素有关。
4 结语
PLT-F通道在全血模式、低值白细胞模式及稀释模式均可检测,标本检测前只要按照国际血液学复检规则41条及XN-9000分析仪本身要求,复检规则中设定好只要违反PLT复检规则就进行PLT-F通道检测PLT,其操作非常简单,临床工作中只需根据临床需要修改复检规则便可与血常规一同检查,并得出准确可靠的PLT结果,而且XN-9000分析仪检测PLT的线性范围和临床可报告范围很广,适用各种浓度标本的检测。
[1]Elkin Simson.全自动血液分析仪的复检标准[J].崔巍译.中华检验医学杂志,2007,30(4):371-373.
[2]National Committee for Clinical Laboratory Standards.Evaluation of Precision performance of clinical chemistry devices,approved guideline[S].NCCLS,Wayne,PA:EP5-A,1999.
[3]National Committee for Clinical Laboratory Standards.User demonstration of Performance for Precision and accuracy[S].NCCLS,Wayne PA:EP15-P,1998.
[4]National Committee for Clinical Laboratory Standards.Method comparison and bias estimation using patient samples,approved guidline[S].NCCLS,2nd ed.Wayne,PA:EP9-A2,2002.
[5]叶应妩,王毓三,申子瑜,等.全国临床检验操作规程[M].3版.南京:东南大学出版社,2006:312-319.
[6]National Committee for Clinical Laboratory Standards.Preliminary evaluation of quantitative clinical laboratory methods,approved guideline[S]. NCCLS,2nd ed.Wayne,PA:EP10-A2,2002.
[7]王梅,昊燕.XT-4000i多功能全自动血细胞分析仪体液模式性能验证[J].重庆医学,2013,42(33):4002-4006.
[8]白雪丽.XT-4000i多功能全自动血细胞分析仪在体液细胞检测中与手工法的应用比较[J].中国医疗设备,2012,27(1):75-76.
[9]马科,左路广,李宝亮,等.Sysmex XE-5000全自动血细胞分析仪检测血液标本性能评价研究[J].医疗卫生装备,2013,34(12):80-82.
[10]温科梅,兰海丽,缪丽韶,等.应用NCCIS相关文件验证和评价ADVIA1650检测系统性能[J].国际检验医学杂志,2008,29(8):737-739.
[11]阳苹,周爱娥,张莉萍,等.罗氏MODULAR E170全自动电化学发光免疫分析仪性能验证[J].重庆医学,2009,38(19):2395-2397.
[12]杨有业,张秀明.临床检验方法学评价[M].北京:人民卫生出版社,2008:118.
[13]张磊,宋清福,高素芳,等.迈瑞BC5300型全血细胞分析仪的性能评价[J].河北医学,2013,35(19):2943-2945.
[14]王礼法.Sysmex XN-9000全自动血液分析仪性能评价[J].中国医学装备,2014,11(12):38-41.
[15]周芸,周强,邓小燕,等.BC-5800型血液细胞分析仪临床应用评价[J].检验医学与临床,2010,7(22):2459-2461.
Blood analyzer Sysmex XN-9000 testing in low whole blood platelet performance evaluation
WU Min, WEN Yan, LIU Ai-sheng
China Medical Equipment,2015,12(8)∶51-53.
Objective∶ To evaluate the performance of Sysmex XN-9000 automatic blood analyzer (hereinafter referred to as XN-9000) in whole blood with the low platelet (PLT). Methods∶ A total of 48 whole blood samples with platelet count less than 70×109/L were randomly collected from XN-9000 correlation analysis to evaluate XN-9000 the accuracy and precision of detection in low whole blood PLT and carry pollution rate, use XN-9000 and microscope count, respectively. Results∶ XN-9000 detection in low whole blood PLT between batch and batch of CV% 1.13% and 1.29%, respectively; XN-9000 with microscope PLT count results have high correlation, The regression equation for Y=0.917X+3.217,correlation coefficient r=0.964; XN-9000 detection in low whole blood PLT carry pollution at a rate of 0.12%. Detection accuracy of PLT Bias, %(-1.25%~1.8%); Linear range(0~1206)×109/L; Clinical reportable range (0~6030)×109/L. Conclusion∶ The detection of XN-9000 blood analyzer is in low whole blood PLT has high precision and accuracy, carry pollution rate is extremely low, the result has the reliability, can be directly applied to clinical.
XN-9000 blood analyzer; Low platelet; Microscopic examination; Performance evaluation
1672-8270(2015)08-0051-03
R446.111
A
吴敏,女,(1981- ),本科学历,主管技师。深圳市龙华新区人民医院检验科,从事临床检验与免疫工作。
2014-12-25
①深圳市龙华新区人民医院检验科 广东 深圳 518109
②深圳市光明新区人民医院ICU 广东 深圳 518106
