腹腔穿刺放气结合胃肠减压在内镜下胃全层切除术后的应用*
2015-12-03周静芳戴伟杰陶国全杨晓钟
周静芳 戴伟杰 陶国全 王 琼 杨晓钟*
腹腔穿刺放气结合胃肠减压在内镜下胃全层切除术后的应用*
周静芳①戴伟杰①陶国全②王 琼①杨晓钟①*
目的:探讨腹腔穿刺放气结合胃肠减压在胃黏膜下肿瘤(SMT)行内镜全层切除术(EFR)后伴发气腹中的应用。方法:选取15例行EFR治疗的SMT患者,术后常规进行腹腔穿刺放气并放置胃肠减压管,对所有病例从病灶大小、起源部位、穿孔直径、气腹量以及术后恢复时间等方面进行系统分析。结果:15例患者中1例因穿孔直径过大未能在内镜下缝合,转腹腔镜腔外缝合,其余均在内镜下成功缝合,平均肿瘤大小为(2.0±0.5)cm,平均手术时间为(84.9±8.9) min,穿孔平均直径为(0.8±0.4)cm,缝合所需钛夹平均为(4.5±1.9)枚,术后腹部立位片右侧膈下游离气体深度平均值为(6.2±3.3)cm,术后平均进食时间为(4.1±1.5)d,术后平均住院天数为(6.4±3.5)d,术后随访气腹完全吸收时间为(12.6±5.1)d。结论:腹腔穿刺放气结合胃肠减压是一种安全有效的处理胃黏膜下肿瘤行EFR术后伴发气腹的有效方法。
胃黏膜下肿瘤;内镜下全层切除术;腹腔穿刺;胃肠减压
DOI∶ 10.3969/J.ISSN.1672-8270.2015.08.003
[First-author’s address] Department of Gastrogenterology, The First Hospital of Huaian with Nanjing Medical University, Huaian 223300, China.
胃黏膜下肿瘤(submucosal tumor,SMT)是指起源于胃上皮层以下的肿瘤,主要包括胃平滑肌瘤、间质瘤、脂肪瘤、神经源性肿瘤以及血管瘤等[1-2]。临床中最为常见的是胃平滑肌瘤和间质瘤,其有向恶性肿瘤转化的可能,需要及时治疗,因此内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)成为SMT病变首选的治疗方法[3-4]。但对ESD方法只能切除起源于浅固有肌层的病变,对于起源于深固有肌层或浆膜层的病变只能通过新近发展起来的内镜全层切除术(endoscopic full-thickness resection,EFR)进行根治[5-6]。EFR的手术中必然要发生胃壁穿孔,而内镜下的操作要求在胃腔内不断注气,因此患者术后往往有较严重的气腹,影响患者的呼吸及循环功能,而气腹的处理直接关系到患者生命安全、手术质量以及术后的恢复[7]。本研究应用腹腔穿刺放气结合胃肠减压处理EFR患者的术后气腹取得了较好的临床效果[8-9]。
1 资料与方法
1.1 一般资料
选取2010年7月至2013年1月在南京医科大学附属淮安第一医院行EFR手术的15例SMT患者,所有患者均因非特异性的消化道症状行胃镜检查而发现病变,其中男性9例,女性6例;年龄34~66岁,平均年龄(51±12.5)岁。
1.2 纳入与排除标准
(1)纳入标准:①起源于胃黏膜下肿瘤;②肿瘤<3 cm;③手术方式为胃的全层切除;④在内镜下顺利缝合。
(2)排除标准:①一般情况差,不能耐受内镜手术;②术中穿孔未能成功行内镜下缝合;③术中发生较大并发症,内镜无法处理转为开腹手术。
1.3 仪器设备
采用Olympus GIF-Q 260J胃镜(日本,奥林巴斯);EU-M 2000内镜超声系统(日本,奥林巴斯);NM-4L-1注射针(日本,奥林巴斯);FD-430L热活检钳(日本,奥林巴斯);HX-610-35止血夹(日本,奥林巴斯);ERBE VIO200s高频电切装置和APC 2氩离子凝固器(德国,ERBE);Olympus KD-620LR HOOK刀(日本,奥林巴斯);OlympusKD-611L IT刀(日本,奥林巴斯);NOE342216-C圈套器(日本,奥林巴斯)。
1.4 手术方法
手术在全身麻醉、气管插管及心电监护下进行。操作前内镜头端常规安装透明帽:①应用钩刀或APC于病灶边缘进行电凝标记;②生理盐水+美兰于标记点范围内进行黏膜下注射,如病变为明显凸向腔内也可不予标记;③针状刀行病变周围黏膜切开,配合IT刀沿黏膜下层或固有肌层进行剥离,术中出血使用APC或热活检钳止血,如病变起源于深固有肌层,可用针状刀或IT刀沿病变周围剥离并尽量保留浆膜层完整,最后再沿病变周围切开浆膜层造成主动穿孔,配合圈套器完整切除肿瘤;④迅速吸净胃腔内液体和大部分气体,在胃镜直视下应用金属夹自创面两侧向中央完整对缝创面。
1.4.1 术前准备
术前常规检查心电图、凝血功能、血常规及生化,手术当日患者禁食,适当给予营养支持治疗,向患者及其家属交代术中和术后可能出现的问题,并签署手术知情同意书,特别告知患者及家属手术中如有较大穿孔不能在内镜下缝合则转用腹腔镜或开腹行腔外缝合。
1.4.2 术后处理
(1)患者取半卧位,禁食、胃肠减压,并记录胃肠减压引流量,吸氧和心电监护。胃肠减压管常规留置3 d,观察是否有腹痛、腹胀及发热等腹膜炎症状体征,观察是否有呕血、黑便等迟发性出血症状。
(2)常规用穿刺针于右上腹部穿刺排气减压,如气腹严重导致明显腹胀或呼吸困难者,留置穿刺针直至症状好转。
(3)术后定期复查腹部立位片、腹腔彩超,复查血常规,2~3 d后行泛影葡胺造影,观察是否有造影剂胃腔内外渗。如无造影剂外渗,术后3 d可进食流质饮食。
2 结果
在15例行EFR的患者中1例胃穿孔直径达2.5 cm未能在内镜下缝合,转腹腔镜腔外缝合,其余14例均在内镜下成功缝合,平均肿瘤大小为(2.0±0.5)cm,平均手术时间为(84.9±8.9)min,穿孔平均直径为(0.8±0.4) cm,缝合所需钛夹平均为(4.5±1.9)枚,术后腹部立位片右侧膈下游离气体深度平均值为(6.2±3.3)cm(如图1所示)。
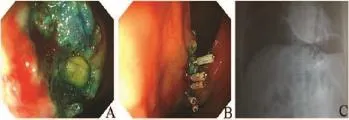
图1 SMT患者行EFR后腹部影像图
所有患者术后均恢复良好,无腹腔感染、迟发性出血、皮下气肿及气胸发生,术后平均进食时间为(4.1±1.5)d,平均住院天数为(6.4±3.5)d,术后随访气腹完全吸收时间为(12.6±5.1)d,见表1。
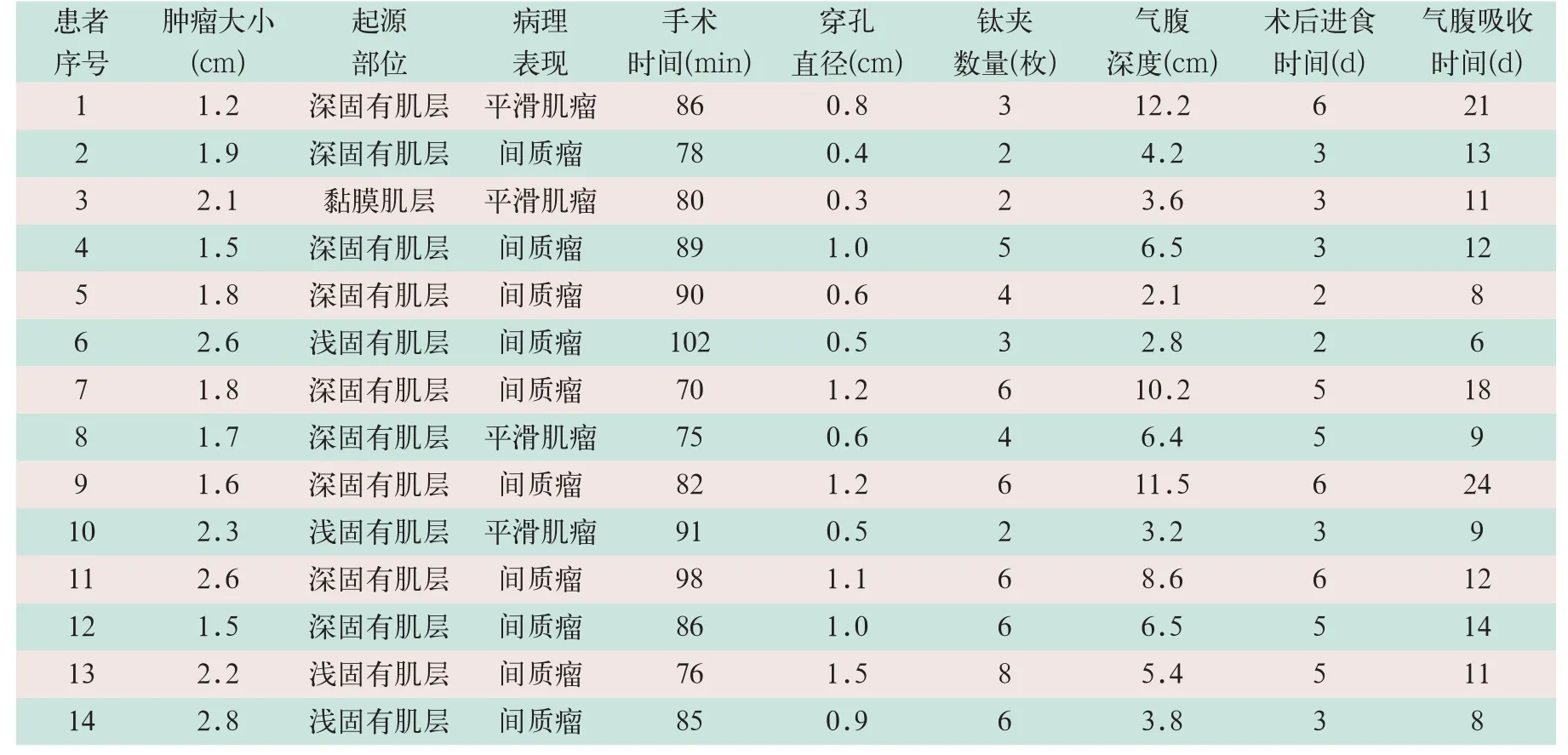
表1 EFR患者的临床资料
3 讨论
胃SMT的大部分病变如间质瘤、平滑肌瘤均为良性病变,但其存在着潜在向恶性肿瘤转化的可能,因此临床中在治疗方法的选择上倾向于早期行ESD切除病变。而起源于深固有肌层或浆膜层的SMT是ESD的禁区,因为如果强行切除必然导致胃壁的穿孔,但随着内镜技术的快速发展,通过EFR手术方式已达到能将上述病变完全切除的能力,其优点不仅在于手术创伤小,同时使得胃的完整性得到保留,避免了胃大部切除后患者发生残胃炎、吻合口炎甚至继发癌变的可能[10-12]。
EFR虽然使得起源于深固有肌层或浆膜层的胃黏膜下肿瘤成为可能,但由于是全层切除,术中必然会发生胃壁穿孔并导致气腹,严重的气腹可影响心肺功能,同时可继发腹腔内感染、消化道腹腔漏等诸多棘手的后续问题,因此必须妥善处理气腹问题才能保障患者术后的安全及恢复质量[13-14]。
临床中主要应用腹腔穿刺放气结合胃肠减压来处理EFR术后气腹,并起到了较好的临床效果。①胃肠减压负压吸引能及时的排除胃腔内的酸性胃液和气体,有效控制胃内压力,使得EFR的缝合面摆脱了低张力的状态和高酸的环境,有利于创面的愈合,同时还能帮助观察是否有继发性出血;②通过腹腔内穿刺放气减少腹腔内的压力,大部分患者在行腹腔穿刺放气后腹胀、腹痛等相关症状能迅速缓解,同时还有效减少了术后腹腔内继发感染的概率。本研究中的14例EFR手术患者,无1例发生术后感染、迟发性出血、心肺功能意外以及延迟愈合等并发症,术后的平均进食时间为4.1 d,平均住院时间只有6.4 d,有效的减少了患者的住院费用。
本研究发现,患者术后气腹的量和恢复的时间密切相关,因此术中控制患者的气腹量对术后的恢复尤为关键,同时患者发生穿孔后的气腹程度与穿孔的直径并不是相对应的,这可能还与手术过程中患者胃腔内的压力、穿孔后操作的时间以及钛夹的夹闭方式等多种因素相关。
EFR手术在治疗胃深固有肌层和浆膜层肿瘤中发挥着重要的作用,术中需行胃壁全层切除,因此必然发生胃壁穿孔并导致术后气腹,通过胃肠减压和腹腔穿刺放气能有效改善患者术后气腹症状,减少患者术后并发症及平均住院时间和费用,是一种安全有效的处理胃黏膜下肿瘤EFR术后气腹方法。
[1]周平红,姚礼庆,秦新裕,等.内镜粘膜下剥离术在早期胃肠肿瘤中的应用与评价[J].中华胃肠外科杂志,2010,13(2):324-326.
[2]Farhat S,Chaussade S,Ponchon T,et al.Endoscopic submucosal dissection in a European setting. A multi-institutional report of a technique in development[J].Endoscopy,2011,43(8):664-670.
[3]Lee HL,Kwon OW,Lee KN,et al.Endoscopic histologic diagnosis of gastric GI submucosal tumors via the endoscopic submucosal dissection technique[J].Gastrointest Endosc,2011,74(3):693-695.
[4]Nakamura M,Shibata T,Tahara T,et al.Usefulness of transnasal endoscopy where endoscopic submucosal dissection is difficult[J].Gastric Cancer,2011,14(4):378-384.
[5]Chang YW,Hwangbo Y,Lee JW,et al.Clinical parameters including serum pepsinogen level and management strategy inpatients with premalignant gastric dysplasia[J].Eur JGastroenterol Hepatol,2011,23(5):405-410.
[6]Chun HJ,Keum B,Kim JH,et al.Current status of endoscopic submucosal dissection for the management of early gastric cancer:a Korean perspective[J].World J Gastroenterol,2011,17(21):2592-2596.
[7]周平红,姚礼庆,秦新裕,等.无腹腔镜辅助的内镜全层切除术治疗源于固有肌层的胃黏膜下肿瘤[J].中华消化内镜杂志,2009,26(12):617-621.
[8]时强,钟芸诗,姚礼庆,等.内镜全层切除术的研究进展[J].中华消化内镜杂志,2011,28(10):595-598.
[9]焦健华,李学良,于连珍,等.内镜下胃壁全层切除术对胃间质瘤的治疗价值研究[J].中华消化内镜杂志,2011,28(11):632-634.
[10]Choi J,Kim SG,Im JP,et al.Endoscopic prediction of tumor invasion depth in early gastric cancer[J].Gastrointest Endosc,2011,73(5): 917-927.
[11]Kikuchi D,Iizuka T,Hoteya S,et al.Usefulness of endoscopic ultrasound for the prediction of intraoperative bleeding of endoscopic submucosal dissection for gastric neoplasms[J].J Gastroenterol Hepatol,2011,26(1):68-72.
[12]Tanizawa Y,Bando E,Kawamura T,et al. Surgical resection for mucosal gastric cancer in the era of endoscopic submucosal dissection[J]. Hepatogastroenterology,2010,57(104):1620-1624.
[13]陈虹.胃肠间质瘤内镜下粘膜剥离术的护理[J].实用临床医药杂志,2010,14(14):3-4.
[14]何赛琴.内镜粘膜下剥离术治疗早期胃癌患者的护理[J].全国消化内镜清洗消毒暨消化内镜新进展学术会议暨福建省第六届消化内镜学术会议,2008:196-198.
The application of abdominocentesis and gastrointestinal decompression during the endoscopic full-thick-ness resection for gastric submucosal tumors
ZHOU Jing-fang, DAI Wei-jie, TAO Guo-quan, et al
China Medical Equipment,2015,12(8)∶7-10.
Objective∶ To summarize the application of abdominocentesis and gastrointestinal decompression during the endoscopic full-thick-ness resection for gastric submucosal tumors. Methods∶ There were 15 gastric SMTs were treated by EFR, we summarized the researches from the tumor size, the tumor origin, the diameter of perforation, the pneumoperitoneum and the recovery period, et al. Results∶ One of them failed to suture because the perforation size was too large, the median tumor size was 2.0±0.5cm, the median operation time was 84.9±8.9min, the median diameter of perforation was 0.8±0.4cm, the median hemostatic clips was 4.5±1.9, the median recovery period was 6.4±3.5 days, the median absorb time of pneumoperitoneum was 12.6±5.1 days. Conclusion∶ Abdominocentesis and gastrointestinal decompression is safe and effective method to deal with pneumoperitoneum after the EFR for gastric SMT.
Gastric submucosal tumor; Endoscopic full-thick-ness resection; Abdominocentesis; Gastrointestinal decompression
1672-8270(2015)08-0007-04
R656.61
A
周静芳,女,(1982- ),硕士研究生,主治医师。南京医科大学附属淮安第一医院消化科,研究方向:消化道肿瘤的发病机制。
2014-12-21
国家自然科学基金(81302490)“PI3K/Akt/mTOR信号通路基因遗传变异与胃癌易感及其机制研究”
①南京医科大学附属淮安第一医院消化科 江苏 南京 223300
②南京医科大学附属淮安第一医院胃肠外科 江苏 南京 223300
*通讯作者:xz_yang1023@aliyun.com
