替加环素联合头孢哌酮-舒巴坦治疗广泛耐药鲍曼不动杆菌医院获得性肺炎临床疗效观察
2015-12-02秦又发朱永坤
秦又发,吴 雷,朱永坤,张 扬
鲍曼不动杆菌(Acinetobacter baumannii)属于不动杆菌属,是一种不发酵糖类、革兰阴性、无动力的双球菌或球杆菌,是医院感染的重要致病菌之一[1]。主要引起呼吸机相关性肺炎、泌尿系感染、菌血症等[2]。近年来随着广谱抗菌药物的大量应用,广泛耐药鲍曼不动杆菌(extensively drug resistant Acinetobacter baumannii,XDRAB)菌株逐渐增多,甚至呈暴发流行的趋势。根据美国临床和实验室标准化协会(CLSI)的定义:XDRAB 是指对氨基糖苷类、碳青霉烯类、氟喹诺酮类、头孢菌素类、β内酰胺酶抑制剂的复合制剂、四环素类、单环β内酰胺类、叶酸代谢抑制剂等8类抗菌药物均耐药,但不包括替加环素和多黏菌素[3-4]。XDRAB 的出现给临床治疗带来挑战,而国内外进行临床随机对照研究的报道至今少见。本文旨在观察替加环素联合大剂量头孢哌酮-舒巴坦治疗XDRAB的临床疗效,现报道如下。
1 材料与方法
1.1 临床资料
1.1.1 纳入标准 选择2012年2月—2014年11月本院确诊XDRAB 呼吸道感染的患者。确诊标准:①符合2005 年美国提出医院获得性肺炎(HAP)的诊断标准,即肺部出现新的或进展性浸润影加3项临床表现中的2项(体温>38℃,白细胞升高或降低,气道出现脓性分泌物);②连续3 d痰培养(至少有1次为纤维支气管镜吸引的痰标本)均检出鲍曼不动杆菌(≥+++),药敏结果为广泛耐药,但均对替加环素敏感。排除标准:①既往有糖尿病、肿瘤、肝硬化、粒细胞减少或缺乏、免疫功能低下等易导致感染难以控制的基础性疾病;②近期正在接受大剂量激素冲击治疗、放化疗或服用免疫抑制剂的患者;③合并其他细菌感染;④中途放弃治疗,不能完成治疗疗程。
1.1.2 临床资料和分组 该试验经过医院伦理委员会批准,患者均签署知情同意书。共有53例患者纳入本研究,其中重症监护病房(ICU)28 例、神经外科15例、呼吸科8例,其他科室2例,均为医院获得性感染。按试验前设定的随机数字表分别进入头孢哌酮-舒巴坦联合替加环素组(试验组,27 例)和单用替加环素组(对照组,26例)。两组患者一般情况比较差异无统计学意义,见表1。53株病原菌药敏结果均为对头孢他啶、头孢曲松、头孢吡肟、头孢哌酮-舒巴坦、哌拉西林-他唑巴坦、氨曲南、亚胺培南、美罗培南、阿米卡星、妥布霉素、米诺环素、甲氧苄啶-磺胺甲口恶唑等耐药,仅对替加环素和多黏菌素敏感。53例中40例在试验前有过气管插管呼吸机辅助呼吸的治疗经历,都曾给予过头孢曲松、哌拉西林-他唑巴坦、头孢哌酮-舒巴坦、阿米卡星、亚胺培南-西司他丁、美罗培南、左氧氟沙星等药物中的1种或2种治疗5~7 d且无效。

表1 试验前两组患者一般情况比较Table 1 Baseline patient characteristics in the two treatment groups
1.2 方法
1.2.1 药敏试验 采用美国BD 公司生产PHOENIX-100型全自动细菌鉴定和药敏测试系统。替加环素的药敏试验参照美国FDA 的标准判断:最低抑菌浓度(MIC)<2 mg/L为敏感;2~8 mg/L为中介;>8 mg/L为耐药[5]。
1.2.2 给药方法 试验组给予注射用头孢哌酮-舒巴坦(1∶1)3.0g+5%葡萄糖注射液100 mL静脉滴注,每6小时1次,完毕后2 h内给予替加环素注射液50 mg+0.9%氯化钠注射液100 mL静脉滴注,每12小时1次;对照组给予5%葡萄糖注射液100 mL静脉滴注,每6小时1次,完毕后2 h内给予替加环素注射液50 mg+0.9%氯化钠注射液100 mL静脉滴注,每12小时1次。两组替加环素首剂均加倍,疗程均为14 d。
1.2.3 观察项目 包括临床症状、体征,治疗前以及14 d后血、尿、粪便常规,C-反应蛋白,肝肾功能,细菌药物敏感性试验,胸部X线或肺部CT 及药物不良反应(包括恶心、呕吐等胃肠道反应,黄疸、肝氨基转移酶升高、肌酐升高等肝肾功能改变,凝血功能异常,皮疹等)。
1.2.4 临床疗效判定标准[6]痊愈:症状、体征、实验室检查及病原学检查4项均恢复正常;显效:病情明显好转,但上述4项中有1项未恢复正常;进步:用药后病情有所好转,但不够明显,上述4项中>1项未恢复正常;无效:用药72 h病情未改善或有加重。有效率(%)=(痊愈例数+显效例数)/总例数×100%
1.2.5 细菌学疗效 按病原菌清除、未清除、替换进行评定,并计算细菌清除率(细菌清除率=清除例数/总例数×100%)。清除:治疗结束后没有分离到致病菌;未清除:治疗结束后致病菌仍存在;替换:用药结束后,原有病原菌被清除,但分离到另一种新的病原菌,患者无感染征象,无需抗菌治疗。
1.2.6 统计学方法 组间有效率、细菌清除率以及不良反应发生率的显著性检验采用χ2,两组试验前一般情况的显著性检验采用方差分析(ANOVA),均应用SPSS 20.0版软件进行分析,P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效比较
治疗14 d后,试验组有13例痊愈,6例显效,临床有效率为70.4%;对照组有5例痊愈,5例显效,临床有效率为38.5%;临床有效率试验组明显高于对照组(P=0.020),见表2。
2.2 细菌学疗效
治疗14 d后,试验组病原菌清除15例,未清除12例,无发生替换病例,细菌清除率55.6%,对照组病原菌清除9例,未清除13例,4例发生替换,细菌清除率38.5%;两组细菌清除率差异无统计学意义(P=0.213),见表3。
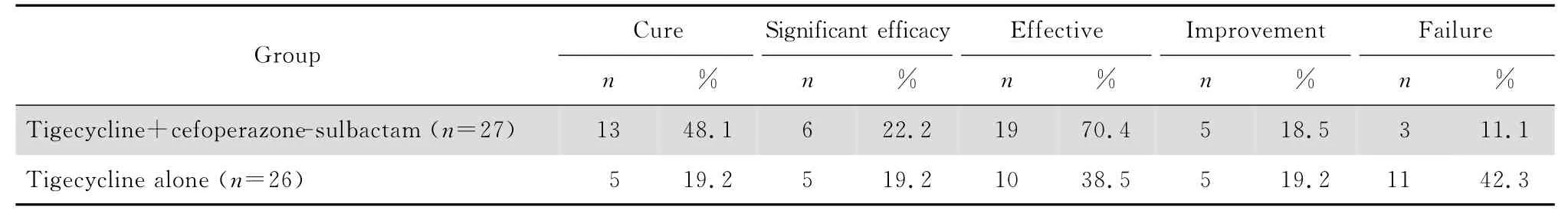
表2 治疗14 d后两组疗效比较Table 2 Clinical efficacy of tigecycline plus cefoperazone-sulbactam versus tigecycline alone as evaluated 14 days post-treatment
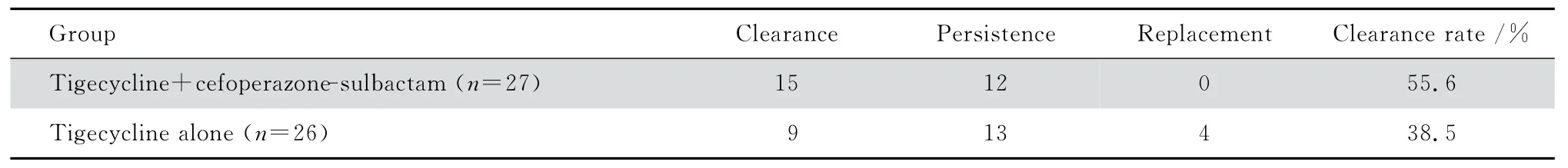
表3 治疗14 d后两组细菌清除率比较Table 3 Bacterial clearance rate 14 days after treatment with tigecycline plus cefoperazone-sulbactam versus tigecycline alone
2.3 不良反应发生率比较
两组患者均未出现肝肾功能受损、凝血功能异常、皮疹等,两组各出现2例(14.3%和15.4%)表现为恶心、呕吐等消化道症状,不良反应发生率差异无统计学意义(P>0.05)。
3 讨论
鲍曼不动杆菌具有强大的获得性耐药和克隆传播,其对常用抗菌药物的耐药率呈逐年升高的趋势[7],XDRAB医院获得性肺炎患者逐渐增多。而XDRAB的耐药机制主要包括产生多种β 内酰胺酶、氨基糖苷类药物修饰酶、主动外排泵系统、外膜孔蛋白缺失、核糖体保护以及整合子介导的耐药基因积累[8-9]。而替加环素独有的甘氨酰氨基使其克服了鲍曼不动杆菌对四环素类药物耐药的主要机制——由TetA 和TetB 转座子介导的外排泵以及核糖体保护,故其对耐药的鲍曼不动杆菌仍有效[10]。然而,国内外均没有批准替加环素用于治疗耐药菌引起的医院获得性肺炎,因为其对医院获得性感染的有效性未能证明,特别是对呼吸机相关性肺炎的有效率反而低于对照组(注射用替加环素说明书,2011年9月2日)。但国内外有限的临床实践均证实替加环素联合其他抗菌药物对XDRAB感染具有良好的临床疗效[11-13]。这一现象的出现,我们推测可能与研究样本量不够大、替加环素需要联合用药或替加环素剂量过低有关。
舒巴坦为青霉烷砜酸结构的β内酰胺酶抑制剂,对不动杆菌属细菌具有抗菌作用,大剂量的舒巴坦(6.0~8.0 g/d)复合制剂甚至可用 于治疗XDRAB感染[14],其联合替加环素治疗广泛耐药菌感染已写进了专家共识[15],但目前仍缺乏大规模的临床随机对照研究[11]。本研究结果表明,替加环素联合大剂量头孢哌酮-舒巴坦治疗XDRAB 医院获得性肺炎的有效率,显著高于替加环素单药,且两组不良反应发生率差异无统计学意义。两组的细菌清除率差异无统计学意义(55.6%对38.5%),且此结果也与Curcio等[16]的研究有较大差异(其研究显示,替加环素治疗呼吸机相关肺炎的细菌清除率高达80%),这种反差提示:XDRAB 更容易定植,更难清除,可能需要更多种药物的联合和更长的治疗疗程。本研究还显示,单用替加环素更容易发生病原菌的替换,对照组11例治疗无效的患者中有4例病原菌替换为铜绿假单胞菌,推测可能与替加环素对铜绿假单胞菌无抗菌活性有关,而联用头孢哌酮-舒巴坦正好可以弥补替加环素的这种“遗憾”,这可能也是二者联合效果更好的原因。综上所述,本研究通过前瞻性临床随机对照研究证实大剂量的头孢哌酮-舒巴坦可提高替加环素对XDRAB 医院获得性肺炎的临床疗效,为XDRAB 感染的治疗提供了一种可行的策略。而替加环素加大剂量是否具有和小剂量联用头孢哌酮-舒巴坦一样的疗效,这需要进一步研究来证实。
[1]Gordon NC,Wareham DW.Multidrug-resistant Acinetobacter baumannii:mechanisms of virulence and resistance[J].Int J Antimicrob Agents,2010,35(3):219-226.
[2]Fournier PE,Richet H.The epidemiology and control of Acinetobacter baumannii in health care facilities[J].Clin Infect Dis,2006,42(5):692-699.
[3]李春辉,吴安华.医疗机构耐药菌MDR、XDR、PDR 的国际标准化定义专家建议(草案)[J].中国感染控制杂志,2011,10(3):238-240.
[4]Peleg AY,Seifert H,Paterson DL.Acinetobacter baumannii:emergence of a successful pathogen[J].Clin Microbiol Rev,2008,21(3):538-582.
[5]王辉,俞云松,王明贵,等.替加环素体外药敏试验操作规程专家共识[J].中华检验医学杂志,2013,36(7):584-587.
[6]卫生部抗生素临床药理基地.抗菌药物临床研究指导原则[J].中国临床药理学杂志,1987,3(2):126-130.
[7]胡付品,朱德妹,汪复,等.2013年中国CHINET 细菌耐药性监测[J].中国感染与化疗杂志,2014,14(5):369-378.
[8]Chiu CH,Lee HY,Tseng LY,et al.Mechanisms ofresistance to ciprofloxacin,ampicillin/sulbactam and imipenem in Acinetobacter baumannii clinical isolates in Taiwan[J].Int J Antimicrob Agents,2010,35(4):382-386.
[9]Chang-Tai Z,Yang L,Zhong-Yi H,et al.High frequency of integrons related to drug-resistance in clinical isolates of Acinetobacter baumannii[J].Indian J Med Microbiol,2011,29(2):118-123.
[10]Guay DR.Oritavancin and tigecycline:investigational antimicrobials for multidrug-resistant bacteria [J].Pharmacotherapy,2004,24(1):58-68.
[11]林孟相,郭蕾,郭献阳,等.替加环素联合头孢哌酮-舒巴坦治疗泛耐药鲍氏不动杆菌感染临床疗效观察[J].中华医院感染学杂志,2013,23(8):1906-1907.
[12]Fishbain J,Peleg AY.Treatment of Acinetobacter infections[J].Clin Infect Dis,2010,51(1):79-84.
[13]亓梅,韩其政,贾曰林.替加环素治疗泛耐药鲍曼不动杆菌肺部感染1例[J].中国感染与化疗杂志,2013,13(3):224-225.
[14]Garnacho-Montero J,Amaya-Villar R.Multiresistant Acinetobacter baumannii infections:epidemiology and management[J].Curr Opin Infect Dis,2010,23(4):332-339.
[15]陈佰义,何礼贤,胡必杰,等.中国鲍曼不动杆菌感染诊治与防控专家共识[J].中国医药科学,2012,2(8):3-8.
[16]Curcio D,Fernander F,Stevenson KB,et al.Late onset ventilator-associated pneumonia due to multidrug-resistant Acinetobacter spp.:experience with tigecycline[J].J Chemother,2009,27(7):58-62.
