抗丙肝新药Dasabuvir
2015-11-24刘恕张曼唐小枚蒋智
刘恕,张曼,唐小枚,蒋智
(药渡经纬信息科技(北京)有限公司,北京100085)
抗丙肝新药Dasabuvir
刘恕,张曼,唐小枚,蒋智
(药渡经纬信息科技(北京)有限公司,北京100085)
编者按:丙型肝炎是由丙肝病毒(HCV)感染引起的急慢性传染病。HCV是单链RNA病毒,存在于人体的血液和体液中,主要通过血液和母婴传播。丙型肝炎患者占病毒性肝炎总数的3%,而在中国这一比率高达16%。全球感染HCV患者超过1亿,每年有超过300万的新增患者,其中80%以上发展为慢性肝炎,并可能发展为肝癌、肝硬化最终导致死亡。自2013年吉利德的Sovaldi(sofosbuvir)上市,丙肝的治愈率得到极大的提升,吉利德也由此开始领跑全球丙肝市场。然而Sovaldi的高昂定价,一开始就使吉利德处于舆论的风口浪尖。除了定价之外,吉利德的Sovaldi还面临专利被拒和后续产品竞争的问题,同时近期还被曝出或可导致心率降低。自Sovaldi上市以来,强生、百时美施贵宝和艾伯维(AbbVie)都相继推出了新的丙肝治疗药物和治疗组合,同时默沙东也在积极开发新药,以期重新在丙肝市场占据一席之地。其中,艾伯维曾于2014年末公布了其丙肝复方药物积极的临床数据,宣称其药物对复发或难治患者表现出极佳的疗效,显然已准备好与吉利德展开直接的竞争,以撼动其独占鳌头的局面。2015年1月,该复方药的成分之一dasabuvir已作为单药获得欧洲药品管理局批准。《药学进展》本期将重点对这一药物进行介绍。
Dasabuvir是2015年1月15日以单药成份获得欧洲药品管理局批准的抗丙肝新药,该药于2014年12月19日以复方药形式(dasabuvir/ombitasvir/paritaprevir/ritonavir)获得美国食品药品管理局批准用于治疗基因1型慢性丙肝病毒感染,包括有代偿性肝硬化患者的治疗。Dasabuvir是一种HCV RNA聚合酶NS5B抑制剂,干扰HCV的正常复制而发挥抗病毒作用。介绍dasabuvir的化学合成、临床前药理学研究、临床研究及专利保护情况等,为抗丙肝新药的研发提供参考。
dasabuvir;NS5B聚合酶抑制剂;丙型肝炎
Dasabuvir(商品名为Exviera,1)于2015年1月15日被欧洲药品管理局(EMA)作为单药批准,用于与ViekiraxTM(ombitasvir/paritaprevir/ritonavir)联用治疗基因1型(GT 1)慢性丙型肝炎病毒(HCV)[1]。该药是由美国艾伯维制药公司(AbbVie)研发的HCV RNA聚合酶NS5B抑制剂,是2014年12月19日美国食品药品监督管理局(FDA)批准的复方药商品名为Viekira PakTM(ViekiraxTM+ ExvieraTM)的一个组分,这种复方给药方案是一种全口服的无干扰素的丙肝鸡尾酒疗法,可单用或与利巴韦林(RBV)联用[1-2]。

1
Dasabuvir的英文名为N-{6-[5-(2,4-Dioxo-3,4-dihydro-1(2H)-pyrimidinyl)-2-methoxy-3-(2-methyl-2-propanyl)phenyl]-2-naphthyl}methanesulfonamide;分子式为C26H26N3O5S;CAS登记号为1132935-63-7。
Dasabuvir为片剂(250 mg),推荐剂量为每日2片,早晚各1片,早上与2片ViekiraxTM(ombitasvir/ paritaprevir/ritonavir,12.5/75/50 mg)同时服用,晚上单独服用,但不建议有失代偿肝病患者使用。
1 合成方法[3]
1.1 方法1
市售的2-叔丁基苯酚(2)经硝化反应、三溴化吡啶鎓酸性条件下的苯环溴化反应,两步以35.6%的收率得到中间体4,随后中间体4与三甲基硅基重氮甲烷(TMSCHN2)反应以92%的收率得到含甲醚的中间体5。钯碳催化条件下,氢气还原硝基成氨基后,叔丁氧羰基保护氨基,随后与8发生Suzuki反应,三步以43%的收率得到中间体9。三氟乙酸脱除中间体9氮原子上的叔丁氧羰基后得到关键中间体10。然后与异氰酸酯11反应生成取代脲后,再于10%硫酸溶液中、高温条件下发生环合反应,最终以7.4%的总收率,经最长线性步骤9步生成dasabuvir。
其中,中间体8可由市售化合物13经碱性水解、Curtius重排(定量收率)后得到萘胺中间体15。再与甲磺酰氯缩合,最后与双链硼酸酯17反应得到中间体8(见图1)。

图1 Dasabuvir的合成方法1Figure 1 Dasabuvir synthesis: route 1
1.2 方法2
市售2-叔丁基苯酚(2)与碘化钠、次氯酸钠反应,以93%的收率得到含有二取代碘的中间体18,随后与碘甲烷反应,以99%的收率得到中间体19。然后在碘化亚铜催化下与尿嘧啶20经Ullmann反应以70%的收率得到关键中间体21,随后在Pd2(dba)3催化下与硼酸酯8发生Sukuzi反应,最终以54.1%的总收率经4步反应得到dasabuvir(见图2)。
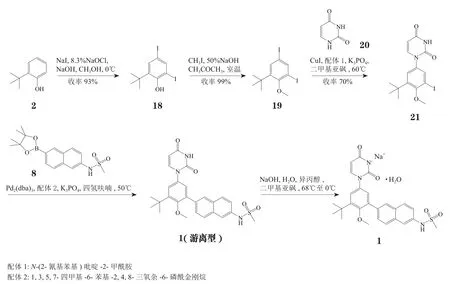
图2 Dasabuvir的合成方法2Figure 2 Dasabuvir synthesis: route 2
1.3 方法3
市售2-叔丁基苯酚(2)经硝化反应,以35.6%的收率得到含硝基的中间体3,随后与氯化碘发生亲电取代反应,以96%的收率得到中间体22。中间体22与三甲基硅基重氮甲烷反应,以84%的收率得到中间体23。铁粉、氯化铵加热条件下还原中间体23的硝基,以定量收率得到含苯胺的中间体24,随后与异氰酸酯25反应,以57%的收率生成取代脲26,再经10%硫酸溶液、高温条件下环合,以90%的收率生成含尿嘧啶的中间体27。最后,中间体27与硼酸酯8在Pd(dppf)Cl2催化下发生Suzuki反应,最终以3.7%的总收率经7步反应得到dasabuvir(见图3)。
2 临床前药理学研究
NS5B蛋白基因编码HCV复制所必需的RNA依赖的RNA聚合酶(RdRp),它作为核心酶在HCV的复制过程中起到关键作用。Dasabuvir是一种非核苷类NS5B聚合酶抑制剂(见图4),与NS5A蛋白酶抑制剂ombitasvir以及NS3/4A蛋白酶抑制剂paritaprevir以多靶点共同阻止HCV的复制,发挥直接抗病毒作用,而ritonavir作为细胞色素P450 3A4抑制剂,本身无抗HCV活性,但能提高partitaprevir的血药浓度[4-6]。Dasabuvir的体外药效学、体内和体外药物代谢参数、药物相互作用及安全性评价数据见表1[1-2]。

图3 Dasabuvir的合成方法3Figure 3 Dasabuvir synthesis: route 3
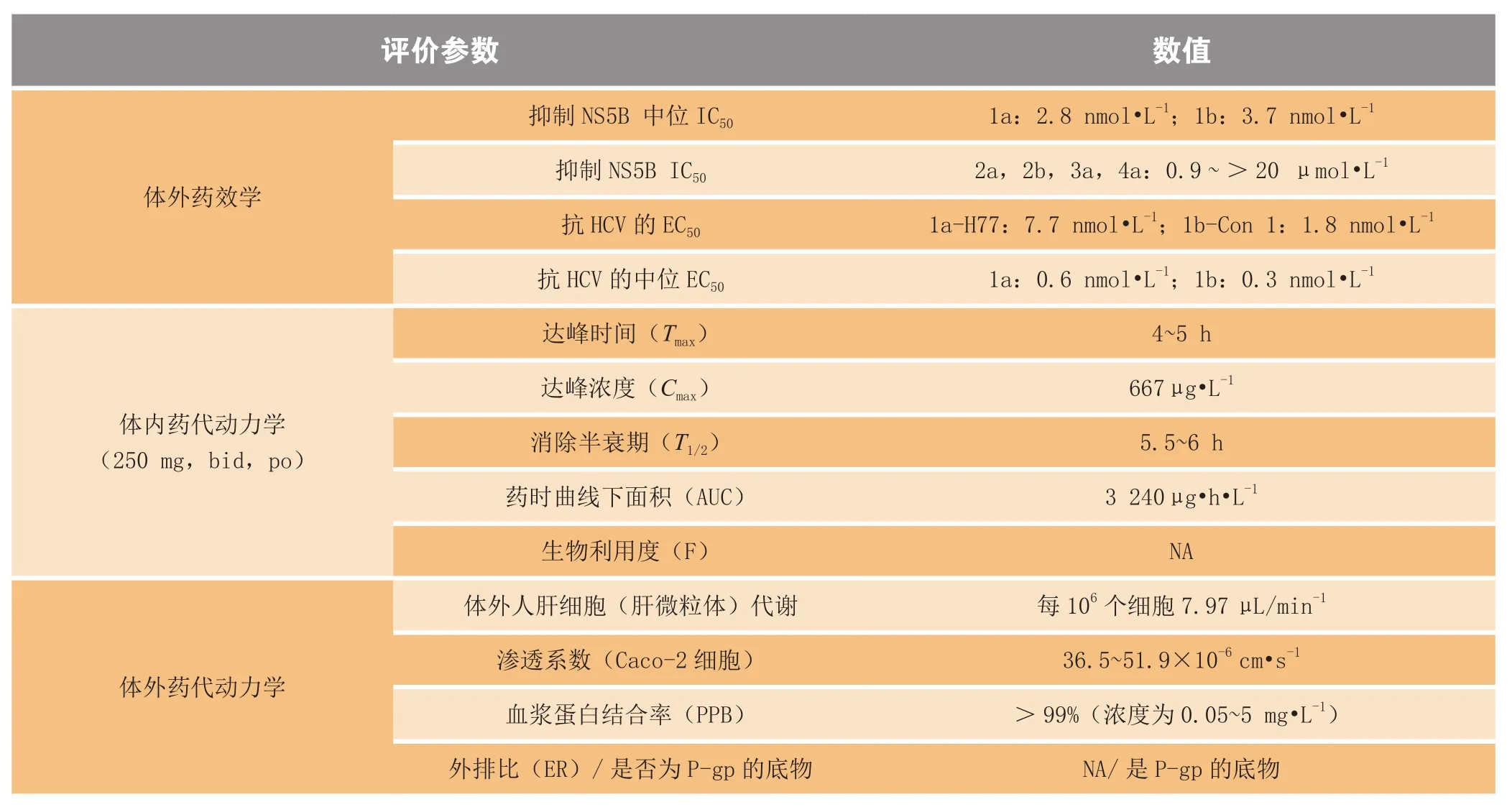
表1 Dasabuvir临床前药理学数据Table 1 Preclinical pharmacology of dasabuvir
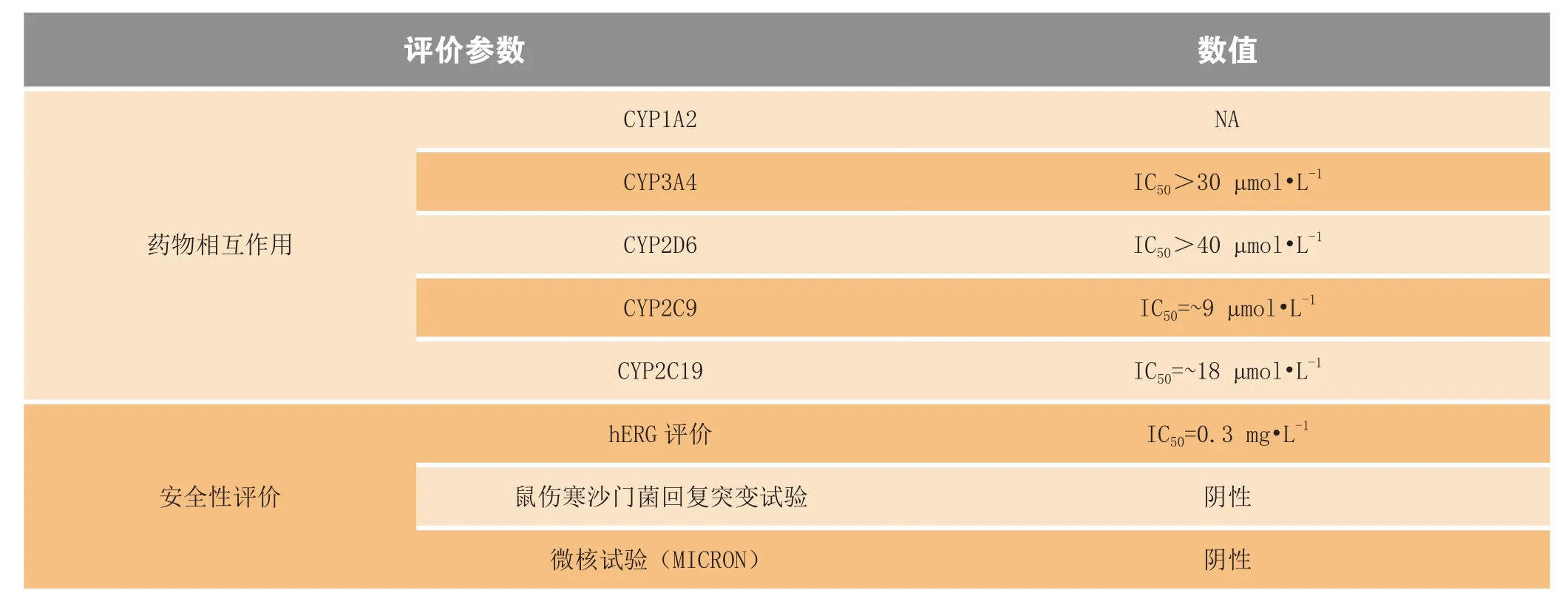
续表1
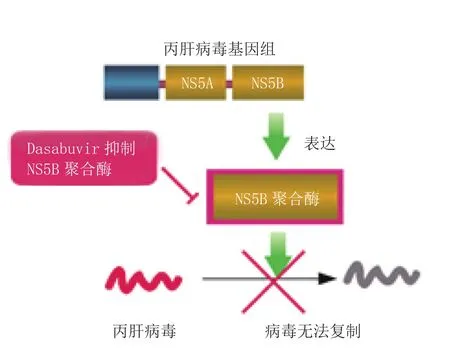
图4 Dasabuvir的作用机制Figure 4 Acting mechanism of dasabuvir
3 临床研究
Dasabuvir的批准是基于复方药Viekira PakTM的6项随机、多中心的Ⅲ期临床试验数据。共招募了2 308例基因1型慢性丙肝患者,分别为未经治疗的或曾经接受聚乙二醇干扰素和利巴韦林(RBV)治疗后复发或有部分病毒学应答及无应答的患者。给药方案为每天服用1次ombitasvir/paritaprevir/ritonavir(12.5/75/50 mg),2次dasabuvir(250 mg)或加服RBV,治疗周期为12或24周。主要终点指标是治疗结束后病毒学持续应答SVR12(FDA定义为治疗结束12周之后的丙型肝炎病毒达到不可测的水平)。这6项Ⅲ期临床试验的关键数据见表2[1]。
服用Viekira Pak和利巴韦林的患者中,最常见的不良反应(10%)为疲劳、恶心、皮肤瘙痒、失眠和神经衰弱。而在不加服利巴韦林的患者中,最常见的不良反应(≥5%)为恶心、皮肤瘙痒和失眠。

表2 关键临床试验数据Table 2 Clinical data of dasabuvir
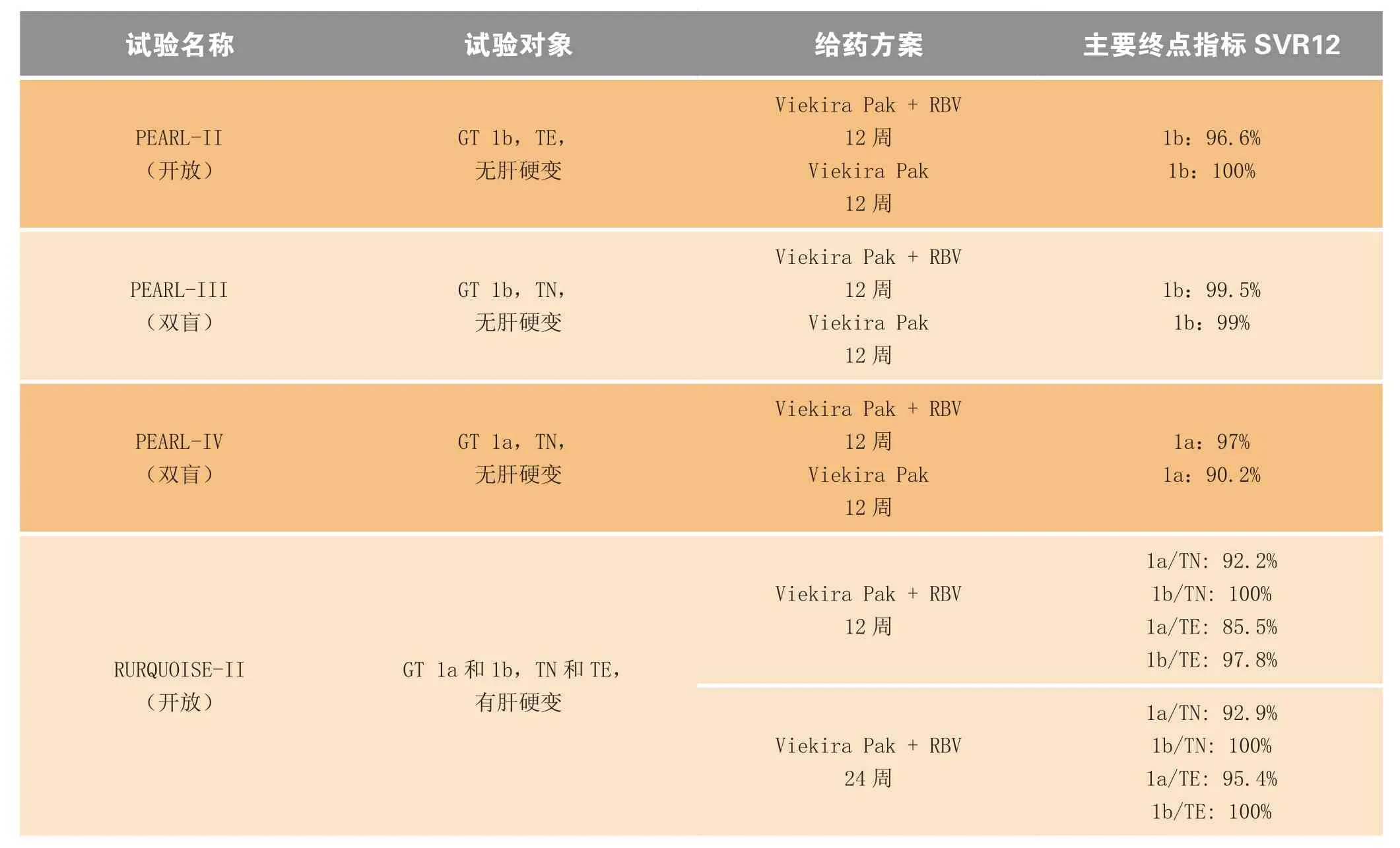
续表2
4 专利布局
4.1 Exviera®化合物专利的全球布局
Exviera®的化合物专利是由雅培(Abbott)公司以PCT申请(公开号WO2009039134A1)公开,并陆续在日本、欧洲、美国及中国获得授权,现专利权已转移给AbbVie公司(见表3)。
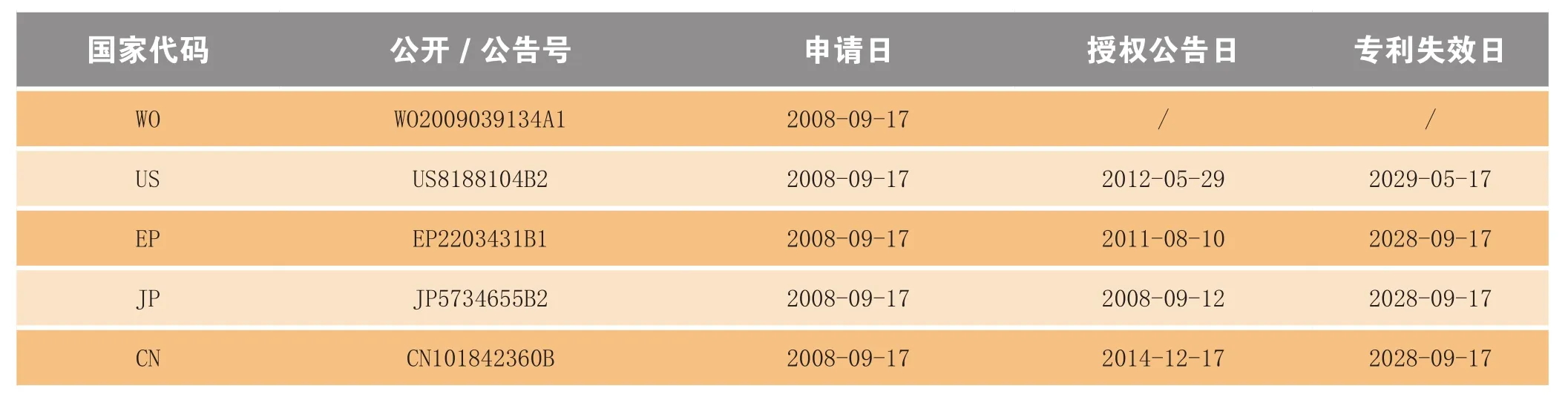
表3 Exviera®化合物专利的全球布局Table 3 Worldwide patent portfolio of active ingredient in Exviera®
4.2 Exviera®外围专利的全球布局
在研发过程中,雅培/AbbVie公司主要针对其核心及关键专利进行保护,公开号WO2009039134的专利中涉及了结构通式、晶型、盐类、制备方法和联合用药等内容;后又申请了制备方法、中间体及联合用药的专利,其中主要保护和利巴韦林的药物联用(见表4)。
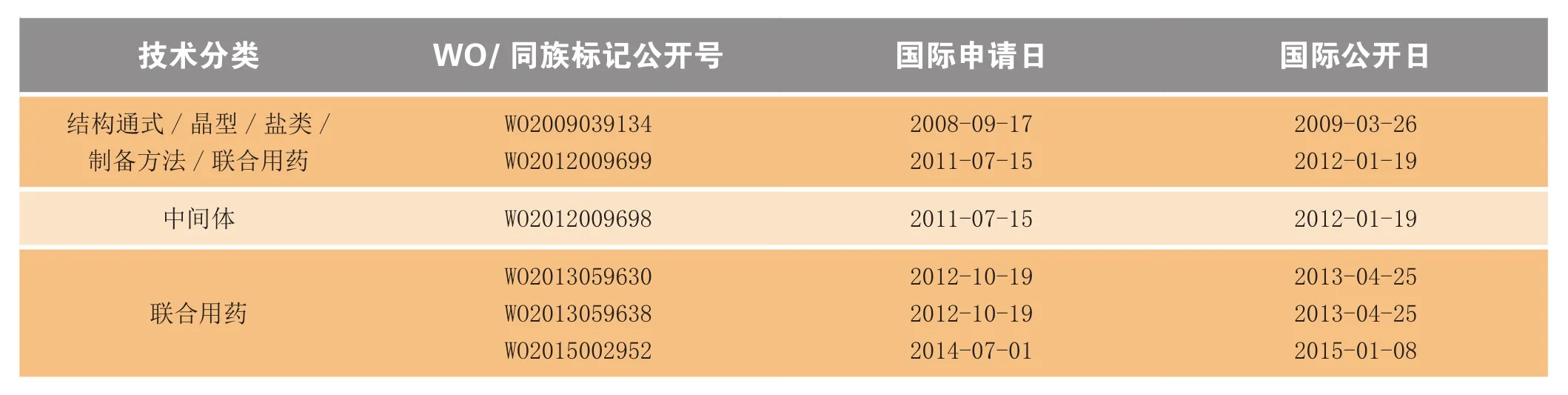
表4 Exviera®外围专利的全球布局Table 4 Worldwide peripheral patent portfolio of Exviera®
4.3 Exviera®在中国的专利申请情况
Exviera®的化合物专利在中国已获得授权(授权公开号CN101801935B),以结构通式形式进行保护,此篇专利还涉及适应证和联合用药。其晶型、制备方法、中间体和联合用药的专利都处于实审状态,专利权现均为AbbVie公司所有(见表5)。

表5 Exviera®在中国的专利保护情况Table 5 Patent protection of Exviera®in China
目前,吉利德的NS5B聚合酶抑制剂sofosbuvir在抗丙肝药物市场上占领绝对地位,其高昂的价格,在一片争议中扶摇直上,成为抗丙肝药物的重磅炸弹。AbbVie丙肝药物的上市,打开了抗丙肝药物市场的新局面,他们正在加紧布局丙肝药物市场,从复方药物抢先上市到单品随后补位,同时化合物专利在药品主流国家都获得授权,并有复方及适应证等外围专利,吉利德同样布局了sofosbuvir的化合物专利及复方,但是其化合物专利被中国专利局驳回(待复审)。
5 Dasabuvir同靶点药物
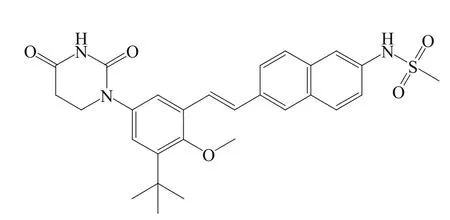
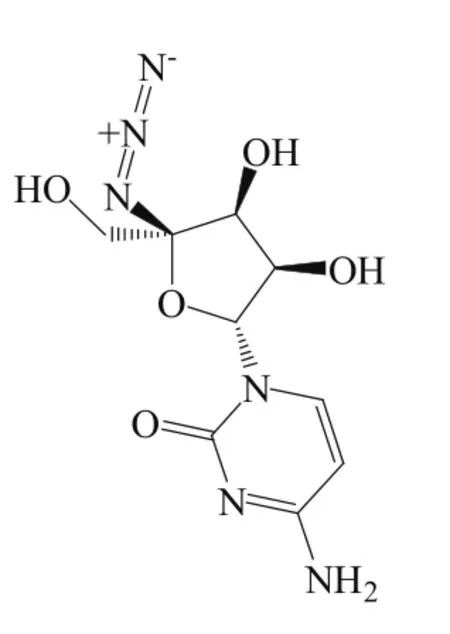
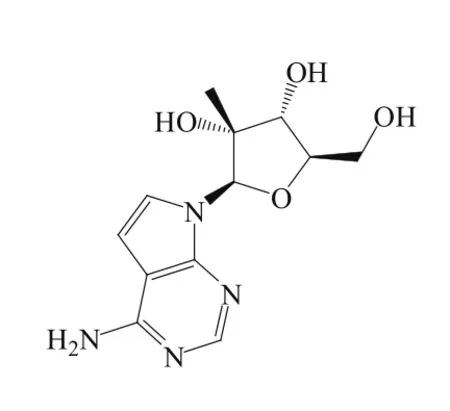
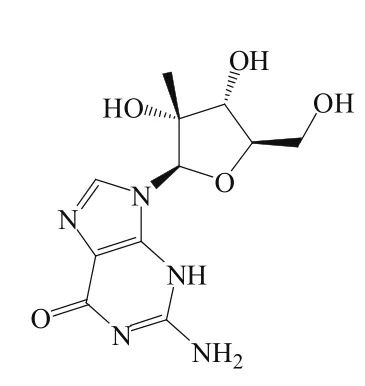
Dasabuvir是继Sofosbuvir上市后的第2个NS5B聚合酶抑制剂。目前还有多个NS5B聚合酶抑制剂处于不同的研发阶段(见表6)。其中,1个药物处于Ⅲ期临床,17个药物处于Ⅱ期临床,5个药物处于Ⅰ期临床。由此可见,丙型肝炎药物市场的竞争将会越来越激烈。
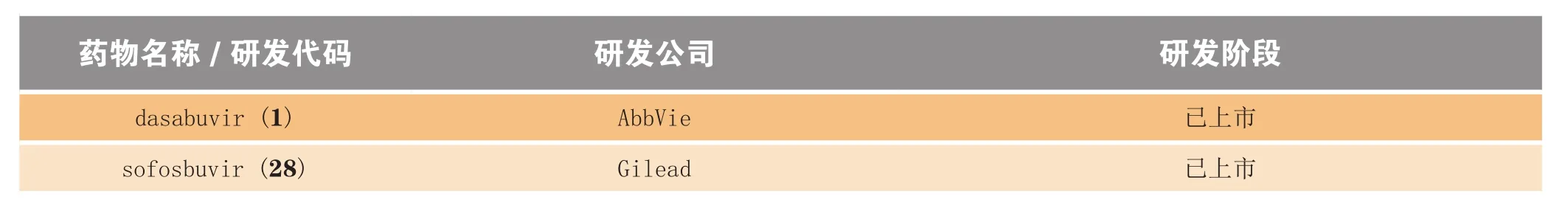
表6 处于不同研发阶段的NS5B聚合酶抑制剂Table 6 NS5B polymerase inhibitors in various development stages
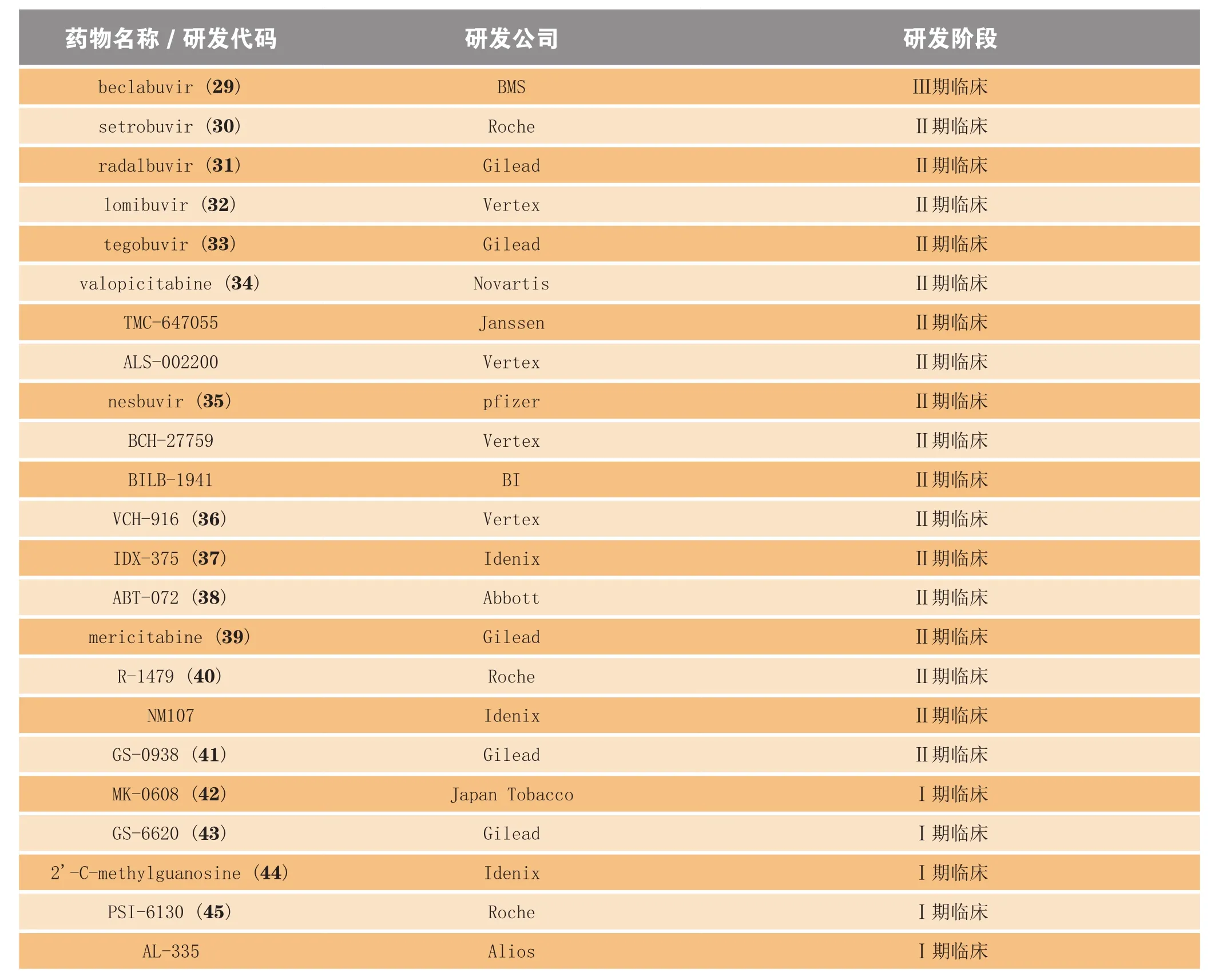
续表6

31

32

33
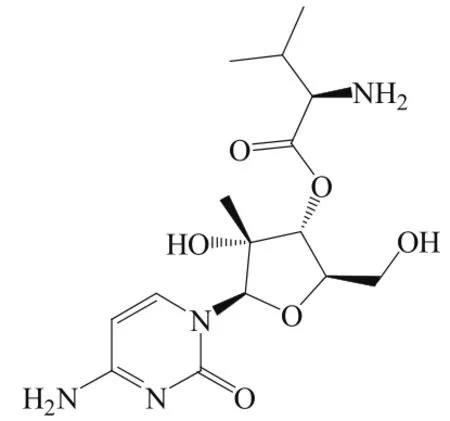
34
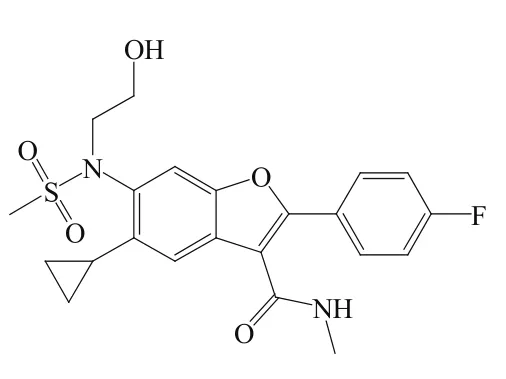
35
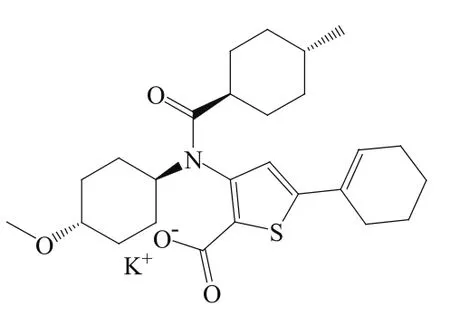
36

37
38

39
40

41
42

43
44
45
6 结语
近年来,以NS5B聚合酶为靶点的抗HCV药物颇受关注。Dasabuvir是继sofosbuvir后的另一种新型非核苷类NS5B聚合酶抑制剂,与其他直接作用于病毒的药物联用治疗基因Ⅰ型慢性丙型肝炎病毒感染。这种无干扰素的联合用药方案在治疗HCV感染上的持续病毒应答率达到90%以上,可单用或与利巴韦林联用,这也给丙肝患者的完全治愈带来了新的希望。
[1]AbbVie Inc.ExvieraTM: EMA human medicineinformation [EB/OL].(2015-02-12) [2015-09-03]. http://www.ema.europa.eu.
[2]AbbVie Inc. Viekira PakTM: US prescribing information [EB/OL]. (2014-12-19) [2015-8-27]. http://www.accessdata.fda.gov.
[3]Flentge C A, Hutchinson D K, Betebenner D A, et al. Anti-infective pyrimidines and uses thereof: WO, 2009039134A1 [P]. 2009-03-26.
[4]Pilot-Matias T, Koev G, Krishnan P,et al. In vitro combinatory effect of HCV NS3/4A protease inhibitor ABT-450, NS5A inhibitor ABT-267 and nonnucleoside NS5B polymerase inhibitor ABT-333 [J]. J Hepatol,2012, 56: S338.
[5]Feld J J, Kowdley K V, Coakley E, et al. Treatment of HCV with ABT-450/r-ombitasvir and dasabuvir with ribavirin [J]. N Engl J Med, 2014,370 (17): 1594-1603.
[6]Zeuzem S, Jacobson I M, Baykal T, et al. Retreatment of HCV with ABT-450/rombitasvir and dasabuvir with ribavirin [J]. N Engl J Med,2014, 370(17): 1604-1614.
Dasabuvir: a New Drug Approved for Hepatitis C Virus
LIU Shu, ZHANG Man, TANG Xiaomei, JIANG Zhi
(Pharmacodia(Beijing) Co., Ltd., Beijing 100085, China)
On Jan 15, 2015, dasabuvir was approved by European Medicines Agency as monotherapy for the treatment of HCV. The drug was also approved by FDA on Dec 19, 2014 as combined therapy (dasabuvir/ombitasvir/paritaprevir/ritonavir) for the treatment of HCV genotype 1. Dasabuvir is a NS5B RNA-dependent RNA polymerase inhibitor, which exerts anti-viral activity by interfering with HCV replication. The chemical synthesis,preclinical pharmacology, clinical trials and patent protection of dasabuvir were summarized in this article, so as to provide
for the R&D of new anti-HCV drugs.
dasabuvir; NS5B polymerase inhibitor; HCV
R978.7
A
1001-5094(2015)09-0712-09
