含氟酰氯类化合物的合成研究进展
2015-11-23王术成王军祥林胜达于万金刘武灿
张 迪,王术成,王军祥,林胜达,于万金,刘武灿
(1.浙江省化工研究院国家ODS替代品工程技术研究中心,浙江杭州310023;2.中化蓝天集团下沙生产基地,浙江杭州310018)
含氟酰氯类化合物的合成研究进展
张 迪1,王术成1,王军祥2,林胜达1,于万金1,刘武灿1
(1.浙江省化工研究院国家ODS替代品工程技术研究中心,浙江杭州310023;2.中化蓝天集团下沙生产基地,浙江杭州310018)
介绍了包括SO3氧化法、光氧化法、催化氧化法和热分解法等含氟酰氯类化合物的合成方法,评述了各种合成方法的优缺点,并对含氟酰氯类化合物的合成发展趋势作出了展望。
氯二氟乙酰氯;二氟乙酰氯;三氟乙酰氯;光氧化;催化氧化
0 前言
含氟酰氯类化合物是一类重要的脂肪族含氟中间体。由于酰氯基团中的氯原子有吸电子效应,并且Cl-也是一个很好的离去基团,因此酰氯具有很强的亲核酰基取代反应活性,可以与氨/胺反应生成酰胺(氨解),与醇反应生成酯(醇解),与羧酸根离子反应生成酸酐等,从而向一些物质中引入特定的含氟基团,合成出一系列医药和农药等精细化学品或其中间体。
氯二氟乙酰氯,分子式为C2Cl2F2O,分子量148.92,CAS号354-24-5,沸点20℃,是一种高度挥发性、带刺激性气味的无色液体,易水解,在空气中会发烟,易溶于有机溶剂。氯二氟乙酰氯及其衍生物可用于合成治疗疟疾和癌症的药物、氟代氮杂环丁酮类抗生素、吡唑甲酰胺类杀菌剂、除草剂等[1-2]。
二氟乙酰氯,分子式为C2HClF2O,分子量114.48,CAS号381-72-6,沸点25℃,主要用于合成二氟乙酸[3]、二氟乙醇[4]等二氟系列产品及其下游衍生物,如二氟吡唑类杀菌剂、二氟代酮类抑制剂[5]。
三氟乙酰氯,分子式为C2ClF3O,分子量132.47,CAS号354-32-5,熔点-146℃,沸点-27℃,是一种有刺激性气味的无色气体,在空气中易水解、易发烟,易溶于有机溶剂。三氟乙酰氯主要用来合成三氟乙酸或其它衍生物,是合成农药和医药的一种重要原料。
1 合成技术进展
含氟酰氯类化合物最早是通过三氯甲苯/氯化锌[6]、苯甲酰氯[7-8]、五氯化磷[9]等与相应的含氟羧酸进行反应制得的。该类方法存在的问题是原料含氟羧酸较难取得。目前,根据反应的特点,可以将含氟酰氯类化合物的合成方法分为SO3氧化法、光氧化法、催化氧化法和热分解法四大类。
1.1 SO3氧化法
1.1.1 以1,1,1,2-四氯-2,2-二氟乙烷为原料制备氯二氟乙酰氯
Haloearbon Prod.专利[10]报道了1,1,1,2-四氯-2,2-二氟乙烷(R112a,CClF2-CCl3)与SO3反应制备一氯二氟乙酰氯的方法。在反应器中加入712 g的Rl12a,3g的HgSO4,3g的Hg2SO4,加热回流,6 h内加入753 g 65%的发烟硫酸,之后继续反应1 h,氯二氟乙酰氯的收率为94%。
Kali-Chemie AG专利[11]同样介绍了通过R112a与SO3反应制备氯二氟乙酰氯的方法,所不同的是以SO2Cl2作为R112a的溶剂。例如,在含有5 mol的SO3、0.4 mol的SO2Cl2、0.25 mol的H2SO4和1 g HgSO4、1 g Hg2SO4催化剂的混合物中,连续通入1.5 mol/h的R112a以及1.8 mol/h的SO3,反应温度50℃,一氯二氟乙酰氯的收率可达到96.3%。

常熟振氟专利[12]介绍了将1,1,2-三氯-2,2-二氟乙烷(R122,CClF2-CHCl2)通过紫外光催化氯化生成R112a,再将R112a催化氧化制备氯二氟乙酰氯的方法。例如,在40℃下加入4230 g的R122,通入600 g/h的Cl2,紫外灯光照下反应3 h,R112a的收率为84.7%;将3155 g制得的R112a滴加入3840 g的SO3与35 g的氯磺酸混合物中,2 h滴完,反应温度控制在50℃,氯二氟乙酰氯的收率为81.3%。
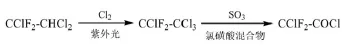
Elf Atochem S.A.专利[13]报道了在氧和化学游离基引发剂存在的条件下使R112a与乙醇反应制备氯二氟乙酸乙酯的方法。在反应器中加入105 g乙醇,150 g含有45 g的R112a的乙醇溶液,加入0.72 g化学游离基引发剂偶氮二异丁腈(AIBN),升温至65℃,搅拌下通入7 L/h空气,反应15 h后R112a转化率为73.4%,氯二氟乙酸乙酯收率为23%。

1.1.2 以1,1-二氟四卤代(含溴/碘)乙烷为原料制备氯二氟乙酰氯
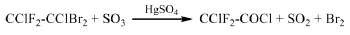
早期德国专利[14]报道了以1,1-二氟-1,2-二氯-2,2-二溴乙烷为原料氧化制备氯二氟乙酰氯的方法。反应温度为50℃,以65%发烟硫酸为氧化剂,在HgSO4的催化下,1,1-二氟-1,2-二氯-2,2-二溴乙烷氧化生成氯二氟乙酰氯,其中Hg-SO4用量为原料的1wt.%,发烟硫酸用量与原料的重量比为1:1,氯二氟乙酰氯的收率为79%。
1.1.3 以1,1,1-三氯三氟乙烷为原料制备三氟乙酰氯
早期Du Pont专利[15]介绍了在汞盐催化下以1,1,1-三氯三氟乙烷(R113a,CF3-CCl3)和SO3为原料制备三氟乙酰氯,再用碱水解、硫酸酸化并蒸出三氟乙酸的方法。各物质的份数比为R113a :SO3:(Hg2SO4+HgSO4)=30:40:0.5。Pennsalt Chemicals专利[16]采用相类似的方法,以汞盐为催化剂,在室温下进行反应,摩尔比为R113a:SO3= 0.23:0.96,反应5 h,再将生成的三氟乙酰氯水解得到三氟乙酸,其中R113a的转化率为74.5%。

Haloearbon Prod.专利[17]报道了R113a与65%发烟硫酸反应制备三氟乙酰氯的方法,催化剂为HgSO4和Hg2SO4。623 g的R113a与3 g的HgSO4、3 g的Hg2SO4混合,在5 h内缓慢加入753 g的65%发烟硫酸,通过蒸馏可以得到399 g的产物三氟乙酰氯,收率为91%。Kali-Chemie Aktiengesellschaft专利[18]同样以HgSO4和Hg2SO4的混合物为催化剂,将R113a与液相SO3、SO2Cl2反应制备三氟乙酰氯。在含有4 mol的SO3、0.5 mol的SO2Cl2、0.25 mol的H2SO4和1 g HgSO4、1 g Hg2SO4催化剂的混合物中通入R113a,反应温度60℃,摩尔比R113a:SO3=1:1~1.3,三氟乙酰氯的收率可达到96%。
浙江大学刘志政[19]研究了R113a和SO3的反应机理:硫酸亚汞(Hg2SO4)加热生成硫酸亚汞自由基(O2S(OH·)2),引发R113a生成三氟二氯乙烷自由基(CF3CCl2)。它和三氧化硫结合生成自由基,然后分解生成三氟乙酰氯和硫酰一氯自由基(·SO2Cl),后者引发R113a从而发生自由基连锁反应。具体反应方程式如下:
(1)自由基链引发

(2)自由基链增长

(3)自由基链终止

研究认为,较优的工艺操作条件为温度65℃、摩尔比SO3:R113a=1.1:1、催化剂(Hg2SO4和HgSO4)的质量分数为1%、硫酸的质量分数为2%,在该条件下三氟乙酰氯的收率可达到93%。
浙江大学专利[20]介绍了R113a和SO3在催化剂氟磺酸汞和氟磺酸亚汞的作用下反应制备三氟乙酰氯,同时将副产物SO2Cl2氟化联产SO2F2的方法。在反应精馏塔中装填已经交换了汞盐和亚汞盐的氟磺酸树脂填料,通入600 mol/h的R113a、600 mol/h的SO3,控制塔釜温度120℃、回流比2.5,从塔顶采出三氟乙酰氯的量为594 mol/h。反应生成的SO2Cl2经分离后,与HF在Pd/C催化剂的作用下反应生成SO2F2。
Kali-Chemie Aktiengesellschaft专利[21]采用较为复杂的催化体系对R113a与SO3进行催化制备三氟乙酰氯。催化剂由汞盐、硼卤化物及卤代磺酸等组成,例如,以2 g的HgSO4、17.5 g的HSO3F、2 g的BF3所组成的混合物作为催化剂,与93.7 g的R113a和162.0 g的SO3反应,反应收率没有报道。
Allied Corporation专利[22]公开了使用卤素催化剂催化R113a和SO3制备三氟乙酰氯的方法,避免使用有毒有害的含汞催化剂。催化剂包括碘、溴、一氯化碘、一溴化碘、一氯化溴,优选溴催化剂。向带有搅拌的三口烧瓶中加入150 g的R113a和7.5 g的溴,室温下30 min内加入145 g的SO3,25℃~60℃反应12 h,R113a的转化率为80%,三氟乙酰氯的选择性为98%。
1.2 光氧化法
1.2.1 以R122为原料制备氯二氟乙酰氯
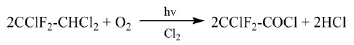
早期Hoechst专利[23]报道了一种在Cl2存在下,在光引发作用下,R122与O2发生光化学氧化连续制备氯二氟乙酰氯的方法。反应温度120~130℃,R122、O2和Cl2的投料速度分别为140 g/h、28 L/h、0.5 L/h,氯二氟乙酰氯的收率约为82.7%。
Solvay专利[24]报道了R122与O2发生光化学氧化反应,连续制备氯二氟乙酰氯的方法。引发光源为高压汞蒸气灯,在温度100℃、摩尔比R122:O2=1:2.2、停留时间30 min的条件下,R122的转化率可达到89%,氯二氟乙酰氯的收率为92.9%,副产物主要为COClX、CO2、COF2。在此基础上,Solvay专利[25]报道了向反应中添加Cl2作为光引发剂,以λ≥280 nm光作为引发光源的方法,在温度100℃、摩尔比R122:O2:Cl2=1:1.4: 0.24、R122进料量为1.82 mol/h的条件下反应,R122的转化率可达到94%,氯二氟乙酰氯的选择性为93%,同时生成少量的R112a。
湖北卓熙专利[26]采用相类似的方法,在高压汞灯下通入R122与O2、Cl2,发生光化学氧化反应得到氯二氟乙酰氯。选用1000 W的高压汞灯作为引发光源,在温度60℃~150℃,摩尔比R122: O2:Cl2=1:0.5:0.35的条件下,氯二氟乙酰氯的收率可达到85%。
1.2.2 以1,1-二氯-2,2-二氟乙烯为原料制备氯二氟乙酰氯
Hoechst专利[29]报道了在紫外灯的照射下,1,1-二氯-2,2-二氟乙烯(R1112a,CF2=CCl2)光氧化制备氯二氟乙酰氯的方法。反应温度120℃~130℃,停留时间9 min,氯二氟乙酰氯的收率为80%。在此基础上,Solvay专利[30]使用高压汞灯作为引发光源,通过入≥280 nm光引发进行R1112a的光氧化反应。在85℃~91℃的温度下,0.6 mol的R1112a与1.0mol的O2、0.11mol的Cl2反应20min,R1112a的转化率达到99.58%,氯二氟乙酰氯的选择性为90.8%。

1.2.3 以1,1-二氯-2,2-二氟乙烷为原料制备二氟乙酰氯
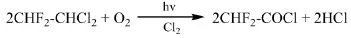
Asahi Glass公司专利JP08053388A[29]介绍了一种以1,1-二氯-2,2-二氟乙烷(R132a,CHF2-CHCl2)为原料光氧化合成二氟乙酰卤及其二氟乙酸酯的制备方法。在80℃条件下,将摩尔比R132a:O2:Cl2=1:3:0.5的混合物用400 W高压汞灯照射5 min,得到二氟乙酰氯,R132a的转化率为99%,二氟乙酰氯选择性为99%。二氟乙酰氯进一步水解可以得到二氟乙酸。
1.2.4 以2,2-二氯-1,1,1-三氟乙烷为原料制备三氟乙酰氯
Haszeldine等[30]提出了气相光氧化1,1,1-三氯三氟乙烷(R113a,CCl3-CF3)、2,2-二氯-1,1,1-三氟乙烷(R123,CF3-CHCl2)、2-氯-1,1,1-三氟乙烷(R133a,CF3-CH2Cl)分别制备三氟乙酰氟、三氟乙酰氯和三氟乙酸的方法,认为通过添加光引发剂Cl2可以大幅提升目标产物的收率。
Pennsalt Chemicals专利[31]描述了通过加热,紫外光、γ光线、X射线或高能电子辐射等方式引发自由基,将含卤乙烷CF2MCXYZ(其中,M=F或Cl,X,Y=H,Cl或Br)氧化生成相应含卤乙酰氯或含卤乙酸的方法。在光引发剂Cl2存在的情况下,采用加热的方式,反应温度优选200℃~250℃;采用紫外光或其它辐射的方式,则反应温度可以在-30℃以下。专利实施例中,在紫外光辐射下,通入摩尔比为R123:O2:Cl2=1:4:2的物料,在2个大气压的条件下反应,R123可达到完全转化,生成的产物中绝大多数为三氟乙酰氯。
Halocarbon Products专利[32]描述了通过紫外灯辐射气相氧化R123制备三氟乙酰氯的方法。将含有2%杂质CFCl2-CF2Cl的R123、O2分别以45.36 kg/h、5.44 kg/h的速率通入反应器中,以2000 W紫外灯作为光源,在温度105℃、压力120 psig(即0.83 MPa)的条件下反应,R123的转化率为95%,三氟乙酰氯的收率可达到99%。
Du Pont专利[33]介绍了在Cl2存在下通过液相氧化R123或者R133a制备三氟乙酰氯的方法。向装满R123的1.6 L玻璃反应器中持续1.5 h通入80 mL/min的O2,接着添加Cl2直至溶液中氯的浓度达到0.0033 mol/L,打开450 W、波长>280 nm的中压汞灯,通入O2、Cl2进行反应,期间O2的流速为80 mL/min,保持溶液中氯的浓度≤0.0035 mol/L,可以获得纯度为99.0%的三氟乙酰氯。研究认为,当辐射光波长≤280 nm,容易导致副产物HF的生成;而在Cl2存在的情况下,使用波长>280 nm的高压或中压汞灯光源,有助于提高反应的选择性,同时可以避免玻璃反应器的腐蚀问题。
Solvay专利[34]报道了R123与氧气发生光氧化反应连续制备三氟乙酰氯的方法。选用700 W的高压汞蒸汽灯作为引发光源,在100℃、摩尔比R123:O2=1:2.28、停留时间30 min的条件下,R123的转化率达到95%,三氟乙酰氯的收率为85%,副产物主要为COCl2、CO2、COF2。在此基础上,Solvay专利[35]报道了向反应中添加Cl2作为光引发剂的方法,选用500 W的高压汞蒸汽灯作为引发光源,通过滤光片滤去λ<280nm的光,在温度100℃、摩尔比R123:O2:Cl2=1:1.23:0.2、R123的进料量为1.92 mol/h的条件下,R123的转化率接近100%,三氟乙酰氯的选择性为100%。

杭州原正化工专利[36]介绍了将三氟乙烷氯化混合物与O2、Cl2在汞灯辐射下进行光氧化反应制备三氟乙酰氯的方法。向反应釜中加入5 L的三氟乙烷氯化混合物(9%的R133a、90%的R123、1%的R113a),搅拌下连续通入500 mL/min的O2、250 mL/min的Cl2,反应温度5℃,压力0.09 MPa,汞灯辐射,共生成10.3 mol的三氟乙酰氯。该公司专利CN101735033A[37]、CN101735034A[38]介绍了在Cl2存在的情况下,R123与O2进行液相光氧化反应制备三氟乙酰氯的方法。为防止生成的三氟乙酰氯被汞灯辐射分解,分别采用了在物料泡点温度或泡点温度以上进行反应,在反应器气液相界面以下加装遮光构件的方法。

1.2.5 以R113a为原料制备三氟乙酰氯
Pennsalt Chemicals专利[39]介绍了以紫外线为引发光源,R113a与O2在Cl2存在的条件下反应制备三氟乙酰氯的方法。当反应中存在水时,生成的三氟乙酰氯进一步反应生成三氟乙酸。例如,将摩尔比为R113a:O2:Cl2=5:2:3的物料在2个大气压的条件下反应72 h,当存在水时,三氟乙酸的收率为50%。
Daikin专利[40]介绍了以紫外线为引发光源,R113a与SO3或发烟硫酸在Br2存在的条件下反应制备三氟乙酰氯的方法。60℃、常压下反应,紫外灯功率为20 W,三氟乙酰氯的收率可达到90.1%。当没有紫外灯照射时,反应产物几乎没有。

1.3 催化氧化法
1.3.1 以1,2-二氯-1,1,2-三氟乙烷为原料制备氯二氟乙酰氯
Asahi Glass专利[41]报道了1,2-二氯-1,1,2-三氟乙烷在少量水的存在下,与O2发生热氧化反应,反应温度优选150℃~500℃,得到CClF2-COCl、CClF2-COF及CClF2-COOH混合物,该混合物与水反应,得到CClF2-COOH。

1.3.2 以R123为原料制备三氟乙酰氯
Asahi Glass专利[42]介绍了在水存在的条件下R123气相氧化制备三氟乙酰氯和三氟乙酸的方法。向反应器中通入R123、O2、H2O,R123的流量为103 mol/h,物料摩尔比R123:O2:H2O=1:1: 0.1,在温度300℃、压力30 kg/cm2、停留时间8.4 min的条件下反应,通过搅拌桨搅拌避免反应器内局部过热,R123的转化率为95%,三氟乙酰氯的选择性为68%,三氟乙酸的选择性为26%。在该反应中,水起到了催化剂的作用,但不可避免地将R123氧化得到的三氟乙酰氯水解生成三氟乙酸,而水与三氟乙酰氯、三氟乙酸分离较为困难。此外,水的含量过高会导致其与氟化氢形成氢氟酸而腐蚀设备。
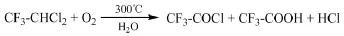
Du Pont专利[43]介绍了通过活性炭催化氧化R123制备三氟乙酰氯的方法。将R123、O2分别以0.10 mL/min、25 mL/min的速率通入装填有活性炭催化剂的反应管,活性炭的比表面积为600~1500 m2/g,反应温度275℃、停留时间16 s,R123的转化率可达到100%,但三氟乙酰氯的选择性仅为39%,其它副产物包括R113a、R13、R23,这可能是由于较高的反应温度导致部分原料中CC键的断裂。
宁丹等[44]以活性炭为催化剂,在连续流动固定床反应器上将R123催化氧化制备三氟乙酰氯。研究认为,反应的转化率和选择性随着活性炭比表面积和孔容增大而增加,活性炭表面的酸性也有助于其催化性能的提高。例如,在比表面积921 m2/g的活性炭催化下,反应温度270℃~280℃,物料摩尔比R123:O2=0.65:1,HCFC-123空速0.55 h-1,三氟乙酰氯最高收率为71.1%。

1.4 热分解法
1.4.1 以1,3-二氯-1,1,3,3-四氟丙酮为原料制备氯二氟乙酰氯
Allied Chemical&Dye专利[45]报道了1,3-二氯-1,1,3,3-四氟丙酮热分解制备氯二氟乙酰氯及四氟乙烯的方法,选择的热解温度范围为500℃~750℃。例如,将原料汽化后通入反应器,流速2.00 mol/h,在675℃、停留时间0.6 s的条件下进行热解,反应转化率为37%,氯二氟乙酰氯的收率为72%。

1.4.2 以1-烷氧基-1,1,2,2-四氟乙烷为原料制备二氟乙酰氯
中央硝子专利[46]介绍了由1-烷氧基-1,1,2,2-四氟乙烷(ATFE)热分解得到的二氟乙酰氟高效率地转变为二氟乙酰氯的方法。首先将ATFE在温度140℃~200℃、反应时间10~300 s的条件下催化热分解生成二氟乙酰氟及氟代烷;将蒸馏得到的二氟乙酰氯通入填充有粒状无水CaCl2的反应管中,反应温度160℃时得到的氯化产物中,二氟乙酰氯的含量为93.7%。

1.5 其它方法
1.5.1 三氟乙醛光氯化制备三氟乙酰氯
Hoechst AG专利[47]介绍了将Cl2通入液相三氟乙醛中,通过光氯化制备三氟乙酰氯的方法。将124份的Cl2通入装有162份三氟乙醛的反应器中,在紫外灯照射下,-30℃进行反应,三氟乙酰氯的收率为87%。此反应过程不易控制,通入Cl2较为危险。
1.5.2 R123超临界氧化制备三氟乙酰氯
Du Pont专利[48]介绍了在超临界状态下氧化R123制备三氟乙酰氯的方法。将41.3 g的R123通入充填有O2,压力为120 psig(即0.83 MPa)的反应器中,在220℃、700 psig(即4.8 MPa)的条件下反应15 min,R123的转化率为90%,三氟乙酰氯的选择性为91%,反应中有副产物HF、三氟乙酸、R113a产生。由于超临界状态下的高温高压对反应器要求苛刻,工业上较难实现,不适合大规模生产。
2 结论与展望
作为一类重要的脂肪族含氟中间体,含氟乙酰氯类化合物的经济价值已日益凸显。其合成技术的选择与发展方向如下:
SO3氧化法的主要优点是可以在较低的反应温度和常压下进行,反应条件比较温和,对设备的要求不是十分苛刻,主要缺点是需采用SO3等危险化学品和有毒的汞盐作催化剂,反应过程中产生的硫酰氯的分离和利用问题也有待解决。
光氧化法,即在紫外光照射下,氯氟烷烃/烯烃和O2在一定温度和压力下反应制得相应的含氟酰氯。该方法反应条件较为温和,在反应中加入少量的卤素化合物,如Cl2、Br2等,可提高反应速度。值得注意的是,光氧化反应器的设计是该方法实现工业化的关键,需避免光照引起的产物分解问题。
催化氧化法需要在高温条件下进行,研究主要集中在水和活性炭两类催化剂。由于会产生氢氟酸的腐蚀问题,在工业生产中采用水催化的氧化反应是不合适的;而开发的活性炭催化剂,则会使反应的副产物较多,仍需进一步研究改进。
热分解法的反应条件较为苛刻,并且需要特定的原料,目前研究相对较少。
[1]徐卫国,陈先进,徐宇威,等.一氯二氟醋酸的合成与应用[J].浙江化工,2004,35(6):20-21.
[2]赵卫娟,徐卫国,刘毓林,等.一氯二氟乙酰氯及其衍生物的制备及应用[J].浙江化工,2013,44(7):1-3.
[3]Ooharu,Kazuya,Kumai,Seisaku.Preparation of difluoroacetyl halides and difluoroacetic acid:JP,08053388[P]. 1996-12-27.
[4]Olivier B,Roland J.Production of difluoroethanol:US, 7902409B2[P].2011-03-08.
[5]陈伟,徐卫国,李华,等.二氟醋酸的合成方法研究[J].有机氟工业,2014,(1):43-46.
[6]Gryszkiewicz-Trochimowski M E,Sporzyn?ski A,Wnuk J.Recherches sur les Composés Organiques Fluorés dans la Série Aliphatique:II.Sur les dérivés des acides mono-, di-et tri-fluoro-acétiques[J].Recueil des Travaux Chimiques des Pays Bas,1947,66(7):419-426.
[7]Tinker J M.Trifluoroacetyl halide and a process of making it:US,2257868[P].1941-10-07.
[8]Henne A L.Alm R M,Smook M.Trifluoroethanol[J].J. Am.Chem.Soc.,1948,70(5):1968.
[9]Saunders J H,Slocombe R J,Hardy E E.The preparation of α-trifluoro-p-phenylacetophenone[J].J.Am.Chem. Soc.,1949,71(2):752.
[10]Dittman A L,Zager R I.Preparation of perfluoro-and perchlorofuoro-acetyl chloride:US,3160659[P].1964-12-08.
[11]Paucksch H,Massonne J,Bohm H,et al.Process of preparing fluorine containing perhalogencarboxylic acid fluorides or chlorides:US,3725475[P].1973-04-03.
[12]沈达.一种三氟乙酸的制备方法:CN,103524325[P]. 2014-01-22.
[13]Drivon G.,Gillet J P,Ruppin C,et al.Process for the preparation of alkyl halodifluoroaceates:US,5619023[P]. 1997-04-08.
[14]Dieter G.Verfahren zur herstellung von perhalogencarbonsaurefluoriden order-chloriden,deren halogengehalt zu mehr als 50 molprozent aus fluor besteht:DE,1020970B [P].1957-12-19.
[15]Benning A F,Park J D.Preparation of trifluoro acetic acid: US,2396076[P].1946-05-05.
[16]Lawlor F E,Braid M.Oxidation process for preparing car-boxylic acid anhydrides:US,3102139[P].1963-08-27.
[17]Dittman A L,Zager R I.Preparation of perfluoro-and perchlorofuoro-acetyl chloride:US,3160659[P].1964-12-08.
[18]Paucksch H,Massonne J,Bohm H,et al.Process of preparing fluorine containing perhalogencarboxylic acid fluorides or chlorides:US,3725475[P].1973-04-03.
[19]刘志政.CF3CCl3衍生物的合成及反应机理研究[D].杭州:浙江大学,2012.
[20]尹红,袁慎峰,陈志荣,等.一种连续合成三氟乙酰氯和硫酰氟的方法:CN,102351681A[P].2012-02-15.
[21]Rudolph W,Fernschild G,Hirsch W.Process for preparing trifluoracetylchlorid:EP,0029591A1[P].1980-11-21.
[22]Anello L G,Eibeck R E,Robinson M A.Process for the preparation of perhaloalkanoyl chloride:US,4340548[P]. 1982-07-20.
[23]Otto S,Heinrich K,Heinrich M.Verfahren zur herstellungvon fluor und chlor enthahenden essigssaure chloride: DE,1069137[P].1958-01-10.
[24]Braun M,Rudolph W,Einchholz K.Process for preparing polyfluorocarboxylic acid chlorides and perfluotocarboxylic acid chlorides:US,5545298[P].1996-08-13.
[25]Braun M,Rudolph W,Einchholz K.Process for preparing polyfluorochlorocarbonyl chlorides and perfluorocarbonyl chlorides with addition of chlorine:US,5569782[P].1996-10-29.
[26]谢学归,张雨寒.一种一氯二氟乙酰氯的制备方法:CN, 103351292A[P].2013-10-16.
[27]Otto S,Heinrich K,Heinrich M.Verfahren zur herstellung von fluor und chlor enthahenden essigssaure chloride:DE, 1069137[P].1958-1-10.
[28]Braun M,Rudolph W,Eichholz K.Difluorochloracetyl, dichloracetyl and trichloracetyl chloride preparation:US, 5919341[P].1999-07-06.
[29]Oharu K,Kumai S.Production of difluoroacetic acid halide and difluoroacetic acid:JP,08053388A[P].1996-02-27.
[30]Haszeldine R N,Nyman F.Oxidation of polyhalogenocompounds.PartⅡ.Photolysis and photochemical oxidation of some chlorofluoroethanes[J].J.Chem.Soc.,1959, 387-396.
[31]Braid M,Lawlor F.Synthesis of fluorine compounds:US, 3151051[P].1964-09-29.
[32]Dittman A L.Production of 2,2,2-trifluoroacetyl chloride: US,3883407[P].1975-05-13.
[33]Huang H N.Process for omega-halo-perfluoro acid chlorides:US,5259938[P].1993-11-09.
[34]Braun M,Rudolph W,Einchholz K.Process for preparing polyfluorocarboxylic acid chlorides and perfluotocarboxylic acid chlorides:US,5545298[P].1996-08-13.
[35]Braun M,Rudolph W,Einchholz K.Process for preparing polyfluorochlorocarbonyl chlorides and perfluorocarbonyl chlorides with addition of chlorine:US,5569782[P].1996-10-29.
[36]赵建明,韩箴贤,崔觉剑.一种由三氟乙烷氯化混合物制备三氟乙酰氯的方法:CN,101747176A[P].2009-12-24.
[37赵建明,韩箴贤,崔觉剑.一种由2,2-二氯-1,1,1-三氟乙烷制备三氟乙酰氯的方法:CN,101735033A[P].2009-12-18.
[38]赵建明,韩箴贤,崔觉剑.一种三氟乙酰氯的制备方法: CN,101735034A[P].2009-12-18.
[39]Braid M,Lawlor F.Synthesis of fluorine compounds:US, 3151051[P].1964-09-29.
[40]Yoshida T,Kanetani T,Misaki S.Preparation of perhalogenoalkanoic acid chloride:JP,60237040A[P].1984-05-09.
[41]Kumai S,Seki T.Production of chlorodifluoroacetic acid: JP,6239792A[P].1994-08-30.
[42]Gotoh I,Yoneda H,Kumai S,et al.Process for producing trifluoroaceticacidandtrifluoroacetylchloride:US, 5041647[P].1991-08-20.
[43]Jacobson S E.Process for producing trifluoroacetyl chloride:US,5241113[P].1993-08-31.
[44]宁丹,黄晴,吴银登,等.活性炭在催化氧化三氟二氯乙烷制备三氟乙酰氯中的应用[J].工业催化,2007,15(2): 62-64.
[45]Miller C B,Cyril W.Manufacture of fluorochloroacetyl halide:US,2741634[P].1956-04-10.
[46]冈本正宗,井村英明,高田直门.二氟乙酰氯的制造方法: CN,102822134A[P].2012-12-12.
[47]Scherer O,Hahn H.Process for preparing trifluoroacetyl chloride:US,3320142[P].1967-05-16.
[48]Jacobson S E,Ely W B.Process for preparing perhaloacyl chlorides:US,5296640[P].1994-03-22.
Research Progress in the Synthesis of Fluorinated Acyl Chlorides
ZHANG Di1,WANG Shu-cheng1,WANG Jun-xiang2,LIN Sheng-da1,YU Wan-jin1,LIU Wu-can1
(1.Zhejiang Chemical Industry Research Institute,The National ODS Substitutes Engineering&Technology Research Center,Hangzhou,Zhejiang 310023,China;2.Xiasha Production Base of Sinochem Lantian Co.,Ltd.,Hangzhou,Zhejiang 310018,China)
Several methods for the synthesis of fluorinated acyl chlorides,include SO3-oxidation,photooxidation,catalytic oxidation,thermal decomposition and so on,were introduced and compared.Furthermore, the synthetic trend of fluorinated acyl chlorides was considered.
chlorodifluoroacetyl chloride;2,2-difluoroacetyl chloride;trifluoroacetyl chloride;photo-oxidation;catalytic oxidation
1006-4184(2015)2-0005-07
2014-05-07
张迪(1986-),女,硕士,工程师,2011年7月毕业于浙江工业大学,目前主要从事氟化催化剂及ODS替代品方面的研究。E-mail:zhangdi1@sinochem.com。
