卒中后认知损害的危险因素分析
2015-11-18牛晓波
牛晓波
(安阳市灯塔医院 神经内科 河南 安阳 455000)
卒中后认知损害(post-stroke cognitive impairment,PSCI)是近年来提出的新概念。PSCI会严重影响患者的身体健康和生存质量,给家庭和社会增加了负担,同时也是导致老年人认知损害的主要原因[1]。本研究目的在于统计PSCI的发生率和危险因素,以期通过有效干预危险因素,为早期预防,及时治疗提供临床证据。
1 资料与方法
1.1 一般资料
1.1.1 研究对象 选择2013年9月至2014年6月安阳市灯塔医院神经内科收治的符合标准的急性脑卒中患者152例。
1.1.2 纳入标准 ①卒中的诊断符合全国第四届脑血管病学术会议修订的“各类脑血管病诊断要点”[2],并经至少1次CT或MRI证实;②卒中的类型包括各种亚型的缺血性脑梗死、脑出血及蛛网膜下腔出血;③接受随访,签署知情同意书。
1.1.3 排除标准 ①IQCODE问卷调查高于57分者;②失语及视听觉障碍,不能配合完成认知调查者;③病情不稳定或存在严重的并发症者;④既往有精神疾病或存在营养代谢障碍、脑外伤、颅内占位、中毒及感染性疾病等影响认知功能的疾病史者。
1.1.4 分组方法 所有研究对象均在发病3个月后行蒙特利尔认知评估量表[3](Montreal cognitive assessment,MoCA)评分,总分<26分为认知损害组,≥26分为认知正常组。
1.2 研究方法
1.2.1 设计调查表 内容包括:①人口学资料:年龄、性别、受教育程度(受教育年限≤6 a为低教育水平)、职业(脑力劳动为主/体力劳动为主);②可能的血管性危险因素:高血压、糖尿病、血脂异常、吸烟、房颤、长期饮酒;③卒中临床特征相关因素:卒中类型(缺血性/出血性)、卒中复发、病变部位(额叶、颞叶、丘脑及基底节为关键部位,顶枕叶、小脑、脑干为非关键部位)、3个月后美国国立卫生研究院卒中量表(National Institute of Health stroke scale,NIHSS)评分、3个月后改良Ranking量表(modified ranking scale,MRS)评分。
1.2.2 认知功能检查 所有患者入院后对患者家属进行IQCODE问卷调查,以高于57分表示有卒中前认知损害,拒绝纳入。认知功能的评价采用中文版Mo-CA量表,评价患者发病3月后MoCA评分。以总分<26分为有认知功能障碍,如受教育年限<12 a,则测试评分加1分,如为文盲加2分,以校正教育偏差。
1.3 统计学方法 应用SPSS 20.0统计软件包进行统计学分析,定量资料以(±s)表示,组间比较采用t检验,定性资料的组间比较采用χ2检验,将卒中后认知损害患者与认知功能正常患者进行单因素分析,单因素分析中差异有统计学意义的变量均被纳入Logistic回归分析,采用Enter全变量模型。P<0.05为差异有统计学意义。
2 结果
2.1 卒中后认知损害的发生率 152例卒中患者中,发生认知损害78例,发生率为51.3%。
2.2 人口学因素 两组患者年龄、性别、受教育程度、职业类型因素比较,差异均有统计学意义(P<0.05)。见表1。

表1 两组患者人口学因素比较
2.3 血管性危险因素 两组患者高血压、糖尿病、血脂异常、房颤、吸烟及长期饮酒因素比较,差异均有统计学意义(P<0.05)。见表2。
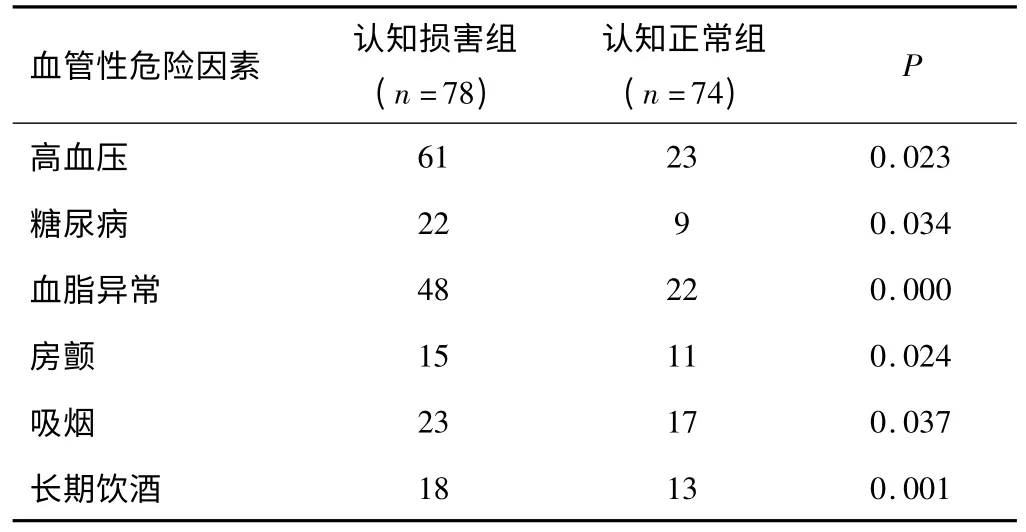
表2 两组患者血管性危险因素比较(n)
2.4 卒中临床特征 两组患者卒中复发、关键部位病变、神经功能缺损(NIHSS)及日常生活能力(MRS)因素比较,差异均有统计学意义(P<0.05);而两组卒中类型比较,差异无统计学意义(P<0.05)。见表3。
2.5 卒中后认知损害的多因素分析 将上述两组差异有统计学意义的因素纳入Logistic回归分析,结果显示年龄、低教育程度、体力劳动为主、糖尿病、长期饮酒、卒中复发、关键部位病变、神经功能缺损严重及日常生活能力低下是独立的危险因素。见表4。

表3 两组患者卒中临床特征因素比较

表4 脑卒中后认知损害多因素Logistic回归分析
3 讨论
目前,有明确的证据表明卒中可导致认知障碍。在过去,学者将卒中后痴呆定义为血管性痴呆[4]。但在临床实践中不是所有的卒中后认知水平下降的患者都符合血管性痴呆的诊断标准,因此“血管性认知损害”(vascular cognitive impairment,VCI)代替了血管性痴呆的概念。然而越来越多的证据表明,卒中后认知损害的发病机制中不仅包括血管性认知损害因素而且有类似阿尔茨海默病(Alzheimer’s disease,AD)机制神经退行性变的因素[5],因此PSCI概念应运而生。基于既往研究的结果,本次研究在传统脑血管病危险因素基础上,加入了人口学特征及卒中临床特征的危险因素,探讨其与PSCI的相关性。
此次研究通过检索Pubmed了解到目前文献报道PSCI发生率存在较大差异,以卒中后3个月评价认知损害水平为截点,欧美国家PSCI发生率为24.0%~47.3%[6-7],亚洲国家PSCI发生率为20.0% ~69.8%[8-9],国内文献报道长沙地区PSCI发生率为41.8%[10]。本研究发现PSCI发生率为51.3%,分析各研究发生率不同的原因可能是种族、生活方式及采用的评价认知损害评分标准不同造成的。
本研究单因素分析表明高龄、男性、低教育水平、体力劳动为主、高血压、糖尿病、血脂异常、房颤、吸烟、长期饮酒、卒中复发、关键部位病变、神经功能缺损严重及日常生活能力差等因素存在统计学意义,均为PSCI可能的危险因素,而卒中类型被单因素分析排除,表明卒中类型与PSCI无关。将以上可能的危险因素作为自变量引入Logistic多因素回归分析,结果提示年龄、低教育程度、体力劳动为主、糖尿病、长期饮酒、卒中复发、关键部位病变、神经功能缺损严重及日常生活能力低下为卒中后认知损害的独立危险因素,而性别、高血压、血脂异常、房颤、吸烟等因素被回归分析所剔除。分析原因可能为性别、高血压、血脂异常、房颤、吸烟等因素在导致PSCI发病机制中存在交互作用。年龄作为PSCI的危险因素,提示PSCI应为血管因素及退行性因素共同作用的结果。人口学因素中低教育程度及体力劳动为主也是PSCI的危险因素,在入选的患者中,低教育程度与体力劳动为主存在一致性,低教育程度患者其智力储备较少,认知功能受损害后代偿能力有限,且低教育程度患者往往从事体力劳动,其生活习惯、健康行为形成率及脑卒中危险因素等方面均不如高教育程度及脑力劳动者。大量证据表明糖尿病、高血压及血脂异常是经典的脑血管病危险因素,其有着相似的血管损害机制,可导致动脉粥样硬化闭塞及微小动脉瘤形成,本研究发现糖尿病亦为PSCI危险因素,而高血压及血脂异常却被回归分析拒绝,分析原因应为糖尿病作为PSCI危险因素其发病机制应存在血管因素以外的作用所致,Duinkerken等[11]报道,糖化血红蛋白水平与认知功能呈负相关,血糖浓度的变化会导致大脑神经元渗透压的改变,神经元变性坏死,出现认知功能损害。研究表明在记忆和认知功能中起重要作用的大脑齿状回及海马区有大量胰岛素受体分布,胰岛素抵抗和高胰岛素血症可使血清肿瘤坏死因子(TNF)-α、α1抗糜蛋白酶、C-反应蛋白(CRP)及白介素-6(IL-6)等炎性因子浓度升高,继发炎性反应导致上述核心区域出现阿尔茨海默病(Alzheimer’s disease,AD)特征性改变如老年斑和神经纤维缠结[12],出现认知损害。长期饮酒为PSCI的危险因素,Randall-James等[13]研究发现酒精通过N-甲基-D-天(门)冬氨酸(NMDA)受体介导,产生钙离子超载,导致细胞毒性作用,引发谷氨酸能神经元受损,而额叶及海马区有着丰富的谷氨酸能神经元分布,其对神经毒性作用耐受极低,易发生认知损害。其他诸如硫胺缺乏、乙醛毒性、自由基、乙酰胆碱受体、5-羟色胺受体、多巴胺受体、γ-氨基丁酸(GABA)受体等均起到协同作用导致认知障碍[14]。
本研究发现在认知损害组3个月内卒中复发率为15.4%,而认知正常组为4.1%,说明卒中复发必将导致脑内神经元损伤,进一步增加认知障碍风险。Gong等[15]研究发现认知损害在很大程度上与病变部位相关,本研究借鉴其研究内容,将额叶、颞叶、丘脑、基底节区病变定义为关键部位病变,顶枕叶、脑干、小脑为非关键部位。多因素回归分析提示关键部位病变为重要的危险因素。额叶、颞叶病变更易破坏与学习、记忆、情感、语言相关的神经递质皮层下环路及相应的高级智能中枢,阻断了与认知密切相关的乙酰胆碱及其他单胺类递质如去甲肾上腺素(NE)和5-羟色胺(5-HT)的传递;额叶-纹状体-苍白球-丘脑-皮质回路参与了执行功能、注意和情感的调节;丘脑中网状结构、板内核团、前部核团、背外侧核、背内侧核团等均是认知的重要结构,其与大脑边缘系统亦存在广泛的神经纤维联系。以上解剖功能结构决定了关键部位病变成为PSCI的重要危险因素的原因。NIHSS评分分析具体的得分项目主要差别为认知损害组在定向、语言及忽略项目上的得分明显高于认知正常组,与Cumming等[16]研究结果相似,同时根据脑解剖结构的功能定位提示主要的差别项目多数为关键部位病变所致,与卒中病变部位存在一定联系。MRS评分升高,提示患者日常生活能力下降,患者丧失了社会能力甚至独立能力,与外界接触减少,信息量下降,大脑学习活动减少,甚至产生消极厌世情绪、焦虑抑郁等,进一步加重了认知损害。
综上所述,本研究发现卒中后3个月认知损害的发生率为51.3%,卒中后认知损害是血管性危险因素与神经退行性变共同作用所致,年龄、低教育程度、体力劳动为主、糖尿病、长期饮酒、卒中复发、关键部位病变、神经功能缺损严重及日常生活能力低下均为PSCI的独立危险因素,通过提高国民教育水平、戒酒、控制糖尿病、积极开展卒中一级预防及卒中后康复治疗对降低PSCI发生率具有重要临床意义。
[1]Sun JH,Tan L,Yu J T.Post-stroke cognitive impairment:epidemiology,mechanisms and management[J].Ann Transl Med,2014,2(8):80.
[2]中华神经科学会,中华神经外科学会.各类脑血管疾病诊断要点[J].中华神经科杂志,1996,29(6):379-380.
[3]Yu K,Zhang S,Wang Q,et al.Development of a computerized tool for the chinese version of the montreal cognitive assessment for screening mild cognitive impairment[J].Int Psychogeriatr,2014,11(3):1-7.
[4]Liebetrau M,Hamann G F.Vascular dementia[J].Fortschr Neurol Psychiatr,2014,82(12):707-718,719-720.
[5]Sun J H,Tan L,Yu J T.Post-stroke cognitive impairment:epidemiology,mechanisms and management[J].Ann Transl Med,2014,2(8):80.
[6]Douiri A,Rudd A G,Wolfe C D.Prevalence of poststroke cognitive impairment:South London Stroke Register 1995-2010[J].Stroke,2013,44(1):138-145.
[7]Jacquin A,Binquet C,Rouaud O,et al.Post-stroke cognitive impairment:high prevalence and determining factors in a cohort of mild stroke[J].JAlzheimers Dis,2014,40(4):1029-1038.
[8]Das S,Paul N,Hazra A,et al.Cognitive dysfunction in stroke survivors:a community-based prospective study from Kolkata,India[J].J Stroke Cerebrovasc Dis,2013,22(8):1233-1242.
[9]Yu K H,Cho SJ,Oh M S,et al.Cognitive impairment evaluated with Vascular Cognitive Impairment Harmonization Standards in a multicenter prospective stroke cohort in Korea[J].Stroke,2013,44(3):786-788.
[10]Tu Q,Ding B,Yang X,et al.The current situation on vascular cognitive impairment after ischemic stroke in Changsha[J].Arch Gerontol Geriatr,2014,58(2):236-247.
[11]Duinkerken E,Brands A M,van den Berg E,et al.Cognition in older patients with type 1 diabetes mellitus:a longitudinal study[J].J Am Geriatr Soc,2011,59(3):563-565.
[12]Clark I,Atwood C,Bowen R,et al.Tumor necrosis factor-induced cerebral insulin resistance in Alzheimer’s disease links numerous treatment rationales[J].Pharmacol Rev,2012,64(4):1004-1026.
[13]Randall-James J,Wadd S,Edwards K,et al.Alcohol screening in people with cognitive impairment:an exploratory study[J].JDual Diagn,2015,11(1):65-74.
[14]Kim JW,Lee D Y,Lee B C,et al.Alcohol and cognition in the elderly:a review[J].Psychiatry Investig,2012,9(1):8-16.
[15]Gong W P,Ding M P,Guo QH,et al.A comparison study on cognitive function in patients with single subcortical lesion stroke of four different areas[J].Zhonghua Yi Xue Za Zhi,2011,91(27):1904-1908.
[16]Cumming T B,Blomstrand C,Bernhardt J,et al.The NIH stroke scale can establish cognitive function after stroke[J].Cerebrovasc Dis,2010,30(1):7-14.
