AR在不同类型乳腺癌中的表达及临床意义
2015-11-18王承正袁鹏杨晗昭谢天
王承正 袁鹏 杨晗昭 谢天
(河南省肿瘤医院 乳腺科 河南 郑州 450003)
乳腺癌是一种激素依赖性肿瘤,雄激素受体在乳腺癌中普遍表达,与乳腺癌的发生、发展具有重要作用[1]。目前分子分型已经成为乳腺癌治疗的依据及靶点,本研究主要探讨雄性激素在不同类型乳腺癌中的表达及预后关系。
1 资料与方法
1.1 一般资料 选取河南省肿瘤医院2014 年1 月至2015 年1 月收治的早期可手术乳腺癌患者200 例,均为女性,中位年龄49.5 岁(23 ~75 岁),所有患者均为可手术的病理确诊的浸润性导管癌,术前未行新辅助化疗及内分泌治疗,免疫组化及Fish 检测明确病理分型,其中Lumina A、Lumina B、Her -2 型及TNB各为50 例。
1.2 检测方法 采用Envision 两步法完成免疫组化染色,检测AR 的表达情况。本研究所用的单克隆抗体和检测试剂盒均购自北京中杉金桥公司。
1.3 AR 判定标准 以细胞核内出现棕黄色颗粒为阳性表达,按阳性细胞数定量,每个标本随机取10 个高倍视野,AR 表达每个高倍视野下平均细胞数>10%为阳性。
1.4 统计学方法 采用SPSS 17.0 软件进行数据处理,采用χ2检验,P <0.05 为差异统计学意义。
2 结果
AR 在Lumina A、Lumina B、Her -2 及TNB 乳腺癌中 的 阳 性 率 分 别 为94. 0%、86. 0%、76. 0%、18.0%。Lumina、Her -2 与TNB 3 组间AR 阳性率差异有统计学意义(P <0.05),而Lumina A 与Lumina B两间差异无统计学意义(P >0.05)。见表1。
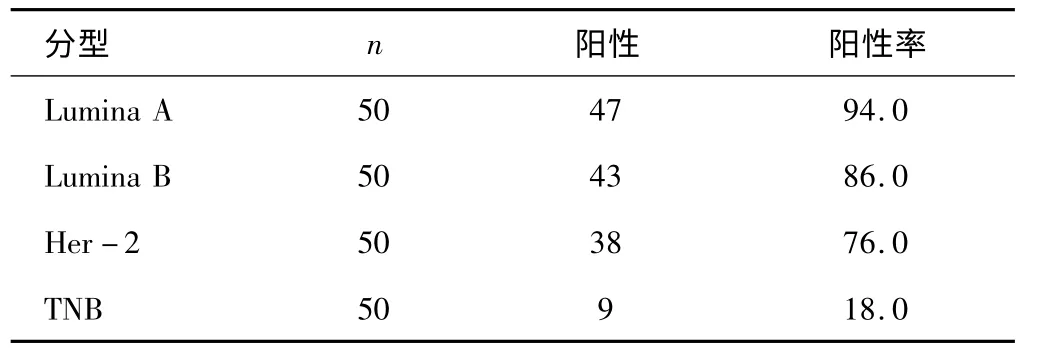
表1 AR 在不同分型乳腺癌中的表达(n,%)
3 讨论
乳腺癌是一种激素依赖性的异质性肿瘤,2000 年由Perou[2]提出的乳腺癌分子分型已经成为研究的热点和治疗的靶点。近年研究显示,AR 也成为划分乳腺癌分子分型的重要指标之一,Guedj 等[3]联合应用AR、ER 和细胞周期调控基因将乳腺癌分为6 个亚型。AR 是一种细胞内(可能细胞核内)蛋白质,以高亲和性和低能量结合活化的雄激素(5α -双羟睾丸酮);激素-受体复合物能与特异的DNA 序列(雄激素反应成分,AREs)相互作用来调节靶细胞的雄激素特异反应基因表达[4],AR 还可通过生长因子MAPK-ER/PR信号通路参与乳腺的发育,并调节乳腺癌细胞的增殖[5]。Macedo 等[6]研究发现雄激素可以通过AR 直接抑制肿瘤细胞的生长。AR 在不同激素状态的乳腺癌中作用不同,雄激素一方面能直接或与雌激素协同刺激乳腺癌细胞的生长,另一方面也可通过间接转化为雌激素的途径发挥其作用。
众所周知,Her-2 在乳腺癌浸润性型乳腺癌中有20% ~30%的表达[7],是临床重要的预后因素,通常表示不良的预后及较高的恶性度。对于AR 和Her -2之间的是否相关有着不同的结论。而三阴性乳腺癌,免疫组化表现为雌激素受体、孕激素受体、人类表皮生长因子均表达阴性,其发病年龄早、侵袭程度高、容易局部复发和远处转移、缺乏有效的内分泌治疗和分子靶向治疗手段、预后差[8-9],目前唯一的治疗手段就是化疗。Lehmann 等[10]根据基因表达谱数据将TNBC进一步分为6 个亚型,其中AR 亚型以检测AR 信号高表达为特征,对于内分泌治疗及靶向治疗缺乏敏感性的TNBC,AR 的研究可能会使此类患者得到更好的治疗。Lumina 作为雌激素受体阳性乳腺癌,往往有较好的预后,尤其是Lumina A 型乳腺癌。但是雄激素与不同类型的乳腺癌的关系尚缺乏研究。目前研究显示,AR 激素在乳腺癌中表达率为30% ~90%,但在不同类型乳腺癌中阳性率差异较大[11],并且AR 阳性与较低的增值活性、组织学分级和淋巴结数目有关。在乳腺癌中,AR 是一个重要的预后指标。本研究显示AR 在Lumina A、Lumina B、Her -2 及TNB 乳腺癌中的阳性率分别为94.0%、86.0%、76.0%、18.0%。这提示AR 的表达可能与乳腺癌的恶性程度及预后有密切关系。
目前研究显示,AR 阳性表达可能是预后良好的重要独立指标,尤其是在TNB 中的阳性表达,可能成为三阴性乳腺癌治疗的新靶点,但是对于AR 表达与不同类型乳腺癌的关系尚需大量研究。
[1]Higgins M J,Wolff A C.The androgen receptor in breast cancer:learning from the past[J]. Breast Cancer Res Treat,2010,124(3):619 -621.
[2]Perou C M,Sorlie T,Eisen M B,et al. Molecular portraits of human breast tumors[J].Nature,2000,406(6797):747.
[3]Guedj M,Marisa L,de Reynies A,et al.A refined molecular taxonomy of breast cancer[J].Oncogene,2012,31(9):1196 -1206.
[4]Kawashima H,Takano H,Sugita S,et al.A novel steroid receptor coactivator protein(SRAP)as an alternative form of steroid receptor RNA-activator gene:expression in prostate cancer cells and enhancement of androgen receptor activity[J]. Biochem J,2003,369(Pt1):163 -171.
[5]Hardin C,Pommier R,Calhoun K,et al. A new hormonal therapy for estrogen receptor- negative breast cancer[J]. World J Surg,2007,31(5):1041 -1046.
[6]Macedo L F,Guo Z,Tilghman S L,et al.Role of anderogens on MCF-7 breast cancer cell growth and on the inhibitory effect of letrozole[J].Cancer Res,2006,66(15):7775-7782.
[7]Agrawal A K,Jeleń M,Grzebieniak Z,et al. Androgen receptors as a prognostic and predictive factor in breast cancer[J].Folia Histochem Cytobiol,2008,46(3):269 -276.
[8]Gerson Ralban F,Villalobos A,et al.Recurrence and survival rates among early breast cancer cases with triple negative immunophenotype[J].Gac Med Mex,2008,144(1):27-34.
[9]Mise M,Higashide S,Hashimoto K,et al. Clinicopathological features of young patients with triple negative breast cancer[J]. Gan To Kagaku Ryoho,2009,36(10):1677 -1681.
[10]Lehmann B D,Bauer J A,Chen X,et al.Identification of human triplenegative breast cancer subtypes and preclinical models for selection of targeted therapies[J].J Clin Invest,2011,121(7):2750-2767.
[11]Liva C,Dainese E,Caprara G,et al.Immunohistochemical study of androgen receptors in breast carcinoma. Evidence of their frequent expression in lubrlar carcinoma[J]. Virchows Arch,2005,447(4):695 -700.
