高分级脑胶质瘤术后残留灶同步放化疗的治疗体会
2015-10-28王洪林陈剑朱虹夏怡肖锋李永春陶
王洪林陈 剑朱 虹夏 怡肖 锋李永春陶 莉
(1 复旦大学附属肿瘤医院闵行分院放疗科,上海 200240;2 复旦大学附属肿瘤医院闵行分院化疗科,上海 200240)
高分级脑胶质瘤术后残留灶同步放化疗的治疗体会
王洪林1陈 剑1朱 虹1夏 怡1肖 锋1李永春1陶 莉2
(1 复旦大学附属肿瘤医院闵行分院放疗科,上海 200240;2 复旦大学附属肿瘤医院闵行分院化疗科,上海 200240)
目的 应用MRI模拟定位、适形调强放疗并同步化疗干预高分级脑胶质瘤术后残留,评价疗效和并发症。方法 高分级脑胶质瘤术后患者,共41例,MRI模拟定位后予同步放化疗。放疗方案:适型调强放射治疗,1.8~2 Gy/(次•d),5次/周,总剂量50~60 Gy/25~33次;3~9个照射野。同步化疗方案:替莫唑胺75 mg/(m2•d),放疗开始即同步使用。放疗后的辅助化疗:第1个疗程替莫唑胺150 mg/(m2•d),第2疗程起200 mg/(m2•d),连续5 d,28 d为1个疗程。治疗每3个月评价1次疗效。结果 治疗后评价为1、2、3、4和5年生存率分别为78.38%、56.76%、29.73%、13.51%和5.41%。Cox比例风险回归模型分析显示:肿瘤病理分级、放疗剂量、辅助化疗疗程对OS有影响。结论 适形调强放疗和同步化学治疗高分级脑胶质瘤术后残留,疗效较好,不良反应和并发症少
适形调强放射治疗;化学治疗;高分级脑胶质瘤
恶性胶质瘤是常见的原发于脑的恶性肿瘤中发病率最高肿瘤之一[1]。因位处中枢神经系统,且有浸润性生长等生物学特点,绝大部分无法经手术完全切除,术后需要放化疗。MRI扫描与CT相比对胶质瘤残留显示优势较为明显。适形调强放疗对肿瘤靶区剂量有所提高,周围正常组织剂量显著降低,从而提高肿瘤局部控制率,提高治疗增益比[2],放疗中同步替莫唑胺化疗,可以提高疗效。我院2004年12月至2010年11月共对高分级脑胶质瘤患者术后明确有残留灶41病例,给予了MRI模拟定位引导下的适形调强放疗和同步化疗,现作如下报道。
1 资料与方法
1.1临床资料:41例高分级脑胶质瘤术后MRI检查明确有肿瘤残留(GTV)患者,男23例,女18例。中位年龄52岁。全部经病例病理学明确诊断为胶质瘤Ⅲ级(16例)或Ⅳ级(25例)(Ⅲ级包括Ⅱ~Ⅲ级,IV级包括Ⅲ~Ⅳ级),病灶位于大脑颞叶、额叶、顶叶,枕叶和小脑及其他部位分别为14、9、9、5、4。
1.2治疗方法。放疗方法:患者仰卧于MRI和CT模拟定位共用体板上,双手置于体侧,头罩固定;平静呼吸,分别使用GE Singa Horizontal 1.5T超导型模拟定位机和PHILIPS AcQsim CT模拟定位机对患者头颅扫描,层厚均为5 mm,将MRI和CT图像传输到Pinnacle3三维治疗计划系统,MRI和CT图象融合,采用归一互信息法进行CT和MRI图象配准[3]。结合术前、术后MRI影像学和手术记录等情况在MRI定位图像上确定并勾画肿瘤靶区(GTV、CTV、PTV)和需保护的脑干、脊髓、眼球和晶状体、视神经等重要组织器官。GTV为MRI图像所见肿瘤灶;CTV为肿瘤灶和肿瘤旁水肿区(GTV外放2~2.5 cm);PTV为CTV外放1 cm。剂量为每次1.8~2 Gy,每天1次,每周5次,肿瘤总剂量为60 Gy。同步化疗为口服替莫唑胺胶囊(天津药业生产,批号:H31020593)75 mg/(m2•d),与放疗同步进行。放疗后辅助化疗6程,在放疗后1个月内开始。第1个疗程剂量为150 mg/(m2•d),连续5 d,第2个疗程起200mg/(m2•d),连续5 d,28 d为1个疗程。
1.3疗效及不良反应评价标准:同步放化疗结束后2个月复查头颅MRI,与治疗前进行比较,Recist1.1标准评价疗效。有效率=(完全缓解+部分缓解)/总例数×100%;总生存期(OS)为放疗开始到死亡的时间。不良反应评价:使用RTOG急性放射损伤分级标准和CTCAE3.0标准评价放射性脑损伤。
1.4统计方法:所有统计数据均采用SPSS17.0软件进行处理,研究的终点是总生存期,P≤0.05认为有统计学差异。
2 结 果
2.1疗效:所有患者全部完成放疗计划,除7例患者总剂量50~56 Gy外,总剂量均为60 Gy,有12例放疗后完成辅助化疗1周期,15例完成2周期,3例完成3周期,5例完成4周期,6例完成6周期。回访截止2014年12月30日,随访时间为半年到5年,OS平均26个月。同步放化疗结束2个月后复查头颅MRI,评价胶质瘤残留灶,完全缓解10例,部分缓解18例,无变化10例,进展3例,有效率68.3%。1年的生存率78.4%、2年的生存率56.8%、3年的生存率29.7%、4年的生存率13.5%,5年的生存率5.4%。
2.2影响疗效因素分析:应用Cox比例风险回归模型分析后发现,肿瘤病理分级、辅助化疗疗程数、放疗剂量是否达到60 Gy对OS有影响(P≤0.05)(图1~3)。
2.3毒性反应:并发症和不良反应:骨髓抑制发生率31.6%,绝大部分为Ⅰ~Ⅱ度,其他不良反应包括:恶心、呕吐、乏力、腹泻、皮疹、头部胀痛等,对症处理后可缓解。个别患者有局限性癫痫,专科处理后未有严重后果。
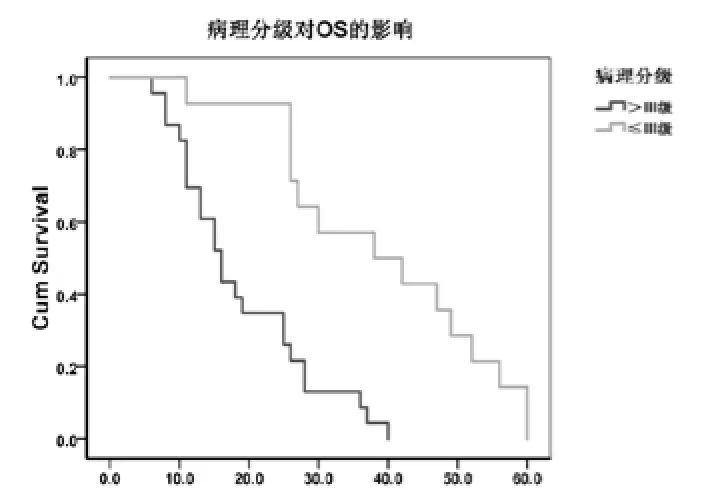
图1

图2

图3
3 讨 论
脑胶质瘤手术完全切除机会小,疗效不佳,高分级胶质瘤预后更差,术后1~3年内几乎全部复发[4]。有研究表明,单独使用不完全手术切除治疗后5年无复发生存率19%,如果加术后放疗可显著提高至46%,所以脑胶质瘤的治疗以手术、放疗和化疗等多学科综合性治疗为主[5]。MRI模拟定位对脑胶质瘤的残留肿瘤灶显示清楚,比较容易确定肿瘤灶范围和勾画肿瘤靶区,与CT相比对胶质瘤残留灶的显示具有显著优势。适形调强放疗是可以提高肿瘤靶区剂量,保护周围正常脑组织的一种较好的放疗技术。

表1 OS影响因素分析(n=41)
近期国内文献提示放、化疗的综合治疗对脑胶质瘤术后残留治疗效果较单纯放疗效果好。放疗开始后,对血脑屏障造成一定程度损伤,这时有利于化疗药物通过血脑屏障,治疗可能获得更大利益[6]。并且一些化疗药物除了本身具有抗癌作用外还有放射增敏作用。脑胶质瘤目前最有效的化疗药物是替莫唑胺。该抗癌药物是口服二代烷化剂-咪唑四嗪类衍生物,服用后迅速吸收,不经过肝脏代谢广泛分布全身,可以透过血脑屏障,进入脑脊液达到有效的药物浓度。脑脊液浓度/血浆药物浓度30%~40%,分布脑肿瘤组织的浓度大于正常脑组织的浓度。替莫唑胺进入体内分解为药物活性物质,通过对DNA链的甲基化造成其单链或双链的断裂,阻断DNA的复制,造成肿瘤细胞的死亡。除外对肿瘤细胞的核酸、蛋白质、肽亲核区也发生作用,具有广谱的抗肿瘤活性,并且服用方便、不良反应少[7-8]。2年生存率是单纯放疗的2倍以上[9]。本组资料显示:手术后有肿瘤残留的患者如能接受足量的放疗剂量和辅助化疗,生存期明显延长。另外,胶质瘤Ⅳ级(胶质母细胞瘤)预后较胶质瘤Ⅲ级明显差,有统计学意义(表1)。文献还报道脑胶质瘤肿瘤细胞要检测特定遗传标志(MCMT基因改变),有MCMT基因改变即MGMT-提示烷化类敏感,使用替莫唑胺有效。MGMT-脑胶质瘤患者服用替莫唑胺并且同步放疗的生存期较单纯放疗长(21.7个月对12.7个月)[10]。本组是高分级脑胶质瘤术后残留病灶的患者,手术减少了肿瘤负荷,同步放化疗降低复发的概率和延长复发时间。治疗中并发症和不良反应少,多表现为骨髓抑制,骨髓抑制发生率31.6%,绝大部分为Ⅰ~Ⅱ度,其他不良反应包括:恶心、呕吐、乏力、腹泻、皮疹、头部胀痛等,对症处理后可很快缓解。个别患者有局限性癫痫,专科处理后未见严重并发症。
总之,MRI模拟定位、适形调强放疗对高分级脑胶质瘤是放疗技术革新,有利肿瘤靶区的确定和治疗以及保护周围正常组织。放疗期间同步化疗,具有协同抗肿瘤作用,能提高治疗有效率,延长OS时间,且安全性好,不增加化疗毒性反应,有较好的应用前景,可作为胶质瘤的有效治疗方案。
[1] 谷铣之,殷蔚伯.肿瘤放射治疗学[M].北京:北京医科大学中国协和医科大学出版社,2008:1123.
[2] 胡逸民,谷铣之.适形放射治疗-肿瘤放射治疗技术的进展[J].中华放射肿瘤学杂志1997,6(3):8-11.
[3] 邵滋汤.上颌窦恶性肿瘤CT/MRI图象融合靶区勾画的研究[D].上海:上海交通大学,2008.
[4] Central Brain Tumor Registry of the United States,2008.
[5] 中华医学会神经外科学会肿瘤学组.中国中枢神经系统恶性胶质瘤诊断和治疗共识[R].2011.
[6] 邓万凯,陈健.高级别脑胶质瘤术后三维适行放疗联合替莫唑胺化疗的疗效观察[J].中国神经肿瘤杂志,2008,6(1):42-44.
[7] Newlands ES,Blackledge GRP.Phase l trial of temozolomide[J].Br J Cancer,1992,65(2):287-291.
[8] Dewit L. Combined treatment of radiation and Cisdiamminedich loroplatinum and clinical data[J]. Int J Radiat Oncol Biol Phye, 1987,13(3):403-426.
[9] Stupp R,Mason WP.Radiotherapy plus concomitant and adjuwant temozolomide for glioblastoma[J].N Engl J Med,2005,352(10): 987-996.
[10] Hegi ME,Diserens AC.MGMT gene silencing and benefit from temozolomide in glioblastoma[J].N Engl J Med,2005,352(10): 997-1003.
R730.5
B
1671-8194(2015)30-0047-02
