热解温度对污泥生物炭稳定性及养分淋溶特性影响
2015-10-15鲁涛袁浩然王亚琢呼和涛力陈勇
鲁涛,袁浩然,王亚琢,呼和涛力,陈勇
热解温度对污泥生物炭稳定性及养分淋溶特性影响
鲁涛1,2,3,袁浩然1,2,王亚琢1,2,呼和涛力1,2,陈勇1,2
(1中国科学院广州能源研究所,广东广州 510640;2中国科学院可再生能源重点实验室,广东广州 510640;3中国科学院大学,北京 100049)
以市政污泥为原料,在300、500、700 ℃条件下热解制备得到污泥生物炭。采用碱液吸收法测定生物炭在培养环境下的CO2释放速率以表征其降解速率,并采用预测模型计算得到生物炭的半衰期。以去离子水为浸提剂考察了生物炭中可溶性养分含量及其淋溶特性。结果表明:在300~700℃范围内,较高温度下制备的生物炭降解缓慢,稳定性更强,可在自然环境中长期存在,具有更好的固碳效果;较低温度下制备的生物炭中水溶性氮、水溶性钾含量更高,但水溶性磷含量更低;生物炭中养分的淋溶效果与其可溶性养分含量一致,较低温度下制备的生物炭的淋溶液中水溶性氮、水溶性钾含量较高,水溶性磷含量较低。
市政污泥;热解;生物炭;降解;养分元素
引 言
生物炭是自然有机质及其衍生物在缺氧燃烧或热解条件下得到的固体剩余物[1-2]。自然界的生物炭主要来自闪电或火山喷发等自然原因引起的森林大火[3],而人工得到的生物炭主要来自各种农林废弃物的热解过程。近年来,由于亚马逊黑土(Terra Preta)的发现,生物炭研究得到了极大关注,其研究热点主要集中于土壤改良及碳减排[4-7]。土壤改良作用主要体现在生物炭施用后土壤有机质含量的提高、透气性和持水性能及保肥能力的改善等[5]。而抑制碳排放的原理在于相比生物质类原料生物炭具有高度的稳定性,在土壤环境中可长期保存成百上千年,储存在生物炭中的碳可长久保存于土壤环境而不会以CO2的形式向大气环境扩散[6-8]。另外,生物炭对土壤CO2排放亦有抑制作用,尽管目前这种抑制作用还存在争议[9-10]。
相比以生物质为原料制备的生物炭,污泥生物炭养分含量更加丰富,增强土壤肥力效果更佳。因此,近年来开展了以市政污泥为原料的生物炭研究,分别考察了生物炭的组成、孔隙结构、表面特性、酸碱性、养分含量等物化性质,并着重考察了不同制备条件下生物炭中重金属含量及浸出毒性[11-13]。研究表明,热解温度对生物炭物化性质有着重要影响。高温下制备的生物炭其碳含量更高,拥有高度芳香化的碳结构,从侧面反映出其良好的稳定性[14];更发达的孔隙结构,利于改善土壤持水能力、透气性和养分吸持能力[12-15];碱性更强,特别适用于酸性土壤[12,15-16]。尽管氮元素含量随热解温度提高而逐渐降低,但磷元素和钾元素含量均随热解温度提高而增加[12,17]。另外,高温下制备的生物炭的重金属浸出毒性也更低,符合相关重金属浸出毒性的规范要求[12,18-19]。因此,将污泥转化为生物炭用于土壤改良是污泥农用的有效改进,既充分利用了养分元素,又有效降低了环境风险。
稳定性是生物炭最重要的性质之一,稳定存在是生物炭改善土壤性质的前提条件,也是发挥碳减排作用的重要保证。生物炭增强土壤肥力的作用主要通过来自自身水溶性养分的输入实现。然而,目前对污泥生物炭的稳定性及养分有效性研究仍然缺乏。在保证生物炭中重金属含量及浸出毒性符合相关规范要求的前提下[20-21],本研究考察了不同热解温度下生物炭的稳定性、水溶性养分含量及养分淋溶特性,为增强土壤肥力和发挥碳减排作用的大规模生物炭开发提供理论依据和基础数据支持。
1 材料与方法
1.1 污泥
污泥样品(含水率78.5%)取自广州市某市政污水处理厂脱水车间,污水处理工艺为改良的厌氧-缺氧-好氧工艺。污泥样品在室温下通风干燥至可粉碎,粉碎至1~2 mm,搅拌均匀,在105℃干燥至恒重,然后保持在密封袋中。绝干污泥的工业分析和元素分析结果见表1。

表1 污泥样品元素分析及工业分析
1.2 生物炭制备
生物炭制备设备为卧式石英管热解炉。100 g±1 g 绝干污泥装入石英管,用99.99 %的氮气以1000 ml·min-1的流量吹扫30 min以排空空气,然后以10℃·min-1的加热速率加热至预设温度 (300、500、700℃)并保留3 h,待生物炭冷却至室温后保存在密封袋中。下文分别以B300、B500、B700表示在300、500、700℃制备的污泥生物炭。
1.3 生物炭降解速率测定
生物炭降解速率测定参考Zimmerman推荐的方法[22],以CO2释放速率表征生物炭降解速率,每种生物炭的培养实验分别设置3个平行样。取50 ml土壤浸出液(用于提供土壤微生物),与0.5 g 生物炭、50 g石英砂(充当介质)均匀混合,滤除多余水分后,置于 500 ml棕色瓶中,棕色瓶内另外放置装有0.20 mol·L-1NaOH溶液的小烧杯用于吸收生物炭降解释放的CO2[23]。培养期为120 d,定期取出小烧杯,用0.10 mol·L-1盐酸以及1.0 mol·L-1BaCl2溶液滴定确定生物炭降解释放的CO2量。
1.4 生物炭水溶性养分测定
参考Zheng等[17]推荐的方法,每种生物炭的水溶性养分测定实验分别设置3个平行样。称取1.0 g生物炭置于45 ml塑料离心管中,加入40 ml 去离子水,在室温(25℃±1℃)下采用水平振荡器以150 r·min-1的频率振荡72 h后,取上清液过滤,然后采用ICP-AES(USA Thermo Jarrell Ash Corporation)测定K+、、以及浓度。
1.5 生物炭养分淋溶实验
参考Mukherjee等[24]推荐的方法,同样以石英砂为载体介质,将5 g生物炭均匀分散在约670 g石英砂中,装载在高度为25 cm、内径为8.5 cm 的聚丙烯管内,管底用尼龙细网包裹以防止生物炭和石英砂流失,聚丙烯管底部再由导管连接至烧杯用于接收淋溶液。在淋溶实验开始前,先用去离子水将石英砂柱淋溶饱和,然后由小型喷洒系统按照250 ml·d-1的淋溶速率缓慢均匀喷洒至石英砂柱上表面。淋溶实验共持续6 d,淋溶总量为1500 ml,淋溶液每天收集,过滤后分别保存在4℃的环境以待分析。淋溶液中K+、、以及浓度采用ICP-AES 测定。
2 结果和讨论
2.1 生物炭降解速率
如图1所示,B300、B500 以及B700的降解速率在培养初期(前14天)较高,然后逐渐降低。生物炭降解可分为非生物降解和微生物降解。非生物降解途径为氧原子在苯环上非饱和位点的化学吸附、羧基形成以及随后的脱羧过程[3,25]。生物炭自身包含有羧酸、酚类等含有羧基官能团物质,因此培养初期释放的CO2主要来源于上述物质的脱羧过程。培养后期生物炭降解速率的迅速降低表明氧原子的化学吸附或羧基形成过程是控制生物炭降解的关键步骤。另外,相比其他生物质类生物炭,污泥生物炭含有更多的金属氧化物,其催化作用导致开环及脱羧过程加速,促进了污泥生物炭的非生物降解[22]。

图1 微生物培养过程中生物炭的降解速率
尽管具体数值不同,此结果与前人的研究结果类似,生物炭的降解速率与制备温度密切相关,低温下制备的生物炭的降解速率较高,高温下制备的生物炭的降解速率较低[22,26]。根据工业分析,生物炭由挥发分、固定碳、灰分构成。挥发分氧含量较高、碳含量较低,此部分碳主要为易于被微生物分解利用的直链碳;固定碳含有较高比例的芳香碳,此部分碳难以被微生物吸收利用;灰分主要为各种无机类矿物质。微生物降解消耗的碳主要为挥发分中的直链碳,而低温下制备的生物炭含有较高比例的挥发分,因此低温下制备的生物炭的降解速率较高。而挥发分中直链碳的大量消耗也是培养后期生物炭降解速率逐渐降低的另一原因。
2.2 生物炭稳定性
一般认为生物炭具有良好的稳定性,在自然环境中可稳定存在成百上千年。而实验监测一般仅持续数月或数年时间,为此Zimmerman 推荐了预测模型,根据生物炭的降解速率预测生物炭的半衰期[22]。生物炭在培养期的降解速率曲线如图1所示。
生物炭降解过程符合一阶降解反应,即

而表观分解速率常数与培养时间符合指数关系,即
(2)
因此,生物炭的半衰期可根据式(3)计算得到
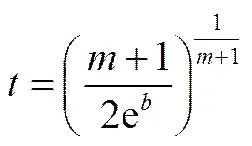
预测结果显示B300、B500和B700的半衰期分别为12、2521和8798年。
此模型建立在培养期外生物炭的降解速率变化趋势与培养期内降解速率的变化趋势一致的基础上,而生物炭的降解速率会随培养期的延长逐渐降低,因此生物炭的实际半衰期会大于预测值。其预测结果的价值在于表明较高温度下制备的生物炭具有更强的稳定性,可在自然环境中长期存在,进而长期发挥土壤改良作用和碳封存作用。
模型计算结果如图2所示。
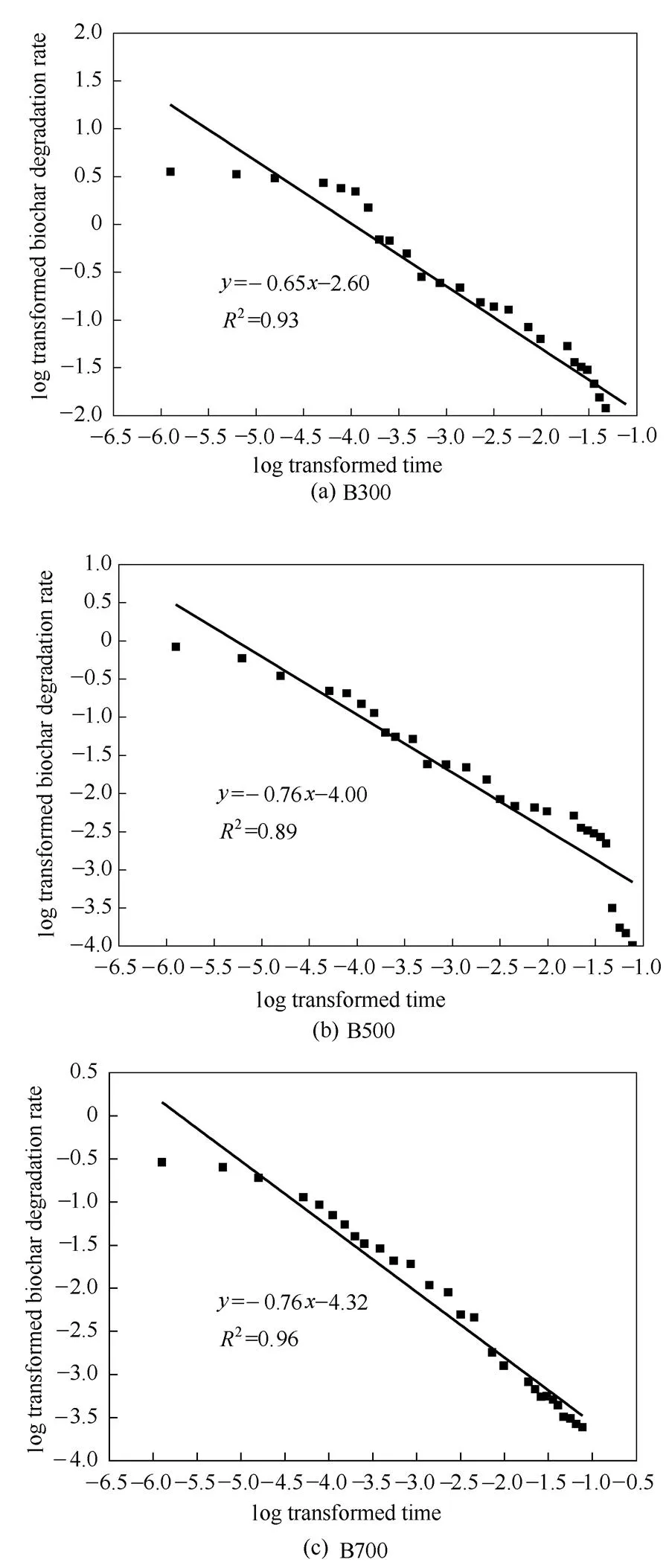
图2 微生物培养期生物炭降解速率与时间自然对数之间的线性相关性
2.3 生物炭水溶性养分含量
如表2所示,水溶性氮含量在1540~2528 mg·kg-1之间,变化趋势与其他报道中的生物炭 中总氮含量变化趋势一致,均随热解温度升高而降低[12,17]。具体来讲,水溶性氨氮从1100 mg·kg-1降低至316 mg·kg-1,水溶性硝氮从1428 mg·kg-1降低至1224 mg·kg-1。含氮物质在高温下的分解是生物炭中水溶性氮含量下降的主要原因[27]。
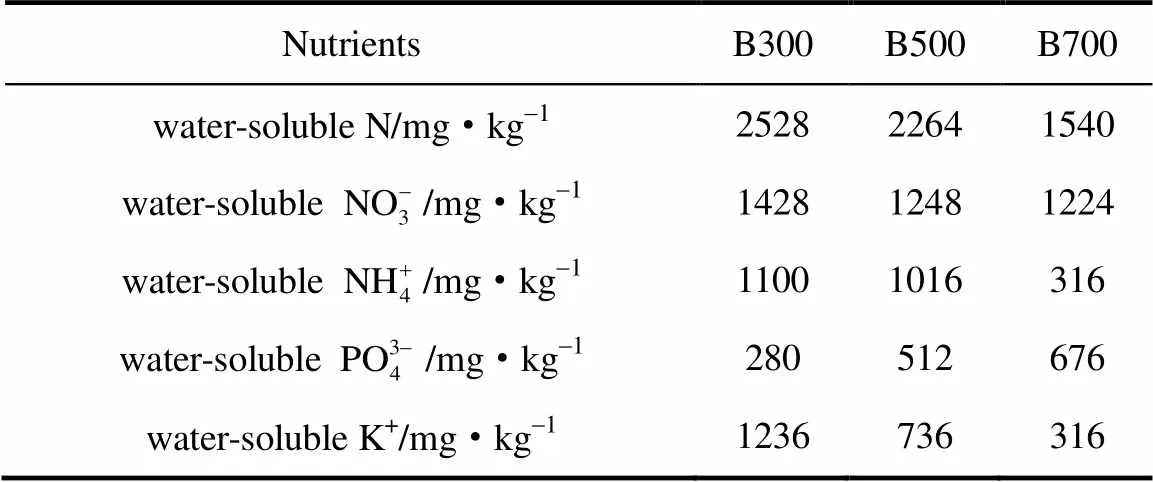
表2 不同温度下制备的生物炭中的水溶性养分含量
生物炭中水溶性磷酸根的含量在280~676 mg·kg-1之间。磷在污泥中主要以无机物形式存在,具有良好的热稳定性,因此生物炭中水溶性磷含量随热解温度升高而增加。
尽管钾主要以无机物形式存在于污泥中,然而生物炭中水溶性钾含量随热解温度升高从1236 mg·kg-1下降至316 mg·kg-1,说明生物炭制备过程中部分含钾无机物挥发损失。
2.4 生物炭养分淋溶特性

图3 不同温度下制备的生物炭淋溶液中养分浓度
3 结 论
生物炭的降解速率与制备温度密切相关,在300~700℃温度范围内,较低温度下制备的生物炭的降解速率较高,较高温度下制备的生物炭的降解速率较低。预测结果显示300、500和700℃制备的生物炭在自然环境中的半衰期分别为12、2521和8798年,因此高温下制备的生物炭具有更强的稳定性,固碳效果更好。生物炭中水溶性浓度、水溶性浓度以及水溶性K+浓度均随热解温 度升高而降低,水溶性浓度随热解温度升高而升高。生物炭淋溶液中养分浓度与生物炭中可溶性养分浓度一致,、、K+浓度大小顺序为 B300>B500>B700,浓度大小顺序为B700>B500>B300。
符 号 说 明

b——生物炭降解速率拟合直线截距(图2) C——生物炭质量,mg C0——生物炭初始质量,mg k——表观降解速率常数 m——生物炭降解速率拟合直线斜率(图2) t——培养时间,a
References
[1] Lehmann J, Joseph S. Biochar for Environmental Management: Science and Technology [M]. London: Earthscan Ltd, 2009.
[2] Bird M I, Wurster C M, Silva P H D, Bass A M, Denys R. Algal biochar-production and properties [J]., 2011, 102 (2): 1886-1891.
[3] Cheng C H, Lehmann J, Thies J E, Burton S D, Engelhard M H. Oxidation of black carbon by biotic and abiotic processes [J]., 2006, 37: 1477-1488.
[4] Glaser B, Haumaier L, Guggenberger G, Zech W. The ‘Terra Preta’ phenomenon: a model for sustainable agriculture in the humid tropics [J]., 2001, 88: 37-41.
[5] Gaskin J W, Steiner C, Harris K, Das K C, Bibens B. Effect of low-temperature pyrolysis conditions on biochar for agricultural use [J]., 2008, 51 (6): 2061-2069.
[6] Kuhlbusch T A J, Crutzen P J. Toward a global estimate of black carbon in residues of vegetation fires representing a sink of atmospheric CO2and a source of O2[J]., 1995, 9: 491-501.
[7] Lehmann J, Gaunt J, Rondon M. Bio-char sequestration in terrestrial ecosystems—a review [J]., 2006, 11: 403-427.
[8] Fowles M. Black carbon sequestration as an alternative to bioenergy [J]., 2007, 31: 426-432.
[9] Wardle D A, Nilsson M C, Zackrisson O. Fire-derived charcoal causes loss of forest humus [J]., 2008, 320: 629.
[10] Steinbeiss S, Gleixner G, Antonietti M. Effect of biochar amendment on soil carbon balance and soil microbial activity [J]., 2009, 41: 1301-1310.
[11] Agrafiotia E, Bourasa G, Kalderisb D, Diamadopoulos E. Biochar production by sewage sludge pyrolysis [J]., 2013, 101: 72-78.
[12] Hossain M K, Strezov V, Chan K Y, Ziolkowski A, Nelson P F. Influence of pyrolysis temperature on production and nutrient properties of wastewater sludge biochar [J]., 2011, 92 (1): 223-228.
[13] Lu H, Zhang W, Wang S, Zhuang L, Yang Y, Qiu R. Characterization of sewage sludge-derived biochars from different feedstocks and pyrolysis temperatures [J]., 2013, 102: 137-143.
[14] Spokas K A. Review of the stability of biochar in soils: predictability of O:C molar ratios [J]., 2010, 1 (2): 289-303.
[15] Méndeza A, Terradillosb M, Gascó G. Physicochemical and agronomic properties of biochar from sewage sludge pyrolysed at different temperatures [J]., 2013, 102: 124-130.
[16] Topoliantz S, Ponge J-F, Ballof S. Manioc peel and charcoal: a potential organic amendment for sustainable soil fertility in the tropics [J]..., 2005, 41 (1): 15-21.
[17] Zheng H, Wang Z, Deng X, Zhao J, Luo Y, Novak J, Herbert S, Xing, B. Characteristics and nutrient values of biochars produced from giant reed at different temperatures [J]., 2013, 130: 463-471.
[18] Méndez A, Gómez A, Paz-Ferreiro J, Gascó G. Effects of sewage sludge biochar on plant metal availability after application to a Mediterranean soil [J]., 2012, 89 (11): 1354-1359.
[19] Jin H, Arazo R O, Gao J, Capared S, Chang Z. Leaching of heavy metals from fast pyrolysis residues produced from different particle sizes of sewage sludge [J]., 2014, 109: 168-175.
[20] Yuan H R, Lu T, Zhao D D, Huang H Y, Noriyuki K, Chen Y. Influence of pyrolysis temperature on physical and chemical properties of biochar made from sewage sludge [J]., 2015, 112: 284-289.
[21] Yuan H R, Lu T, Zhao D D, Huang H Y, Noriyuki K, Chen Y. Influence of temperature on product distribution and biochar properties by municipal sludge pyrolysis [J]....., 2013, 15: 357-361.
[22] Zimmerman A R. Abiotic and microbial oxidation of laboratory-produced black carbon (biochar) [J]..., 2010, 44: 1295-1301.
[23] Zibilske L M. Carbon mineralization//Weaver R W, Angle S, Bottomley P, Bezdicek D, Smith S, Tabatabai A,. Methods of Soil Analysis. Part 2. Microbiological and Biochemical Properties. Soil Science Society of America Book Series [M]. vol.5. Madison: Soil Science Society America Inc, 1994: 835-864.
[24] Mukherjee A, Zimmerman A R. Organic carbon and nutrient release from a range of laboratory-produced biochars and biochar-soil mixtures [J]., 2013, 193-194: 122-130.
[25] Wang M C, Huang P M. Ring cleavage and oxidative transformation of pyrogallol catalyzed by Mn, Fe, Al, and Si oxides [J]., 2000, 165 (12): 934-942.
[26] Peng X, Ye L L, C Wang C H, Zhou H, Sun B. Temperature-and duration-dependent rice straw-derived biochar: characteristics and its effects on soil properties of an Ultisol in southern China [J]., 2011, 112: 159-166.
[27] Cao X, Harris W. Properties of dairy-manure-derived biochar pertinent to its potential use in remediation [J].ce, 2010, 101: 5222-5228.
Influence of pyrolysis temperature on biochar stability and leaching properties of nutrients contained in biochar
LU Tao1,2,3, YUAN Haoran1,2, WANG Yazhuo1,2, HUHETAOLI1,2, CHEN Yong1,2
(1Guangzhou Institute of Energy Conversion, Chinese Academy of Sciences, Guangzhou 510640, Guangdong, China;2Key Laboratory of Renewable Energy, Chinese Academy of Sciences, Guangzhou 510640, Guangdong, China;3University of Chinese Academy of Sciences, Beijing 100049, China)
The biochar was produced from sewage sludge by pyrolysis at 300, 500 and 700 ℃. In this study the biochar degradation rate represented by CO2release rate through alkali absorption method in microbial incubation was investigated and the half-life using a recommended prediction method was predicted. In addition, deionized water was used to investigate the content and leaching properties of the water-soluble nutrients contained in biochar. During the temperature range of 300—700℃, the biochar produced at higher temperature was degraded slowly and had longer half-life, which may exist in soil for a longer time span and then perform a better effect on carbon sequestration than that produced at lower temperature. However, biochar produced at lower temperature contained more water-soluble N and K but less water-soluble P, which was agreed with the concentration of leaching nutrients. The leaching water of biochar produced at lower temperature also contained more much water-soluble N and K but less water-soluble P.
sewage sludge; pyrolysis; biochar; degradation; nutritive element
2015-03-02.
supported by the National Basic Research Program of China (2011CB201501) and the National Natural Science Foundation of China (51406207).
Dr.YUAN Haoran, yuanhr@ms.giec.ac.cn
10.11949/j.issn.0438-1157.20150253
X 705
A
0438—1157(2015)07—2664—06
国家重点基础研究发展计划项目(2011CB201501);国家自然科学基金项目(51406207).
2015-03-02收到初稿,2015-03-27收到修改稿。
联系人:袁浩然。第一作者:鲁涛(1984—),男,博士研究生。
