掺杂Ce、Zr对CO2钙基吸附剂循环特性的影响
2015-10-15张雷张力闫云飞杨仲卿郭名女
张雷,张力,闫云飞,杨仲卿,郭名女
掺杂Ce、Zr对CO2钙基吸附剂循环特性的影响
张雷1,2,张力1,2,闫云飞1,2,杨仲卿1,2,郭名女1
(1低品位能源利用技术及系统教育部重点实验室(重庆大学),重庆 400044;2重庆大学动力工程学院,重庆 400044)
利用湿法混合-煅烧法将元素Ce、Zr掺杂到CO2钙基吸附剂中,利用热重分析仪(TGA)研究了24种改性钙基吸附剂吸附CO2的循环特性。研究发现:CeO2散布在CaO晶粒之间可抑制晶粒融合,对吸附剂烧结有一定的阻碍作用;CeO2可明显提高吸附剂在扩散控制阶段对CO2的吸附速率,原因在于CeO2中丰富的氧空位可促进CO2以离子迁移的方式穿过表面产物层到达内部与CaO反应;吸附剂中CeO2含量越高,稳定性越强;ZrO2与CaO高温化合成具有高塔曼温度的CaZrO3,均匀分散在CaO晶粒间,构成稳固的支撑骨架,有效抑制了吸附剂烧结。
氧空位;钙基吸附剂;吸附;二氧化碳捕集;转化率;稳定性
引 言
在CO2的各种捕集方法中,利用钙基吸附剂对CO2进行脱除是重要的有效的方法之一[1]。天然的石灰石吸附剂经过少数碳化/煅烧循环反应后,其对CO2的捕捉能力迅速衰退[2],主要是由于烧结作用使吸附剂比表面积变小,晶粒内部的微小晶体聚合,微细通道消失,最终使吸附剂的循环吸收率和循环稳定性随吸附/煅烧循环次数的增加而降低[3-5]。
目前,在提高钙基吸附剂循环捕集CO2性能方面研究者们做了大量研究工作。Liu等[6]和Lu等[7]实验发现葡萄糖酸钙、乙酸钙、丙酸钙和乳酸钙表现出优异的CO2吸收效率;Lu等[8]和陈惠超等[9]研究发现对吸附剂进行热处理可提高其机械稳定性,水合作用可有效提高吸收剂的活性;张明明等[10]、Lu等[11]、Reddy等[12]通过向CaO中掺杂金属离子提高吸附剂循环吸附效率和循环稳定性;Bhatia等[13]认为CO2可通过离子迁移的方式穿过CaCO3产物层到达CaCO3-CaO界面;Dudek[14]发现含有丰富氧空位的氧化物具有很强的储存和释放O2-能力,从而明显提高了自身的导电性。因此,本研究假设氧空位的存在可能会促进CO2穿过CaCO3产物层,有利于提高CaO吸附剂循环稳定性。通过将元素Ce、Zr掺杂到钙基吸附剂中,研究氧空位对吸附剂捕集CO2的循环吸收率以及循环稳定性的影响,探索具有氧空位的添加剂对吸附剂脱碳性能的影响机理,为改善及制备高效、稳定的钙基CO2吸附剂提供依据。
1 实验部分
1.1 改性钙基吸附剂的制备
吸附剂的制备均采用操作简便的湿法混合-煅烧法。为了使添加剂在CaO中分布均匀,选用可溶的Ce(NO3)3·6H2O、Zr(NO3)4·5H2O和4种可溶性有机钙[葡萄糖酸钙(CG)、乙酸钙(CA)、丙酸钙(CP)、乳酸钙(CL)]分别作为添加剂前驱物和CaO前驱物。将钙基前驱物与添加剂前驱物按照一定的质量配比(根据目标吸附剂的成分配比计算所得)溶解到等量的去离子水中,使用磁力搅拌器加热至70℃并恒温搅拌,直至大部分水分蒸发,置于110℃干燥24 h,再放置到马弗炉中于900℃煅烧90 min,即为实验用改性吸附剂。未掺杂添加剂的4种吸附剂样品也使用相同的制备方法获得。
吸附剂样品命名格式为:钙基前驱物-M/Ca2+添加剂。其中M代表Zr4+或Ce4+。如CG-1/5CE为葡萄糖酸钙与Ce(NO3)3·6H2O按Ce4+/Ca2+摩尔比为1/5相混合制备的吸附剂,CG-00代表煅烧葡萄糖酸钙获得的未添加掺杂剂的CaO吸附剂。
在吸附剂制备后对样品进行了XRF测试。其中CA-1/5CE的主要成分为(质量分数):Ca 43.78%,Ce 30.86%,O 23.43%,其他(Fe、Cl、Si等)1.93%;CL-1/5ZR的主要成分为(质量分数):Ca 49.32%,Zr 22.18%,O 26.04%,其他(Fe,S,Pb等)2.46%。
1.2 吸附剂的表征方法
比表面积及孔容孔径分析利用ASAP 2020系列全自动快速比表面积及中孔/微孔分析仪进行测试。吸附剂晶型结构采用荷兰帕纳科公司生产的X’Pert X射线衍射仪进行分析,功率为40 kV×40 mA,辐射源为CuKα(0.154056 nm),扫描范围为20°~60°,扫描步长为0.0262°。吸附剂的表面形貌和结构特征通过VEGA3 TESCAN型扫描电子显微镜(SEM)进行扫描。
1.3 实验条件及方法
实验在热重分析仪(德国STA409PC型)上进行。根据热重实验的特点[12,15],反应坩埚每次填料量约为10mg。主要实验步骤如下,详细实验过程可参见文献[15]。
(1)升温及初始煅烧过程:首先在反应器坩埚中装填约10 mg吸附剂;通入70 ml·min-1的N2,以20℃·min-1的升温速率将样品升温至900℃,保持10 min,除去吸附剂在储藏和使用过程中可能与空气接触而吸收的水分和生成的CaCO3。
(2)计算得知国内4种典型煤种(山西阳泉无烟煤、淄博贫煤、山西官地煤、张新矿煤)燃烧后的CO2在烟气中的体积分数为14.10%~15.11%,故将碳化阶段气氛中CO2的体积分数设为15%,85%的N2作为平衡气体。碳化反应:以20℃·min-1的降温速率降温至650℃并稳定后,通入15 ml·min-1的CO2和85 ml·min-1的N2,维持30 min。煅烧反应:停止通入CO2,保持85 ml·min-1的N2氛围,以20℃·min-1的升温速率升温至850℃,恒温10 min。
(3)重复过程(2),共完成10次循环。
1.4 实验数据的分析方法
第次循环吸附剂的转化率c()(循环吸收率)为
式中,0为初始煅烧结束后即第1次吸收反应前吸附剂质量,0为第1次吸收反应前吸附剂中CaO质量分数,为第次吸收完成时吸附剂质量,m为第次煅烧结束后吸附剂质量。
2 实验结果及分析
2.1 掺杂CeO2对不同钙基吸附剂循环特性的影响
图1为CA-1/5CE在第1个循环前和第10个循环后的XRD分析,样品中的Ce均以CeO2物相存在,CeO2未与吸附剂中的CaO反应生成新物质。

图1 CA-1/5CE不同循环后XRD谱图
如图2所示,CG-00、CA-00、CL-00和CP-00首次循环都具有超过85%的转化率,原因是4种有机钙在煅烧过程中热解释放大量的H2O、CO2等气体,使得吸附剂具有发达的孔隙结构,从而使得碳酸化时CO2在颗粒中扩散变得更加容易。CG-1/5CE,CG-1/10CE在第10个循环的吸收率分别保持为89.6%和89.4%,比CG-00分别高20.6%和20.3%;CO2转化率依次为:CG-1/5CE>CG-1/10CE>CG-1/15CE。CG系列改性吸附剂循环吸附率在初始的个数循环中呈现上升趋势。文献[15]中葡萄糖酸钙作为CaO前驱物也出现类似现象,这是由于该系列吸附剂发生了自激活现象[16]。CA-1/5CE、CA-1/10CE、CA-1/15CE的转化率均明显高于同循环CA-00,在10个循环后CA-1/5CE转化率比CA-00高143.2%。从图2还发现,随着Ce4+/Ca2+摩尔比增加,各改性吸附剂循环转化率依次升高。
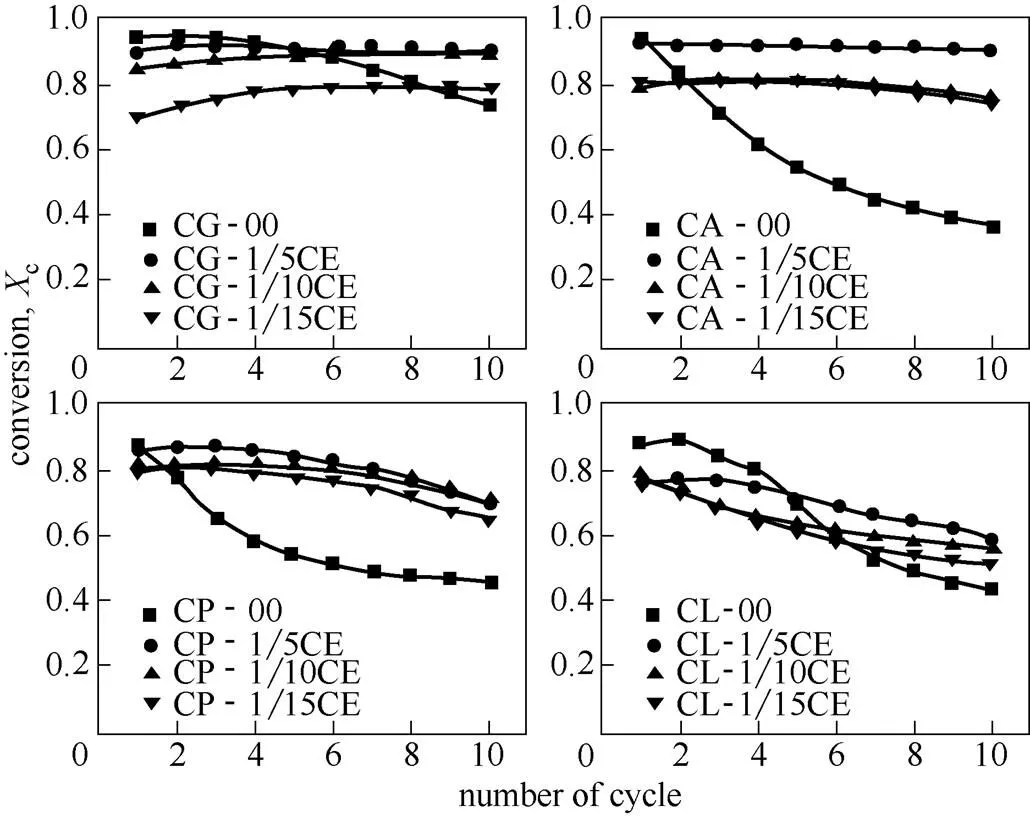
图2 Ce改性吸附剂循环吸附特性
吸附剂的比表面积和孔容积等微观结构参数对CO2吸附剂吸附性能有重要的影响。较大的比表面积和孔容积能够为CaO与CO2反应提供足够的反应场所和反应空间,有利于该反应的快速进行。较大的孔容积还有利于外部CO2向吸附剂颗粒内部渗透,从而提高吸附剂的循环吸收率和稳定性。为深入分析CeO2作用机理,对部分具有代表性的新鲜吸附剂进行了比表面积和孔容孔径测试,测试结果见表1。各吸附剂样品虽然都具有较大的初始比表面积和总孔容积,相比未改性吸附剂样品,CeO2改性后样品无论是初始比表面积还是总孔容积均有所下降。

表1 吸附剂比表面积及总孔容积
文献[17]指出:反应速率达到最大值所对应的CO2转化率为1,21则为动力学控制与扩散控制反应阶段的分界点。如图3所示,在首次循环中CA-00的CO2转化率比CA-1/5CE高7.1%,这主要是由于样品CA-00较CA-1/5CE具有略大的初始比表面积和总孔容积,导致在首次循环中相同的吸附时间内CA-00与CO2反应进度更深一些。比较CA-1/5CE与CA-00第10个循环碳化曲线:在动力学控制反应阶段,CA-1/5CE的CO2转化率较CA-00高169.1%;在3~30 min内,即扩散控制阶段,CA-1/5CE获得的CO2转化率为20.7%,而CA-00为7.2%。第10个循环后,CA-00及改性后的CA-1/5CE的比表面积较新鲜吸附剂分别下降了76.8%和62.9%,这表明CeO2在阻碍吸附剂烧结方面有一定效果,此即CA-1/5CE能够在快速反应阶段获得较高CO2转化率的主要原因。

图3 CA-00与CA-1/5CE单次吸附特性
随着反应的进行,吸附剂表面被CaCO3包裹,CO2向内部渗透愈加困难。CA-00此后对CO2的捕集能力极弱,反应速率低;而CA-1/5CE则表现出较强的CO2亲和力,在扩散控制阶段具有较高的吸收速率。这可能是由于吸附剂中CeO2具有很强的储氧放氧能力,而且存在的氧空位作为氧供体提供O2-,与CO2形成,再次分解成CO2,释放出O2-回到原来占位,下一占位上的O2-与上一占位释放出的CO2形成,然后继续分解成CO2,一层一层穿过CaCO3层,直到CaO和CaCO3界面,即离子迁移[13,18],使得吸附剂颗粒内部的活性CaO能够充分与CO2反应,提高吸附剂的转化率和稳定性。如图4所示,经过第10个循环后,CA-1/5CE微孔大量消失形成大孔,有些许团聚现象产生,这也从某种程度支持了文中“氧空位促进CO2扩散渗透表明产物层”假设的可能性。

图4 CA-1/5CE的SEM照片
Ce的掺杂使改性吸附剂初始比表面积和孔容积略有下降,这也是未改性吸附剂在初始循环中较改性吸附剂有略高转化率的主要原因,但CeO2对吸附剂的抗烧结作用可延缓吸附剂比表面积和孔容积的下降速率,从而保证改性吸附剂在快速反应阶段获得较高的CO2转化率,此外CeO2可明显提高吸附剂在扩散控制反应阶段的CO2转化率。因此,综合CeO2对吸附剂在微观结构参数、抗烧结和促进CO2在扩散控制反应阶段渗透的影响,后两者对转化率的促进作用远大于前者的削弱影响。
2.2 掺杂ZrO2对不同钙基吸附剂循环特性的影响
如图5所示,掺杂过ZrO2的样品获得的初始CO2循环转化率均低于未改性的原始CaO样品,原因在于未改性吸附剂具有更大的初始比表面积和孔容积。掺杂ZrO2后的改性吸附剂的CO2循环稳定性均得到不同程度的提高,CG-1/5ZR和CL-1/5ZR在第10个循环后转化率分别高达86.9%、87.5%,分别比同循环数下的CG-00、CL-00高17.1%、98.9%。随着Zr4+/Ca2+比值增加,Zr改性后吸附剂循环稳定性增强,CO2转化率随循环数的衰减曲线愈趋平缓。可见ZrO2在提高钙基吸附剂稳定性方面起到了重要作用。

图5 Zr改性吸附剂循环吸附特性
图6为CL-1/5ZR样品在第1个循环反应前和第10个循环反应后样品的XRD测试结果。图中显示新鲜吸附剂中存在Ca(OH)2,这可能是样品在保存过程中吸附了空气中的水蒸气导致的。吸附剂样品Zr以CaZrO3相存在,这表明Zr(NO3)4·5H2O高温分解生成的ZrO2完全与吸附剂样品中的活性CaO化合成CaZrO3。为了研究Zr改性吸附剂表面特性对其循环稳定性的影响,随机挑选了两个Zr改性吸附剂进行了比表面积和孔容积测试,见表1。Zr改性吸附剂的初始比表面积和总孔容积均较未改性吸附剂有所下降。
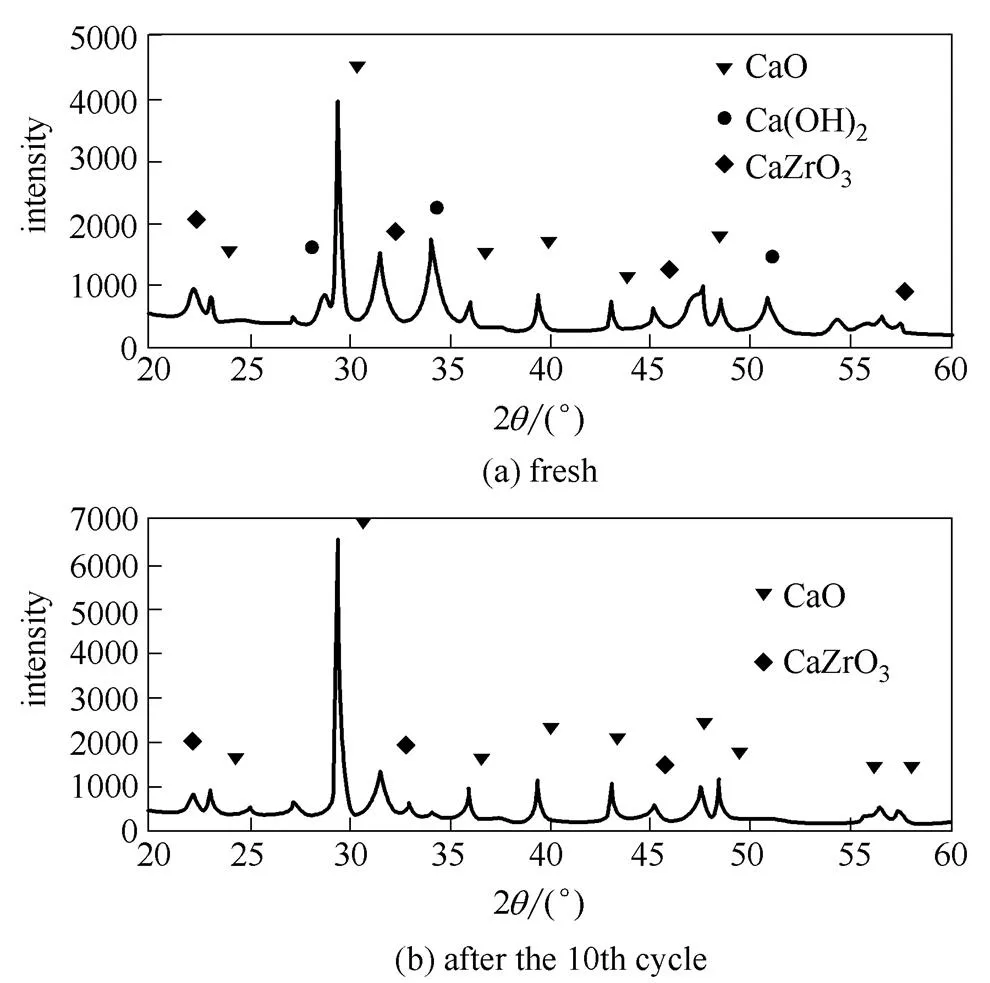
图6 CL-1/5ZR不同循环后XRD分析
从表1可得,CL-1/5ZR在第10个循环后拥有CL-00的3倍左右的比表面积,导致CL-1/5ZR的转化率较CL-00在快速反应阶段高95.3%,如图7所示。比较两者在慢速反应阶段CO2转化率随碳化时间的曲线,均显平缓,CL-1/5ZR获得12.4%的转化率,而CL-00仅为6.1%,这是由于反应产生的CaCO3覆盖了吸附剂表面并堵塞了其内部孔隙结构,外部CO2向内部扩散渗透阻力较大,以致吸附剂内部活性CaO无法完全与CO2反应。根据图3和图7,CL-1/5ZR在扩散控制阶段获得的转化率仅为12.4%,而富含氧空位的CA-1/5CE高达20.7%,所以本研究氧空位离子转移的假设在一定程度上得到了论证。
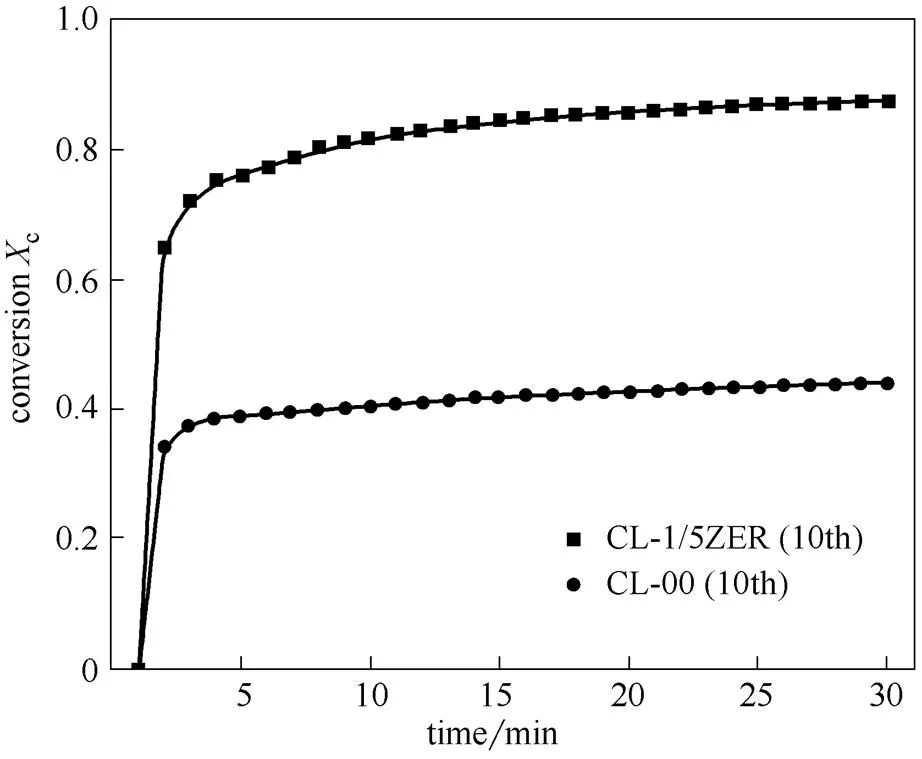
图7 CL-00与CL-1/5ZR单次吸附特性
如图8所示,SEM测试发现微粒依然维持最初的形状,孔隙结构清晰,未发现明显烧结现象。文献[14]研究发现,CaZrO3是相当弱的氧离子导体,但是向CaZrO3中引入2%~4%的CaO能产生氧空位缺陷,使得导电性明显增强。由于所有样品中CaO含量远远高于4%,该吸附剂样品中几乎不存在氧空位。CaZrO3塔曼温度(烧结温度)为1036℃[11],而CaCO3仅为533℃[19]。综合上述分析,应用湿法混合-煅烧法掺杂Zr后的改性吸附剂能够将CO2转化率以及循环稳定性维持在较高的水平,原因在于高塔曼温度的CaZrO3能够均匀分布在CaO晶粒之间,构成稳定结构骨架,有效地抑制了CaO晶粒间的熔化烧结,使得吸附剂微孔结构得以保存,从而CO2能有效进入到内部与活性CaO反应。Broda等[20]的研究也发现CaZrO3能为CaO提供稳固的支撑,大大减弱了高温造成的吸附剂烧结影响。

图8 CL-1/5ZR的SEM照片
3 结 论
(1)采用湿法混合-煅烧法将CeO2分散到CaO中,可明显提高改性吸附剂的循环转化率和稳定性。CG-1/5CE和CG-1/10CE在第10个循环后转化率分别高达89.6%和89.4%,比CG-00分别高20.6%和20.3%;10个循环内转化率大小为CG-1/5CE>CG-1/10CE>CG-1/15CE;CA-1/5CE在第10个循环后转化率仍高达90.2%,比同循环数下的CA-00高143.2%。
(2)CeO2可提高吸附剂在碳化反应扩散控制阶段对CO2的吸附速率;在本实验范围内,吸附剂中CeO2含量越高越有利于CO2的吸收,而且吸附剂循环稳定性越高。一方面,CeO2分散在CaO晶粒之间可抑制晶粒融合,对吸附剂烧结有一定的阻碍作用;另一方面,CeO2含有的丰富氧空位在扩散控制阶段通过离子迁移可促进CO2穿过产物层到达内部与CaO反应,提高吸附剂的循环稳定性。
(3)随Zr4+/Ca2+比值的增大,吸附剂稳定性增强。这主要是因为具有高塔曼温度的CaZrO3均匀分散在CaO晶粒之间组成稳定的结构骨架,有效地抑制了CO2晶粒间的熔化烧结。
References
[1] Romano M C. Modeling the carbonator of a Ca-looping process for CO2capture from power plant flue gas [J]., 2012, 69 (1): 257-269
[2] Wang J, Manovic V, Wu Y, Anthony E J. A study on the activity of CaO-based sorbents for capturing CO2in clean energy processes [J]., 2010, 87 (4): 1453-1458
[3] Qiao Chunzhen (乔春珍), Wang Baoli (王宝利), Xiao Yunhan (肖云汉). Activity decline of Ca-based CO2absorbent in repetitive calcination-carbonation [J].(化工学报), 2010, 61 (3): 720-724
[4] Chen Hongwei (陈鸿伟), Zhao Zhenghui (赵争辉). Sequential SO2/CO2capture using CaO-based sorbents reactivated by steam [J].(化工学报), 2012, 63 (8): 2566-2575
[5] Anthony E J. Ca looping technology: current status, developments and future directions [J].., 2011, 1 (1): 36-47
[6] Liu Wenqiang, Low N W, Feng B,. Calcium precursors for the production of CaO sorbents for multicycle CO2capture [J]...., 2010, 44: 841-847
[7] Lu Hong, Khan Ataullah. Relationship between structural properties and CO2capture performance of CaO-based sorbents obtained from different organometallic precursors [J]., 2008, 47: 6216–6220
[8] Lu Hong, Khan Ataullah. Flame-made durable doped-CaO nanosorbents for CO2capture [J]., 2009, 23: 1093-1100
[9] Chen Huichao (陈惠超), Zhao Changsui (赵长遂), Shen Peng (沈鹏). Effect of stream in flue gas on CO2capture for calcium based sorbent [J].(化工学报), 2013, 64 (4): 1364-1372
[10] Zhang Mingming (张明明), Peng Yunxiang (彭云湘). Preparation of ternary composite Ca-based material CaO-Ca3Al2O6-MgO for high-temperature CO2capture [J].(化工学报), 2014, 65 (1): 227-236
[11] Lu Hong, Smirniotis P G. Calcium oxide doped sorbents for CO2uptake in the presence of SO2at high temperatures [J]., 2009, 48: 5454-5459
[12] Reddy E P, Smirniotis P G. High-temperature sorbents for CO2made of alkali metals doped on CaO supports [J]., 2004, 108 (23): 7794-7800
[13] Bhatia S K, Perlmutter D D. Effect of the product layer on the kinetics of the CO2-limereaction [J]., 1983, 29 (1): 79-86
[14] Dudek Magdalena. Electrical properties of stoichiometric and non-stoichiometric calcium zirconate [J]., 2003, 157: 183-187
[15] Guo Mingnü (郭名女). Cyclic reaction characteristic of co-capture CO2/SO2and kinetic study for synthesized anti-sintering calcium-based sorbents[D]. Chongqing: Chongqing University, 2011
[16] Manovic V, Anthony E J, Grasa G, Abanades J C. CO2looping cycle performance of a high-purity limestone after thermal activation/doping [J]., 2008, 22 (5): 3258-3264
[17] Wu S F, Lan L Q. A kinetic model of nano-CaO reactions with CO2in a sorption complex catalyst [J]., 2012, 58 (5): 1570-1577
[18] Kwang Bok Yi, Chang Hyun Ko, Jong-Ho Park. Improvement of the cyclic stability of high temperature CO2absorbent by the addition of oxygen vacancy possessing material [J]., 2009, 146: 241-247
[19] Judd M D, Pope M I. Formation and surface electron-emission properties of coatings [J]...., 1970, 20: 384-388
[20] Broda Marcin, Müller Christoph R. Sol-gel-derived, CaO-based, ZrO2-stabilized CO2sorbents [J]., 2014, 127: 94-100
Effect of Ce, Zr on cyclic performance of CaO-based CO2sorbents
ZHANG Lei1,2, ZHANG Li1,2, YAN Yunfei1,2, YANG Zhongqing1,2, GUO Mingnü1
(1Key Laboratory of Low-grade Energy Utilization Technologies and Systems, Ministry of Education, Chongqing University, Chongqing 400044, China;2School of Power Engineering, Chongqing University, Chongqing 400044, China)
CaO-based sorbents withCe and Zr as dopants were prepared by the method of wet mixing and subsequent calcination. The cyclic CO2sorption/desorption performance of 24 sorbents was tested with thermogravimetric analyzer (TGA). CeO2could increase CO2sorption rate in the diffusion-controlled regime because the large quantity of oxygen vacancies in CeO2could facilitate CO2diffusion through the produced CaCO3layer and then react with the uncreated CaO. Dispersion of CeO2on CaO could also inhibit agglomeration of CaO crystal and its sintering at high temperature. Stability of CaO in sorption/desorption cycle increased with increasing amount of CeO2in the sorbents. With a high Tammann temperature, the newly produced CaZrO3from zirconia and calcium oxide could serve as a supporting framework and effectively restrain sintering.
oxygen vacancy; CaO-based sorbent; adsorption; CO2capture; conversion; stability
2014-07-16.
Prof. ZHANG Li, lizhang@cqu.edu.cn
10.11949/j.issn.0438-1157.20141071
TK 09
A
0438—1157(2015)02—0612—06
中央高校基本科研业务费专项资金(CDJZR12140034);低品位能源利用技术及系统教育部重点实验室访问学者基金项目(LLEUTS-201301)。
2014-07-16收到初稿,2014-09-28收到修改稿。
联系人:张力。第一作者:张雷(1988—),男,硕士研究生。
supported by the Fundamental Research Funds for the Central Universities (CDJZR12140034), the Key Laboratory of Low-grade Energy Utilization Technologies and Systems, Ministry of Education of PRC, the Fund for Visiting Scholars (LLEUTS-201301).
