配合物[Cu(Mba)2(Im)2]的水热合成、晶体结构和量子化学研究
2015-09-26陈志敏杨颖群毛芳芳邝代治曾荣英
陈志敏,杨颖群,毛芳芳,邝代治,曾荣英
(1.衡阳师范学院化学与材料科学学院,湖南衡阳 421008;2.衡阳师范学院功能金属有机材料湖南省普通高等学校重点实验室,湖南衡阳 421008)
配合物[Cu(Mba)2(Im)2]的水热合成、晶体结构和量子化学研究
陈志敏1,2,杨颖群1,2,毛芳芳1,邝代治1,2,曾荣英1
(1.衡阳师范学院化学与材料科学学院,湖南衡阳 421008;2.衡阳师范学院功能金属有机材料湖南省普通高等学校重点实验室,湖南衡阳 421008)
通过水热法,由Hmba(Hmba=methoxybenzoic acid)、Im(Im=imidazole)与Cu2+离子反应,合成标题配合物[Cu(Mba)2(Im)2]。单晶X射线衍射分析表明,晶体属单斜晶系,空间群为P2(1)/c,晶胞参数:a =1.429 64(4)nm,b=1.147 34(3)nm,c=1.356 92(3)nm,β=102.789(2)°,V=2.170 52(1)nm3,Z =4,μ(Mo Kα)=10.54 cm-1,F(000)=1 036,R1=0.037 4,w R2=0.093 0[I>2σ(I)]。在配合物中,中心铜原子与配位原子构成四配位的变形平面四方形构型。最小不对称单元间通过芳环间的π-π堆积、C-H …π弱相互作用和氢键,构筑成三维网状结构。此外,利用量子化学Gaussian03程序包,在lanl2dz基组上,研究了标题配合物的稳定性、配合物的分子轨道能量以及前沿分子轨道的成键特征。
水热合成;铜 (Ⅱ)配合物;晶体结构;量子化学
铜是生物体的微量金属元素,是一些重要酶的活性中心,起着生物电子的递传、氧分子的输运,以及超氧负离子的清除等重要作用[1]。芳香基羧酸类配体具有一定的刚性、稳定性和丰富的配位模式,常与铜等过渡金属离子构筑结构新颖、性能特殊的配合物,因而在结构化学、配位化学、生物无机化学、医药、催化、材料等领域备受关注[2-10]。我们利用过渡金属铜离子与4-甲氧基苯甲酸等配体反应合成了标题配合物,以便进一步探索该类配合物的结构,以及结构与性能的关系 。研究表明,中心铜原子处于变形平面四边形环境中,且最小不对称单元间,通过氢键、π-π堆积和C-H…π相互作用构成了三维网状结构。同时采用密度泛函理论(DFT)的b3lyp法,对配合物进行了单点能计算,在此基础上探讨了配合物的稳定性、配合物的分子轨道能量,以及前沿分子轨道组成和成键特征。
1 实验
1.1仪器与试剂
4-甲氧基苯甲酸{Hmba},分析纯,中国医药集团化学试剂公司;咪唑(Im),分析纯,天津市科密欧化学试剂开发中心,其它试剂均是分析纯。Rigaku 007型X射线单晶衍射仪,日本岛津FTIR-8700红外光谱仪(4000~400cm-1)。
1.2配合物的合成
将0.3 mmol的Hmba和0.3 mmol的Im溶于乙醇水溶液(体积比1∶1)中,调节溶液p H值约为5,于容器内加入0.15 mmol Cu(Cl O4)2,搅拌。然后将反应混合物转移至聚四氟乙烯内衬的不锈钢反应釜中,于130℃下晶化24小时,冷却至室温,数日后得深蓝色立方晶体。IR主要吸收峰(KBr压片,υ/cm-1):3 132.2(s),1 631.7(m),1 604.7 (Vs),1 560.3(w),1 521.7(m),1 427.2(s),1 398.3(Vs),1 251.7(s),1 143.7(m),1 026.1(m),846.7(m),783.0(m),721.3(m),628.8(m),513.0.(w),405.5(w)。
1.3配合物的晶体结构分析
于296(2)K,在Rigaku 007型单晶衍射仪上,用石墨单色化的MoKα射线(λ=0.071 073 nm),对0.20 mm×0.20 mm×0.20 mm尺寸的单晶,以ω~2θ方式进行扫描,在2.30≤θ≤27.51范围内共收集18 598个衍射强度数据,其中4 932个独立衍射点(Rint=0.0248),I>2σ的可观察衍射点3 788个。运用SHELXL-97程序,由直接法解析结构,并用全矩阵最小二乘法对结构加以精修,以理论加氢法确定氢原子在晶胞中的位置。晶体学数据列于表1。
CCDC:822102。
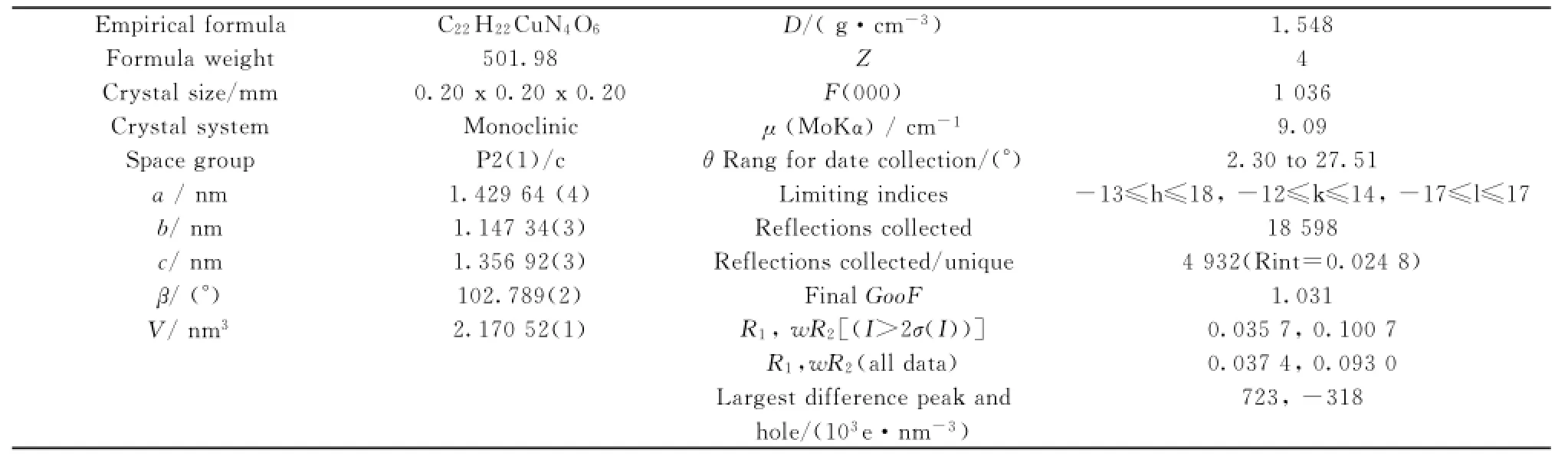
表1 配合物的晶体学数据Table 1 Crystallographic Date of the Title Complexes
2 结果与讨论
2.1晶体结构描述
配合物[Cu(Mba)2(Im)2]含有2个Mba和2 个Im,中心Cu(1)原子与2个Mba的2个羧基氧原子、2个Im的2个氮原子形成4配位的平面四方形构型(见图1)。由表2知,Cu(1)-N平均键长0.199 51 nm(Cu(1)-N(1)0.199 96 nm,Cu(1)-N(3)0.199 06 nm)大于Cu(1)-O平均键长0.193 58 nm(Cu(1)-O(1)0.192 39 nm,Cu(1)-O(4)0.194 78 nm),说明配体Mba羧基氧的配位能力强于Im的N原子。配位平面原子间的夹角分别为:O(1)-Cu(1)-N(1)89.53(7)°、O(1)-Cu (1)-N(3)91.03(7)°、O(4)-Cu(1)-N(3)90.95 (7)°、O(4)-Cu(1)-N(1)91.69(7)°,夹角之和为363.2°,与360.0°偏离3.2°。且Cu(1)、O(1)、N (1)、O(4)、N(3)原子的平面方程为:0.359x+ 11.470y-0.109z=-1.242 7,各原子偏离最小二乘平面值依次为:-0.008 50、-0.023 81、0.027 65、-0.022 97、0.027 62 nm,平均偏差为0.022 11 nm,由上说明O(1)、N(1)、O(4)、N(3)与Cu(1)原子基本处于同一平面。O(1)-Cu(1)-O(4)、N (3)-Cu(1)-N(1)键角分别为171.17(8)°、159.10(8)°,二者均偏离180°,上数据可说明上述几何体为变形平面四边形。
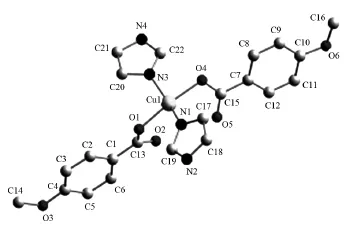
图1 [Cu(Mba)2(Im)2]的结构(氢原子被省略,椭球率为35%)Fig.1 Structrue of complex[Cu(Mba)2(Im)2]. -molecules.Hydrogen atoms have been omitted for clarity.Thermal ellipsoids are drawn at the 35% probability level.
在晶体中,最小不对称单元相互交错重叠堆砌,此间存在着氢键、π-π堆积,以及C-H…π等相互作用(见表3)。相邻单元之间,两Im环错位面对面重叠,两平面的二面角为2.5°,平面垂直距离为0.311 81 nm,质心间距为0.359 71(1)nm。以此作用,最小不对称单元延伸为链状结构。而链间,Mba的甲基与Mba的苯环之间存在C-H…π相互作用[11],两环相隔距离为0.339 23(2)nm。由此弱相互作用,链延伸为层状结构。在层间,Mba的羰基氧与Mba的苯环H之间存在氢键,由此作用,层则延伸为有序的三维网状结构(见图2)。显然,氢键、π-π堆积和C-H…π相互作用的存在增加了晶体的稳定性。
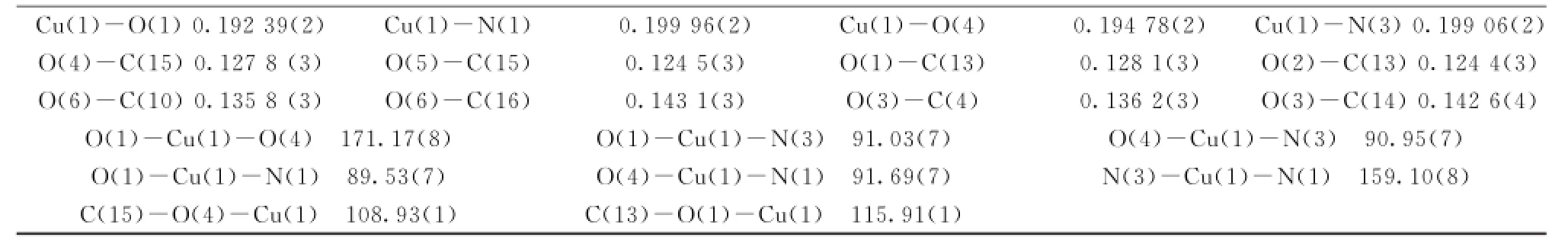
表2 配合物的部分键长和键角Table 2 Selected of Bond Lengths(nm)and Angles(°)
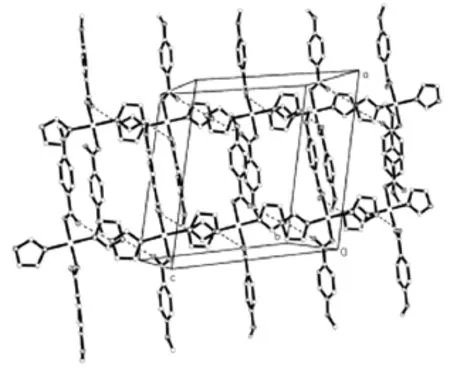
图2 配合物的晶胞堆积图Fig.2 Packing diagram of the complex

表3 配合物的氢键和键角Table3.hydrogen-Bonds and angles for complex[nm and°]
2.2量子化学研究
运用Gaussian 03程序,在B3LYP/lanl2dz基组水平上,以晶体结构中原子坐标为依据,对配合物进行量子化学单点计算。计算涉及55个原子,354个原子基函,941个初始高斯函数,125个α电子,124个β电子,系统电荷为0,多重度为2。全部计算在P4计算机上完成。
2.2.1配合物的能量和前沿分子轨道组成
计算得标题化合物的最高占据轨道HOMO能量为-0.204 20 a.u,最低空轨道LUMO能量为-0.00658 a.u,两前沿轨道能量间隙△E(EHOMOELUMO)为0.197 62 a.u,配合物的总能量为-1 717.494 15 a.u,。由于体系能量和前沿占据轨道能量均较低,说明该配合物基态较稳定[12-13]。此结论与实验结果相吻合。
为分析配合物的电子结构和成键特征[14],采用参与组合的各类原子轨道系数的平方和表示该部分在分子轨道中的贡献,并经归一化。将配合物的原子分为7个部分:(a)铜原子Cu,(b)氮原子N,(c)羧基氧原子O(Ⅰ),(d)甲氧基氧原子O(Ⅱ),(d)Mba碳原子C(Ⅰ),(e)Im碳原子C(Ⅱ),(f)氢原子H。前沿占据轨道和未占轨道各取5个,计算结果见表4和图3。
计算结果可反应各类原子轨道对前沿分子轨道的贡献。在配合物的最高占据轨道HOMO中,贡献较大的有(%):羧基氧原子44.132 12,Mba碳原子42.803 97(其中苯环碳原子为40.344 16),甲氧基氧原子11.033 85,其它原子的贡献均较少;在最低未占轨道LUMO中,贡献较大者分别为(%):Mba碳原子60.72864(其中苯环碳原子53.156 61),咪唑碳原子14.155 24,氮原子10.051 45,羧基氧原子9.015 75,其它原子贡献较少。由此可说明,配体Mba的羧基氧原子、苯环碳原子以及甲氧基氧原子是HOMO轨道的主要贡献者,这些较大占有轨道成分的配位原子在反应中易给出电子,成为反应的活性部位;LUMO轨道的主要贡献者为配体Mba的苯环碳原子、羧基氧原子、羧基碳原子,以及Im的氮原子和碳原子。比较HOMO和LUMO轨道成分,显然各原子轨道对二者的贡献变化较明显,知当电子从HOMO激发到LUMO轨道时,主要是配体Mba的羧基氧原子和甲氧基氧原子的电子向Mba的碳原子,以及Im的氮原子、碳原子轨道转移,形成电荷转移激发态配合物。此外,苯环碳原子对HOMO轨道的贡献较大,为40.344 16%,说明苯环具有好的共轭离域性和稳定性;羧基碳和甲氧基碳的贡献分别为:2.314 45%、0.145 36%,说明羧基、甲氧基与苯环的共轭作用小。
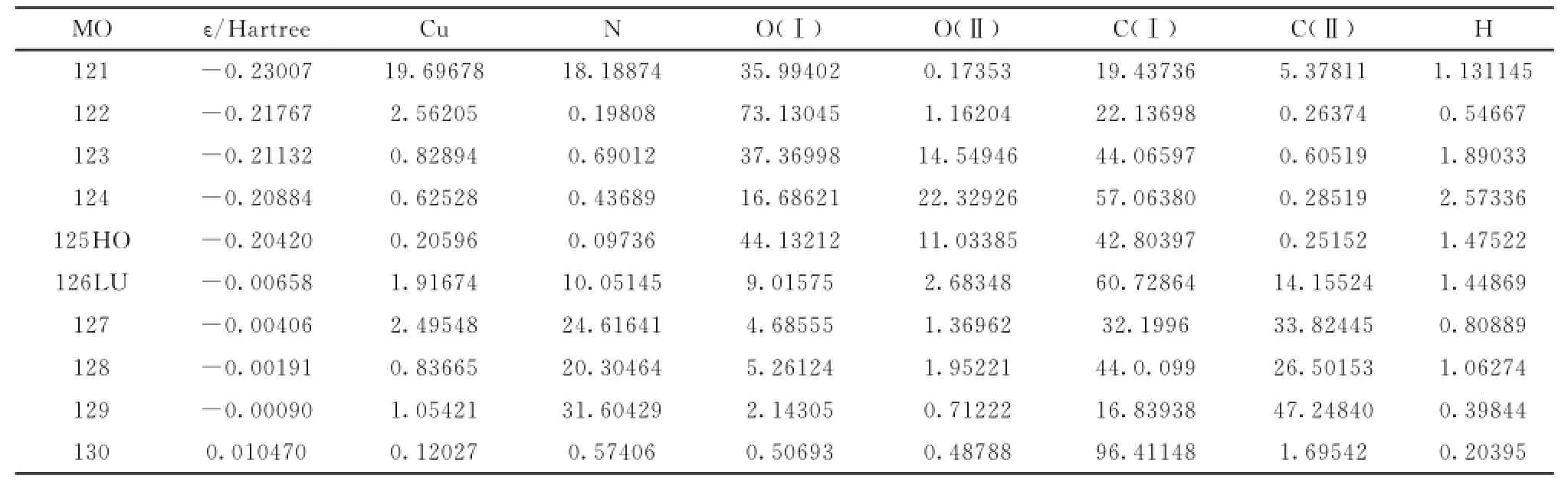
表4 前沿分子轨道组成/%Table 4 The calculated some f rontier molecular orbitales composition of complex/%
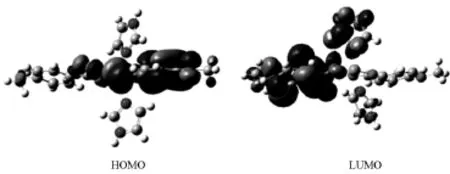
图3 配合物前沿分子轨道示意图Fig.3 The schematic diagram of frontier MO for the complex
2.2.2电子结构布居分析(原子净电荷布居分析)
由Mulliken布居分析得结构单元的原子静电荷,见表5,由此知:(1)铜原子、氢原子、不连氢的碳原子均带正电荷,氧原子、氮原子、连接氢的碳原子均带负电荷;(2)+2价铜离子配位后,净电荷为0.650 341,说明O、N原子对Cu2+的明显配位给电子作用,也可以预见此配合物中铜离子仍具有成键能力,会显示出一定的活性;(3)铜原子的配位原子所荷净电荷分别为:O(1)-0.489 284、O(4)-0.513 307、N(1)-0.237 019、N(3)-0.233 909,表明铜原子分别通过Cu-O、Cu-N键将电荷转移给了O原子、N原子,于是这些键具较强的极性;(4)H(5)、H(6)带较多正电荷,分别为0.331 723、0.364 057,可与相邻单元的氧原子形成分子间氢键,此与实验结果相一致(见表3)。

表5 配合物的原子电荷Table 5 Atomic charge populations of complex
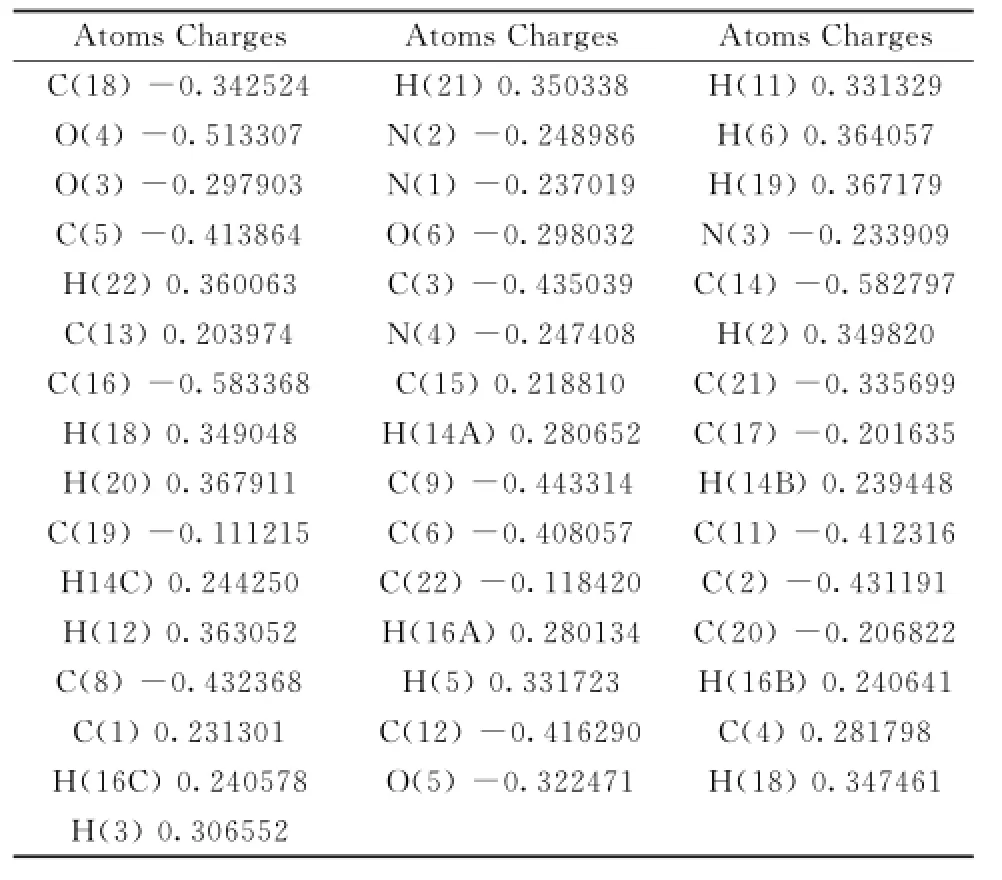
续表
2.3配合物的红外光谱研究
在标题配合物中,自由配体Hmba的υC=O(COOH)(1 695.0 cm-1)和υC-O(COOH)(1 026.0 cm-1)吸收峰消失,出现了吸收峰υas(COO)(1 604.7 cm-1)和υs(COO)(1 398.3 cm-1),表明配体Hmba的羧基氧原子与中心铜离子配位,且Δυ=υas-υs=206.4 cm-1,Δυ>200 cm-1,进一步说明羧基氧以单齿形式与中心离子配位[2]。配体Im的特征吸收峰υ(C=N)1 668.3cm-1,在配合物中红移至1 635.5 cm-1,说明Im中的3位N原子与Cu2+配位[5,15]。显然,红外分析与晶体结构分析所得结论一致。
[1]孙为银.配位化学[M].北京:化学工业出版社,2004.
[2]陈志敏,张复兴,曾荣英,等.[Cu(m-NBA)(2,2′-bipy)(H2O)].m-NBA.H2O的合成、晶体结构及电化学性质[J].无机化学学报,2009,25(3):548-551.
[3]石敬民,廖代正,程鹏,等.2-溴代对苯二甲酸根桥联双核钴(Ⅱ)配合物的合成、磁性及抗癌活性[J].无机化学学报,1996,12(4):372-376.
[4]朱恩静,刘琦,陈群,等.二维层状铜配位聚合物[Cu2(TFBDC)2(DMF)2]2.3MeOH·2DMF的合成、晶体结构和磁性(TFBDC=四氟对苯二甲酸根;DMF=N,N-二甲基甲酰胺)[J].无机化学学报,2008,24(9):1428-1433.
[5]李东平,陈志敏,匡云飞,等.配合物[Cu(NPA)2(Im)2(H2O)]·H2O的合成、晶体结构及电化学性质[J].无机化学学报,2007,23(5):892-896.
[6]杨颖群,李昶红,李薇.化合物Mn(C6H4O2N)2(H2O)4的水热合成、晶体结构及量子化学计算[J].计算机与应用化学,2010,27(12):1669-1672.
[7]陈志敏,邹建陵,杨颖群,等.基于大茴香酸与邻菲咯啉的异双桥联双核铜配合物的水热合成、结构、荧光和电化学性质[J].无机化学学报,2011,27(11):2167-2171.
[8]S.Youngme,J.Phatchimkun,N.Wannarit,et al.New ferromagnetic dinuclear triply-dyidged Copper(Ⅱ)compouns containning carboxylato bridges:Synthesis,X-pay structure and magnetic properties[J].Polyhedron,2008,27(1):304-318.
[9]安金,陈志达,卞江,等.混合价十二核锰配合物的合成、结构及磁性研究[J].北京大学学报:自然科学版,2000,36(4):439-447.
[10]Chen Z M,Feng Y L,Yang Y Q,et al.Hydrothermal synthesis,crystal structure and fluorescence properties of a three-dimensional triply-bridged binuclear zinc(Ⅱ)complex[Zn2(Mba)3(Phen)2EtOH)]·ClO4[J].Chinese J.Struct.Chem.,2012,31(12):1803-1809.
[11]郭辉瑞,陶朱,祝黔江,等.配位化学中的C-H…π非键弱相互作用[J].无机化学学报,2002,18(5):435-441.
[12]石智强,季宁宁,何国芳,等.以邻氯苯甲酸及联吡啶为配体的双核铜配合物的水热合成、晶体结构及量子化学研究[J].无机化学学报,2011,27(8):1507-1512.
[13]邝代治,冯泳兰,许金生,等.茂金属配合物[(eat5-C5H4R)Mo(CO)3]2(R:SiMe3,Si2Me5)的电子结构研究[J].化学物理学报,2003,16(1):59-63.
[14]邝代治,冯泳兰,张复兴,等.铜(11)配合物[Cu(pydc)(H2O)]2:合成、结构和量子化学的研究[J].计算机与应用化学,2008,25(3):319-322.
[15]杨一心,杨宜康,白晋涛,等.稀土与丙氨酸、咪唑三元配合物的FTIR和UV/VIS光谱[J].光子学报,2002,31(9):1120-1123.
On Hydrothermal Synthesis,Crystal Structure and Theoretical Calculation of Complex[Cu(Mba)2(Im)2]
CHEN Zhi-min1,2,YANG Yin-qun1,2,MAO Fang-fang1,KUANG Dai-zhi1,2,ZENG Rong-ying1
(1.College of Chemistry and Materials Science,Hengyang Normal University,Hengyang Hunan 421008,China;2.Key Laboratory of Functional Organometallic Materials of Universities in Hunan Province,Hengyang Normal University,Hengyang Hunan 421008,China)
The novel complex[Cu(Mba)2(Im)2]has been hydrothermally synthesized by Hmba and Im with copper(II),where Hmba=methoxybenzoic acid and Im=imidazole.The crystal structure of the complex has been determined by X-ray diffraction .The crystal belong to monoclinic system,space group P2(1)/c.The cell parameters are:a=1.429 64(4)nm,b=1.147 34 (3)nm,c=1.356 92(3)nm,β=102.789(2)°V=2.170 52(1)nm3,Z=4,μ(Mo Kα)=10.54 cm-1,F(000)=1 036,R1=0. 037 4,w R2=0.093 0[I>2σ(I)].The centric copper(Ⅱ)ions are four-coordinated in the distorted planar tetragon arrangement for the complex.Three-dimensional network is formed through weak interaction ofπ-πpacking,C-H…π,and hydrogen bonds.The study on the complex has been performed with quantum chemistry calculation by means of Gaussian 03 software package and taking Lanl2dz basis set.The stabilities of the complex,the orbital energies and bonding characteristics of some frontier molecular orbital have been investigated.
ydrothermal synthesis;copper(Ⅱ)complex;crystal structure;quantum chemistry
O614.121
A
1673-0313(2015)06-0001-05
2015-10-23
功能金属有机材料湖南省普通高等学校重点实验室开放基金资助项目(13 K07);衡阳师范学院省级平台开放基金项目(GN15K02);“材料物理与化学”湖南省十二五重点建设学科资助;“功能金属有机化合物”湖南省高校科技创新团队资助;功能金属有机材料湖南省普通高等学校重点建设实验室资助
陈志敏(1956-),女,湖南长沙人,教授,主要从事配位化学的研究。
