邻苯二甲酸与铜镍配合物合成与光谱性质
2015-08-02赵文通禹元元
赵文通,禹元元,武 文
(周口师范学院 化学化工工学院,河南 周口466001)
邻苯二甲酸因有两个羧基,具有较强的配位能力,可以作为构建超分子的有效多原子桥基,四个羧基氧能以多种方式与金属离子配位[1].铜是一种重要的生命元素,其结构变化奇异、特殊的性质及配位数引起了科学工作者的兴趣.随着医药化学的发展,铜配合物的药用价值亦越来越引起人们的重视.不仅如此,铜配合物还在信息贮存、催化等方面有重要的价值.近年来,镍配合物的应用成为相当活跃的一个领域,尤其是镍酶有关配合物的应用得到了显著发展.除此之外,镍配合物在材料、催化、磁性材料以及光学性质方面都有重要的研究意义.邻苯二甲酸的金属配合物在热敏变色和彩色热敏记录材料及光电器件透明封装材料等方面也有重要应用价值[2-4].
邻苯二甲酸盐是一种非常典型的芳香族羧酸盐,对其热分解的研究同样具有上述的意义.邻苯二甲酸铜、镍的配合物的合成方法主要有流变相反应法、室温固相反应法和固液法等[5].邻苯二甲酸的铜配合物和镍配合物随制备方法和反应条件不同,可得到具有不同磁性质的多种变体[6].室温固相合成法的优势和其最大的特点是操作简便、反应速度快、选择性好、产率高以及污染少等,且作为一种绿色的化学合成手段日益受到重视[7].因此本文以邻苯二甲酸为配体,分别采用室温固相研磨法和流变相反应成功地合成了邻苯二甲酸铜配合物和邻苯二甲酸镍配合物,并对其组成、结构等进行了表征,取得了比较满意的结果.
1 实验部分
1.1 实验所用仪器及试剂
WQF-510型红外光谱,磁力搅拌器,电子天平,Lambda25紫外可见分光光度计;邻苯二甲酸(C8H4O4),邻苯二甲酸氢钾(C8H5KO4),六水合氯化镍(NiCl2·6H2O)二水合氯化铜(CuCl2·2H2O),无水乙醇,蒸馏水.所有试剂均为AR.
1.2 配合物的合成
室温固相合成:用分析天平准确称取后,将1.661 3g固体邻苯二甲酸与1.688 8g固体六水合氯化镍(NiCl2·6H2O)与 (C8H6O4)以1∶1的物质的量比混合,在室温常压下研磨,反应物经研磨2h后,开始变得黏稠许多,用钥匙不断翻松,然后继续研磨1h,结束其反应.将所得产物置于电热鼓风干燥箱内干燥1h,用少量乙醚分3次洗涤,抽滤,在30℃下干燥,得到草绿色的产品.用同样的方法将1.661 3g固体邻苯二甲酸(C8H6O4)与二水合氯化铜(CuCl2·2H2O)以1∶1的物质的量比混合合成得到淡蓝色的产品.
流变相反应合成:将2.046 3g邻苯二甲酸氢钾配成溶液,然后按照等物质的量与六水合氯化镍溶液(NiCl2·6H2O)混合,用磁力搅拌器在不停搅拌下缓慢反应.(控制温度60~70℃,pH=4.5~5.0),生成沉淀,恒温静止1.5h,抽滤,用乙醇洗涤3次,烘干,得到产品.同样的操作步骤可得到邻苯二甲酸的铜的配合物.
2 结果与讨论
2.1 不同方法对配合物产率的影响
在相同实验条件下,分别对上述两种不同的方法合成的样品进行比较和分析:当采用室温固相合成方法时,邻苯二甲酸镍的配合物和邻苯二甲酸铜的配合物能分别达到85.5%和80.3%的最高产率.而当采用流变相反应合成方法时,产率分别是73.2%和74.7%.因此,在室温条件下,可通过固相研磨法高产率合成邻苯二甲酸的铜镍配合物,且该法操作简单,反应速度较快,是一种绿色的合成方法.
2.2 配合物的红外光谱分析
为研究配合物的成键方式,以KBr为基质,在500~4 000cm-1范围内测定了邻苯二甲酸的镍配合物的红外光谱,如图1所示.配合物中羧基的反对称υas(coo-)和 对 称υs(coo-)吸收频率的差值(△υ)约为150cm-1,由于其小于自由配体△υ自由,由此可推断出羧基与 Ni2+是以双齿桥式配位[8].另外,位于3 500cm-1处的吸收峰推断为结晶水的伸缩振动,位于480cm-1处的吸收峰可归属为Ni-O伸缩振动[9],表明Ni与O形成了配位键.
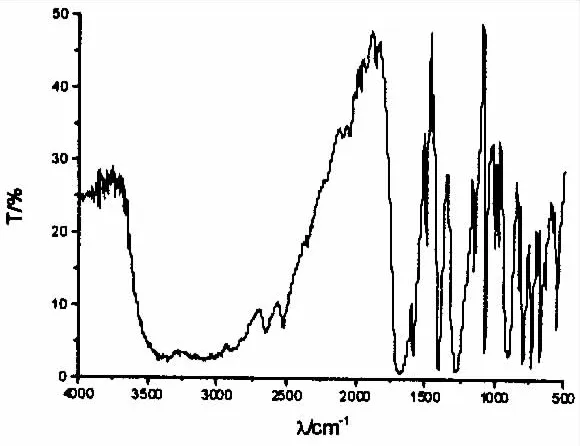
图1 邻苯二甲酸镍配合物的红外光谱
同样,以KBr为基质,在500~4 000cm-1范围内测定了邻苯二甲酸的铜配合物的红外光谱如图2.配合物中羧基的反对称υas(coo-)和对称υs(coo-)吸收频率的差值(△υ)大约为140cm-1,小于自由配体△υ自由,可推断出羧基与Cu2+是以双齿桥式配位.另外,约3 050cm-1处宽而强的吸收峰为产物中水的伸缩振动吸收峰,而且1 620cm-1处为水的变形振动吸收峰.
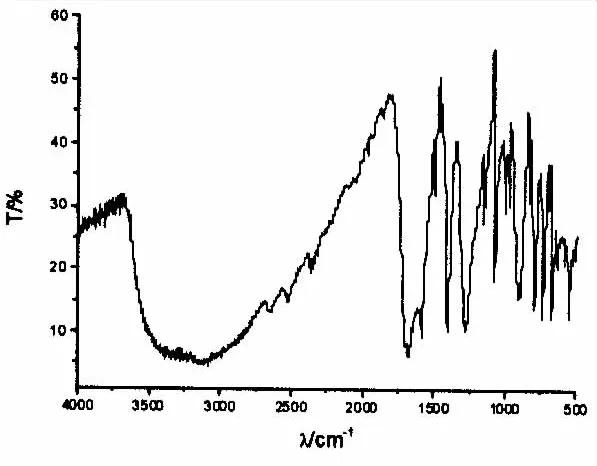
图2 邻苯二甲酸铜配合物的红外光谱
邻苯二甲酸与金属中心离子在羧基位置发生配位.当羧基失去质子之后,与碳原子连接的两个氧原子几乎是相同的,降低了原来的C=O键的特征,使吸收峰发生红移,从而使原C-O键的双键特征增强,于是吸收频率蓝移.羧基的反对称伸缩振动在1 620~1 540cm-1,其强度较大,是特征吸收峰;对称伸缩振动(1 430~1 370cm-1)强度相比于反对称伸缩振动较弱一些,也是其特征吸收.苯环(C-C)振动特征吸收峰出现在1 500cm-1及1 600cm-1附近,且由于苯环与羧基发生共轭,使得谱带发生分裂,强度亦增强[10].
在相同的条件下,以1∶1的原料配比合成时,得到的两种配合物IR图谱基本相同,吸收频率几乎一致.并且,邻苯二甲酸镍的配合物和邻苯二甲酸铜的配合物的红外光谱图吸收峰较少,说明两种配合物结构基本相似,而且对称性较高.
2.3 配合物的紫外光谱分析
将得到的邻苯二甲酸镍的配合物加蒸馏水配成溶液,进行紫外吸收光谱分析.其紫外吸收光谱见图3.

图3 邻苯二甲酸镍配合物的紫外吸收光谱
由图3可知,邻苯二甲酸镍的配合物在紫外区有明显的吸收峰,最大特征吸收峰在270nm处,此峰归属于羧基上n→π*跃迁.与羧基的特征吸收峰204nm相比,偏移了66nm,可能是由于苯环和羧基中的C=O键共轭从而使吸收峰发生转移[11];270nm处的吸收峰的出现归结于C-O键的π→π*跃迁[12].将得到的邻苯二甲酸铜的配合物加蒸馏水配成溶液,进行紫外吸收光谱分析.其紫外吸收光谱见图4.

图4 邻苯二甲酸铜配合物的紫外吸收光谱
由图可知:苯二甲酸铜的配合物在紫外区有明显的吸收峰,其最大特征峰在280nm处,此峰归属于羧基上n→π*跃迁.与羧基的特征吸收峰204 nm相比,偏移了76nm,可能是由于苯环和羧基中的C=O键共轭从而使吸收峰发生转移;280nm处的吸收峰的出现归结于C-O键的π→π*跃迁.
邻苯二甲酸的铜的配合物在紫外区有明显的吸收峰且吸收强度与图3中邻苯二甲酸镍的配合物基本相同.对比得知,两种配合物的紫外吸收峰型相似,这与红外光谱图的结果一致.
2.4 配合物的荧光光谱分析
在室温下,入射光和发射光狭缝宽度均为3 nm时,测定了邻苯二甲酸的镍的配合物的荧光激发和发射光谱.其图谱见图5、图6.
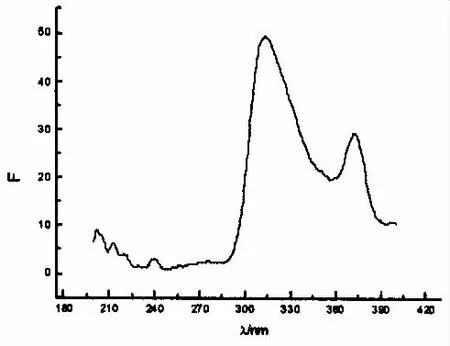
图5 λem=425nm时,邻苯二甲酸镍配合物的激发光谱
λex=310nm时,邻苯二甲酸镍的配合物出现最大放射吸收峰,有较强的荧光强度,并且在这两个波长处的荧光性质基本相同.在两最大激发波长处,其发射波长都为425nm.同样,在室温下,入射光和发射光狭缝宽度均为3nm时,测定了邻苯二甲酸的铜的配合物的荧光激发和发射光谱.其图谱见图7、图8.

图6 λex=310nm时,邻苯二甲酸镍配合物的发射图谱

图7 λem=425nm时,邻苯二甲酸铜配合物的荧光图谱

图8 λex=370nm时,邻苯二甲酸铜配合物的荧光图谱
由图8得知,λex=370nm时,邻苯二甲酸铜的配合物出现最大放射吸收峰,有较强的荧光强度,并且在这两个波长处的荧光性质基本相同.且在两最大激发波长处,其发射波长都为425nm.
通过比较邻苯二甲酸镍的配合物和邻苯二甲酸铜的配合物的荧光激发和发射图谱,得知这两种配合物的荧光性质基本相同.
3 结论
本实验在流变相法合成邻苯二甲酸铜镍配合物的既有方法的基础上,通过室温固相合成邻苯二甲酸的铜镍配合物,以此比较两种方法在产率方面的优劣,得出室温固相合成配合物是更简便,更高效,更绿色的一种方法.研究邻苯二甲酸的铜镍配合物的红外光谱,分析邻苯二甲酸与金属离子的配合方式和结构特点.邻苯二甲酸的铜镍配合物的紫外吸收效果好.λex=310nm和λex=370nm时,邻苯二甲酸铜镍的配合物出现最大放射吸收峰,其发射波长都为425nm.
[1]王春光,李静,李章朋,等.稀土-邻苯二甲酸配合物Eu2(1,2-BDC)3(H2O)n的合成、结构及发光性质研究[J].北华大学学报:自然科学版,2008,9(4):309-313.
[2]沈同,王镜岩,赵邦梯,等.生物化学(上册)[M]2版.北京:高等教育出版社,1990:426.
[3]阳芳,郭红.NaYF4∶Yb,Er/Tm上转换发光强度的影响因素[J].材料导报,2009,23(7):24-27.
[4]Sun Jutang,Chen Chun,Qin Zibin.Terbium and Europium Activated Lanthanum Phthalate Phosphors[J].Journal of Lu-minescence,1988(40 -41):246-247.
[5]罗兆福,杨毅涌,袁良杰,等.酸式邻苯二甲酸铜的合成与晶体结构的研究[J]分析科学学报,2000,16(2):113-117.
[6]宋立,钟鸣,宋玲,等.邻苯二甲酸镍配合物的流变相法合成及热分析[J].信阳师范学院学报:自然科学版,2007,20(2):167-170.
[7]宋力,陈强,张克立.水合碱式苯甲酸铁的流变相法合成及热分解研究[J].化学研究与应用,2006,18(2):195-198.
[8]Taylor M D,Carter C P.The infrared spectra and structure of the rare earth benzoates[J].Journal of Inorganic and Nuclear Chemistry,1968,30(6):1503-1511.
[9]胡付欣,张春霞,郑涛丽.邻苯二甲酸盐(Sr2+)的制备及热分解反应研究 [J].信阳师范学院学报:自然科学版,2004,17(3):285-287.
[10]Pavks,ovic F Anir.Study of benzoate complexes[J].Journal of Inorganic and Nuclear Chemistry,1971,33(5):1475-1479.
[11]崔运成,黄艳菊,杜刚.由邻苯二甲酸和 Medpq配体构筑的锌的配合物的水热合成及晶体测定[J].无机化学学报,2009,25(4):734-737.
[12]Burtis CA,Ashwood ER.Tietz textbook of clinical chemistry [M].Philadelphia:W B Saunders,1998:1570-1572.
