利用B-Z化学振荡体系检测原花青素
2015-07-25赖红伟徐明吴博听姜涛陶然王宇茁杜娟曹宏梅吉林医药学院吉林吉林132013
赖红伟,徐明,吴博听,姜涛,陶然,王宇茁,杜娟,曹宏梅(吉林医药学院,吉林吉林132013)
利用B-Z化学振荡体系检测原花青素
赖红伟,徐明,吴博听,姜涛,陶然,王宇茁,杜娟,曹宏梅*
(吉林医药学院,吉林吉林132013)
摘要:利用原花青素对B-Z振荡体系的扰动,建立测定原花青素的新方法。结合电化学技术,在振荡反应的不同阶段加入原花青素,考察其对振荡参数(诱导期、周期和振幅)的影响。原花青素在一定的浓度范围内,与诱导期时间、振荡周期和振幅的改变量存在良好的线性关系,同时也分析了原花青素可能的振荡机制。
关键词:B-Z振荡;化学振荡;原花青素;测定
原花青素(Proanthocyanidins,简称PC)是一类黄烷醇单体及其聚合体的多酚化合物,广泛存在于各种植物的核、皮或种籽等部位。人们对原花青素的研究已有近50年的历史,尤其是近年来由于其具有优异的抗氧化活性,常被用作天然的功能食品添加剂和食源性防腐剂等[1]。研究发现,原花青素的抗氧化能力是VE的50倍,VC的20倍。另外原花青素还具有显著的清除自由基的能力,故也可作为食源性药物用于疾病的治疗[2-3]。因此,原花青素的检测分析就显得非常重要。诚然,高效液相色谱法和分光光度法早已用于原花青素的检测并已取得了满意的结果,但也存在着自身无法克服的一些弊端[4-5]。
近年来,化学振荡(Chemical oscillations)作为一种新兴的检测技术在化学、食品和药物分析领域中已得到广泛应用[6-7]。化学振荡是一种典型的非平衡非线性现象,在振荡过程中体系中的组分浓度随时间(或空间)发生的是周期性变化[8]。通过被测物与振荡体系中的组分发生的某种相互作用,从而改变振荡参数,因此实现对被测物的定性定量分析[6]。
本文中利用B-Z化学振荡体系研究了原花青素的化学振荡行为,建立了一种简便的测定原花青素的新方法,分析了其可能的振荡机制,这为进一步开发和利用原花青素提供了一定的理论参考。
1 材料与方法
1.1仪器与试剂
原花青素:合肥博美生物科技有限责任公司;丙二酸、溴酸钾、浓硫酸、硫酸铈铵,均为分析纯;水为二次蒸馏水。
新世纪紫外可见分光光度计:北京普析通用仪器有限责任公司;FA1104N型电子分析天平:上海精密科学仪器有限公司;ZH-1C型超级恒温水浴:南京多助科技发展有限公司;KH5200DB型数控超声波清洗器:麗山水利超声有限公司;BZ振荡实验装置:南京多助科技发展有限公司;HJ-1型磁力搅拌器:江苏省金坛市荣华仪器制造有限公司;232型饱和甘汞电极:上海越磁电子科技有限公司;213型铂片电极:天津市兰立科化学电子高技术有限公司;玻碳电极:上海辰华仪器有限公司。
1.2方法
1.2.1构建B-Z振荡体系
在100 mL恒温夹套玻璃反应容器中,以铂电极为工作电极,饱和甘汞电极为参比电极。首先加入一定浓度的丙二酸、H2SO4和KBrO3水溶液各15.00 mL,搅拌均匀,设定温度为37℃且恒温10 min。然后再加入已恒温的一定浓度的硫酸铈铵水溶液15.00 mL,混合液总体积为60.00 mL,同时开始记录电位(E)-时间(t)曲线。1.2.2原花青素对B-Z振荡体系的振动待B-Z振荡体系达稳定后,分别在诱导期处,第7个波峰和第8个波谷处加入一定浓度的原花青素水溶液,观察电位(E)-时间(t)变化并记录振荡曲线。
2 结果与分析
2.1反应条件对振荡图谱的影响
在对阿莫西林的B-Z振荡研究中,我们确定了最优的B-Z振荡条件,本研究中丙二酸、硫酸、溴酸钾和硫酸铈铵浓度分别为0.45、3、0.25 mol/L和4×10-3mol/L[9]。
反应温度对振荡图谱有较大影响[10-11]。根据Arrhenius公式,温度较低时,反应速率常数变小,反应速率减慢,因此诱导时间较长,同时振荡周期也较长,振荡波形亦不稳定。温度较高时,反应速率常数增大,反应速率大大加快,因此诱导时间明显缩短,振荡周期也随之减小。随温度升高,诱导期和周期变化较大,但振幅变化基本不变。因此,为得到规则且稳定的振荡图谱和方便研究原花青素的药代动力学机制,本研究中反应温度为37℃,此温度为人体的正常温度[12]。
搅拌有利于反应物(或产物、中间体)的迅速扩散,反应速率增大,从而影响振荡周期和振幅的变化[13-14]。搅拌速率也影响氧在B-Z振荡体系中的溶解量,溶解氧作为体系中的一种物质有可能参与振荡反应[15]。当搅拌速率增大时,反应器中产生的气泡量增大,会吸附到电极上,在振荡波形上表现为一些无规律的毛刺,因此振荡图谱的稳定性较差。本研究中磁力搅拌器的转速控制在500 r/min,能够保证振荡图谱的稳定性。
2.2原花青素对B-Z化学振荡体系的扰动
原花青素的加入对B-Z振荡体系所产生的影响见图1。

图1 原花青素对B-Z振荡体系的影响Fig.1 The influence of proanthocyanidins on the B-Z oscillating system
由图1可知,在振荡过程的不同阶段加入一定量的等浓度等体积的原花青素水溶液,发现它们的诱导时间、振荡周期和振幅均发生了不同程度的改变。从这3个阶段的诱导时间可知,在诱导期处加入原花青素时诱导时间最长,为162 s,而波峰和波谷处则均为157 s。这表明原花青素可能与丙二酸一起作为B-Z振荡的有机底物参与了振荡反应,因此其振荡波形与波峰和波谷处时有所不同。在波峰和波谷处加入原花青素后,二者振荡波形相似。与原B-Z振荡体系相比,它们振荡周期所持续的时间均明显增加,其中波峰处增加最多。此外,它们的平衡电位都在0.9 V左右。
在B-Z振荡反应的诱导期处加入原花青素之后建立的线性关系见图2。
由图2可知,我们在诱导期处加入原花青素后,当其浓度在8.2×10-3g/L~4.5×10-2g/L范围内时,其浓度与振荡周期的改变量(ΔT)和振幅的改变量(ΔA)之间具有良好的线性关系,

在B-Z振荡过程中的波峰和波谷处加入原花青素之后建立的线性关系见图3。

图2 诱导期处引入原花青素的线性关系Fig.2 The linear relationships for proanthocyanidins at induction period
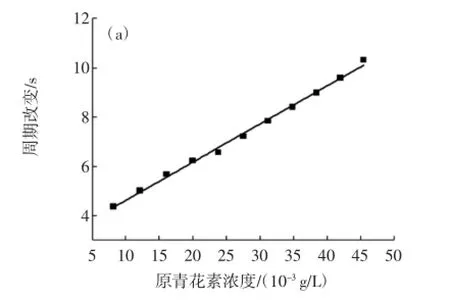
从图3中可知,随原花青素浓度的增加,在波峰处比波谷处的周期增加幅度稍大。当其浓度在8.2× 10-3g/L~4.5×10-2g/L范围内时,周期改变量在4 s~11 s之间,其相应的线性方程分别为
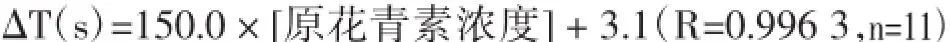

显然,在波峰和波谷处的相关系数均大于在诱导期处的相关系数,这表明了更好的线性关系。此外,在诱导期处加入原花青素,其周期改变量明显大于在波峰和波谷处加入(图2(b))。
为了确保测定原花青素具有较高的准确度和精密度,在各反应条件保持不变的情况下,连续重复了6组试验。对于诱导期、波峰和波谷,经计算它们的相对标准偏差分别为1.5%、1.0%和1.0%,均小于5%,这表明该试验的准确性和重现性良好。原花青素的检测限为1.0×10-4g/L。
以波峰处加入原花青素为例,B-Z振荡体系测定原花青素的稳定性结果如图4所示。
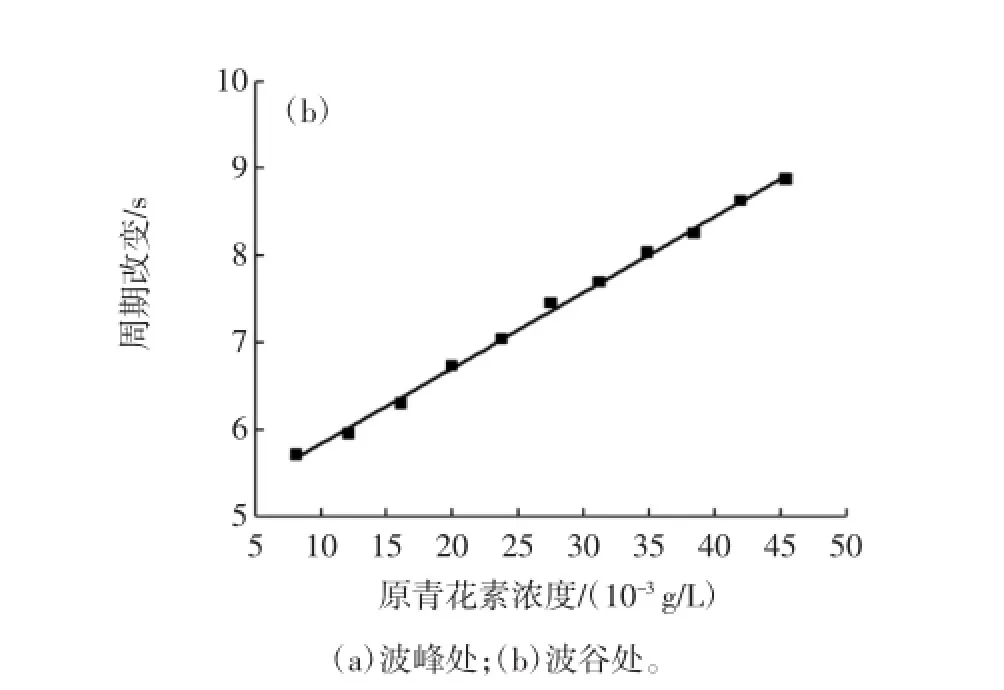
图3 波峰和波谷处引入原花青素的线性关系Fig.3 The linear relationships for proanthocyanidins at peak and valley

图4 原花青素的稳定性Fig.4 The stability of proanthocyanidins
在1 h内原花青素的稳定性下降百分比<1%。而在1 h~2.5 h内,原花青素的稳定性下降较快,接近7%。随后下降趋势比较平缓。以上试验表明,新配的原花青素水溶液需在1 h以内完成测定,否则会出现较大的误差,这与紫外-可见分光光度法的结果是相一致的[16]。
2.3原花青素可能的扰动机理
原花青素是由不同数量的儿茶素和表儿茶素缩合而成的一种多酚类化合物。在各类原花青素中,二聚体分布最广,研究最多,是最重要的一类原花青素。这是因为原花青素的生物活性和聚合度成反比,聚合度越小的原花青素其生物活性越高,低聚体的活性高于高聚体[17]。
由图1可知,在B-Z振荡过程的不同阶段加入原花青素,振荡体系的诱导期时间,振荡周期和振幅都发生了较明显的改变,这表明原花青素可能与振荡体系中的产生的某些组分之间发生了相互作用。原花青素分子中含有大量的酚羟基(Ar-OH),其中B环的邻位酚羟基为主要的还原部位,邻位酚羟基作为H供体可以捕获振荡过程中产生的自由基,自身形成的自由基可以通过形成分子内氢键半醌式自由基甚至邻苯醌等形式,从而对B-Z振荡反应产生扰动[18]。振荡过程中生成的单质溴也易与苯环结构发生亲电取代反应,从而影响Br-离子浓度的变化,因此B-Z反应的振荡周期会发生相应改变。
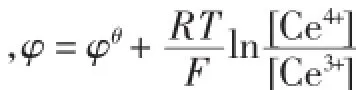
结合FKN机理和高执棣,张泰铭等人提出的振荡机制[19-20],原花青素的振荡反应如下:
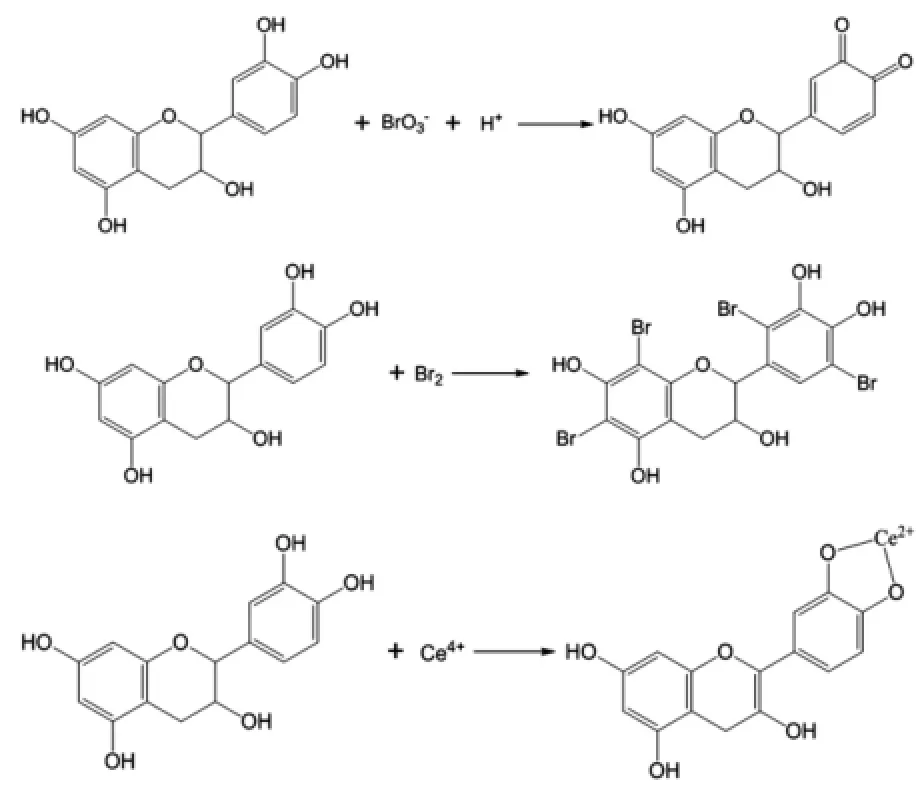
3 结论
本文研究了原花青素对B-Z振荡体系的扰动,根据浓度与振荡周期的改变量之间存在的线性关系,建立了一种检测原花青素的化学振荡新方法。该方法具有仪器设备简单、易于操作、灵敏度高和耗时少的特点。扰动机理的研究表明,原花青素在酸性的条件下可与体系中存在的氧化性成分发生氧化作用,与Ce4+发生络合反应及与溴发生取代反应。显然,这与其独特的酚羟基结构密切相关,并在一定程度上解释了其优异抗氧化性的原因。
参考文献:
[1] 叶春苗.原花青素的提取方法及稳定性研究进展[J].农业科技与装备,2014(7):64-65
[2]石翠芳,孙智达,谢笔钧.沙枣果肉原花青素的提取、纯化及抗氧化性能的研究[J].农业工程学报,2006,22(3):158-161
[3]吴娟,魏和平,许远.原花青素提取工艺的优化及稳定性分析[J].食品工业科技,2010,31(6):103-104,343
[4] 姚开.葡萄籽提取物中原花青素含量不同测定方法比较[J].化学研究与应用,2002,14(2):230-232
[5]Guyot S,Marnet N,Drilleau J F.Thiolysis-HPLC characterization of apple procyanidins covering a large range of polymerization states [J].Journal of Agricultural and Food Chemistry,2001,49(1):14-20
[6]苏适,迟彩霞,王斌,等.化学振荡反应在分析检测中的应用及前景[J].化学世界,2013(10):634-637
[7] 胡刚,刘婷婷.化学振荡在分析化学中的应用综述[J].安徽大学学报(自然科学版),2015,39(2):97-108
[8]辛厚文.非线性化学[M].合肥:中国科学技术大学出版社,1999: 1-3
[9]赖红伟,曹宏梅,董顺福,等.阿莫西林对B-Z振荡反应的影响及其振荡指纹图谱[J].应用化学,2014,31(3):361-366
[10]李村,谢复新,倪诗圣.双四氮杂大环镍(Ⅱ)配合物催化的化学振荡反应[J].无机化学学报,2000,16(1):136-138
[11]任杰,王明强,姬良亮,等.利用BZ化学振荡体系检测中草药中的姜黄素[J].甘肃农业大学学报,2013,48(3):172-175
[12]陈振华,程旺兴,方成武,等.大黄的非线性化学指纹图谱研究[J].分子科学学报,2013,29(3):190-197
[13]王融融,程旺兴,王晓钰,等.半夏的电化学指纹图谱研究[J].化学世界,2013(4):197-200,222
[14]安从俊,方贤安,刘义,等.碘离子对B-Z振荡反应的影响及其应用[J].武汉大学学报,1993(4):56-60
[15]GAO J Z,YANG H,LIU X H.Determination of Glutamic Acid by an Oscillating Chemical Reaction use the Analyte Pulse Perturbation Technique[J].J Talanta,2002,57(1):105-114
[16]张琦,孟宪军,孙希云,等.葡萄籽中原花青素的稳定性研究[J].沈阳农业大学学报,2006,37(2):232-234
[17]Déprez S,Mila I,Huneau J F,et al.Transport of proanthocyanidin dimer,trimer,and polymer across monolayers of human Intestinal epithelial Caco-2 Cells[J].Antioxidants and Redox Signaling,2001, 3(6):957-967
[18]赵平,任鹏,张月萍.原花青素抗氧化活性测定方法比较[J].现代化工,2012,32(5):119-122
[19]高执棣,刘君利,韩德刚,等.间二苯酚-K BrO3-H2SO4体系化学振荡的研究[J].物理化学学报,1993,9(2):218-223
[20]张泰铭,梁逸曾,袁斌,等.中药电化学指纹图谱的原理、特点和用途[J].科学通报,2007,52(13):1513-1522
DOI:10.3969/j.issn.1005-6521.2015.23.032
收稿日期:2015-08-20
基金项目:吉林市科技计划项目(201032240)
作者简介:赖红伟(1979—),男(蒙古),讲师,博士,从事电化学、能源材料和高分子研究。
*通信作者:曹宏梅(1978—),女(蒙古),高级实验师,学士,从事高分子和电化学研究。
Determination of Proanthocyanidins by Using B-Z Oscillation
LAI Hong-wei,XU Ming,WU Bo-ting,JIANG Tao,TAO Ran,WANG Yu-zhuo,DU Juan,CAO Hong-mei*
(Jilin Medical University,Jilin 132013,Jilin,China)
Abstract:A new method for the determination of proanthocyanidins based on the perturbation caused by different ammounts of proanthocyanidins on the B-Z chemical oscillating system was reported.Together with the electrochemical technologies,the changes of the oscillating parameters(induction period,oscillating period and amplitude)at different stages of the oscillating reaction were investigated.A well linear relationships existed between the changes of oscillating period(ΔT),amplitude(ΔA)and a certain concentration of Procyanidine. The possible oscillating mechanism of Procyanidine was also discussed.
Key words:B-Z oscillation;chemical oscillations;proanthocyanidins;determination
