金银花抗自由基能力的检测
2015-07-22刘桂芹曾庆华聊城大学农学院山东聊城252059
樊 琛,杜 晓,程 霜,李 燕,刘桂芹,曾庆华(聊城大学农学院,山东聊城252059)
金银花抗自由基能力的检测
樊琛,杜晓,程霜,李燕,刘桂芹,曾庆华
(聊城大学农学院,山东聊城252059)
摘要:对金银花抗多种自由基能力进行检测。通过正交试验分析溶剂浓度、料液比、处理时间以及提取温度等对金银花提取物清除自由基能力的影响。不同处理的金银花提取物均对2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐自由基(ABTS+·)、1,1-二苯基-2-三硝基苯肼自由基(DPPH·)和超氧阴离子自由基(O2-·)有明显的清除作用,对羟基自由基(HO·)的清除作用较小。金银花提取物对各种自由基具有清除能力。
关键词:金银花;1,1-二苯基-2-三硝基苯肼(DPPH)自由基;2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(ABTS)自由基
金银花为忍冬科植物忍冬的花蕾[1],它属我国公布的既是食品又是药品的植物,具有清热解毒、疏风通络等功效[2]。金银花中有挥发油、黄酮类、有机酸、三萜类、无机元素等多种类型的化学成分[3]。有研究表明,绿原酸类和黄酮类化合物具有抗氧化、清除自由基的作用。目前,国内研究金银花抗氧化性主要是对抗氧化成分绿原酸和类黄酮中的一种进行研究,而对金银花总抗氧化成分进行研究的较少。
本文以金银花为原料,运用正交试验法,以料液比、提取时间、乙醇浓度、提取温度为因素,提取金银花中总抗氧化成分,并研究不同溶剂提取物对自由基的清除作用,为金银花的综合利用提供理论参考。
1 材料与方法
1.1材料与试剂
金银花:北京同仁堂健康药业(福州)有限公司,无腐烂、无虫蛀。
乙醇、乙酸乙酯、NaNO2、水杨酸、H2O2、FeSO4、三羟基甲基氨基甲烷(Tris)、邻苯三酚、HCl均为分析纯;芦丁、1,1-二苯基-2-三硝基苯肼(DPPH):sigma公司;2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(ABTS):生工生物工程(上海)有限公司。
1.2仪器与设备
UV-1700紫外可见分光光度计:日本岛津公司;SK1200H超声清洗机:上海科导超声仪器有限公司;79-2双向磁力加热搅拌器:江苏省金坛市医疗仪器厂;SB-2000水浴锅:上海爱朗仪器有限公司;TD5台式多管架离心机:长沙英泰仪器有限公司。
1.3方法
1.3.1样品处理
称取干金银花样本,用研钵研成粉末,悬于溶剂中,超声处理浸提后抽滤,滤液于3 000 r/min离心15 min后,置于冰箱中保藏,备用。
1.3.2正交试验的设计
依据单因素预试验的结果,确定选取四因素三水平条件,分别为:料液比、提取时间、溶剂(乙醇)浓度、提取温度。其中,料液比(g/mL)为1∶200、1∶300、1∶400,提取(超声处理45 W)时间为15、30、45 min,乙醇浓度为0%、30%、60%,提取温度为20、40、60℃。按上述条件选取L9(34)正交试验设计表,如表1。分别检测提取物清除自由基(HO·、O2-·、ABTS+·、DPPH·)的能力。

表1 正交试验设计表Table 1 Orthogonal test
1.3.3体外抗自由基试验
1.3.3.1清除HO·能力的测定[4-6]
采用Fenton反应体系法,2 mL 1.96 mmol/L H2O2,2 mL 1.8 mmol/L FeSO4和2 mL 1.8 mmol/L水杨酸-乙醇,0.1 mL样品溶液。其中,H2O2最后加入并启动整个反应。反应体系37℃反应30 min,以蒸馏水为参比,在510 nm处测量溶液的吸光度值。以蒸馏水代替样品溶液作空白对照。每个试样作3个平行,取其平均值。根据下式计算HO·清除率:
K/%=[A0-(AX-A1)]/A0×100
式中:A0为空白对照组的吸光度;AX为加入样品溶液后的吸光度;A1为不加显色剂H2O2样品溶液本底的吸光度值;K为清除率。
1.3.3.2清除O2-·能力的测定[7-9]
采用邻苯三酚自氧化法。取1 mmol/L的三羟基甲基氨基甲烷-盐酸缓冲溶液(pH 8.2)4.5 mL,置25℃水浴中预热20 min后,分别加入1 mL试样溶液和0.4 mL 5 mmol/L邻苯三酚溶液,混匀后于25℃水浴中反应5 min,加入1.6 mmol/L HCl 1 mL终止反应,用紫外-可见分光光度计在波长325 nm处测定溶液的吸光度(AX)。空白对照组以相同体积的蒸馏水代替样品溶液,用紫外-可见分光光度计在波长325 nm处测定溶液的吸光度(A0),每个试样作3个平行,取其平均值。数据代入下式计算清除率。
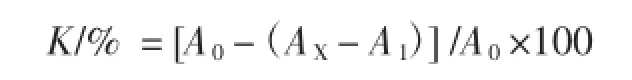
式中:A0为空白对照组的吸光度值;AX为加入样品溶液后的吸光度值;A1样品空白的吸光度值;K为清除率。
1.3.3.3清除ABTS+·能力的测定[10-12]
将2 mL样品溶液加入2 mL稀释后的ABTS溶液中,记录7 min时反应溶液在734 nm处的A值,记为AX。空白对照组为浸提溶剂与ABTS溶液混合。清除率公式如下:
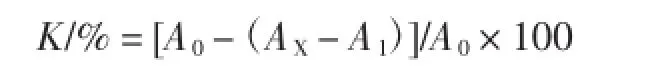
式中:A0为空白对照液的吸光度值;AX为加入样品溶液后的吸光度值;A1为样品空白的吸光度值;K为清除率。
1.3.3.4清除DPPH·能力的测定[12-13]
将DPPH以无水乙醇配制成0.2 mmol/L的溶液,分别吸取2 mL的样品溶液和2 mL的DPPH,避光混匀,反应30 min于517 nm处测定吸光度值AX。空白对照组为浸提溶剂与DPPH溶液混合。清除率公式如下:
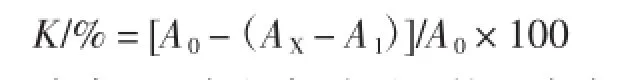
式中:A0为空白对照组的吸光度值;AX为加入样品溶液后的吸光度值;A1为样品空白的吸光度值;K为清除率。
2 结果与分析
2.1正交试验
以料液比、超声波处理时间、浸提溶剂的浓度、提取温度为正交因素,正交试验L9(34)结果见表2~表5。
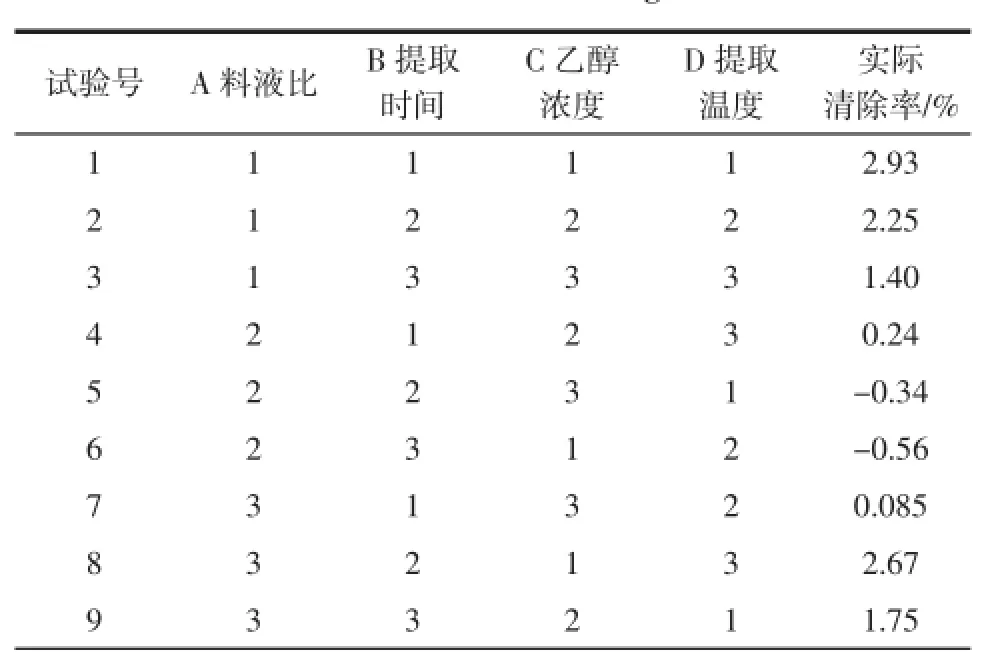
表2 HO·正交试验结果Table 2 Results of HO·orthogonal test
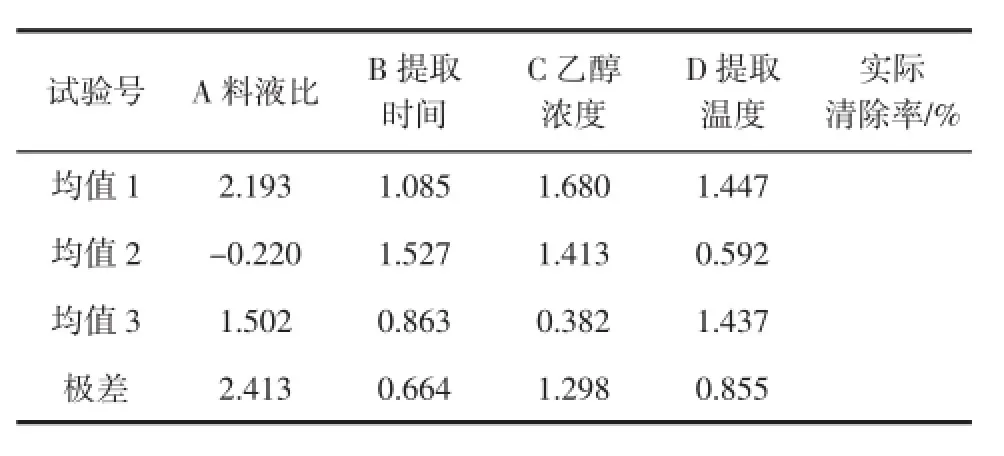
续表2 HO·正交试验结果Continue table 2 Results of HO·Orthogonal test
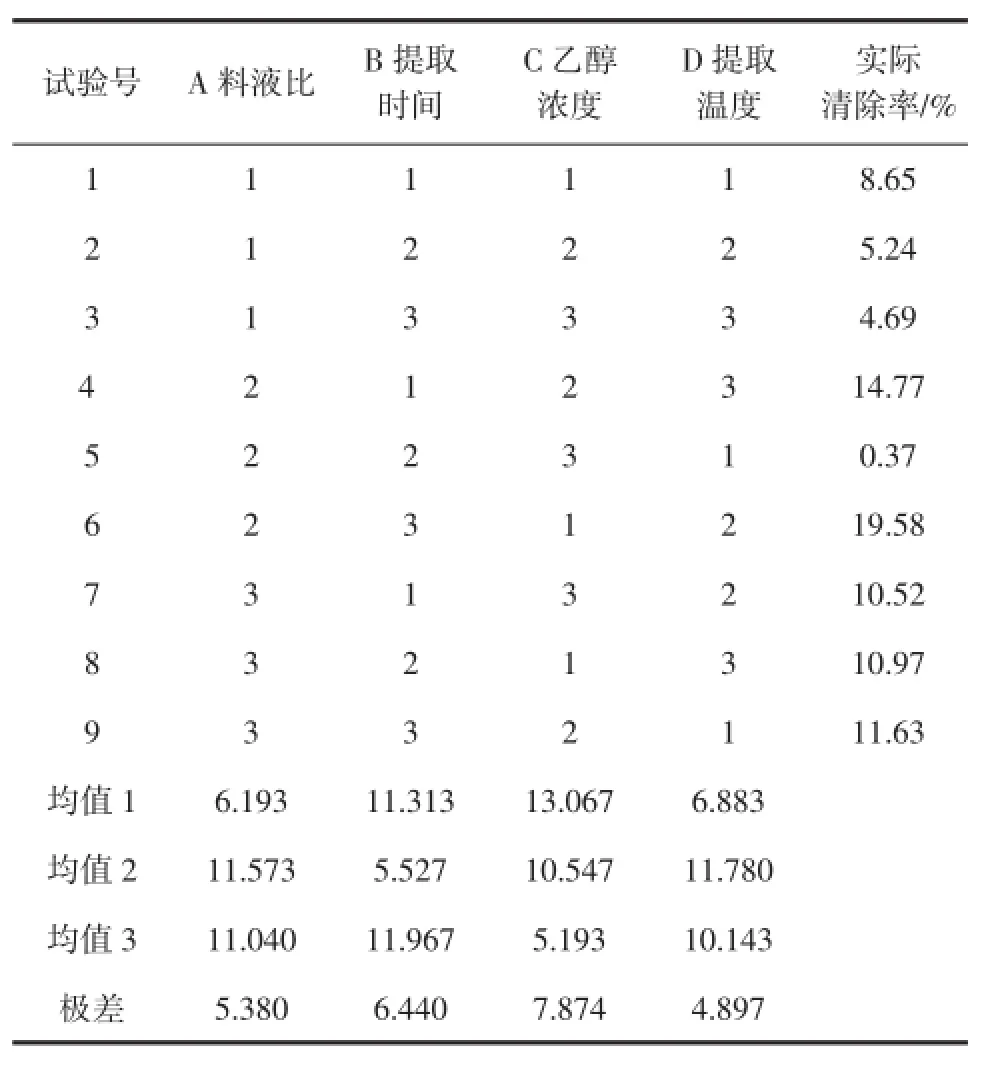
表3 O2-·正交试验结果Table 3 Results of O2-·orthogonal test
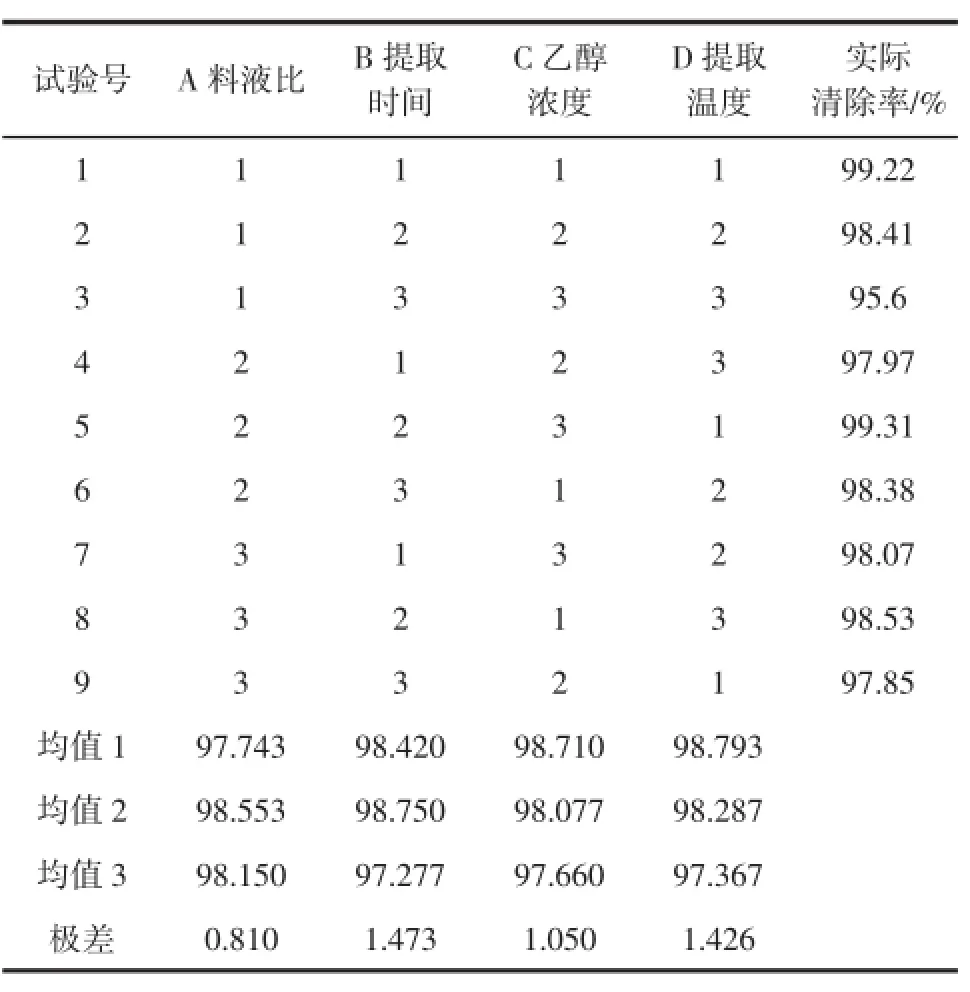
表4 ABTS+·正交试验结果Table 4 Results of ABTS+·orthogonal test
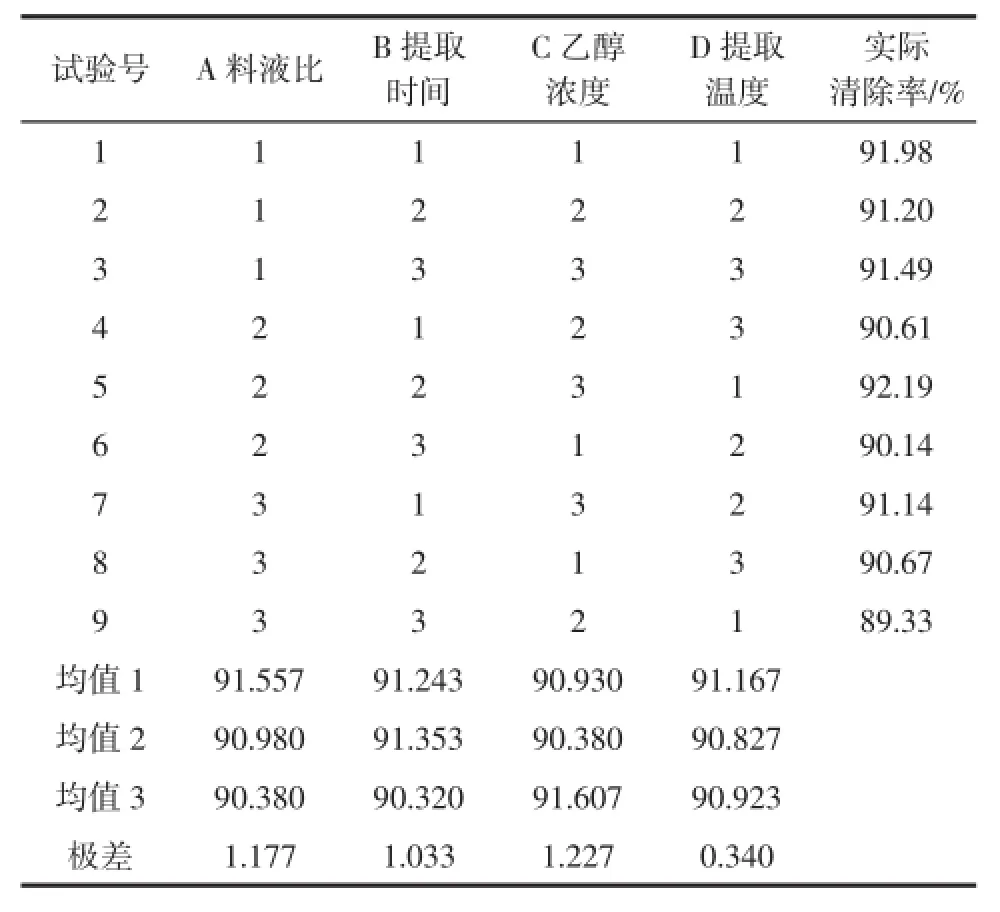
表5 DPPH·正交试验结果Table 5 Results of DPPH·orthogonal test
由表2可知,影响清除羟基自由基能力的各因素的主次顺序是:料液比﹥乙醇浓度﹥提取温度﹥提取时间。最佳组合为A1B2C1D1,即料液比为1∶200(g/mL)、提取时间为45 min、乙醇浓度为60%、提取温度为60℃。经验证,此条件下,清除率为3.08%。
由表3可知,影响清除超氧阴离子自由基能力的各因素的主次顺序是:乙醇浓度>提取时间>料液比>提取温度。清除超氧阴离子自由基能力最佳的组合为A2B3C1D2,即料液比为1∶300(g/mL)、提取时间为15min、乙醇浓度为60%、提取温度为40℃,清除率为19.58%。
如表4可知,各组金银花提取物均对ABTS+·有较强的清除作用。影响较大的因素是提取时间和提取温度,时间越长,温度越高,清除率越大。其次,乙醇浓度增大,清除率增大;料液比增大,清除率先增大后减小。最佳组合为A2B2C1D1,即料液比为1∶300(g/mL)、提取时间为45 min、乙醇浓度为60%、提取温度为60℃,经验证,此条件下,清除率为99.38%。
由表5可知,影响清除DPPH自由基能力的各因素的主次顺序是:乙醇浓度>料液比>提取时间>提取温度。最佳组合为A1B2C3D1,即料液比为1∶200(g/mL)、提取时间为45 min、乙醇浓度为0、提取温度为60℃,经验证,此条件下,清除率为92.36%。
3 结论
金银花提取物对HO·、O2-·、DPPH·、ABTS+·4种自由基均有清除作用。其中,对DPPH·、ABTS+·两种自由基的清除能力强,对O2-·的清除能力次之,而对HO·的清除能力弱。提取物清除各自由基的最佳提取条件差异较大。
参考文献:
[1] 董熙,丁立,崔耀章.金银花叶中有效成分含量的研究[J].中药通报,1895,10(5):31-33
[2]兰华,申鸿,高丹,等.金银花不同贮藏时期有效成分与抗氧化力的研究[J].中国食品学报,2008(6):43-45
[3]吴晓春,杨苏亚.金银花的成分及药理作用分析[J].青海医药杂志,2007,37(5):88-89
[4]田迪英,杨荣华.微波辐射对生姜抗氧化活性物质的浸提作用[J].中国调味品,2006(12):17-21
[5]范方宇,阚欢,刘建琴,等.澳洲坚果蛋白酶解工艺及抗氧化性研究[J].食品科技,2011,36(12):230-233
[6] 程超,李伟.平菇水溶性多糖结构表征与体外抗氧化作用[J].食品科学,2005(8):55-56
[7]税单,王立峰,袁建,等.酸法提取菜籽多糖的抗氧化活性研究[J].食品科学,2011(21):98-101
[8]严成,严复.枸杞多糖提取工艺比较及抗氧化性研究[J].食品科学,2008,29(17):183-187
[9] 熊建华,闵嗣璠,董开发,等.南瓜不同部位抗氧化活性的比较[J].食品研究与开发,2011,32(11):135-138
[10]董青春,樊琛.紫甘蓝乙醇提取物清除体外自由基活性研究[J].安徽农业科学,2009,37(31):15432-15434
[11]梁丽雅,张泽生,吕晨,等.桦褐孔菌抗氧化活性物质的提取工艺[J].食品研究与开发,2009,30(4):40-43
[12]陈晋明,王世平,马俪珍.虾青素抗氧化活性研究[J].营养学报, 2007,29(2):163-165,169
[13]ETSUO N.Assessment of Antioxidant Capacity in Vitro and in Vivo [J].Free Radical Biology and Medicine,2010,49(4):503-515
DOI:10.3969/j.issn.1005-6521.2015.20.036
收稿日期:2013-10-24
基金项目:聊城大学博士科研启动基金(31805)
作者简介:樊琛(1978—),女(汉),副教授,博士,主要从事食品营养与卫生学方向的研究。
Detection of Flos Lonicerae Anti-radical Ability
FAN Chen,DU Xiao,CHENG Shuang,LI Yan,LIU Gui-qin,ZENG Qing-hua
(Agricultural School,Liaocheng University,Liaocheng 252059,Shandong,China)
Abstract:This paper detects anti-radical ability of Flos Lonicerae.Effects of solvent concentration,solidliquid ratio,extraction time and extraction temperature on extractive scavenging radicals were investigated by orthogonal test.The results showed that each group of extractive had a scavenging capacity on 1,1-Diphenyl-2-picrylhydrazyl radical(DPPH·),2,2'-Azinobis-(3-ethylbenzthiazoline-6-sulphonate)radical(ABTS+·)and superoxide radical(O2-·),but had a small scavenging capacity on hydroxyl radical(HO·).Flos Lonicerae extractive showed scavenging radicals activity.
Key words:Flos Lonicerae;1,1-Diphenyl-2-picrylhydrazyl(DPPH)radical;2,2'-Azinobis-(3-ethylbenzthiazoline-6-sulphonate)(ABTS)radical
