4种氨基酸氯消毒后典型卤代碳、氮类消毒副产物生成潜能的研究
2015-07-19鲁金凤刘烜安怡然赵洪辰周心怡
鲁金凤 , 刘烜 辰,冯 瑛,安怡然,郭 昊,赵洪辰,周心怡
(1. 南开大学环境科学与工程学院,天津 300071;2. 环境污染过程与基准教育部重点实验室(南开大学),天津 300071)
早在 1974年,Rook就发现,氯消毒会产生三氯 甲烷,随后研究者在氯消毒后的饮用水中陆续检出了其他三卤甲烷(trihalomethane,THM)和卤乙酸(haloacetic acids,HAAs)等消毒副产物[1-2],近年来,研究者发现,水中存在含氮类物质时,氯化消毒会生成毒性更高的含氮消毒副产物[1-3].含氮消毒副产物主要分卤代和非卤代两大类.卤代硝基甲烷(HNMs)就是其中一类含氮类卤代消毒副产物. HNMs比THMs、HAAs有着更强的毒性,研究表明 HNMs的动物细胞遗传毒性甚至超过了卤代呋喃酮,其对DNA的破坏效应远远超过了溴酸盐[3],具有更强的致突变性,HNMs已被USEPA列入优先控制消毒副产物的最高等级[4].HNMs有9种物种,当前在饮用水中能被检出的主要是三氯硝基甲烷(TCNM),因此研究者常把TCNM作为HNMs的代表来研究.
氨基酸是天然水体中最常见的含氮类物质,已被证实是饮用水中消毒副产物的前驱物[5],但当前对水中天然氨基酸的卤代碳、氮类消毒副产物生成潜能的研究相对较少,现有的一些研究也存在结论不统一的问题:王超等[6]对污水中常见氨基酸类物质消毒副产物生成情况的研究发现,氨基酸类物质氯化后生成了较高浓度的三卤甲烷;而 Hong等[7]的研究表明,氨基酸氯化后三卤甲烷的生成量极低,一般只有几微克每升;对氨基酸氯化后卤代含氮消毒副产物 TCNM生成潜能方面的研究也存在不同的研究结论;Bond等[8]的研究表明,氨基酸等一些亲水性 NOM 的替代物,氯化后形成 TCNM 的浓度都很低,基本不形成TCNM;而王超等[6]对污水中常见的一些氨基酸进行的消毒实验表明,氨基酸是TCNM的前驱物,但各种氨基酸生成TCNM的潜能不同,其中苏氨酸、色氨酸的 TCNM 生成潜能最高;Hu等[9]的研究则发现,带有酸性官能团的短链氨基酸才是 TCNM 的前驱物,一些具有高稳定官能团的氨基酸不是TCNM的前驱物.不同结构组成的氨基酸对生成 HAAs潜能的影响大小及哪种特性侧链组成的氨基酸是 HAAs最主要的前驱物,当前研究领域尚鲜见报道.而当前国内外对水中的氨基酸在氯化过程中生成 THMs、HAAs和 TCNM 的机理尚不清楚,一些研究报道只是简单推测其生成机理可能与氨基酸的—R侧链有关[6],但对不同—R侧链结构的氨基酸与这几类典型碳、氮类消毒副产物生成潜能之间到底有什么关联,目前也尚未明确.
为了明确水中的氨基酸是否是 THMs、HAAs等含碳类消毒副产物和TCNM 这一高毒性卤代含氮类消毒副产物的主要前驱物的来源,并进一步探明氨基酸的结构组成与这几类典型碳、氮类消毒副产物生成潜能之间的关联.笔者选取天然水体中 4种典型氨基酸(色氨酸、赖氨酸、苏氨酸、甘氨酸)作为研究对象,考察它们在氯化消毒过程中 THMs、HAAs和TCNM 的生成潜能,了解不同结构特性的氨基酸在消毒过程中典型卤代碳、氮类消毒副产物的生成特性,为更加深入地研究氯化消毒过程中卤代碳、氮类消毒副产物的生成规律和机理提供一定的参考.
1 实验材料与方法
1.1 实验用水水质
实验用水为分别用超纯水配制的氨基酸水溶液(色氨酸 C11H12N2O2、赖氨酸 C6H14N2O2、甘氨酸C2H5NO2和苏氨酸 C4H9NO3),浓度均为 0.5,mmol/L.对各类氨基酸水溶液测定了 pH值、总有机碳(TOC)、总有机氮(TON)和水温,其对应的测定结果如表1所示.
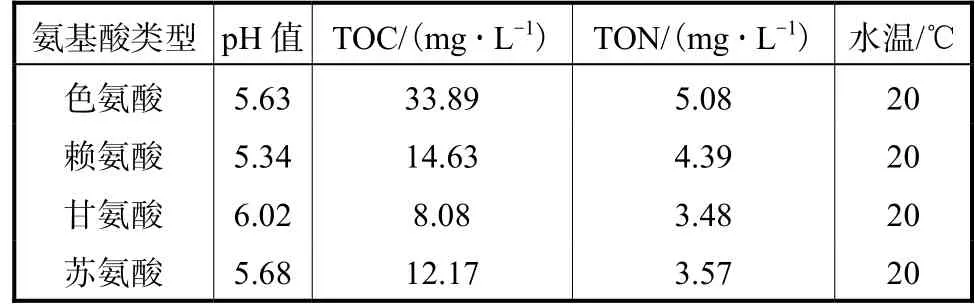
表1 实验用水水质Tab.1 Characteristics of the water used in the experiment
1.2 实验方法
本研究选取了 4种代表性的氨基酸,分别是:芳香族类侧链具有吲哚杂环结构的色氨酸、碱性氨基酸类的赖氨酸、脂肪族类的甘氨酸和侧链具有羟基官能团结构的苏氨酸,进行氯化消毒实验,进一步明确氨基酸产生碳、氮类消毒副产物的特性.氯化实验方法参照AWWA Standard Method(1992),并做了一些修改.取200,mL氨基酸水样,用0.1,mol/L的H2SO4或NaOH 溶液调 pH 值至(7.0±0.2),之后按照 Cl和TOC质量比为5∶1投加次氯酸钠溶液进行氯化,25,℃恒温反应 72,h,之后用氯化铵中止反应,预处理后待测.
1.3 分析方法
采用USEPA Method 551.1方法分析测定THMs和 TCNM,气相色谱为 Agilent 6890(ECD检测器,DB-5,30,m×0.25,mm 硅胶柱).采用 USEPA Method 552.3测定HAAs.采用Agilent 6890气相色谱(ECD检测器,尺寸为30,m×0.25,mm的DB-5型硅胶柱).
采用岛津 TOC/TN测定仪分析 TOC和总氮(TN).采用 752型紫外/可见分光光度计测出氨氮、硝酸盐氮和亚硝酸盐的无机氮(TIN)浓度后,用 TNTIN计算得到TON.
2 结果与讨论
2.1 THMs的生成潜能研究
4种典型氨基酸在本实验条件下的 THMs生成潜能情况如图 1所示.结果表明,4种氨基酸生成的THMs种类都为三氯甲烷(CHCl3).4种氨基酸生成THMs的产量顺序为:色氨酸>赖氨酸>苏氨酸>甘氨酸.侧链带有吲哚环的氨基酸的 THMs生成能力最强,碱性氨基酸类和侧链带有羟基官能团结构的氨基酸的 THMs生成潜能次之,侧链为脂肪族类的氨基酸的 THMs生成潜能最低.这可能主要是由于侧链带有吲哚环的氨基酸,其吲哚环具有较高的氯反应活性[5],导致苯环断裂进而水解,形成了较高的CHCl3.
本研究结果中,4种氨基酸氯化后均能生成THMs,但其 THMs的生成潜能均较低,只有几微克每升,甘氨酸的 THMs生成量甚至只有 0.4,μg/L,本研究结论与 Hong等[7]的结论一致,这就进一步明确水中的氨基酸尽管都能生成 THMs,但并不是 THMs主要的前驱物.
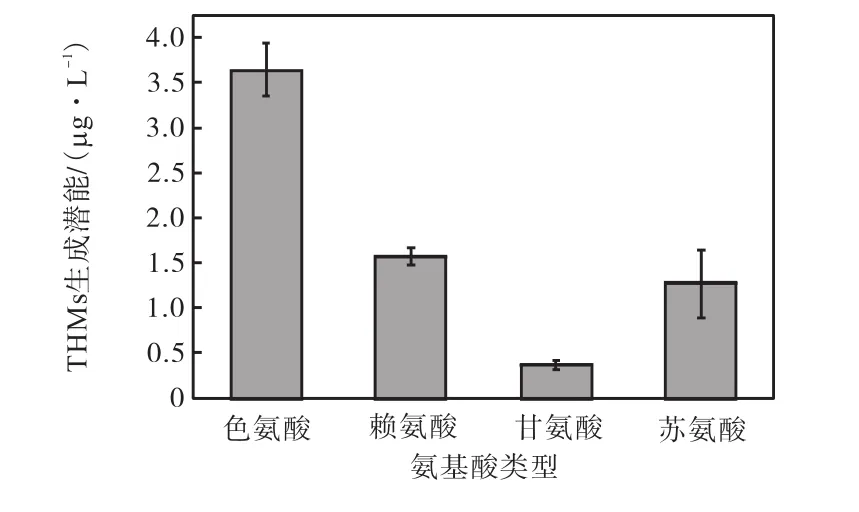
图1 4种氨基酸的THMs生成潜能情况Fig.1 Formation potential of THMs for the four selected amino acids
此外,4种氨基酸的 THMs生成潜能与其 TOC浓度高低(见表 1)的顺序一致,这也表明,三氯甲烷的生成与TOC在很大程度上有很好的相关性.
2.2 HAAs的生成潜能研究
本研究也测定了 4种代表性氨基酸氯化消毒后5种卤乙酸的生成潜能,如图2所示.结果表明,4种氨基酸都能生成卤乙酸,且 HAAs的生成潜能(33.8~176.7,μg/L)远高于 THMs,表明水中的氨基酸是 HAAs这一毒性更高的含碳类消毒副产物的主要前驱物.
4种氨基酸的HAAs生成潜能总量顺序为:甘氨酸>色氨酸>赖氨酸>苏氨酸.与三卤甲烷的生成潜能顺序略有差别,对卤乙酸而言,甘氨酸的卤乙酸生成潜能最高,远高于色氨酸.这表明脂肪族类氨基酸的 HAAs生成潜能要远高于芳香族类侧链带有吲哚环的氨基酸;而侧链具有羟基官能团结构的氨基酸的HAAs生成潜能相对最低.但4种氨基酸的HAAs生成潜能与总有机碳(TOC)浓度高低没有相关性.这表明,总有机碳这一代表有机物浓度高低的宏观指标对 HAAs的生成情况没有指示作用,不同结构组成才是影响氨基酸氯化后 HAAs生成潜能的最直接的原因.
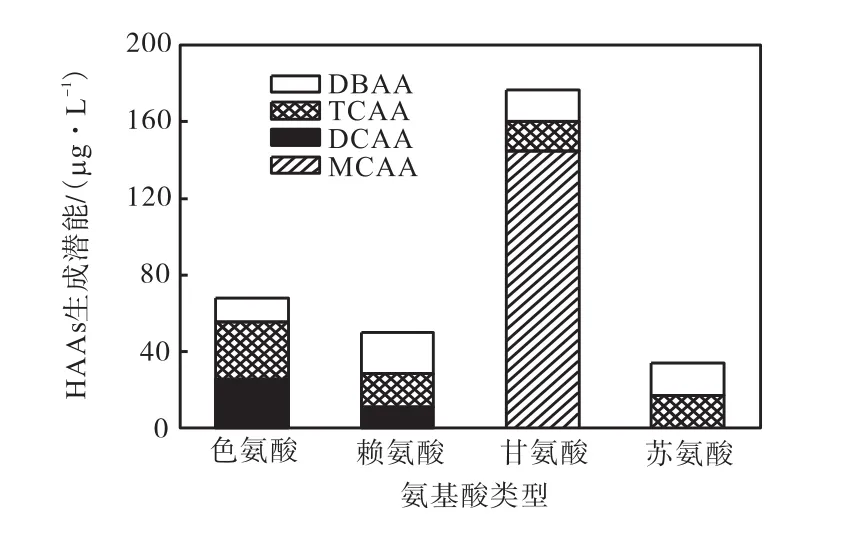
图2 4种氨基酸的HAAs生成潜能情况Fig.2 Formation potential of HAAs for the four selected amino acids
本研究中,具有吲哚环侧链的色氨酸,其中的吡咯环具有不饱和性和不稳定性[10-11],环上的电子云密度较大,易发生亲电取代反应,其氯化活性较高,根据Reckhow等[12]推导的THMs和HAAs形成机理的理论,这种存在吲哚环侧链结构的氨基酸容易发生开环反应,吲哚杂环和羧基互相影响,使氯取代和开环更易发生,因此,氯化后更易形成 CHCl3、三氯乙酸(TCAA);此外,文献[12]表明,TCAA的前驱物是高芳香度(SUVA254)物质,而色氨酸就是一种高SUVA254的物质,因此色氨酸是 TCAA的主要前驱物.
而脂肪类的氨基酸由于其是结构简单的羧基类物质也较容易被自由氯攻击,而这种脂肪类前驱物更易于形成一氯乙酸(MCAA),由于其芳香度较低[13],其 TCAA和二氯乙酸(DCAA)的生成量相对较低,在本研究中,脂肪类的甘氨酸就是由于生成了大量MCAA,致使其总HAAs生成潜能最高.
甘氨酸的卤乙酸生成潜能中 MCAA占到了其HAAs总量的 82%,脂肪类结构的甘氨酸是 MCAA的主要前驱物.具有碱性官能团的赖氨酸和具有羟基官能团的苏氨酸其 HAAs生成物种则主要是TCAA和二溴乙酸(DBAA).
2.3 TCNM的生成潜能研究
氨基酸、氨基糖等一些含氮物质被认为是饮用水中 TCNM 的主要前驱物[8-9,14].但并不是水中所有的氨基酸氯化后都能形成 TCNM.有些研究者认为,水中的氨基酸 TCNM 的生成潜能很低[8],而也有报道发现,污水中的主要氨基酸氯化后均能形成TCNM[6];另一些研究者却认为,部分特定结构的氨基酸才是 TCNM 的前驱物,不具备这种结构的氨基酸则不是 TCNM 的前驱物[9].为了明确水中典型的一些氨基酸到底是不是 TCNM 的主要前驱物,本研究考察了4种不同结构的天然氨基酸的TCNM生成潜能,如图3所示.
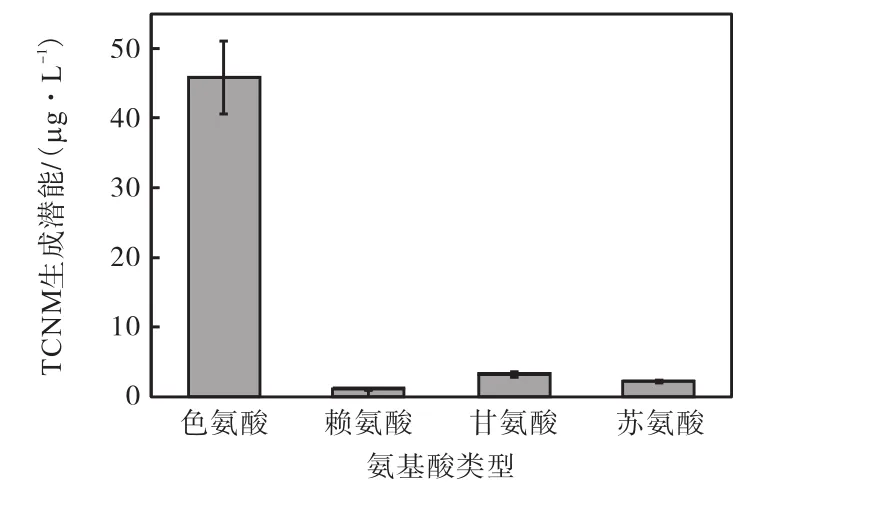
图3 4种氨基酸的TCNM生成潜能情况Fig.3 Formation potential of TCNM for the four selected amino acids
结果表明,4种天然氨基酸氯化后的 TCNM 生成潜能相差较大,赖氨酸的生成潜能很低,基本不生成 TCNM,笔者认为赖氨酸不是 TCNM 的主要前驱物,而其余 3种氨基酸(色氨酸、甘氨酸和苏氨酸)的TCNM 生成潜能都高于水体中检测出来的数据水平,笔者认为这 3种氨基酸都是 TCNM 的主要前驱物,且色氨酸的 TCNM 生成潜能为 45.86,μg/L,远高于其他 3种氨基酸.由此,笔者得出,具有特定结构的氨基酸才是TCNM 的主要前驱物,这与Bond等[8]的研究结论完全相反,与 Hu等[9]的研究结果相似.结合氨基酸结构中的羧基官能团在氯化过程中易发生脱羧断裂的过程,笔者推测 TCNM 的形成机理可能是,氨基酸主要是在交替进行的脱羧和取代反应过程中完成了分解,最终生成 TCNM.而这种具有吲哚环侧链的色氨酸,其具有不饱和性和不稳定性的吡咯环,比其他几种氨基酸更易发生取代和开环反应,是主要的TCNM前驱物.
3 结 论
(1) 4种氨基酸氯化后生成的三卤甲烷的物种只有三氯甲烷,其 THMs生成潜能顺序为:色氨酸>赖氨酸>苏氨酸>甘氨酸.但 4种氨基酸氯消毒后THMs的生成潜能很低,并不是THMs主要的前驱物.
(2) 氯消毒后 4种氨基酸的 HAAs生成潜能远高于 THMs的,水中的这些氨基酸是 HAAs这一毒性更高的含碳类消毒副产物的主要前驱物.4种氨基酸的 HAAs生成潜能顺序为:甘氨酸>色氨酸>赖氨酸>苏氨酸.脂肪族类氨基酸的卤乙酸生成潜能要远高于芳香族类侧链带有吲哚环的氨基酸;而侧链具有羟基官能团结构的氨基酸其 HAAs生成潜能相对最低.
(3) 4种氨基酸氯化后会生成 4种 HAAs的物种,包括 MCAA、TCAA、DCAA 和 DBAA.具有吲哚杂环结构的色氨酸是 TCAA的主要前驱物;具有脂肪类结构的甘氨酸更易于生成 MCAA,其 TCAA和 DCAA的生成量相对较低;具有碱性官能团的赖氨酸和具有羟基官能团的苏氨酸其 HAAs生成物种则主要是TCAA和DBAA.
(4) 4种氨基酸氯化后的 TCNM 生成潜能相差较大,赖氨酸基本不生成 TCNM,不是 TCNM 的主要前驱物,芳香族类侧链具有吲哚杂环结构的色氨酸是TCNM主要的前驱物.
[1] 高乃云,方 诚,楚文海. 常规净水工艺中三氯硝基甲烷质量浓度分布调查[J]. 同济大学学报:自然科学版,2012,40(6):890-893.Gao Naiyun,Fang Cheng,Chu Wenhai. Concentration of trichloronitromethane in conventional water treatment process[J]. Journal of Tongji University:Natural Science,2012,40(6):890-893(in Chinese).
[2] Yang X,Guo W,Shen Q. Formation of disinfection byproducts from chlor(am)ination of algal organic matter[J]. J Hazard Mater,2011,197:378-388.
[3] Krasner S W,Weinberg H S,Richardson S D,et al.Occurrence of a new generation of disinfection byproducts[J]. Environ Sci Technol,2006,40(23):7175-7185.
[4] Woo Y T,Lai D,McLain J L,et al. Use of mechanism-based structure-activity relationships analysis in carcino-genic potential ranking for drinking water disinfection by-products[J]. Environmental Health Perspectives,2002,110(1):75-87.
[5] 刘 芸,付荣恕. 氨基酸氯化消毒副产物的生成机理研究[J]. 山东林业科技,2010,40(1):86-88.Liu Yun,Fu Rongshu. Formation and mechanism of byproducts during amino acids chlorination[J]. Shandong Forestry Science and Technology,2010,40(1):86-88(in Chinese).
[6] 王 超,胡洪营,王丽莎. 典型含氮有机物的氯消毒副产物生成潜能研究[J]. 中国给水排水,2006,22(15):9-12.Wang Chao,Hu Hongying,Wang Lisha. Chlorination by-products formation potentials of typical nitrogenous organic compounds[J]. China Water & Wastewater,2006,22(15):9-12(in Chinese).
[7] Hong H C,Wong M H,Liang Y. Amino acids as precursors of trihalomethane and haloacetic acid formation during chlorination[J]. Arch Environ Contam Toxicol,2009,56(4):638-645.
[8] Bond T,Templeton M R,Graham N. Precursors of nitrogenous disinfection by-products in drinking water—A critical review and analysis[J]. Journal of Hazardous Materials,2012,235/236:1-16.
[9] Hu J,Song H,Addison J W,et al. Halonitromethane formation potentials in drinking waters[J]. Water Research,2010,44(1):105-114.
[10] 赵新华,王熠宁,周广宇,等.配水管网中三氯甲烷风险概率及影响因素分析[J]. 天津大学学报:自然科学与工程技术版,2014,47(4):343-348.Zhao Xinhua,Wang Yining,Zhou Guangyu,et al.Analysis on chloroform risk probability and impact factors for water distribution network[J]. Journal of Tianjin University:Science and Technology,2014,47(4):343-348(in Chinese).
[11] 陈忠林,李 安,王胜军,等. 色氨酸氯化消毒生成卤乙酸的影响因素研究[J]. 黑龙江大学自然科学学报,2010,27(6):731-734.Chen Zhonglin,Li An,Wang Shengjun,et al.Haloacetic acids formation from tryptophan during chlorination disinfection[J]. Journal of Natural Science of Heilongjiang University,2010,27(6):731-734(in Chinese).
[12] Reckhow D A,Singer P C. Mechanisms of organic halide formation during fulvic acid chlorination and implications with respect to preozonation[C]// Jolley R L,Brungs W A,ed. Water Chlorination:Chemistry,Environmental Impact and Health Effects.Chelsea,MI,UK,1985: 1229-1257.
[13] 洪华嫦,林红军,丁林贤,等. 几种模型物质在氯化中形成 THMs、HAAs 的特性研究[J]. 环境科学学报,2012,32(8):1850-1855.Hong Huachang,Lin Hongjun,Ding Linxian,et al.THMs and HAAs formation upon chlorination of several model compounds[J]. Acta Scientiae Circumstantiae,2012,32(8):1850-1855(in Chinese).
[14] Shan J,Hu J,Kaplan-Bekaroglu S S,et al. The effects of pH,bromide and nitrite on halonitromethane and trihalomethane formation from amino acids and amino sugars[J]. Chemosphere,2012,86(4):323-328.
