奥沙利铂联合替吉奥(SOX)与奥沙利铂联合卡培他滨(XELOX)治疗中国进展期胃癌患者的Meta分析
2015-07-07李远军邢娟吴翰昌魏旭张红梅
李远军,邢娟,吴翰昌,魏旭,张红梅
(1.解放军空军总医院,北京 100142;2.北京大学 城市与环境学院,北京 100871;3.第四军医大学 学员旅,陕西 西安 710032;4.第四军医大学第一附属医院 肿瘤科,陕西 西安 710032)
奥沙利铂联合替吉奥(SOX)与奥沙利铂联合卡培他滨(XELOX)治疗中国进展期胃癌患者的Meta分析
李远军1,邢娟2,吴翰昌3,魏旭3,张红梅4Δ
(1.解放军空军总医院,北京 100142;2.北京大学 城市与环境学院,北京 100871;3.第四军医大学 学员旅,陕西 西安 710032;4.第四军医大学第一附属医院 肿瘤科,陕西 西安 710032)
目的 本研究对奥沙利铂联合替吉奥(SOX)或奥沙利铂联合卡培他滨(XELOX)治疗进展期胃癌的有效性及安全性进行荟萃分析,以期更有效地指导临床用药。方法 在CNKI、万方、维普、PUBMED 数据库中,检索SOX和XELOX 2组方案治疗进展期胃癌的随机对照临床研究(randomized controlled trials,RCT),按照JADAD质量计分法对所纳入的每篇文献逐篇进行方法学质量评估;荟萃分析采用RevMan 5.2.0(Cochrane-information Management System)进行系统评价,评价内容为2种化疗方案的有效性(即临床缓解率,PR+CR)与安全性。结果 共有8个临床研究纳入本系统评价,共计603例中国进展期胃癌患者,其中应用SOX方案化疗患者293例,应用XELOX方案治疗患者310例。分析结果显示2种方案治疗进展期胃癌患者的有效率无显著差异(OR=1.19,95%CI:0.86~1.64,P=0.29)。就不良反应而言,SOX方案口腔黏膜炎的发生率明显高于XELOX方案(OR=2.29,95%CI:1.74~4.89,P<0.0001),其他不良反应差异无明显统计学意义。总体看来,SOX方案与XELOX方案不良反应发生率无差异(OR=0.88,95%CI:0.66~1.19,P=0.41)。结论 在中国进展期胃癌患者的临床治疗中,SOX方案在临床缓解率方面与XELOX方案不相上下,但其口腔黏膜炎的发生率明显高于XELOX方案。
进展期胃癌;SOX;XELOX;Meta分析
胃癌是我国最常见的恶性肿瘤之一,病死率仅次于肺癌[1]。全球每年新发病例逾百万,其中41%发生在中国;全球每年约有70万患者死于胃癌,中国约占35%[2-3]。胃癌起病隐匿,早期因缺乏典型症状常被漏诊,大多数患者确诊时已处于中晚期,失去手术时机;即使接受手术治疗的患者,术后5年的复发率也高达50%。因此,化疗是这部分患者的主要治疗手段。氟尿嘧啶是治疗进展期胃癌的重要化疗药物之一,其常用口服剂型包括:卡培他滨(希罗达)和替吉奥(S-1),口服药物生物利用度高,具有较好的抗肿瘤活性[4]。本研究拟通过Meta分析,比较胃癌常用化疗方案:卡培他滨联合奥沙利铂(XELOX)和替吉奥联合奥沙利铂(SOX),治疗进展期胃癌的有效率和安全性,为胃癌化疗方案的优化选择提供循证医学证据。
1 资料与方法
1.1 文献检索 在万方、维普、CNKI及PUBMED数据库中检索SOX与XELOX 2组化疗方案治疗中国进展期胃癌的随机对照临床研究;语种为中文或英文。中文检索词包括:卡培他滨(希罗达)、替吉奥、奥沙利铂、胃癌,英文检索词包括SOX、XELOX、Capecitabine(Xeloda)、S-1、Oxaliplatin、Gastric cancer。检索时间范围:2000年1月1日~2013年10月23日。
1.2 筛选标准
1.2.1 纳入标准:纳入的文献均采用随机对照临床研究(randomized controlled trial,RCT);研究对象均经病理组织学确诊为进展期胃癌,具有可测量或评估病灶。
1.2.2 排除标准:对于质量差、重复、数据不全等无法进行统计的文献进行剔除;对于相似或相同的文献,只选用最新文献;样本量小于20例的文献予以剔除。
1.2.3 干预措施:化疗方案应为XELOX与SOX方案的比较。评价指标为治疗有效性和安全性,有效性即总缓解率,为完全缓解率(complete remission,CR)+部分缓解率(particial remission,PR),按照实体肿瘤的疗效评价标准1.1版[response wvaluation criteria in solid tumours (version 1.1),RECIST 1.1]标准[5]进行评判:CR-所有靶病灶消失,无新病灶出现,且肿瘤标志物正常,至少维持4周,PR-靶病灶最大径之和减少≥30%,至少维持4周;安全性主要按照WHO抗肿瘤药物急性与亚急性毒性分级标准[6]进行分析:0度表示无毒性,Ⅰ、Ⅱ度表示轻度毒性,Ⅲ、Ⅳ度表示重度毒性。
1.3 研究特征及质量评价 记录各纳入研究文献的基本特征,包括研究方法、研究对象基本资料、治疗方案及结果测量等。按照JADAD质量计分法[7]对所纳入的文献逐篇进行质量评估,评价内容包括:各研究中心伦理委员会批件、受试者知情同意书、方案设计、盲法、随机化、基线的一致性等。对每项指标进行各自评分,0~2分为低质量研究,3~5分为高质量研究。每篇文献均由2名分析员独立提取及评价。
1.4 统计学方法 采用RevMan 5.2.0 software (Cochrane-information Management System)进行统计学分析,首先进行齐性检验,若结果显示各研究同质性佳,则应用固定效应模型分析(fixed effects model,FEM);若各研究的同质性较差,则应用随机效应模型分析(random effects model,REM);评价指标采用优势比(odds Ratio,OR)和95%可信区间(confidence interval,CI)。绘制森林图,进行敏感度分析,利用Egger[8]回归分析评价发表偏倚,并绘制Egger发表偏倚图,从而客观地评估发表偏倚。
2 结果
2.1 纳入研究的情况 通过阅读题目、摘要和全文最终纳入8篇文献共8项研究,共计603例进展期胃癌患者,其中应用SOX方案化疗293例,XELOX方案化疗310例。纳入研究的基本特征包括设计方法、研究对象情况、治疗方法及结果测量指标等具体数据详,见表1。疗效根据RECIST 1.1实体瘤疗效评价标准,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)。安全性测量指标选择不良反应,包括Ⅰ~Ⅱ级白细胞减少、恶心呕吐、外周神经毒性、手足综合征、口腔黏膜炎及腹泻等。
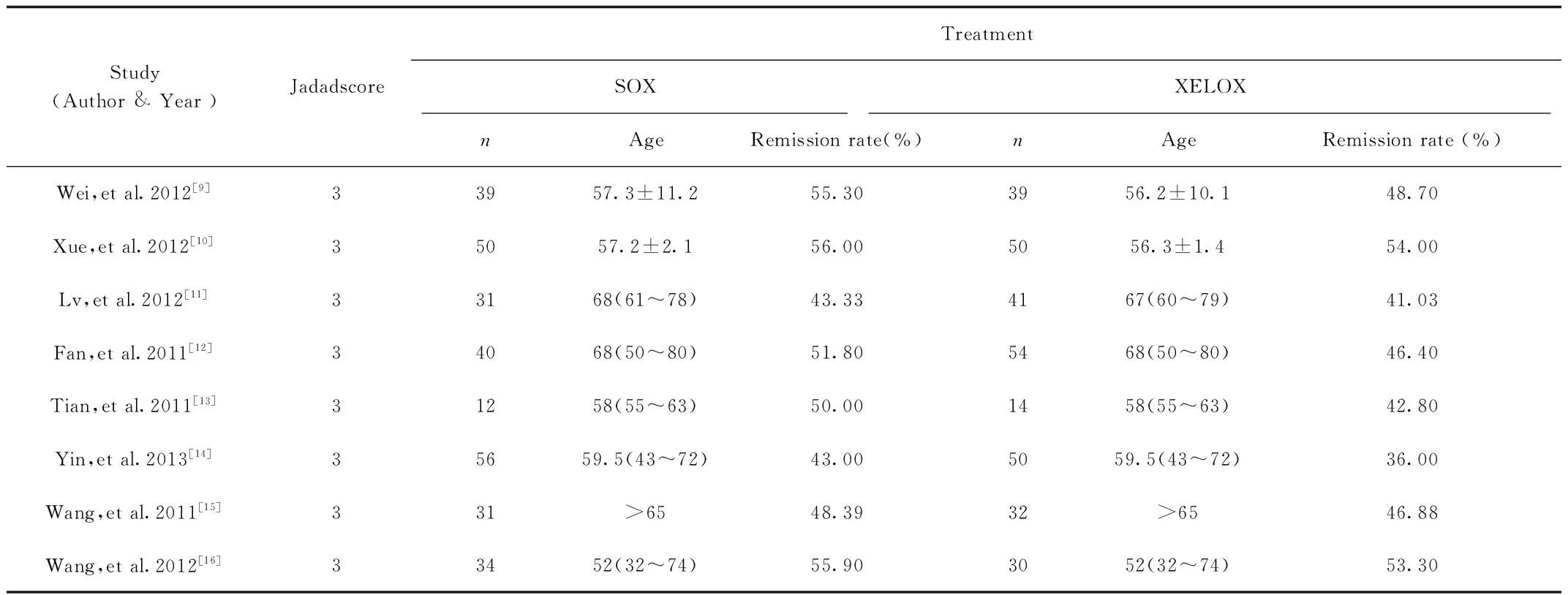
表1 8项纳入Meta分析研究的数据资料Tab.1 Characteristics of 8 RCTs included in the Meta-analysis
2.2 2种化疗方案的有效性评价 本研究纳入的8篇文献均详细记录了进展期胃癌患者化疗的有效率。首先提取数据进行异质性检验(P=1.00),结果显示此8项研究无异质性,因此采用固定效应模型分析。经RevMan 5.2.0软件分析,SOX与XELOX方案的缓解率无显著差异(OR=1.19,95%CI:0.86~1.64,P=0.29),见图1。运用Egger’s测试,8项研究的发表偏倚系数<0.001,认为无发表偏倚[图2,截距线段横跨0点,95%可信区间包含0(t=0.000,95%CI:-0.827~0.827,P=1.000)],结论可靠。

图1 SOX方案与XELOX方案化疗有效性评价森林图矩形及横线分别代表OR的点估计值和95% CI;棱形代表合并OR值和95% CIFig.1 Forest plot of the remission between SOX and XELOXThe estimate of OR and its 95% CI is plotted with a box and a horizontal line.◆,pooled OR and its 95% CI

图2 8项研究发表偏倚的Egger检验Fig.2 Egger’s test of the publication bias among 8 case-control studies
2.3 安全性评价 SOX方案与XELOX方案常见的毒性反应包括粒细胞、血小板减低,贫血,恶心、呕吐、腹泻,手足综合征,口腔溃疡及周围神经损伤等。本研究选择Ⅰ~Ⅱ级白细胞减少、恶心呕吐、外周神经毒性、手足综合征、口腔黏膜炎和腹泻作为毒性反应的研究对象,进行Meta分析。结果显示:SOX方案较XELOX方案口腔黏膜炎的发生率明显升高(OR=2.29,95%CI:1.74~4.89,P<0.0001);而白细胞减少、恶心呕吐、外周神经毒性、手足综合征、腹泻等不良反应无统计学意义;综合比较上述不良反应,SOX与XELOX间无统计学意义(OR=0.88,95%CI:0.66~1.19,P=0.41),见表2、图3。

表2 SOX方案与XELOX方案化疗的不良反应评价Tab.2 Adverse reactions assessment:SOX and XELOX
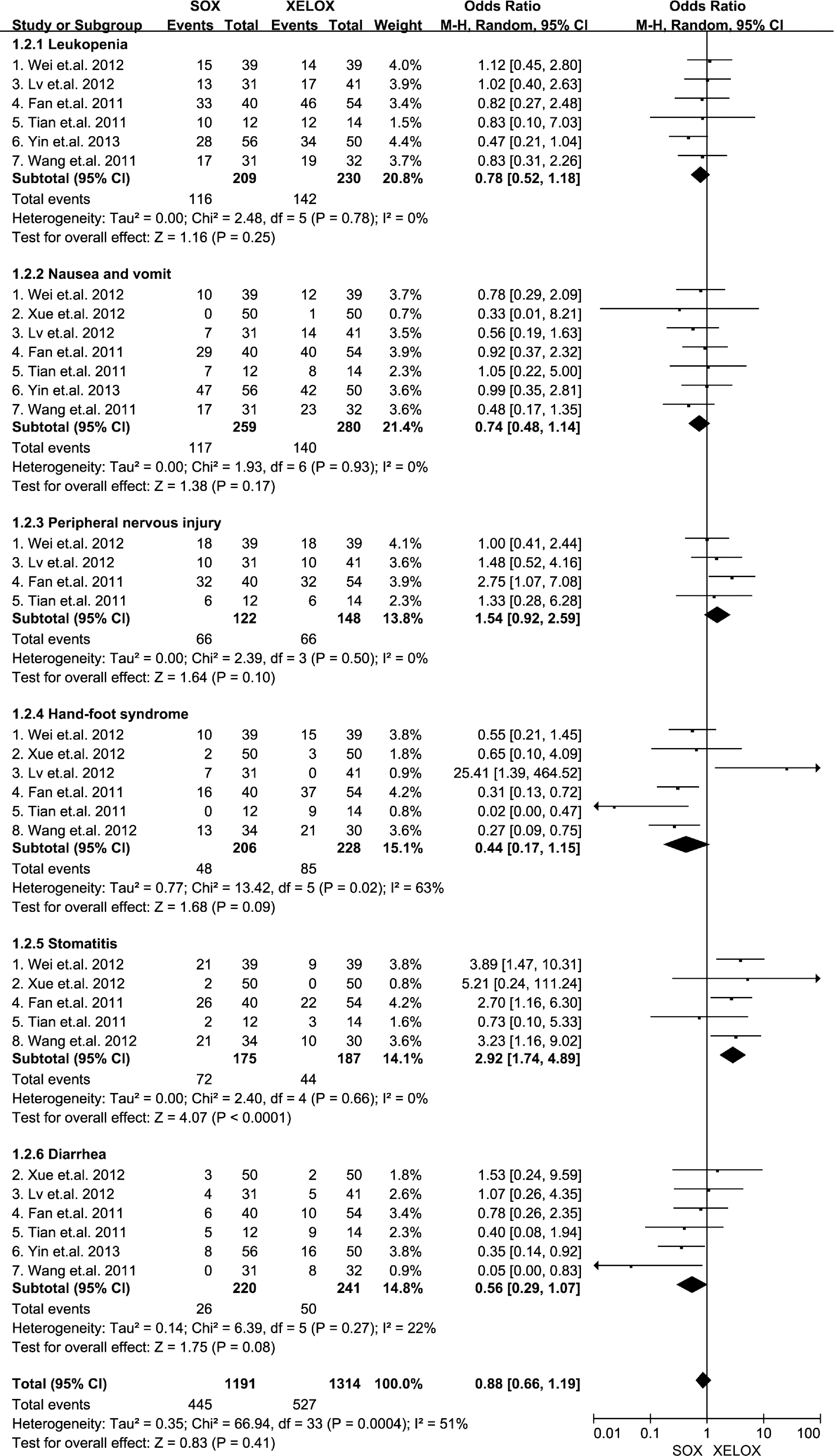
图3 SOX方案与XELOX方案化疗的不良反应评价森林图矩形及横线分别代表OR的点估计值和95% CI;棱形代表合并OR值和95% CIFig.3 Forest plot of the adverse reactions between SOX and XELOXThe estimate of OR and its 95% CI is plotted with a box and a horizontal line; ◆,pooled OR and its 95% CI
3 讨论
奥沙利铂联合替吉奥(SOX)或奥沙利铂联合卡培他滨(XELOX)是目前治疗进展期胃癌的常用化疗方案。其中,奥沙利铂是第二代铂类药物,具有水溶性好、低毒和抗癌谱广的特点,可广泛与其他化疗药物联用,可增强疗效、降低副反应[17]。替吉奥则是氟尿嘧啶的衍生口服剂型,包含替加氟、吉美嘧啶和奥替拉西3种成分[18]。替加氟可在体内转化为氟尿嘧啶,具有口服吸收好、生物利用度高等优点;且替加氟化疗指数为氟尿嘧啶的2倍,毒性仅为氟尿嘧啶的1/4~1/7,抗肿瘤活性较高。卡培他滨也是氟尿嘧啶的口服剂型,能以完整药物经肠黏膜进入肝脏,分别经过羧酸酯酶、胞苷脱氨酶催化,在肿瘤组织中由胸苷磷酸化酶将5’-脱氧-5-氟尿苷水解为5-氟尿嘧啶,提高了癌组织内药物的浓度、减少了全身毒性作用。
本文就替吉奥联合或卡培他滨联合奥沙利铂治疗中国进展期胃癌患者的有效性和安全性进行了Meta分析,结果显示:2种方案治疗进展期胃癌的有效性无差异;不良反应方面,2种方案总的不良反应发生率无显著性差异;但亚组分析显示,SOX方案口腔黏膜炎的发生率明显高于XELOX方案,其他不良反应无差异。
由于本文所纳入的原始文献仅有部分对患者1年或5年生存率进行评价,因此,未能对进展期胃癌患者的中位生存期进行系统评价,可能在一定程度上影响了Meta的质量。本研究潜在的缺陷包括:①纳入文献质量不均,且为二次研究,受原始研究潜在偏倚的限制;②纳入文献均来自中国,存在发表偏倚的可能性较大;③各研究对象的基线情况相同可能会使合并后的结果存在潜在偏倚;④纳入研究在设计实施过程中可能存在一些潜在偏倚。
综上所述,本研究结果证实:在中国人群中,SOX方案和XELOX方案治疗进展期胃癌患者的有效性相当,总体不良反应发生率无显著差异,但SOX方案口腔黏膜炎的发生率较XELOX方案增加。由于受纳入文献质量的限制,本文所得结论需进一步论证,期待有大样本、高质量的随机对照研究进一步证实。
[1] Krejs GJ.Gastric cancer: epidemiology and risk factors[J].Dig Dis,2010,28(4-5):600-603.
[2] Yang D,Hendifar A,Lenz C,et al.Survival of metastatic gastric cancer: Significance of age,sex and race/ethnicity[J].J Gastrointest Oncol,2011,2(2):77-84.
[3] Sasako M,Inoue M,Lin JT,et al.Gastric Cancer Working Group report[J].Jpn J Clin Oncol,2010,40(Suppl 1):i28-i37.
[4] 谭换明,李恩孝.奥沙利铂联合卡培他滨治疗进展期胃癌临床观察[J].中国肿瘤临床与康复,2010,17(4):370-373.
[5] Eisenhauer EA,Therasse P,Bogaerts J,et al.New response evaluation criteria in solid tumours:Revised RECIST guideline(version 1.1)[J].Eur J Cancer,2009,45(2):228-247.
[6] 周际昌主编.实用肿瘤内科学[M].第2版.北京:人民卫生出版社,2003:28-30,45-46.
[7] 曹邦伟,于晶琳,荷欢,等.中国人群中HPV感染与食管癌发生关联的Meta分析[J].首都医科大学学报,2010,31(2):258-263.
[8] Song F,Gilbody S.Bias in meta-analysis detected by a simple,graphical test.Increase in studies of publication bias coincided with increasing use of meta-analysis[J].BMJ,1998,316(7129):471-471.
[9] 魏光敏.奥沙利铂联合卡培他滨或替吉奥治疗进展期胃癌的疗效比较[J].中国老年学杂志,2012,31(2):369-370.
[10] 薛永飞.奥沙利铂联合卡培他滨与奥沙利铂联合替吉奥治疗进展期胃癌的临床效果对比[J].中国实用医药,2012,7(28):133-134.
[11] 吕慧芳,张延新,韩黎丽,等.奥沙利铂联合替吉奥或卡培他滨治疗老年晚期胃癌的临床观察[J].中国医药导报,2012,9(23):61-63.
[12] 樊翠珍,初玉平,戴红.卡培他滨联合奥沙利铂与替吉奥联合奥沙利铂治疗进展期胃癌的对比研究[J].临床肿瘤学杂志,2011,16(8):725-727.
[13] 田姗,李曾.替吉奥与卡培他滨联合奥沙利铂治疗晚期胃癌效果对比分析[J].中国老年保健医学,2011,9(4):48-50.
[14] 殷蓓蓓,李岩,梁婧,等.替吉奥联合奥沙利铂治疗进展期胃癌56例临床观察[J].现代中西医结合杂志,2013,22(18):1971-1972.
[15] 王月,蔡哲,成建,等.替吉奥联合奥沙利铂治疗老年进展期胃癌的疗效[J].中国老年学杂志,2011,31(9):1504-1505.
[16] 王永顺,王延涛.替吉奥联合奥沙利铂治疗晚期胃癌的临床观察[J].中国肿瘤临床与康复,2012,24(5):428-430.
[17] Montagnani F,Turrisi G,Marinozzi C,et al.Effectiveness and safety of oxaliplatin compared to cisplatin for advanced,unresectable gastric cancer: a systematic review and meta-analysis[J].Gastric Cancer,2011,14(1):50-55.
[18] Shirasaka T,Shimamato Y,Ohshimo H,et al.Development of a novel form of an oral 5-fluorouracil derivative (S-1) directed to the potentiation of the tumor selective cytotoxicity of 5-fluorouracil by two biochemical modulators[J].Anticancer Drugs,1996,7(5):548-557.
(编校:王俨俨)
Meta-analysis of regimen SOX versus XELOX in treatment of Chinese patients with advanced gastric carcinoma
LI Yuan-jun1, XING Juan2, WU Han-chang3, WEI Xu3, ZHANG Hong-mei4Δ
(1.Air Force General Hospital, PLA, Beijing 100142, China; 2.College of Urban and Environmental Sciences, Peking University, Beijing 100871, China; 3.The Cadet Brigade, Fourth Military Medical University, Xi’an 710032, China; 4.Department of Clinical Oncology, The First Affiliated Hospital of Fourth Military Medical University, Xi’an 710032, China)
ObjectiveTo compare clinical outcome and adverse reactions between the regimens SOX and XELOX for chemotherapy of advanced gastric carcinoma in Chinese population.MethodsThe original articles on randomized controlled trials (RCTs) comparing the chemotherapy of SOX and XELOX in Chinese patients with advanced gastric carcinoma were recruited from the PUBMED, WANFANG, VIP and CNKI databases.The quality of the selected trials were assessed by JADAD method.Meta-analysis about the efficacy and safety of the two chemotherapy methods was performed by Rev Man 5.2.0 software (Cochrane-information Management System).ResultsEight RCT studies were recruited in our work, including 293 patients in the SOX treatment group and 310 in the XELOX treatment group.The analysis results showed that there was no significant difference in the effect of the two chemotherapy methods (OR=1.19, 95%CI: 0.86-1.64,P=0.29), and referred to the safety evaluation, the stomatitis (OR=2.29, 95%CI: 1.74- 4.89,P<0.0001) incidence in SOX treatment group was higher than XELOX treatment group, and in total, there was no significant difference in adverse reaction incidence of the two chemotherapy methods(OR=0.88, 95%CI: 0.66-1.19,P=0.41).ConclusionIn the chemotherapy of advanced gastric carcinoma in Chinese population, there is no significant difference in clinical response rate between SOX and XELOX, and the stomatitis incidence of SOX is significantly higher than that of XELOX.
advanced gastric carcinoma; SOX; XELOX; Meta-analysis
陕西省科技研究发展计划项目(2013KJXX-91)
李远军,男,本科,研究方向:化疗药物的临床应用,E-mail:yuanjunlee@126.com;张红梅,通讯作者,女,博士,副主任医师,研究方向:恶性肿瘤化疗、靶向治疗及癌痛诊治的临床研究,E-mail:zhm@fmmu.edu.cn。
R655;G642
A
1005-1678(2015)05-0056-05
