急诊再血管化治疗成人肝移植术后肝动脉血栓形成的长期预后
2015-07-07杨轶赵纪春严律南马玉奎黄斌袁丁李波文天夫杨家印王文涛徐明清魏永刚
杨轶 赵纪春 严律南 马玉奎 黄斌 袁丁 李波 文天夫杨家印 王文涛 徐明清 魏永刚
肝移植已经被作为治疗终末期肝病的有效治疗手段[1]。肝动脉血栓形成(hepatic artery thrombosis,HAT)是肝移植术后最主要和严重的血管并发症,显著影响移植物的存活和受者的预后[2-3]。HAT 根据其在肝移植术后的发生时间可分为早期HAT(发生于术后30 d 或4 周以内)和晚期HAT,早期HAT的发生率为4.4%,病死率为33.3%,成人受者病死率高于儿童(34.3%和25%,P <0.03)[3]。早期有学者认为再移植是治疗HAT 的首要措施[4],但受供肝来源短缺的限制[3]。外科手术再血管化通常被作为暂时缓解移植肝缺血或推迟再移植的手段[5]。近期众多研究发现,对于早期诊断或未发生爆发性肝坏死、肝功能衰竭或脓毒血症等严重危急生命的并发症的HAT 患者,急诊再血管化取得了良好效果[3,5-7]。然而Bekker 等[3]报道有30.3%通过再血管化治疗的HAT 患者,最终仍需接受再移植。因此,急诊再血管化治疗肝移植术后HAT 的有效性还需进一步的研究。本研究总结了四川大学华西医院肝移植中心肝移植术后发生HAT 的情况,不同治疗方式以及随访情况,并对其预后进行分析,旨在进一步研究急诊再血管化治疗肝移植术后HAT 的有效性。
1 资料与方法
1999 年2 月至2013 年12 月,本中心共完成925 例成人同种异体原位肝移植。其中,男性782 例(84.5%),女性143 例(15. 5%);平均年龄(45 ±10)岁。按照前文提到的HAT 判定及分类标准,共出现24 例(2. 6%)HAT,其中早期HAT 17 例(1.8%),晚期HAT 7 例(0.8%)。13 例(76.5%)早期HAT 患者经DUS 全数字超声系统诊断或怀疑,动脉造影或术中探查证实,立即予急诊再血管化;1 例(5.9%)于确诊HAT 后10 d 行再移植;3 例(17.6%)行介入溶栓或保守治疗。7 例晚期HAT患者中3 例(42.9%)行再移植;4 例(57.1%)因临床症状较轻予以保肝对症治疗,未行外科干预及介入治疗。
所有HAT 患者临床及随访资料由中国肝移植注册数据库和患者原始病历获得,研究随访时间截至2013 年12 月31 日。
1.1 肝移植手术方式
供者类型为心脏死亡器官捐献供者及活体供者,供者评估及筛选按照常规进行。肝移植手术过程按本中心常规进行。肝动脉吻合采取个体化重建方案,选择直径相近的供、受者动脉进行吻合。对于受者肝总动脉闭塞、内膜夹层、动脉变异或供者动脉过短不适合直接端端吻合时,采用自体大隐静脉或冷冻保存的尸体髂动脉间置搭桥或采用上述血管搭桥行肾下腹主动脉受者肝动脉吻合。吻合在3.5 倍手术放大镜下完成,多数采用7-0/8-0 prolene 线后壁缝合第1 针的连续缝合方式。
1.2 HAT 预防及监测
吻合完成并开放动脉血流后,予以静脉滴注前列地尔20 μg。术后在确定无活动性出血且密切监测凝血功能的情况下,予以低分子肝素钙注射液(速碧林®)0.4 mL 皮下注射,每12 小时1 次。
肝动脉吻合完成后予以术中超声检查,判断吻合口血流情况;肝移植术后第1 周每12 小时行床旁DUS 检查,第2 周每天行床旁DUS 检查监测肝动脉血流是否通畅。出院后1 ~6 个月根据患者具体情况定期随访复查DUS,了解肝动脉血流情况。
1.3 HAT 处理方式
一经DUS 检查发现或怀疑HAT,马上进行动脉造影确诊。确诊HAT 后,在患者无严重出血倾向的前提下,放置溶栓导管于肝动脉血栓近端,予以持续性灌注尿激酶50 万U(用生理盐水稀释到50 mL)溶栓,6 h 后复查动脉造影。若肝动脉血流恢复则继续行抗凝治疗;若肝动脉血流未恢复,则根据患者情况尽快进行剖腹探查,行肝动脉再血管化,主要包括肝动脉血栓切除、血管成形和肝动脉再重建3 个过程。具体为:(1)拆除原肝动脉吻合口,采用3 F Fogarty 取栓导管取出动脉内血栓,观察供者端肝动脉返流血的情况,若无明显返流血,则向供者端肝动脉内直接推注尿激酶25 万U(生理盐水稀释到20 mL),并用无损伤血管阻断钳夹闭供者端肝动脉10 min;(2)供者端肝动脉回血良好后,观察供、受者端肝动脉内膜情况,予以5%肝素生理盐水冲洗管腔并适当修整、成形;(3)若血管长度不够,可行自体大隐静脉间置搭桥;如受者动脉因夹层、外膜下血肿或闭塞难以重建时,采用自体大隐静脉或冷冻保存尸体髂动脉间置搭桥行受者肾下腹主动脉-供者肝动脉吻合,再次重建肝动脉血流。
本研究中围手术期急诊再血管化治疗HAT 成功的定义为:围手术期无肝动脉血栓复发;无HAT所致的移植物功能衰竭、肝脓肿、脓毒血症;无HAT导致的再移植;无HAT 导致的患者死亡。治疗失败的定义为:围手术期肝动脉血栓复发;发生HAT 所致移植物功能衰竭、肝脓肿、脓毒血症;HAT 导致再移植;HAT 导致患者死亡。
1.4 统计学方法
采用SPSS 17.0 统计软件进行数据处理。计量资料用均数±标准差)或中位数表示,组间比较采用Student t 检验或Mann-Whitney U 检验。计数资料用百分比表示,组间比较采用χ2检验或Fisher 确切概率法。采用Kaplan-Meier 法计算肝移植术后发生HAT 患者再血管化治疗后的生存率。P <0.05 为差异有统计学意义。
2 结 果
17 例早期HAT 患者诊断为HAT 的中位时间为肝移植术后3 d(1 ~20 d),其中13 例行急诊再血管化治疗的HAT 患者,在明确诊断后立即行急诊肝动脉血栓切除+受者肾下腹主动脉供者肝动脉自体大隐静脉间置搭桥术;围手术期9 例(69.2%)患者再血管化成功,肝动脉血流恢复,痊愈出院;4 例(30.8%)患者再血管化治疗失败。未进行外科干预治疗的3 例早期HAT 患者均发生院内死亡,其中2 例(66.7%)仅行保守治疗,分别于肝移植术后3 d和28 d 死于多器官功能障碍综合征(multiple organ dysfunction syndrome,MODS);1 例(33.3%)行介入导管溶栓治疗后,肝动脉血流恢复,但于肝移植术后36 d 死于急性排斥反应所致的MODS。1 例行再移植治疗的早期HAT 患者存活至今。13 例行急诊再血管化的患者及移植物1 年生存率为61.5%。
9 例围手术期行急诊再血管化治疗成功的早期HAT 患者资料见表1。随访至2013 年12 月31 日,患者与移植物1、3、5 年生存率分别为88. 9%、77.8%和62.2%。3 例患者死亡,死亡前均未出现因HAT 所致的肝脓肿、移植物功能不全或胆道并发症;1 例恶性肝病患者于肝移植术后5 个月因肿瘤复发死亡;1 例于肝移植术后26 个月死于心血管意外;1 例于肝移植术后14 个月出现慢性排斥反应致移植物失功,家属放弃治疗后死亡。其余6 例至今存活,未出现明显的HAT 相关并发症及移植物失功。
4 例血管化失败的早期HAT 患者中,1 例在肝移植术后第7 天发生HAT,再血管化术后多发肝脓肿,移植物功能衰竭,行再移植术后第1 天死于弥漫性血管内凝血和MODS;1 例在肝移植术后第12 天发生HAT,再血管化后出现移植物功能衰竭,于肝移植术后第18 天死于MODS;1 例再血管化后2 个月复发HAT,导致肝脓肿及移植物功能不全,家属放弃治疗后死亡;1 例患者肝移植术后移植物功能不全,且在术后第3 天出现急性排斥反应,术后第12 天发生HAT,于再血管化后11 d 死于MODS。
13 例行急诊再血管化治疗的早期HAT 患者,治疗成功的患者肝移植术后到确诊HAT 的中位时间早于治疗失败患者,差异有统计学意义(3 d 和9.5 d,P=0.005)。两组性别、年龄、原发病、Child 评分、MELD 评分、总手术时间、热缺血时间、冷缺血时间、动脉吻合时间、术中输血量等临床指标相比差异均无统计学意义(P 均>0.05)。详见表2。
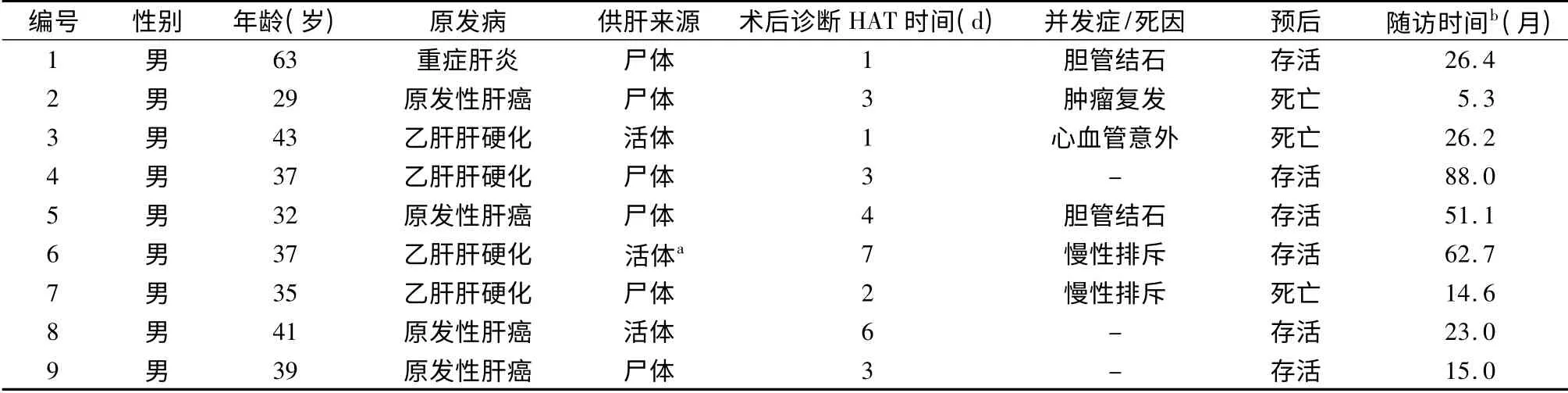
表1 9 例急诊再血管化治疗成功的早期HAT 患者资料

表2 急诊再血管化治疗成功和失败的早期HAT 患者临床资料比较
7 例晚期HAT 患者肝移植术后到诊断为HAT的中位时间为52 d (30 ~70 d)。3 例行再移植的晚期HAT 患者中,1 例于死于胃漏所致的腹腔大出血,1 例死于MODS,1 例至今存活。4 例未经外科干预的晚期HAT 患者中,1 例死于HAT 所致的移植物功能衰竭,另外3 例至今存活。
3 讨 论
HAT 是肝移植术后一种非常严重的并发症,通常发生在肝移植术后早期,并且伴随着肝移植受者移植物功能衰竭和死亡率的增高[3]。早期HAT 若不及时发现,通常导致爆发性移植物功能衰竭或胆道坏死[4,8]。晚期HAT 则因为肝动脉侧支循环的形成,可能表现相对轻微[8-10]。20 世纪80 年代开展肝移植的初期,早期HAT 患者若不进行再移植则预后极差[4]。但再移植受限于供肝短缺[3],并且再移植本身就被很多学者认为是发生HAT 的危险因素之一[11-12]。
外科手术再血管化仅被作为一部分早期HAT 患者或临床症状较轻的肝移植术后HAT 患者避免再移植的措施[2-3,5]。一些缺乏急诊再移植条件[13]或主要以活体肝移植为主[14-16]的移植中心也将急诊再血管化作为治疗HAT 的首选。再血管化包括手术探查、血栓切除、血管成形及再重建等方式。随着众多移植中心在肝移植术后常规行DUS 监测和筛查HAT[3],使HAT 患者得以在未出现严重的移植物功能衰竭、严重脓毒血症或胆道坏死之前被发现和诊断[17]。本中心常规在肝移植术后第1 周,每12 小时进行1 次超声检查,第2 周内每天1 次以确定肝动脉的血流通畅,出院后1 ~6 个月根据患者具体情况定期随访复查DUS 以了解肝动脉通畅情况[18]。本研究中,早期HAT 患者肝移植术后到诊断为HAT 的中位时间为3 d (1 ~20 d),晚期HAT 患者为52 d (30 ~70d)。
本文分析了肝移植术后发生早、晚期HAT 患者在不同治疗方案下的长期预后情况。925 例肝移植受者中,共发生24 例HAT,其中早期HAT 17 例,晚期7 例。早期HAT 发生率与其他学者的报道接近[3],但晚期HAT 发生率相对较低[12]。7 例晚期HAT 患者中3 例行再移植,其中有2 例死于术后并发症,1 例至今存活。13 例早期HAT 患者中有1 例接受再移植,存活至今。因此,4 例接受再移植的HAT 患者1 年生存率仅为50%。我们分析本中心HAT 患者再移植治疗预后不佳的原因在于:患者在等待肝源的过程中病情恶化,接受再移植手术时一般情况均较差,且再次手术必然带来更多的失血,手术时间亦更长。Singhal 等[19]总结了目前世界上不同移植中心报道的69 例采用血管腔内介入溶栓治疗HAT,取得了比较好的效果(成功率为68%)。本研究3 例接受保守或腔内介入溶栓治疗的早期HAT 患者均发生院内死亡,由于病例数较少,对于非外科干预治疗早期HAT 的疗效还需要更多病例进一步研究方能合理评价。
出现HAT 后,能否早期恢复肝脏的动脉血供对于胆道的意义重大,因为胆道的血供完全依靠肝动脉,HAT 使胆道缺血,可能导致胆道坏死或晚期形成狭窄[5]。本研究对9 例行急诊再血管化成功的患者进行长期随访,中位随访时间26.2 个月(5.3 ~88 个月),患者肝动脉血流保持通畅,移植物功能正常,仅有2 例术后出现胆管结石,并未出现胆道狭窄或因胆道并发症引发的移植物功能衰竭。
Duffy 等[2]报道86 例HAT 患者(儿童+成人)急诊再血管化的成功率仅为10%。Warnnar 等[17]报道儿童HAT 再血管化成功率为38%。近期Bekker 等[3]系统评价中报道HAT 再血管化的总体成功率为50%,儿童和成人类似,但最终30.3%患者仍需接受再次移植。Pinna 等[7]也报道17 例因HAT 行急诊肝动脉血栓切除+再血管化的患者中,11 例(64.7%)在没有再移植的情况下存活(平均随访时间17 个月)。出现这种差异可能是由于各中心再血管化的手术方式、是否需再移植的纳入标准、患者耐受程度、再血管化时的移植物功能各有不同造成[19]。本研究中13 例早期HAT 患者接受急诊再血管化后,1 年内有4 例(30.8%)出现了血栓复发或移植物功能不全,需要接受再次移植,围手术期再血管化成功的患者比例为69. 2% (9/13)。对9 例再血管化成功的早期HAT 患者进行长期随访,6 例在不需要再移植的情况下存活,3 例发生非HAT 相 关 性 死 亡;其1、3、5 年 生 存 率 分 别 为88.9%、77.8%和62.2%。提示再血管化成功后可以给早期HAT 患者带来相当大的获益。
众多学者认为从发生HAT 到诊断的时间间隔长短是急诊再血管化能否成功的关键因素[17,20]。Bekker 等[3]报道将DUS 作为术后常规HAT 筛查方式的移植中心,HAT 后再血管化的成功率高于不用DUS 常规筛查的中心(66.1%和44.9%)。Scarinci等[20]报道在肝移植术后1 周内进行急诊再血管化能有效地减少移植物功能衰竭的发生并改善患者的预后。本研究将急诊再血管化成功和失败患者进行分析比较,试图找出引起再血管化失败的危险因素。结果发现,再血管化成功患者肝移植术后诊断HAT的时间早于再血管化失败的患者,两组患者中位诊断时间分为肝移植术后3 d 和9.5 d(P <0.05),其余临床资料差异无统计学意义。
本研究结果提示,肝移植术后早期HAT 的发生率高于晚期HAT,HAT 显著影响肝移植受者及移植物生存率。急诊再血管化治疗肝移植术后早期HAT 患者,约70%可以长期保持肝动脉通畅,有效地提高了受者及移植物生存率,尤其是对肝移植术后1 周内发生HAT 的患者。急诊再血管化治疗HAT 成功的关键在于早期诊断和治疗。
1 Consensus Conference on Indications of Liver Transplantation. Paris,France,June 22-23,1993[J]. Hepatology,1994,20(1 Pt 2):1S-68S.
2 Duffy JP,Hong JC,Farmer DG,et al. Vascular complications of orthotopic liver transplantation:experience in more than 4,200 patients[J]. J Am Coll Surg,2009,208(5):896-905.
3 Bekker J,Ploem S,de Jong KP. Early hepatic artery thrombosis after liver transplantation:a systematic review of the incidence,outcome and risk factors[J]. Am J Transplant,2009,9(4):746-757.
4 Tzakis AG,Gordon RD,Shaw BW Jr,et al. Clinical presentation of hepatic artery thrombosis after liver transplantation in the cyclosporine era[J]. Transplantation,1985,40(6):667-671.
5 Langnas AN,Marujo W,Stratta RJ,et al. Hepatic allograft rescue following arterial thrombosis. Role of urgent revascularization[J].Transplantation,1991,51(1):86-90.
6 Sheiner PA,Varma CV,Guarrera JV,et al. Selective revascularization of hepatic artery thromboses after liver transplantation improves patient and graft survival[J]. Transplantation,1997,64(9):1295-1299.
7 Pinna AD,Smith CV,Furukawa H,et al. Urgent revascularization of liver allografts after early hepatic artery thrombosis[J]. Transplantation,1996,62(11):1584-1587.
8 Bhattacharjya S,Gunson BK,Mirza DF,et al. Delayed hepatic artery thrombosis in adult orthotopic liver transplantation-a 12-year experience[J]. Transplantation,2001,71(11):1592-1596.
9 Wozney P,Zajko AB,Bron KM,et al. Vascular complications after liver transplantation: a 5-year experience [J]. AJR Am J Roentgenol,1986,147(4):657-663.
10 Segel MC,Zajko AB,Bowen A,et al. Hepatic artery thrombosis after liver transplantation:radiologic evaluation[J]. AJR Am J Roentgenol,1986,146(1):137-141.
11 Silva MA,Jambulingam PS,Gunson BK,et al. Hepatic artery thrombosis following orthotopic liver transplantation: a 10-year experience from a single centre in the United Kingdom[J]. Liver Transpl,2006,12(1):146-151.
12 Oh CK,Pelletier SJ,Sawyer RG,et al. Uni-and multi-variate analysis of risk factors for early and late hepatic artery thrombosis after liver transplantation[J]. Transplantation,2001,71(6):767-772.
13 Matsuda H,Yagi T,Sadamori H,et al. Complications of arterial reconstruction in living donor liver transplantation:a single-center experience[J]. Surg Today,2006,36(3):245-251.
14 Uchiyama H,Hashimoto K,Hiroshige S,et al. Hepatic artery reconstruction in living-donor liver transplantation:a review of its techniques and complications[J]. Surgery,2002,131(1 Suppl):S200-S204.
15 Okazaki M, Asato H, Takushima A, et al. Hepatic artery reconstruction with double-needle microsuture in living-donor liver transplantation[J]. Liver Transpl,2006,12(1):46-50.
16 Inomoto T,Nishizawa F,Sasaki H,et al. Experiences of 120 microsurgical reconstructions of hepatic artery in living related liver transplantation[J]. Surgery,1996,119(1):20-26.
17 Warnaar N,Polak WG,de Jong KP,et al. Long-term results of urgent revascularization for hepatic artery thrombosis after pediatric liver transplantation[J]. Liver Transpl,2010,16(7):847-855.
18 Yang Y,Yan LN,Zhao JC,et al. Microsurgical reconstruction of hepatic artery in A-A LDLT:124 consecutive cases without HAT[J]. World J Gastroenterol,2010,16(21):2682-2688.
19 Singhal A,Stokes K,Sebastian A,et al. Endovascular treatment of hepatic artery thrombosis following liver transplantation[J]. Transpl Int,2010,23(3):245-256.
20 Scarinci A,Sainz-Barriga M,Berrevoet F,et al. Early arterial revascularization after hepatic artery thrombosis may avoid graft loss and improve outcomes in adult liver transplantation[J]. Transplant Proc,2010,42(10):4403-4408.
