气相色谱-质谱法测定香桂化浊胶囊中桂皮醛的含量*
2015-06-24吴丹张辰辰杨继章刘红淼
吴丹,张辰辰,杨继章,刘红淼
(河北医科大学第一医院药剂科,石家庄 050031)
气相色谱-质谱法测定香桂化浊胶囊中桂皮醛的含量*
吴丹,张辰辰,杨继章,刘红淼
(河北医科大学第一医院药剂科,石家庄 050031)
目的 建立气相色谱-质谱法测定香桂化浊胶囊中桂皮醛含量。方法 采用HP-5弹性石英毛细管色谱柱(30 m×0.25 mm,0.25 μm),载气:氦气,流速:1.0 mL·min-1,分流比:50:1,程序升温,进样量1.0 μL。结果 香桂化浊胶囊中桂皮醛和其他成分的分离度良好,在0.02~4.00 mg·mL-1范围内线性关系良好,相关系数为0.999 4。桂皮醛的平均加样回收率为96.2%,RSD<2.11%。结论 该方法操作简便,定量准确,适用于香桂化浊胶囊中桂皮醛的含量测定。
香桂化浊胶囊;桂皮醛;气相色谱-质谱法;含量测定
香桂化浊胶囊处方为河北医科大学第一医院临床应用多年的经验方,由肉桂、土大黄、广藿香等组成。具有芳香醒脾、清化湿浊之功。主治因各种疾病后邪留未尽、脾胃内伤所致长期大便溏泄或有黏液、腹胀肠鸣、纳呆或有低热、舌苔白腻或白滑或见微黄、脉濡缓;主要用于慢性肠炎、真菌感染致肠炎证属脾虚湿困的治疗。关于本方制剂工艺、HPLC-PDA指纹图谱、毒理学研究及该胶囊中百秋里醇、大黄素的含量测定已有报道[1-8]。鉴于香桂化浊胶囊在化学组成上是一个复杂体系,其主要的挥发油成分为桂皮醛和广藿香醇,关于广藿香醇的气相色谱研究已有报道[3],为更好控制香桂化浊胶囊的质量,完善其检测标准,笔者在本实验采用气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)法[9-11],建立香桂化浊胶囊中桂皮醛的含量测定方法。
1 仪器与材料
1.1 仪器 7890-5975N型气相色谱-质谱仪(美国Agilent公司 );7890-5975N型弹性石英毛细管色谱柱(美国Agilent Technologies公司);BS210S型电子分析天平(北京赛多利斯天平有限公司,量程:210 g,分度值:0.1 mg);套式恒温器(浙江新华医疗器械厂);KQ2200E型超声波清洗仪(频率:40 kHz,功率:100 W,昆山市超声仪器有限公司),EYELA 旋转薄膜蒸发仪(上海爱郎仪器有限公司)。
1.2 试药 乙酸乙酯(天津市凯通化学试剂有限公司,色谱纯),其他试剂均为分析纯。香桂化浊胶囊(河北医科大学第一医院制剂室,批号:120607,120611,120625)。桂皮醛对照品(四川省维克奇生物科技有限公司,批号:101114,纯度:≥98%)。
2 方法与结果
2.1 GC-MS条件 HP-5弹性石英毛细管色谱柱(30 m×0.25 mm,0.25 μm) ;载气:氦气,流速:1.0 mL·min-1,分流比:50:1;采用程序升温:起始温度100 ℃,保持2 min,以3 ℃·min-1升到 130 ℃,保持5 min,再以10 ℃·min-1升到210 ℃ ,保持 5 min;进样口温度230 ℃ ,进样量1.0 μL;电子轰击(EI)离子源,离子源温度230 ℃,电子能量70 eV;柱前压65.072 kPa;四级杆质量分析器;扫描方式:全扫描;质核比范围:10~400 amu。
2.2 溶液的配制
2.2.1 对照品溶液的配制 取桂皮醛对照品20.031 8 mg精密称定,置25 mL 量瓶中,加乙酸乙酯溶解并稀释至刻度,摇匀,得对照品溶液。
2.2.2 供试品溶液的配制 取1粒胶囊内容物,精密称定0.391 7 g,加乙酸乙酯20 mL,超声30 min,过滤,旋蒸至残留液3 mL,转移至10 mL量瓶,用乙酸乙酯稀释至刻度。过筛孔内径0.45 μm微孔滤膜,取续滤液,摇匀作供试品溶液。
2.3 方法学验证
2.3.1 系统适用性实验与专属性实验 在上述色谱条件下,分别吸取对照品溶液、供试品溶液各1.0 μL,注入气质联用仪,色谱图见图 1。桂皮醛与其他成分分离良好,分离度> 1.5,理论板数>50 000。
2.3.2 线性关系考察 精密量取对照品溶液 0.25,0.5,1.0,2.0,2.5,5.0 mL置 10 mL量瓶中,分别用乙酸乙酯稀释至刻度,摇匀得 1~6号工作液。在上述色谱条件下,吸取1.0 μL,注入气质联用仪,记录色谱峰面积。以桂皮醛成分峰面积(Y)为纵坐标,浓度(C)为横坐标,绘制标准曲线。得线性回归方程Y=281 786C+2×106,r=0.999 4,桂皮醛在0.02~4.00 mg·mL-1范围内线性关系良好。
2.3.3 检测限和定量限 取线性最低点对照品溶液对倍稀释,以S/N=3计,桂皮醛最低检测限为0.75 μg·mL-1,以S/N=10计,桂皮醛定量限为2.51 μg·mL-1。
2.3.4 精密度实验 取 “2.2.2”项供试品溶液,重复进样 6次,计算桂皮醛的色谱峰峰面积RSD为1.64%,表明该方法精密度良好。
2.3.5 稳定性实验 取 “2.2.2”项供试品溶液,在制备后 0,2,4,8,12,24 h进样,桂皮醛色谱峰峰面积的RSD为1.76%,表明桂皮醛供试品溶液在 24 h内稳定。
2.3.6 重复性实验 取同一批号的香桂化浊胶囊,按“2.2.2”项制备供试品溶液6份,按上述色谱条件进行测定,桂皮醛含量的RSD为1.81%,表明该方法的重复性良好。
2.3.7 加样回收率实验 取已知桂皮醛含量的同一批号样品6份,每份约0.08 mg,加入对照品溶液(每毫升含桂皮醛0.1 mg) 1 mL,按 “2.2.2”项方法配制溶液,分别进样测定,计算加样回收率。桂皮醛的回收率为96.2%,RSD为2.11%。
2.4 样品含量测定 按 “2.2.2”项下方法制备 3批供试品溶液,进样1.0 μL,每份样品进样 3次,以标准曲线法计算香桂化浊胶囊中桂皮醛的含量。样品含量测定结果见表1。根椐此结果,同时考虑药材的来源以及制剂生产、贮藏等因素,以每粒胶囊0.39 g装量计,暂定本品每粒含桂皮醛不得少于 0.48 mg。
表1 香桂化浊胶囊中桂皮醛成分的含量测定结果
Tab.1 Content determination of cinnamic aldehyde inXiangguiHuazhuocapsulesn=3

3 讨论
本研究采用GC-MS法对香桂化浊胶囊中的桂皮醛含量进行测定,通过对色谱和质谱条件的优化,比较不同流速、柱温等,确定了测定香桂化浊胶囊中桂皮醛含量的方法,大大提高定量结果的可靠性和准确性。
香桂化浊胶囊中含有桂皮醛、百秋李醇、长叶醛、甘菊蓝、邻甲氧基桂皮醛等多种挥发性成分,其极性和沸点相差较大,本实验采用程序升温法,在较短的时间内保证溶剂乙酸乙酯和其他低极性、低沸点成分达到良好分离。
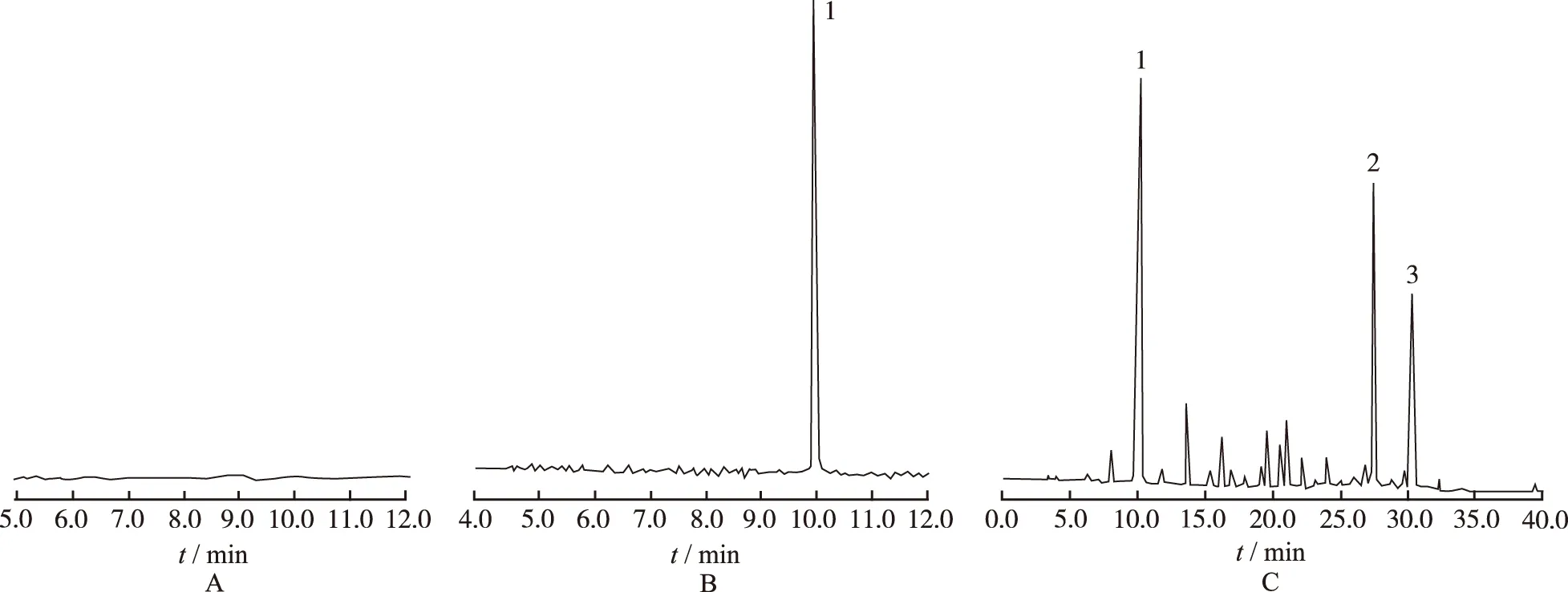
A.阴性对照品;B.桂皮醛对照品;C.桂皮醛供试品;1.桂皮醛;2.百秋李醇;3.长叶醛
A.negative control;B.cinnamic aldehyde control;C.sample of cinnamic aldehyde;1.cinnamic aldehyde;2.patchouli alcohol;3.Long leaf aldehyde
Fig.1 The gas chromatogram of cinnamic aldehyde of negative reference substance, reference substance and sample
本研究所建立的GC-MS分析色谱条件,精密度、稳定性、重复性良好,采用HP-5毛细管气相色谱法测定香桂化浊胶囊中桂皮醛的含量,该方法操作简便、重复性好、专属性强、准确可靠,可作为香桂化浊胶囊中桂皮醛的质量控制。
[1] 刘红淼,姜少灏,张振杰,等.正交实验优选香桂化浊胶囊中挥发油的包合工艺[J].中国药房,2010,21(47):4449-4450.
[2] 刘红淼,房桂珍,李艳玲,等.香桂化浊胶囊成型工艺研究[J].中国药房,2011,22(11):990-991.
[3] 刘红淼,杨继章,王云志,等.香桂化浊胶囊质量标准研究[J].中国药房,2011,22(27):2553-2554.
[4] 杨继章,刘红淼,李艳玲.肉桂油的研究进展[J].中国药房,2011,22(27):2579-2581.
[5] 刘红淼,杨继章,李艳玲.HPLC法测定香桂化浊胶囊中大黄素的含量[J].中国药房,2012,23(15):1397-1398.
[6] 刘红淼,李艳玲,杨继章,等.香桂化浊胶囊毒理学研究[J].医药导报,2013,32(2):159-162.
[7] 刘红淼,李艳玲,杨继章,等.香桂化浊胶囊的药效学研究[J].医药导报,2014,33(3):325-328.
[8] 张辰辰,杨继章,吴丹,等.香桂化浊胶囊的HPLC-PDA指纹图谱研究[J].医药导报,2014,33(1):86-89.
[9] 董岩,魏兴国,刘明成.肉桂挥发油化学成分的CG/MS分析[J].齐鲁药事,2004,23(3):34-35.
[10] 李玲玲,袁文杰.肉桂油气相色谱与气质联用分析[J].药物分析杂志,2000,20(2):116-118.
[11] 张桂芝,周恩芳.肉桂的红外光谱鉴定与气相色谱-质谱分析[J].现代中药研究与实践,2006,20(2):25-27.
DOI 10.3870/yydb.2015.03.025
Determination of Cinnamic Aldehyde Content inXiangguiHuazhuoCapsules by Gas Chromatography-Mass Spectrometry
WU Dan, ZHANG Chenchen, YANG Jizhang, Liu Hongmiao
(DepartmentofPharmacy,theFirstHospitalofHebeiMedicalUniversity,Shijiazhuang050031,China)
Objective To establish a method for determining cinnamic aldehyde content inXiangguiHuazhuocapsules by gas chromatography-mass spectrometry (GC-MS). Methods The content of cinnamic aldehyde was determined by GC-MS.Separation was performed on a capillary column (30 m×0.25 mm, 0.25 μm) with HP-5 as the stationary phase.A programmed temperature was employed.The flow rate was 1 mL·min-1with He as carrier gas, and split ratio was 50:1.The injection volume was 1.0 μL. Results The cinnamic aldehyde was well isolated from the other ingredients.A good linear relationships of cinnamic aldehyde in range of 0.02-4.00 mg·mL-1was observed.The correlation coefficient was 0.999 4.The average recovery of cinnamic aldehyde was 96.2%, and RSD was less than 2.11%. Conclusion The method is simple, accurate and suitable for determination of cinnamic aldehyde content.
XiangguiHuazhuocapsules; Cinnamic aldehyde; Gas chromatography-mass spectrometry; Content determination
2014-02-23
2014-06-11
*河北省中医药管理局科研计划课题资助项目(2013007)
吴丹(1989-),女,河北保定人,硕士,研究方向:药剂学。E-mail:1066912424@qq.com。
杨继章(1957-),男,河北邢台人,主任药师,教授,硕士研究生导师,研究方向:药物新剂型、药物稳定性。电话:0311-85917352,E-mail:yjzh1957@163.com。
R286;R927.2
B
1004-0781(2015)03-0376-03
