早期静脉应用β受体阻滞剂对急性心肌梗死患者预后影响的Meta分析
2015-06-09王丹宁陈鹏飞黄颖陈侃王磊廖德宁
王丹宁,陈鹏飞,黄颖,陈侃,王磊,廖德宁
荟萃分析
早期静脉应用β受体阻滞剂对急性心肌梗死患者预后影响的Meta分析
王丹宁,陈鹏飞,黄颖,陈侃,王磊,廖德宁
目的 系统评价再灌注时心肌梗死后早期静脉应用β受体阻滞剂对患者预后的影响。方法 检索Pubmed 、Embase 、Cochrane 图书馆、中国知网、万方数据知识服务平台、维普期刊资源整合服务平台、中国生物医学文献数据库,收集比较再灌注背景下心肌梗死后早期静脉使用β受体阻滞剂(试验组)不使用或者使用安慰剂(对照组)对患者预后影响的研究。主要观察指标为短期及长期的全因病死率及恶性心律失常、心肌再梗死、心源性休克等发生率。采用Revman5.2软件对提取的数据进行荟萃分析。结果 纳入8项临床研究,共48 367例患者。Meta分析显示,试验组与对照组相比,心肌梗死患者恶性室性心律失常发生率下降(OR=0.83, 95%CI 0.75~0.93,P=0.000 9);心源性休克、心力衰竭发生率增加(OR=1.29,95%CI 1.18~1.41,P<0.01),2组心肌梗死患者全因病死率、再梗死、缺血等不良事件发生率差异无统计学意义(OR=0.98 , 95%CI 0.92~1.05,P=0.63;OR=0.95 , 95%CI 0.88~1.03,P=0.21)。结论 在心肌梗死早期静脉给予β受体阻滞剂可以降低梗死后恶性室性心律失常发生率,但同时也有增加心源性休克、心力衰竭发生的风险,在改善病死率方面没有明显获益。
心肌梗死,急性;β受体阻滞剂;Meta分析
近几十年来,β受体阻滞剂始终在急性冠状动脉综合征尤其是急性心肌梗死的治疗中占有重要地位。MIAMI、ISIS-I等几个大规模的临床试验都提出早期静脉应用β受体阻滞剂可以降低急性心肌梗死患者早期病死率,长期用药可以降低病死率及再梗死率[1,2]。因此,2013年ACCF/AHA急性心肌梗死管理指南[3]强调无禁忌证者应口服β受体阻滞剂(Ib),而静脉给予β受体阻滞剂则作为IIa类推荐。然而,上述大多数研究均在药物治疗为主的背景下进行的,再灌注背景下进行的一些类似试验得到的结果却是褒贬不一,Roberts等[4]研究急性心肌梗死早期即刻静脉给予β受体阻滞剂与延迟给药对患者的影响时发现,尽管早期即刻给药降低了缺血事件的发生,却没有得到降低病死率的结论;Pfisterer等[5]在分析GUSTO试验资料时发现,静脉给予阿替洛尔后预后反而变差了。然而,也有研究获得了在经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)术前给予β受体阻滞剂可以改善预后的结论[6~9]。可见,随着β受体阻滞剂的广泛应用,对其的质疑与争议从未间断过,尤其在心肌梗死的治疗中,何时给药、以何种方式给药能得到最大获益?这些均未有明确结论。现采用Meta分析方式,回顾分析再灌注时代相关的研究,评价早期静脉给予β受体阻滞剂对心肌梗死患者预后的影响。
1 资料与方法
1.1 检索策略 通过计算机系统检索Pubmed、Embase、Cochrane图书馆、中国知网、万方数据知识服务平台、维普期刊资源整合服务平台、中国生物医学文献数据库。采用主题词与自由词结合的检索方式,语种仅限中英文,英文检索词为:“myocardial infarction ” “β-blockers” “ alprenolol” “atenolol” “bisoprolol” “carvedilol” “metoprolol”“practolol” “propranolol”“timolol”; 中文检索词为 :“心肌梗死”“β受体阻滞剂”“阿普洛尔”“阿替洛尔”“比索洛尔”“卡维地洛”“美托洛尔”“普拉洛尔”“普萘洛尔”“噻吗洛尔”。检索从1980年-2014年12月正式发表的文献。此外,还通过所获文献的引用文献及相关杂志的网站进行手工检索。
1.2 文献的纳入与排除标准 文献的纳入标准包括:(1)文献主要内容为比较再灌注治疗背景下心肌梗死早期静脉给予β受体阻滞剂的患者(试验组)与空白对照或安慰剂对照患者(对照组)的预后;(2)文献纳入患者需接受再灌注治疗,溶栓或PCI均可;(3)研究对象为诊断明确的心肌梗死患者或临床症状符合未明确诊断的疑似心肌梗死患者,除外β受体阻滞剂使用禁忌证,如有心力衰竭的体征、低心排状态、发生心源性休克的危险性高、高度房室传导阻滞及其他相对禁忌证;(3)预后指标包括患者随访期间的全因病死率及恶性室性心律失常、心源性休克、心力衰竭、心肌再梗死、心脏骤停等心脏不良事件发生率;(4)研究病例数量超过30例;(5)对于同一研究机构所发表的系列研究报道,选择与纳入标准相符的最新文献。文献的排除标准包括:(1)病例报道、经验交流、综述及评论类文献;(2)信息不全,不足以行Meta分析;(3)无研究关注的指标。
1.3 文献筛选与评价 由2名独立的研究者分别阅读检索到的文献,根据纳入与排除标准对文献进行筛选。文献的纳入需经2名研究者共同讨论才能决定;如遇到分歧,通过第3名研究者介入解决。根据Cochrane协助网推荐的方法对筛选文献进行质量评价,主要评估指标为:随机分配方案的产生、隐蔽分组、对患者和医生实施盲法、对结果评价实施盲法、不完整的结果数据、选择性的结果报告、其他偏倚。
1.4 资料的提取 提取的资料包括:(1)文献的一般信息,包括第一作者,发表年份,研究单位所在地;(2)研究对象的基本特征,样本数量,研究类型与方法学特征;(3)干预措施;(4)预后指标,随访时间,失访情况。
1.5 文献质量评价标准 采用Jadad质量计分法评价纳入研究的质量。评价内容:(1)是否随机序列;(2) 盲法的采用;(3)撤出与退出例数。评分1~2分为低质量研究,3~5分为高质量研究。
1.6 结局指标 主要观察指标为短期及长期的全因病死率及恶性心律失常、心肌再梗死、心源性休克等发生率。
1.7 统计学方法 采用Revman5.2软件对所提取的数据资料进行分析。计数资料采用优势比(OR)、相对危险度(RR)及其95%的可信区间(CI)作为效应量进行分析。采用χ2检验对文献进行异质性分析,当P≥0.10,I2≤50%时,采用固定效应模型进行Meta分析;当P<0.10,I2>50% 时,首先寻找异质性的原因,对可能导致异质性的因素进行亚组分析,采用随机效应模型进行Meta分析。发表偏倚通过目测漏斗图来评估。
2 结 果
2.1 纳入文献基本情况 经过检索相关数据库后,共检出文献2 583篇,通过浏览标题和摘要后剔除2 432篇,其余文献获取全文后仔细阅读,评估是否满足纳入及排除标准,最终筛选出8篇文献[4,9~15],计48 367例患者,进行荟萃分析。4项研究所选择的β受体阻滞剂为美托洛尔,其余4项分别为兰地洛尔、艾司洛尔、卡维地洛、阿替洛尔。4项研究对照组为安慰剂,3项研究对照组为空白对照,1项研究对照组选择延迟口服给药方式。纳入文献的基本信息见表1。
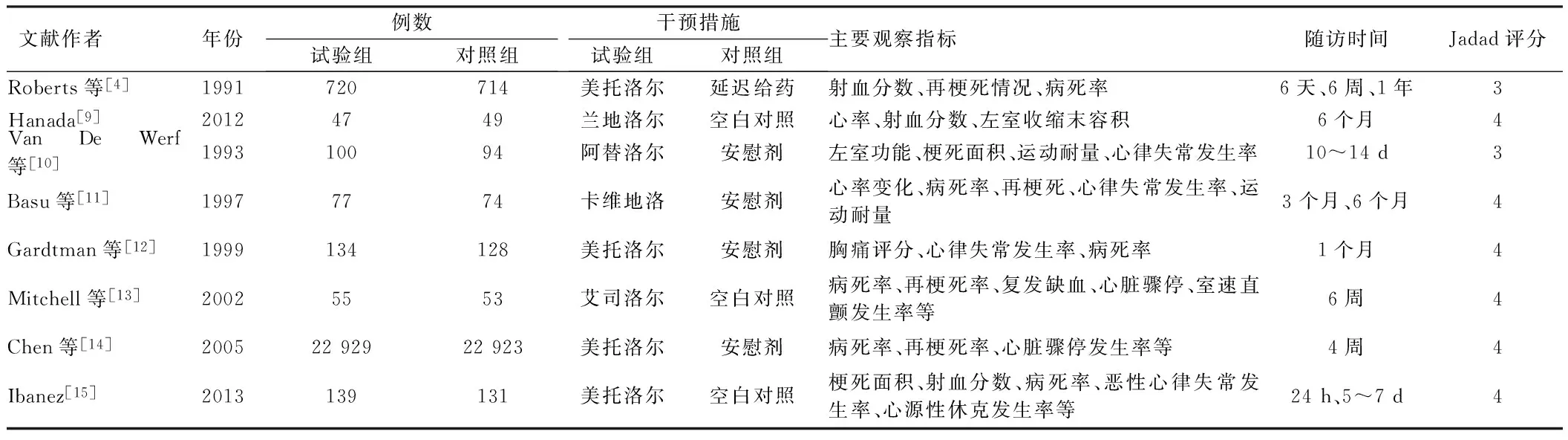
表1 纳入文献基本信息
2.2 Meta结果分析
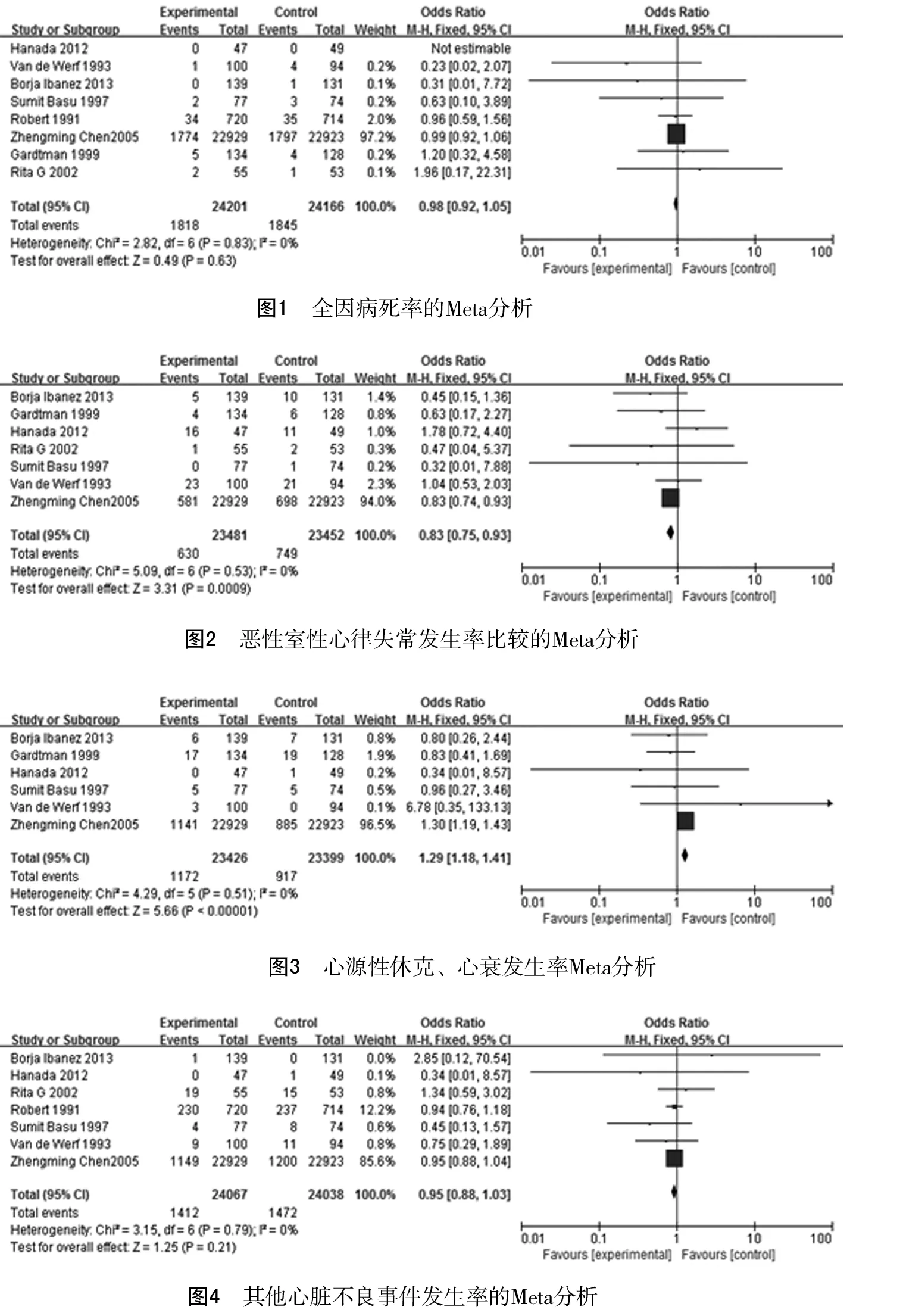
2.2.1 全因病死率: 8篇文献中均报道了全因病死率数据,试验组全因病死率7.5%,对照组全因病死率为7.6%,异质性检验I2= 0 %,提示合并分析文献间无统计学异质性(χ2= 2.82,P=0.83),选择固定效应模型合并分析,结果显示试验组与对照组的全因病死率之间无统计学差异(OR=0.98,95%CI 0.92~1.05,P=0.63)。见图1
2.2.2 恶性室性心律失常发生率: 8篇文献均分析了心律失常发生率,但Roberts等[4]的研究中对于心律失常的记录没有明确区分类型,没有记录到室速、室颤这类恶性室性心律失常发生情况,其余纳入文献均明确记录了室速、室颤的发生情况,因此在该项指标合并分析时,仅合并分析7篇文献,异质性检验I2= 0%,提示合并分析文献间无统计学异质性(χ2= 5.09,P=0.53),选择固定效应模型合并分析。试验组合并恶性心律失常发生率(2.7%)低于对照组(3.2%),差异有统计学意义(OR=0.83, 95%CI 0.75~0.93,P=0.000 9)。见图2。
2.2.3 心源性休克、心力衰竭发生率: 6篇文献报道了心源性休克、心力衰竭发生率。合并分析,异质性检验I2= 0%,提示合并分析文献间无统计学异质性(χ2=4.29,P=0.51),选择固定效应模型分析。试验组心源性休克、心力衰竭发生率为5%,对照组为3.9%,差异有统计学意义(OR=1.29,95%CI 1.18~1.41,P<0.01)。见图3。
2.2.4 再梗死、缺血等其他心脏不良事件: 该项指标主要包括心肌再梗死、复发缺血、心脏停跳等心脏不良事件的发生率,Gardtman等[12]的研究中主要分析了应用美托洛尔后短期内胸痛评分的变化及心律失常发生率、心衰发生率、病死率等几个指标,没有记录上述心肌再梗死、缺血等指标情况,因此分析该项指标时,仅合并分析其余7篇文献,异质性检验I2= 0%,提示合并分析文献间无统计学异质性(χ2= 3.15,P=0.79),表明研究结果间均无统计学异质性,选择固定效应模型分析。试验组合并后上述心脏不良事件发生率为5.9%,对照组为6.1%,差异无统计学意义(OR=0.95,95%CI 0.88~1.03,P=0.21)。见图4。
2.3 发表偏倚 以研究的OR值为横坐标,OR对数值标准误为纵坐标绘制漏斗图,几个分析的结果绘制漏斗图基本对称,以全因病死率的分析为例,漏斗图对称(见图5),纳入的文献所含数据不存在明显的偏倚性,Meta分析结果可信。
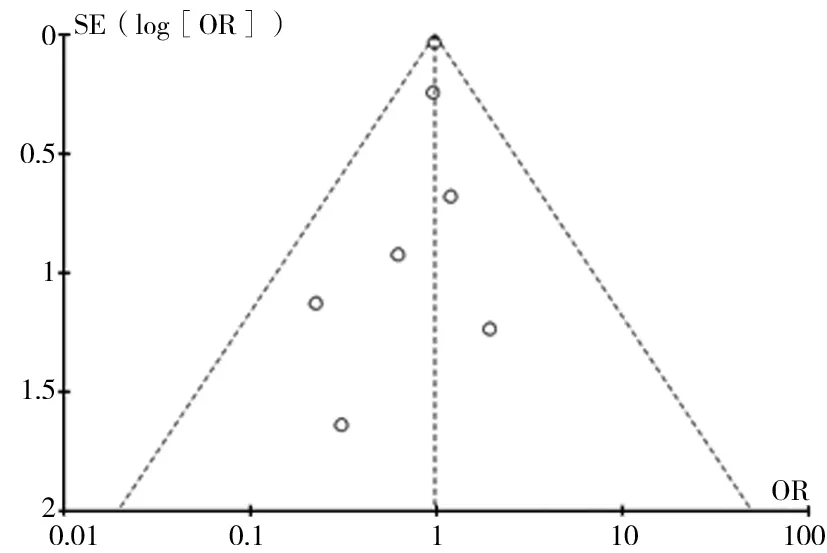
图5 全因病死率分析的漏斗图
3 讨 论
本研究共纳入了8篇文献,均满足再灌注治疗背景下对心肌梗死患者早期静脉应用β受体阻滞剂疗效分析的标准。通过对全因病死率、恶性室性心律失常发生率、心源性休克、心力衰竭发生率、再梗死、缺血等其他心脏不良事件发生率的分析,发现心肌梗死早期静脉应用β受体阻滞剂可以降低恶性室性心律失常发生率,但与对照组相比,在全因病死率、再梗死、缺血等事件发生率方面没有明显获益,同时增加了心源性休克、心力衰竭的发生率。
早期静脉用药可以使β受体阻滞剂在心肌梗死后尽早发挥作用,降低心肌耗氧、增加冠状动脉血流、降低梗死面积、提高射血分数等,从而更好地改善预后。既往许多研究也都提出了β受体阻滞剂可以降低心肌梗死后长期的病死率[16],但本研究中,在分析早期病死率这一指标时,与对照组相比,试验组并没有使心肌梗死患者得到明显获益。一方面可能由于本研究中纳入文献平均随访时间均在1年以内,得到的是短期预后的评价,与改善长期预后的观点并不矛盾;另一方面可能是由于既往研究大多集中在药物治疗为主的背景下,本身心肌梗死后病死率就比较高,应用β受体阻滞剂与不用药或服用安慰剂对比,β受体阻滞剂所带来的降低心肌耗氧、增加冠状动脉血流、降低梗死面积、提高射血分数这些作用显著,从而明显地降低了病死率,然而在再灌注时代,本身由于溶栓、介入手段的优势及药物治疗的辅助,心肌梗死后的病死率有了明显下降,在这样的背景下对比是否早期静脉应用β受体阻滞剂,用药的优势可能没有过去明显了。
β受体阻滞剂可以竞争性阻断心肌细胞上的β1受体,从而抑制心肌收缩力,减慢心率、降低心脏指数、降低体循环动脉血压从而降低心肌耗氧,改善心肌缺血、缺氧情况;另一方面通过阻断β受体,可以减弱心脏局部交感神经释放儿茶酚胺,降低局部及全身儿茶酚胺水平,降低心脏局部交感神经兴奋性,从而减低心律失常发生率。本研究对48 367例患者的情况综合分析发现,对合适的心肌梗死患者早期静脉应用β受体阻滞剂可以降低恶性室性心律失常的发生率。既往研究发现,心肌梗死后恶性室性心律失常多发生在缺血早期,缺血早期体内及心肌局部儿茶酚胺分泌均迅速增加,含量超过平时几十倍,我们推测,正因为如此,早期静脉给予β受体阻滞剂,可以及早阻断β受体,降低儿茶酚胺水平,从而改善恶性心律失常的发生情况。 本研究分析存在一定的局限性,再灌注治疗的时机与患者预后是相关的,研究表明,早期接受急诊PCI的心肌梗死患者病死率较低[17]。纳入研究中β受体阻滞剂使用种类不一致、在灌注前给药还是再灌注治疗后给药并未统一,这些对患者预后均会造成一定程度的影响,文中未能进一步分层分析;研究设计时考虑纳入条件限制较多,导致最终符合标准的试验较少,不排除存在各种偏倚的可能性,因此,虽然研究结果认为心肌梗死早期静脉给予β受体阻滞剂可以降低恶性心律失常发生率,但尚需要更多的涉及多中心、大样本的随机双盲对照试验来明确这一结论,在临床治疗中,仍需根据每一位患者的情况权衡利弊,谨慎选择早期静脉给药。
1 No authors Iisted.Metoprolol in acute myocardial infarction (MIAMI).A randomised placebo-controlled international trial. The Miami Trial Research Group[J].Eur Heart J,1985,6(3):199-226.
2 ISIS-1 collaborate group.Randomised trial of intravenous atenolol among 16 027 cases of suspected acute myocardial infarction: ISIS-1[J].Lancet,1986,2(8498):57-66.
3 American College of Emergency Physicians,Society for Cardiovascular Angiography and Interventions,O'gara PT,et al.2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines[J].J Am Coll Cardiol,2013,61(4):e78-140.
4 Roberts R,Rogers WJ,Mueller HS,et al.Immediate versus deferred beta-blockade following thrombolytic therapy in patients with acute myocardial infarction. Results of the Thrombolysis in Myocardial Infarction (TIMI) II-B Study[J].Circulation,1991,83(2):422-437.
5 Pfisterer M,Cox JL,Granger CB,et al.Atenolol use and clinical outcomes after thrombolysis for acute myocardial infarction: the GUSTO-I experience. Global Utilization of Streptokinase and TPA (alteplase) for Occluded Coronary Arteries[J].J Am Coll Cardiol,1998,32(3):634-640.
6 Harjai KJ,Stone GW,Boura J,et al.Effects of prior beta-blocker therapy on clinical outcomes after primary coronary angioplasty for acute myocardial infarction[J].Am J Cardiol,2003,91(6):655-660.
7 Halkin A,Grines CL,Cox DA,et al.Impact of intravenous beta-blockade before primary angioplasty on survival in patients undergoing mechanical reperfusion therapy for acute myocardial infarction[J].J Am Coll Cardiol,2004,43(10):1780-1787.
8 Valle JA,Zhang M,Dixon S,et al.Impact of pre-procedural beta blockade on inpatient mortality in patients undergoing primary percutaneous coronary intervention for ST elevation myocardial infarction[J].Am J Cardiol,2013,111(12):1714-1720.
9 Hanada K,Higuma T,Nishizaki F,et al.Randomized study on the efficacy and safety of landiolol, an ultra-short-acting β1-adrenergic blocker, in patients with acute myocardial infarction undergoing primary percutaneous coronary intervention[J].Circ J,2012,76(2):439-445.
10 Van De Werf F,Janssens L,Brzostek T,et al.Short-term effects of early intravenous treatment with a beta-adrenergic blocking agent or a specific bradycardiac agent in patients with acute myocardial infarction receiving thrombolytic therapy[J].J Am Coll Cardiol,1993,22(2):407-416.
11 Basu S,Senior R,Raval U,et al.Beneficial effects of intravenous and oral carvedilol treatment in acute myocardial infarction. A placebo-controlled, randomized trial[J].Circulation,1997,96(1):183-191.
12 Gardtman M,Dellborg M,Brunnhage C,et al.Effect of intravenous metoprolol before hospital admission on chest pain in suspected acute myocardial infarction[J].Am Heart J,1999,137(5):821-829.
13 Mitchell RG,Stoddard MF,Ben-Yehuda O,et al.Esmolol in acute ischemic syndromes[J].Am Heart J,2002,144(5):E9.
14 Chen ZM,Pan HC,Chen YP,et al.Early intravenous then oral metoprolol in 45,852 patients with acute myocardial infarction: randomised placebo-controlled trial[J].Lancet,2005,366(9497):1622-1632.
15 Ibanez B,Macaya C,Sánchez-Brunete V,et al.Effect of early metoprolol on infarct size in ST-segment-elevation myocardial infarction patients undergoing primary percutaneous coronary intervention: the Effect of Metoprolol in Cardioprotection During an Acute Myocardial Infarction (METOCARD-CNIC) trial[J].Circulation,2013,128(14):1495-1503.
16 Freemantle N,Cleland J,Young P,et al.Beta blockade after myocardial infarction: systematic review and meta regression analysis[J].BMJ,1999,318(720):1730-1737.
17 陈育苗,代明岩,邓国强,等.急性ST段抬高心肌梗死临床特点及院内再灌注方式对远期死亡的影响[J].中国现代医药杂志,2014,16(7):57-60.
The effect of early intravenous beta blockers on prognosis in patients with acute myocardial infarction: a Meta analysis
WANGDanning*,CHENPengfei,HUANGYing,CHENKan,WANGLei,LIAODening.*DepartmentofCardiology,ChangzhengHospital,SecondMilitaryMedicalUniversity,Shanghai200003,China
Correspondingauthor:LIAODening,E-mail:liao6007@163.com
Objective To evaluate the effect of early intravenous beta blockers on prognosis in patients with acute myocardial infarction(AMI).Methods Searched on PubMed, Embase, Cochrane library, CNKI, Wanfang Data,VIP journal resources integration service platform, the Chinese biomedical literature database, collected and compared AMI reperfusion patients
early intravenous beta blockers (test group) and does not use beta blockers or placebo (control group) to study the impact on prognosis. Main outcome measurements included short-term and long-term all-cause mortality and malignant arrhythmia, myocardial infarction, cardiogenic shock incidence. Using the Revman5.2 software to extract the data.Results 8 studies with 48 367 patients were enrolled. Meta-analysis showed that, compared to the control group, experimental group’s myocardial infarction malignant ventricular arrhythmia incidence decreased (OR=0.83, 95% CI 0.75-0.93,P=0.000 9); cardiogenic shock, heart failure incidence increased (OR=1.29, 95% CI 1.18-1.41,P<0.01); 2 groups’ all-cause mortality, re-myocardial infarction, ischemic adverse events rates were showed no statistically significant (OR=0.98, 95% CI 0.92-1.05,P=0.63;OR=0.95, 95% CI 0.88-1.03,P=0.21).Conclusion In early stage of AMI, intravenous beta blockers can reduce infarction related malignant ventricular arrhythmia rate, but also increase the risk of heart failure, cardiogenic shock, there is no obvious benefit in the aspects of decreasing mortality rate.
Myocardial infarction,acute;Beta blocker; Meta analysis
国家自然科学基金资助项目(No.8127024)
200003 上海,第二军医大学长征医院心内科(王丹宁、黄颖、陈侃、王磊、廖德宁); 第二军医大学临床医学 八年制博士(陈鹏飞)
廖德宁,E-mail:liao6007@163.com
10.3969 / j.issn.1671-6450.2015.05.021
2015-01-29)
