肺癌脑转移患者应用靶向治疗联合放化疗同步治疗的疗效及安全性
2015-06-09李伟张海燕宋霆婷胡芳娟
李伟,张海燕,宋霆婷,胡芳娟
论著·临床
肺癌脑转移患者应用靶向治疗联合放化疗同步治疗的疗效及安全性
李伟,张海燕,宋霆婷,胡芳娟
目的 探讨肺癌脑转移患者采用靶向药物治疗联合同步放化疗的临床效果及安全性。方法 2010年1月—2012年6月收治肺癌脑转移患者66例,采用随机数字表法分为联合组和对照组各33例,对照组采用全脑同步放疗结合同步化疗,联合组在对照组基础上采用靶向药物治疗,比较2组患者的近期疗效、远期预后及不良反应情况。结果 联合组的近期疗效显著优于对照组(Z=-2.501,P=0.012);联合组的总有效率为93.94%,高于对照组的81.82%,但差异不显著(χ2=2.276,P=0.131)。联合组的无疾病进展生存中位时间为8.0个月,显著长于对照组的5.0个月(χ2=10.742,P=0.001);联合组的2年生存率为36.36%,对照组的2年生存率为27.27%,比较差异无统计学意义(χ2=0.629,P=0.428);联合组的总生存中位时间为16.0个月,显著长于对照组的9.0个月(χ2=4.054,P=0.044);联合组和对照组各种不良反应的发生率比较差异均无统计学意义(P>0.05)。结论 肺癌脑转移患者采用靶向药物治疗联合同步放化疗治疗对延长患者的无疾病进展生存期、总生存时间及近期疗效具有积极意义。
肺癌脑转移;靶向给药;同步放化疗;临床效果;安全性
脑转移是肺癌治疗失败及肺癌患者致死的重要原因之一[1],当肺癌发生脑转移后,化疗或靶向药物无法有效通过血脑屏障在肿瘤局部达到治疗浓度,影响化疗的效果[2]。临床上对于脑转移癌的治疗多采用全脑放疗,但是受到照射剂量的限制,效果欠佳;放疗联合靶向药物可以通过放射增加血脑屏障通透性从而使靶向药物通过血脑屏障达到病灶部位发挥作用,很大程度上提高了肺癌脑转移患者的生存期限[3]。盐酸埃克替尼(凯美纳)是表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor,EGFR-TKI),通过抑制EGFR自身磷酸化而阻滞传导,能够阻断肿瘤细胞生长实现肺癌的靶向治疗[4]。本研究对肺癌脑转移患者应用凯美纳靶向治疗联合放疗进行治疗效果良好,现将结果报道如下。
1 资料与方法
1.1 临床资料 2010年1月—收2012年6月我院肿瘤内科收治肺癌脑转移患者66例。纳入标准[5]:肺癌诊断均经过CT、X线片、MR及病理组织学活检证实;肺癌脑转移均经过MR检查发现明显的脑部转移性病灶;年龄40~80岁;患者预计生存期≥3个月。排除标准:对本次研究的治疗药物严重不耐受的患者;合并严重肝肾功能障碍的患者;依从性差未能严格按照研究要求进行治疗的患者。采用随机数字表法分为联合组和对照组各33例;联合组33例,其中男18例,女15例;年龄40~78(58.9±6.8)岁;鳞癌3例,腺癌24例,腺鳞癌4例,大细胞癌2例;KPS评分67~77(73.3±3.8)分;具有肿瘤家族史4例。对照组33例,其中男21例,女12例;年龄40~80(59.7±7.6)岁;鳞癌2例,腺癌26例,腺鳞癌2例,大细胞癌3例;KPS评分65~79(72.9±3.5)分,肿瘤家族史2例。2组患者的临床资料比较差异无统计学意义(P>0.05),具有可比性。所有患者签订知情同意书,本研究通过本院医学伦理委员会批准。
1.2 治疗方法
1.2.1 放化疗同步治疗方法: 对照组患者给予全脑放疗及化疗方案,采用X 线8 mV等中心水平对穿照射,剂量为40 Gy/f,5f/周,4周,同时给予全身化疗:采用含铂为主的方案,紫杉醇135~175 mg/m2,第1天;爱宁达500 mg/m2,第l天,顺铂25 mg/m2,第1天;4周为1个周期,治疗期间均给予常规脱水及必要的对症支持治疗[6]。
1.2.2 靶向治疗方法: 联合组患者在全脑放化疗的基础上给予靶向用药,凯美纳(浙江贝达药业生产),125 mg/次,3次/d,治疗4周。
1.3 随访 治疗开始后每1个月对患者进行1次电话或登门随访,或者患者自行到医院进行随诊,对患者进行头颅MR、CT等相关检查,对治疗情况作出评估。
1.4 疗效评价及观察指标 观察并记录2组患者的随访情况,疗效评价主要为近期疗效、2年生存率及生存时间、不良反应情况。(1)近期疗效评价标准:参照RECIST实体瘤疗效评价标准[7]分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)。CR:可见病灶完全消失,维持1个月以上;PR:肿瘤最大直径及最大垂直直径的乘积缩小达到50%以上;SD:肿瘤最大直径及最大垂直直径的乘积缩小<50%,增大<25%;PD:患者出现1个或多个病灶的肿瘤最大直径及最大垂直直径的乘积>25%。总有效率=(CR+PR+SD)/总样本量×100%。(2)无疾病进展生存期(progression free survival,PFS)是指患者从首次治疗到观察到有客观证据证实的疾病进展或因任何原因死亡的时间间隔;总生存期(overall survival,OS)指患者首次治疗到由于任何原因死亡的时间。在随访截止日期仍存活的患者将以随访截止日期作为截尾数值进行分析。(3)不良反应:主要观察2组患者用药治疗期间发生的脱发、皮疹、肝功能损害、骨髓抑制、消化道反应等症状。
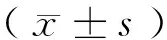
2 结 果
2.1 近期疗效比较 联合组临床疗效优于对照组(Z=-2.501,P=0.012);联合组总有效率为93.94%,高于对照组的81.82%,但差异无统计学意义(χ2=2.276,P>0.05)。见表1。

表1 2组患者近期疗效情况比较 [例(%)]
2.2 生存时间 联合组的无疾病进展生存中位时间为8.0个月,显著长于对照组的5.0个月(χ2=10.742,P=0.001),见图1;联合组的2年生存率为36.36%(12/33),高于对照组的27.27%(9/33),但差异无统计学意义(χ2=0.629,P=0.428);联合组的总生存中位时间为16.0个月,显著长于对照组的9.0个月(χ2=4.054,P=0.044),见图2。
2.3 不良反应 联合组和对照组各种不良反应的发生率比较差异均无统计学意义(P>0.05)。见表2。
3 讨 论
肺癌脑转移是指在肺癌的发展过程中肺癌细胞转移至颅内形成肿瘤,多数患者是肿瘤细胞经血流、淋巴系统侵入颅内,其发生部位与病灶处血流的动力状况及组织体积有关,皮髓交界处、功能区、脑干部位多发[8]。肺癌脑转移后患者可出现颅内压增高、偏瘫、偏身感觉障碍、共济失调等症状,目前临床对于肺癌脑转移的患者主要是采取全脑放疗、糖皮质激素、化疗等[9],均能够一定程度上提高患者的生存时间并改善患者的生活质量,肺癌脑转移患者未经治疗生存期<7周,经过激素治疗中位生存期可延长至2个月左右,经全脑放疗联合激素治疗可将中位生存期延长至3~6个月[10]。全脑放疗虽然能够起到一定的治疗效果,受到正常脑组织和重要结构照射耐受量的限制,肿瘤区局部放射剂量很难达到肿瘤致死剂量,局部控制失败率较高[11];全身化疗是治疗肿瘤的有效途径,因为在治疗原发病灶的同时也可以对脑部等多发肿瘤进行治疗,但是由于血脑屏障特殊结构的存在很多药物无法在肿瘤局部形成有效治疗浓度,疗效欠佳[12~14]。

图1 2组患者的无疾病进展生存期函数图
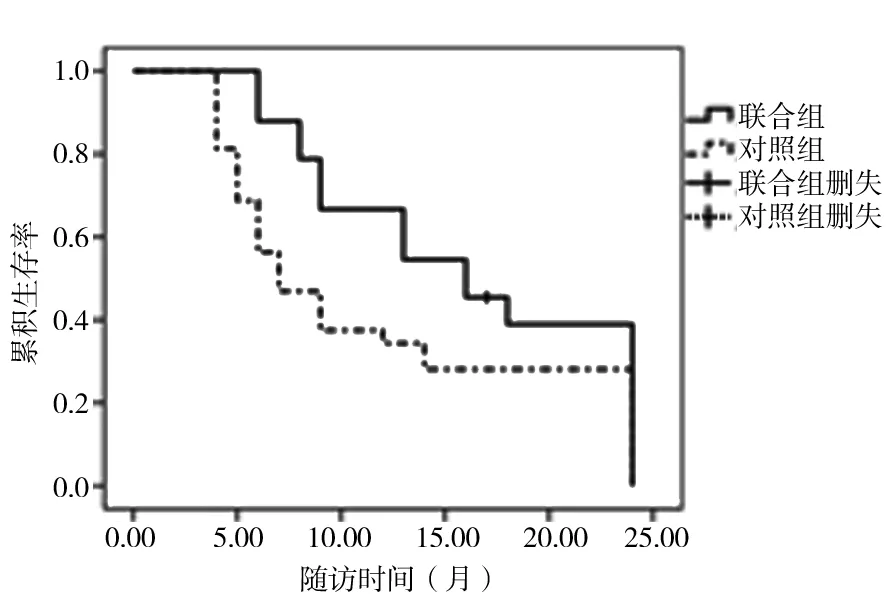
图2 2组患者总生存时间函数图
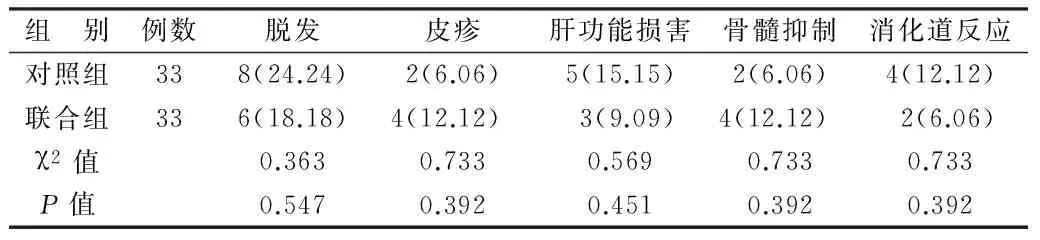
表2 2组患者的不良反应发生情况 [例(%)]
近年来越来越多的靶向药物应用于肿瘤的临床治疗,针对EGFR的靶向药物在肺癌患者中广泛应用,目前广泛应用于临床的EGFR-TKI有吉非替尼和厄洛替尼等[15],吉非替尼与厄洛替尼的分子量比较小,分别为 446.90 kDa 和429.90 kDa,在肺癌脑转移患者血脑屏障由于肿瘤细胞侵袭或血管生成而遭到破坏后可以通过血脑屏障增加脑脊液中EGFR-TKI的浓度,可使EGFR基因发生突变的肺癌患者获得较好的临床受益,有效延长了肺癌患者的生存期[16]。凯美纳是小分子酪氨酸激酶抑制剂,其分子结构式类似于吉非替尼和厄洛替尼,凯美纳与两者疗效相当,但安全性高[17]。凯美纳通过抑制EGFR自身磷酸化而阻滞传导,阻断与细胞生长、增殖有关的信号传导通路,从而抑制肿瘤细胞增殖,实现靶向治疗[18]。本研究中使用凯美纳联合全脑放化疗对肺癌脑转移的患者进行治疗,结果显示联合组的治疗有效率优于对照组,说明凯美纳在脑转移癌的治疗过程中发挥了重要作用,可能原因是分子量小,可以较多地通过血脑屏障,使得肿瘤局部的药物浓度较高,有效抑制肿瘤生长;其次凯美纳作为EGFR抑制剂,可以直接阻断调控肿瘤细胞生长增殖的信号通路,从而杀死肿瘤细胞[19]。因此联合组使用凯美纳进行靶向治疗提高肺癌脑转移患者的生存期限。
肿瘤放化疗主要不良反应是脱发、皮疹、肝功能损害、骨髓抑制、消化道反应,本研究对2组患者的不良反应发生情况进行了对比,结果没有明显差异,提示凯美纳在提高治疗效果的同时没有增加患者的不良反应,说明凯美纳作为靶向治疗药物安全性较高,在提高患者生存期限的同时可以有效改善患者的生活质量。
综上所述,应用靶向药物联合同步放化疗治疗肺癌脑转移患者疗效显著,在提高治疗有效率、延长患者生存时间的同时,并未增加不良反应的发生,明显改善患者的生活质量,值得临床推广。
1 李勇,潘绵顺,邱书珺,等.非小细胞肺癌脑转移瘤的立体定向放射治疗[J].中华神经外科杂志,2014,30(7):711-714.
2 王震,王社军,杜长生.脑转移瘤临床特点手术疗效及预后分析[J].中国实用神经疾病杂志,2015,(1):58-60.
3 刘小军,胡义德.非小细胞肺癌脑转移综合治疗进展[J/CD].中华肺部疾病杂志:电子版,2012,5(4):371-375.
4 谷田露.非小细胞肺癌脑转移者应用替莫唑胺联合全脑放疗的随机对照研究[J].现代仪器与医疗,2015,(1):36-38, 52.
5 高力英,冉俊涛,郭浩楠,等.放化综合治疗在脑转移癌治疗中的临床应用研究[J].现代肿瘤医学,2015,23(2):195-197.
6 李洁,季枚,朱丽娜,等.顺铂时辰化疗治疗晚期非小细胞肺癌的随机对照研究[J].中华肿瘤杂志,2013,35(1):43-44.
7 殷力佳.同期放疗联合表皮生长因子受体-酪氨酸激酶抑制剂治疗非小细胞肺癌脑转移的研究进展[J].肿瘤研究与临床,2014,26(5):351-353.
8 李曦,杨新杰,孙怡芬,等.盐酸埃克替尼治疗晚期非小细胞肺癌的临床观察[J].中华肿瘤杂志,2012,34(8):627-631.
9 傅华,许瑜,田仲泽,等.影响非小细胞肺癌脑转移患者放射治疗后生存的临床相关因素分析[J/CD].中华肺部疾病杂志:电子版,2014,7(3):41-44.
10 廖恺,毕卓菲,何艳,等.全脑放疗联合替莫唑胺治疗非小细胞肺癌脑转移的荟萃分析[J].中华医学杂志,2012,92(45):3199-3203.
11 Liu R,Wang X,Ma B,et a1.Concomitant or adjuvanttemozolomide with whole-brain irradiation for brain metastases:ameta-analysis[J].Anticancer Drugs,2010,21:120-128.
12 徐永峰,周启臻.肺癌脑转移16例手术治疗[J].中国煤炭工业医学杂志,2005,8(5):513-513.
13 彭玉珍.以脑转移为首发表现的肺癌15例误诊分析[J].临床误诊误治,1999,12(2):105.
14 张彦红.肺癌脑转移综合治疗35例临床分析[J].中国煤炭工业医学杂志,2009,12(11):1746-1747.
15 Kim SH,Lee JE,Yang SH,et al.Induction of cytokines and growth factors by rapamycin in the microenvironment of brain metastases of lung cancer[J].Oncol Lett,2013,5(3):953-958.
16 王孟昭,陈闽江.表皮生长因子受体-酪氨酸激酶抑制剂对非小细胞肺癌患者中枢神经系统转移的疗效[J].中华结核和呼吸杂志,2014,37(3):169-171.
17 周荻,徐欣,谢华英,等.全脑放疗联合靶向治疗与同步放、化疗治疗非小细胞肺癌脑转移疗效分析[J].上海交通大学学报:医学版,2013,33(4):480-484.
18 李曦,杨新杰,孙怡芬,等.盐酸埃克替尼治疗晚期非小细胞肺癌的临床观察[J].中华肿瘤杂志,2012,34(8):627-631.
19 傅华,张雪淋,肖瑜,等.吉非替尼联合放射治疗在非小细胞肺癌脑转移患者治疗中的作用[J].中华医学杂志,2012,92(8):524-527.
Efficacy and safety of combination of radiotherapy and chemotherapy in treatment drug therapy of patients with target of brain metastases origin from lung cancer
LIWei,ZHANGHaiyan,SONGTingting,HUFangjuan.DepartmentofInternalMedicine,QingdaoCityCenter(Tumor)Hospital,ShandongProvince,Qingdao266042,China
Objective To investigate the clinical effect and safety of target drug therapy combined with synchronous radiotherapy and chemotherapy in treatment of brain metastases from lung cancer.Methods From 2010 January to 2012 June, 66 cases of brain metastases origin from lung cancer patients were enrolled, using random number table, they were divided into combination group and control group with 33 cases in each group, the control group treated with whole brain radiotherapy, combined with synchronous chemotherapy, combination group based on the therapy of control group, also treated with target drug therapy, long term prognosis and adverse reaction were compared between the two groups of patients.Results The short term efficacy of combined group was significantly better than the control group (Z=-2.501,P=0.012); combination group's total effectiveness was 93.94%, which was higher than that of the control group(81.82%), but the difference was not significant (χ2= 2.276,P=0.131). The combination group’s median disease free survival was 8.0 months, which was longer than 5.0 months in the control group (χ2=10.742,P=0.001); the 2 year survival rate was 36.36% in combination group, control group’s 2 years survival rate was 27.27%, 2 years survival rate revealed no significant difference between the two groups of patients (χ2= 0.629,P=0.428); overall survival in the combination group showed a median of 16.0 months, which was longer than 9.0 months in the control group (χ2=4.054,P=0.044); combination group and the control group’s incidence of adverse reaction revealed no significant differences (P<0.05).Conclusion Patients with target drug therapy combined with radiotherapy and chemotherapy has positive significance to the progression of free survival, overall survival and efficacy for patients with brain metastasis from lung cancer.
Brain metastasis of lung cancer; Target drug therapy;Concurrent chemotherapy; Clinical effect;Safety
266042 青岛市中心(肿瘤)医院肿瘤内二科
10.3969 / j.issn.1671-6450.2015.05.011
2015-02-02)
