塞北紫堇化学成分的研究*
2015-06-01李怀平任松鹏
李怀平,马 斌,任松鹏,李 丽
1山东阿如拉药物研究开发有限公司,山东 济南 250101;2山东大学药学院
塞北紫堇化学成分的研究*
李怀平1,2,马 斌2,任松鹏1,李 丽1
1山东阿如拉药物研究开发有限公司,山东 济南 250101;2山东大学药学院
目的:对塞北紫堇的化学成分进行研究。方法:通过硅胶柱层析和重结晶法进行分离,根据理化性质及ID-N M R、ESI-M S等波谱方法进行结构鉴定。结果:从塞北紫堇中共分离得到5种生物碱类单体化合物,分别为:α-比枯枯灵、原阿片碱、黄紫堇明碱、β-hydrast i ne、β-比枯枯灵。结论:α-比枯枯灵、原阿片碱、β-hydrast i ne为首次从该药材分离得到。
塞北紫堇;化学成分;结构鉴定
1 材料
1.1 仪器 600 MHz核磁共振仪(BRUKER公司); API400(AB公司);UV-2450型紫外可见分光光度计(岛津);EYELA-M-1100型旋转蒸发器(上海爱郎仪器有限公司);AUW220D型电子天平(岛津);5200B型超声波清洗机(昆山市超声仪器有限公司);HH-2恒温水浴锅(常州博远试验分析仪器厂);YRT-3型熔点仪(天津市光学仪器厂)。
1.2 试药 药材来自金诃藏药股份有限公司,经青海省藏医首席专家尼玛教授鉴定为罂粟科紫堇属植物塞北紫堇药材,所用部位为除去根的地上部位。
1.3 试剂 甲醇、乙酸乙酯、二氯甲烷、三氯甲烷、正己烷(天津市富宇精细化工有限公司);氢氧化钠(天津市博迪化工股份有限公司);硅胶G板、柱层析硅胶(100-200目)(青岛海洋化工厂);所用试剂均为分析纯。
2 方法与结果
2.1 提取分离 取塞北紫堇药材粗粉10kg,碱性乙醇回流提取,减压浓缩,干燥,干燥物经酸碱处理后得碱水液,碱液经过二氯甲烷萃取,萃取液回收溶剂并干燥,得到塞北紫堇总生物碱粗提物34 g。称取塞北紫堇总生物碱25 g,以硅胶50 g拌样,加入600 g硅胶湿法装柱(100~200目,Φ75× 1 000 mm),以正己烷与乙酸乙酯为洗脱溶剂,进行梯度洗脱(98∶2,90∶10,80∶20,70∶30,60∶40,50∶50,40∶60,30∶70,20∶80,10∶90),流分以TLC法检测,合并相同的流分,共得到10个部分(Fr.1~10)。Fr.1 (98∶2)500mg,TLC见明显的斑点,二氯甲烷重结晶得到橙红色粉末Ⅲ(85 mg);Fr.2(90∶10)1 200 mg,TLC见两个明显的斑点其中一个斑点比较小,采用甲醇重结晶得到白色粉末Ⅰ(800mg)。Fr.3(80∶20) 1100mg,采用甲醇重结晶得到白色粉末Ⅱ(536mg)。Fr.4(70∶30)为黄色膏状物,采用甲醇重结晶得到淡白色粉末Ⅳ(30 mg),Fr.7(40∶60)为浅棕色物,采用三氯甲烷重结晶得到白色粉V(23 mg)。其余Fr.5(60∶40),Fr.6(50∶50)Fr.8(30∶70),Fr.9(20∶80)Fr.10(10∶90),5个部分得到的组分较少,未能得到单体物质,未做进一步研究。
2.2 结构鉴定
2.2.1 化合物Ⅰ 分子式为C20H17NO6,白色粉末,溶于苯、三氯甲烷、乙酸乙酯,微溶于乙醇和乙醚。m.p.215~218℃,ESI-MS显示分子离子峰368.3 (M+H)m/z。1H-NMR(600 MHz,DMSO-d6)δ∶4.05(1H,d,J=2.4Hz,H-1),6.63(1H,s,H-5),6.90(1H,s,H-8),5.77(1H,d,J=2.4Hz,H-11),7.23(1H,dd,J=7.8,7.8Hz,H-16,17),5.94(2H,d,J=9.6Hz,OCH2O),6.22(2H,d,J=13.8Hz,OCH2O),2.23(3H,s,N-CH3)。13C-NMR (150 MHz,DMSO-d6)δ∶64.7(s,C-1),50.3(s,C-3),26.6(s,C-4),108.2(s,C-5),145.8(s,C-6),145.6(s,C-7),107.4(s,C-8),130.1(s,C-9),126.5(s,C-10),84.6(s,C-11),167.0(s,O=CO),109.2(s,C-13),143.8(s,C-14),148.5(s,C-15),113.5(s,C-16),115.8(s,C-17),141.5(s,C-18),100.8(s,OCH2O),103.3(s,OCH2O),44.7(s,N-CH3),根据以上数据,通过与文献报道[8]235数据对照基本一致,故确定化合物Ⅰ为α-比枯枯灵(α-Bicuculline)。
2.2.2 化合物Ⅱ 分子式为C20H19NO5,为白色粉末,溶于三氯甲烷、乙醚,微溶于甲醇,几乎不溶于水。m.p.206~208℃。ESI-MS显示分子离子峰354.4(M+H)m/z。1H-NMR(600 MHZ,DMSO-d6)δ∶6.95(1H,s,H-1),6.81(1H,s,H-4),6.73(1H,d, J=7.8Hz,H-14),6.69(1H,d,J=8.4Hz,H-15),1.81 (3H,s,NCH3)。13C-NMR(150MHz,DMSO-d6)δ∶107.5 (s,C-1),145.9(s,C-2),147.4(s,C-3),110.5(s,C-4),30.6(s,C-5),57.5(s,C-6),194.8(s,C=O),132.8(s,C-9),136.1(s,C-10),50.8(s,C-11),118.4(s,C-12),129.8(s,C-13),125.1(s,C-14),106.4(s,C-15),145.3(s,C-16),145.4(s,C-17),46.1(s,C-18),101.2(s,OCH2O),100.8(s,OCH2O),41.2(s,NCH3)。根据以上数据,通过与文献报道[8]692数据对照基本一致,故确定化合物为原阿片碱(Protopine)。
2.2.3 化合物Ⅲ 分子式为C22H23NO4,橙红色粉末,溶于丙酮、乙酸乙酯、甲醇等。m.p.190~193℃,ESI-MS显示分子离子峰366.3(M+H)m/z。1H-NMR (600MHZ,DMSO-d6)δ:6.15(1H,s,H-1),6.62(1H,s,H-2),3.42(2H,d,J=19.8Hz,H-8),3.35(2H,t,J=6.6Hz,H-8),7.20(1H,d,J=8.4Hz,H-11),6.88 (1H,t,J=13.8Hz,H-12),1.99(3H,s,NCH3),3.71 (3H,d,J=7.8Hz,OCH3),3.45(3H,s,O-CH3),5.66 (2H,s,=CH2),4.72(2H,s,=CH2)。13C-NMR(150 MHz,DMSO-d6)δ:111.2(s,C-1),147.3(s,C-2),147.7(s,C-3),110.5(s,C-4),126.2(s,C-4α),29.9(s,C-5),37.1(s,C-8),123.6(s,C-8α),142.9 (s,C-9),148.1(s,C-10),108.3(s,C-11),114.0 (s,C-12),136.0(s,C-12α),155.5(s,C-13),71.5 (s,C-14),136.8(s,C-14α),38.9(s,NCH3),101.6 (s,OCH2O),55.9(s,OCH3),55.7(s,OCH3)、106.6(s,=CH2),根据以上数据,通过与文献报道[8-9]数据对照基本一致,故确定化合物Ⅲ为:黄紫堇明碱[(+) -Ochotensimine]。
2.2.4 化合物Ⅳ 分子式为C21H21NO6,淡白色粉末,溶于丙酮、乙酸乙酯等,m.p.130~133℃,ESI-MS显示分子离子峰384.3(M+H)m/z。1H-NMR(600 MHZ,DMSO-d6)δ∶4.04(1H,d,J=2.4Hz,H-1),2.27(3H,s,NCH3),2.54(2H,d,J=2.4Hz,H-3),2.95(2H,m,J=11.4Hz,H-4),2.40(2H,m,J=11.4Hz,H-4),6.85 (1H,s,H-5),6.61(1H,s,H-5),5.70(1H,d,J=2.4 Hz,H-1′),7.43(1H,d,J=8.4Hz,H-6′),7.38(1H,d,J=8.4Hz,H-7′),5.92(2H,s,OCH2O),5.89(2H,s,OCH2O),3.81(3H,d,J=4.8Hz,OCH3)。13C-NMR (150 MHz,DMSO-d6)δ∶64.7(s,C-1),44.6(s,NCH3),50.3(s,C-3),26.9(s,C-4),126.4(s,C-4α),108.2(s,C-5),145.8(s,C-6),145.5(s,C-7),107.3(s,C-8),130.0(s,C-8α),82.6(s,C-1′α),167.6(s,O=CO,119.0(s,C-3′α),146.5(s,C-4′),152.0(s,C-5′),119.3(s,C-6′),118.4(s,C-7′),141.4(s,C-7′α),100.7(s,OCH2O),61.6(s,OCH3),56.6(s,-OCH3)。根据以上数据,通过与文献报道[10]数据对照基本一致,故确定化合物Ⅳ为:β-hydrastine。
2.2.5 化合物Ⅴ 分子式为C20H17NO6,白色粉末,溶于三氯甲烷、丙酮、乙酸乙酯等,m.p.194~196℃,ESI-MS显示分子离子峰368.3(M+H)m/z。1H-NMR(600MHZ,DMSO-d6)δ:4.09(1H,s,H-1),6.71(1H,d,J=14.4Hz,H-5),6.73(1H,d,J=14.4Hz,H-8),5.77(1H,d,J=4.2Hz,H-11),6.10(1H,d,J=4.2Hz,H-16),7.14(1H,d,J=7.8Hz,H-17), 5.97(2H,d,J=7.8Hz,OCH2O),6.10(2H,d,J=4.2Hz,OCH2O),2.44(3H,s,NCH3)。13C-NMR(150MHz,DMSO-d6)δ∶64.8(s,C-1),48.8(s,C-3),26.3(s,C-4),108.3(s,C-5),146.3(s,C-6),145.5(s,C-7),107.9(s,C-8),130.4(s,C-9),125.0(s,C-10),84.2(s,C-11),166.7(s,O=CO),109.5(s,C-13),144.0(s,C-14),148.7(s,C-15),113.5(s,C-16),115.5(s,C-17),140.4(s,C-18),100.9(s,OCH2O),103.4(s,OCH2O),44.9(s,NCH3),根据以上数据,通过与文献报道[8]347,693数据对照基本一致,故确定化合物Ⅴ为β-比枯枯灵(β-Bicuculline)。
以上5种生物碱化合物的结构见图1。
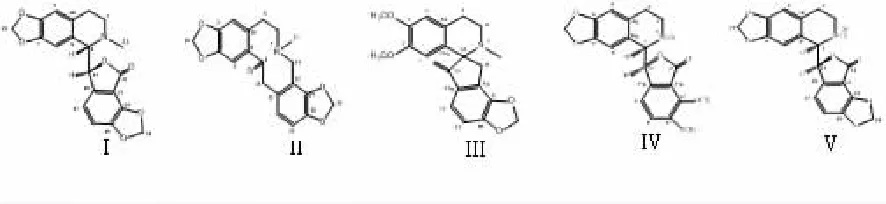
图1 5种生物碱的化学结构
3 讨论
本文采用酸碱法制备总生物碱粗提物,并通过常规的硅胶柱色谱法对其塞北紫堇总生物碱进行了系统研究,以TLC法检测不同流份,合并相同流份,再经过进一步重结晶,分离得到5个化合物,鉴定其结构,均为生物碱类化合物,其中原阿片碱、α-比枯枯灵、β-hydrastine为从本药材中首次分离得到。
[1] 国家中医药管理局.中华本草·藏药卷[M].上海:上海科学技术出版社,2002:325.
[2] 李海丽,吴彤,潘国庆.赛北紫堇总生物碱LD〈sub〉50〈/sub〉的测定[J].湖北农业科学,2013,(10):2371-2372.
[3] 宋晓楠,吴训文,王伟,等.赛北紫堇总生物碱抗炎作用研究[J].湖北农业科学,2013(6):1381-1382.
[4] 李吉昌,林跃华,龙清平,等.紫外分光光度法测定赛北紫堇中总生物碱含量[J].云南化工,2012,39(4):19-21.
[5] 李海丽,潘国庆,酉志亮,等.藏药赛北紫堇总生物碱镇痛药效学研究[J].天然产物研究与开发,2013,25(4):544-546.
[6] 李吉昌,董秀华,邓杰文.赛北紫堇的生物碱成分研究[J].中药材,2010,(2):210-213.
[7] 唐艳丽,杨爱梅,张樱山,等.灰绿黄堇生物碱化学成分的研究[J].中国中药杂志,2005,30(3):195-197.
[8] 于德泉,杨峻山.分析化学手册:第七分册[M].2版.化学工业出版社,2005:235.
[9] D onal d W,H ughrs,Bal a C,et al.13C nucl ear m angnet i c resonance spect ra oft he spri obenzyl i soqui nol i ne al kal oi ds and rel at e m odel com pounds[J].Can J Chem,1977,55(3):3304-3311.
[10]D onal d W,H ughes,H erbrt t L,et al.13C m angnet i c resonance spect ra of som e i soqui nol i ne al kal oi ds and rel at ed m odelcom pounds[J].Can J Chem,1976,54(7):2252-2260.
Research on Chemical Constituents of SaiBei ZiJin
LI Huaiping1,2,MA Bin2,REN Songpeng1,LI Li1
1 Shandong Arura Drug Research and Development Company,Ltd,Jinan 250101,China;
2 Pharmacy College of Shandong University
Objective:To study chemical constituents of SaiBei ZiJin[Corydalis impatiens(pall.)Fisch.]. Methods:SaiBei ZiJin was abstracted by silica column chromatography method and recrystalization method,structure identification were performed according to physicochemical property,ID-NMR,ESI-MS and other spectral methods.Results:Five alkaloid monomer compounds were extracted from SaiBei ZiJin,they were:α-bicuculline, protopine,ochotensimine,β-hydrastine and β-bicuculline.Conclusion:α-bicuculline,protopine and β-hydrastine are isolated from medicinal materials for the first time.
SaiBei ZiJin;chemical constituents;structure identification塞北紫堇为罂粟科紫堇属植物塞北紫堇Corydalis impatiens(Pall.)Fisch.的干燥全草。收载于《中华本草》藏药卷,藏语名称为“帕下嘎”(或译为“帕夏嘎”或“巴夏嘎”),具有除热消肿、活血散瘀功效,用于热性诸症[1-5]。塞北紫堇分布在青海、西藏、甘肃、四川等地,为藏成药中常用药材,应用非常广泛,数据统计显示有25%的藏成药中含有该药材。现代研究中,对塞北黄堇化学成分的报道甚少,因紫堇属植物中含多种生物碱,具有多方面的药理作用[6-7],故笔者提取制备了塞北紫堇总生物碱,并进行了分离,得到5个生物碱类成分,分别为原阿片碱、α-比枯枯灵、黄紫堇明碱、β-hydrastine、β-比枯枯灵。
R284.1
A
1004-6852(2015)10-0043-03
2014-09-27
藏医药产业技术创新服务平台(编号2060503)。
李怀平(1980—),男,硕士学位,工程师。研究方向:民族药质量标准制定及藏药新药研究开发。
