两种方案治疗晚期非霍奇金淋巴瘤临床对照观察
2015-05-24杨军礼赵晶磊
王 捷 杨军礼 赵晶磊 赵 霖
两种方案治疗晚期非霍奇金淋巴瘤临床对照观察
王 捷 杨军礼 赵晶磊 赵 霖
晚期非霍奇金淋巴瘤;CTOP-P;CTOP
非霍奇金淋巴瘤(non-hodgkin’s lymphoma,NHL)是一类原发于淋巴结和其他器官淋巴组织的高度异质性恶性肿瘤,临床表现多样,可发生于任何年龄、任何淋巴组织,但以颈部淋巴结最多见[1]。具有多形性、免疫表型和生物学特征,早期主要以淋巴结肿大以及结外淋巴组织增生为主要表现。NHL诊断主要靠活组织检查,治疗多以放射治疗与化学治疗联合,其中NHL对化疗治疗较敏感,标准的有效化疗方案是COP,但缓解率低,相关的并发症多也较多[2]。晚期NHL患者可发生骨髓浸润,预后差,肿瘤往往累及范围较大,治疗难度大,且身体各个器官功能下降,体能状况差,对化疗的耐受能力降低,影响化疗进程,进而影响治疗的有效性和患者生活质量[3]。笔者应用CTOP-P方案和CHOP方案治疗晚期非霍奇金淋巴瘤,为晚期非霍奇金淋巴瘤患者选用一种临床疗效确切,毒性反应小,化疗后生活质量较高的临床化疗方案。
1 临床资料
1.1 一般资料 选取我院2009年—2013年期间晚期非霍奇金淋巴瘤患者72例,按照随机数字表分为观察组37例,男21例,女16例,平均年龄(46.5± 4.6)岁;Ann Arbor病理分期,Ⅲ期17例,Ⅳ期20例,其中B细胞性26例,T细胞性11例;侵袭性24例,惰性13例;平均KPS评分(68.2±7.5)分。对照组35例,男21例,女14例,平均年龄(48.4±5.1)岁;Ann Arbor病理分期:Ⅲ期15例,Ⅳ期20例,其中B细胞性22例,T细胞性13例;侵袭性23例,惰性占12例;平均KPS评分(69.3±7.2)分。两组治疗前一般资料对比,差异无统计学意义(P<0.05),具可比性。两组患者均签署知情同意书。
1.2 纳入标准 ①组织病理切片确诊NHL者;②除外心、肝、肾功能衰竭,脑血管疾病等重大疾病影响观察疗效者;③预计生存期3个月以上,能配合完成观察者;④年龄18~75岁。
1.3 排除标准 ①早期NHL患者;②有精神障碍患者,或长期服用精神控制类药品者;③治疗配合度差患者;④年龄<18岁或>75岁。
1.4 剔除标准 ①治疗期间病情突然加重或出现心、肝、肾功能衰竭等严重疾病者;②患者中途放弃治疗者;③未能严格按照治疗计划执行者。
2 方法
2.1 化疗方案 观察组37例患者采用CTOP-P方案,环磷酰胺750mg/m2,静脉滴注,1天1次;吡柔比星60mg,静脉滴注,第1天;醋酸泼尼松片,60mg/d,第1~7天,口服;长春新碱1.5mg/m2,静脉滴注,第1、8天;平阳霉素8~16mg,静脉滴注,第1天。对照组采用CHOP方案,环磷酰胺750mg/m2,静脉滴注,1天1次;吡柔比星60mg,静脉滴注,第1天;醋酸泼尼松片60mg,1天1次,口服,第1~7天,阿霉素40mg,静脉滴注,第1天。根据患者个体情况,化疗周期为3~4周期,中位疗程数为3个疗程。
2.2 观察指标 治疗前后两组均进行客观指标的检查,包括血常规,肝肾功能,骨髓检查,心电图,腹部彩超及颈、喉、腹部和盆腔部CT检查。毒性反应根据WHO毒性反应评价标准进行评价,包含血液学、胃肠道、肾、膀胱、肺、发热、过敏、皮肤、脱发、过敏等12项内容,根据药物毒性作用的程度分为0~Ⅳ度。根据本研究药物常见的的毒性反应,选取血液毒性中白细胞、血红蛋白及血小板,非血液毒性中胃肠道反应、发热、脱发、心肌损害、肝肾功能异常、外周神经毒性和骨髓抑制作为观察指标,出现毒性反应后即纳入观察例数。运用EORTC QLQ-C30生活质量评分表,评价两组患者的生活质量状况,共30个条目,15个领域,包含躯体、角色、认知、情绪和社会功能5个功能项目和疲劳、疼痛、恶心呕吐等症状项目,在本研究中选取与本研究相关的功能项目和症状项目评价患者的整体生活质量情况。
2.3 统计学方法 应用SPSS13.0统计软件,计量资料符合正态分布采用t检验,不符合正态用非参数检验,计数资料用χ2检验,P<0.05表示差异有统计学意义。
3 治疗结果
3.1 疗效标准 根据RECIST疗效评价标准进行评价[4],复查CT观察肿瘤的瘤体变化情况。完全缓解(CR):全部肿瘤病灶消失,并维持4周;部分缓解(PR):肿瘤病灶体积减小30%或以上,并维持4周;稳定(SD):疗效介于PR和PD之间,进展(PD):肿瘤病灶增加20%,肿瘤病灶增加前非CR/PR/SD;有效率为(CR+PR+SD)/总数×100%。
3.2 两组疗效比较 观察组有效率64.9%,对照组有效率40.0%,差异有统计学意义(P<0.05),观察组疗效优于对照组。见表1。
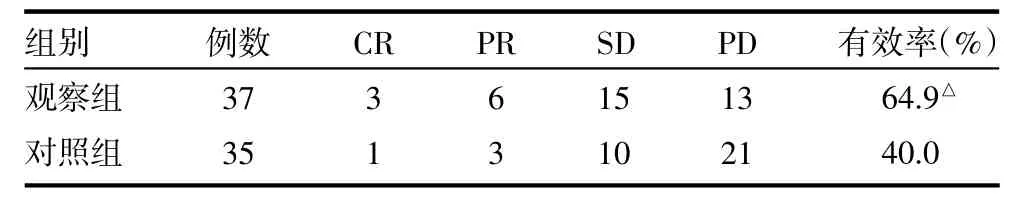
表1 两组疗效比较(例)
3.3 两组毒性反应发生比较 在白细胞毒性、血红蛋白毒性、胃肠道反应、脱发、心脏毒性和骨髓抑制方面,观察组毒性反应明显低于对照组(P均<0.05);两组血小板毒性、发热、脱发、肝肾功能异常和外周神经毒性反应发生率差异无统计学意义(P>0.05)。见表2。
3.4 两组EORTC QLQ-C30生活质量评分比较 在功能项目上,观察组躯体功能、情绪功能、社会功能及认知功能评分低于对照组(P均<0.05),见表3;在症状项目上,观察组食欲减退、恶心呕吐、疼痛、呼吸困难、睡眠不佳及其他不适症状评分低于对照组(P均<0.05),见表4。
4 讨 论
NHL是一种原发于淋巴组织的常见恶性肿瘤。CHOP化疗方案是公认治疗NHL患者的标准方案[5]。但临床观察发现,CHOP方案仍存在缺陷。本研究对照组患者采用CHOP方案,其有效率仅为40%,而其血细胞毒性、胃肠道反应、骨髓抑制、心脏毒性和脱发等毒性反应较常见。晚期NHL患者,各脏器功能差,用药耐受性差,在有效保证疗效的情况下,用普通强度化疗方案对患者的化疗持续性和化疗后的生活质量均有较大的影响[6]。本研究观察组选用CTOPP方案在保证疗效的前提下克服经典CHOP方案的毒性反应,。首先将CHOP方案中的阿霉素(ADM)换用吡柔比星(THP),THP也为蒽环类药物,是阿霉素的一个四氢吡喃衍生物,其化学结构为在阿霉素的4~0位上接上四氢吡喃基,通过抑制肿瘤细胞DNA的复制和转录达到抗肿瘤的效果[7],疗效与ADM相当。但由于THP可以迅速进入肿瘤细胞内,且排泄较慢,使其保持较高的浓度和较长的药效时间,可以充分有效抑制核酸合成,使肿瘤细胞由G2期中止增殖,因此其治疗NHL的临床有效性明显优于传统的ADM[8-9]。另外在CTOP治疗基础上,加用平阳霉素(PYM),可加强抗肿瘤效果,其主要抗肿瘤机制是抑制并切断肿瘤细胞的DNA链,杀死G2期和M期的肿瘤细胞,并且对肿瘤内血管的内皮细胞起到萎缩、退化、减小的作用,对于晚期实体瘤具有缩小肿瘤瘤体的作用[10]。本研究观察组有效率为64.9%,高于对照组的40.0%(P<0.05),说明CTOP-P方案在有效率上明显优于CHOP方案。且CTOP-P治疗的观察组白细胞和血红蛋白毒性、胃肠道反应、心脏毒性、脱发和骨髓抑制的发生例数明显低于对照组(P<0.05),而两组血液毒性中的血小板毒性、发热、肝肾功能异常及外周神经毒性差异无统计学意义(P>0.05)。
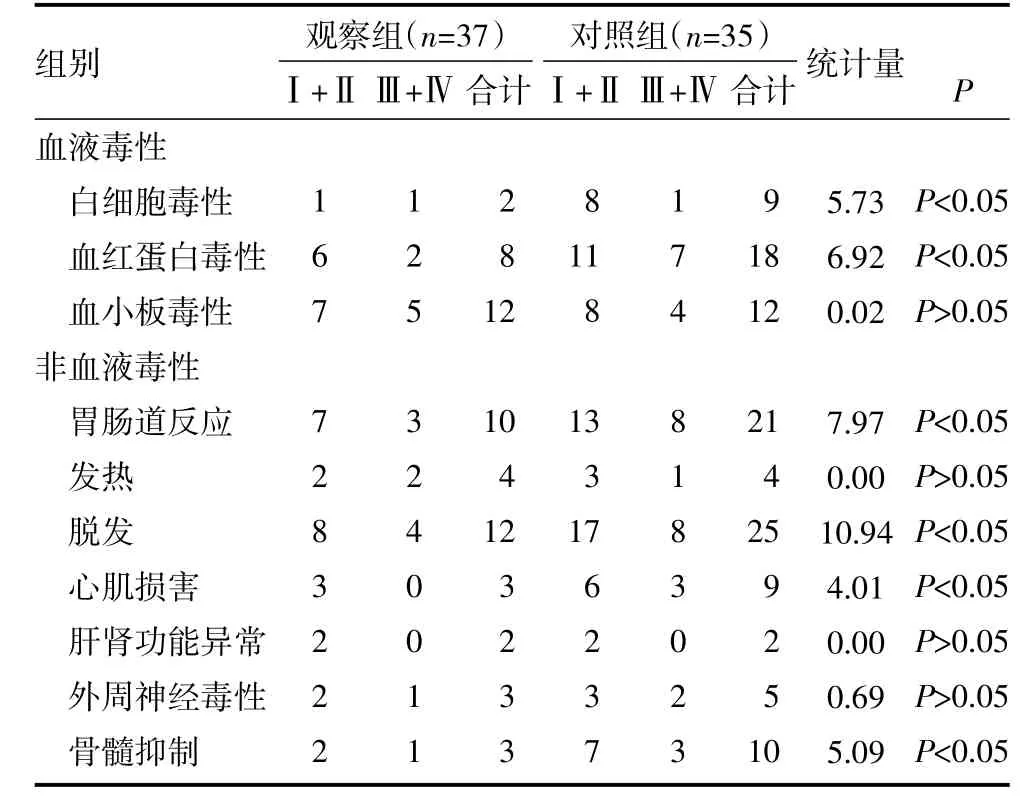
表2 两组毒性反应比较(例)
表3 两组EORTC QLQ-C30生活质量功能项目评分比较(分±s)
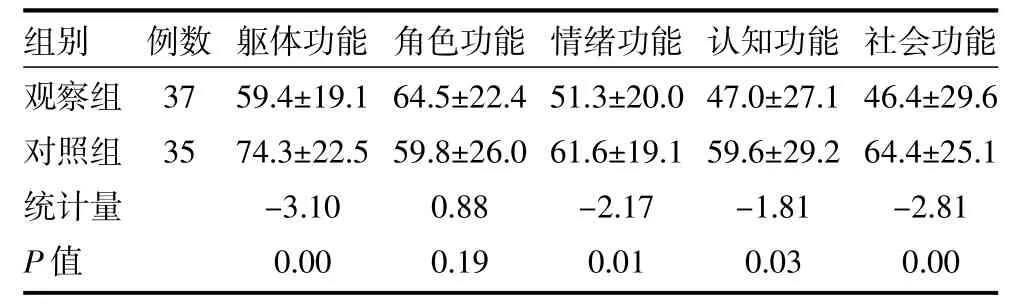
表3 两组EORTC QLQ-C30生活质量功能项目评分比较(分±s)
组别观察组对照组统计量P值例数37 35躯体功能59.4±19.1 74.3±22.5 -3.10 0.00角色功能64.5±22.4 59.8±26.0 0.88 0.19情绪功能51.3±20.0 61.6±19.1 -2.17 0.01认知功能47.0±27.1 59.6±29.2 -1.81 0.03社会功能46.4±29.6 64.4±25.1 -2.81 0.00
表4 两组EORTC QLQ-C30生活质量症状项目评分比较(分±s)
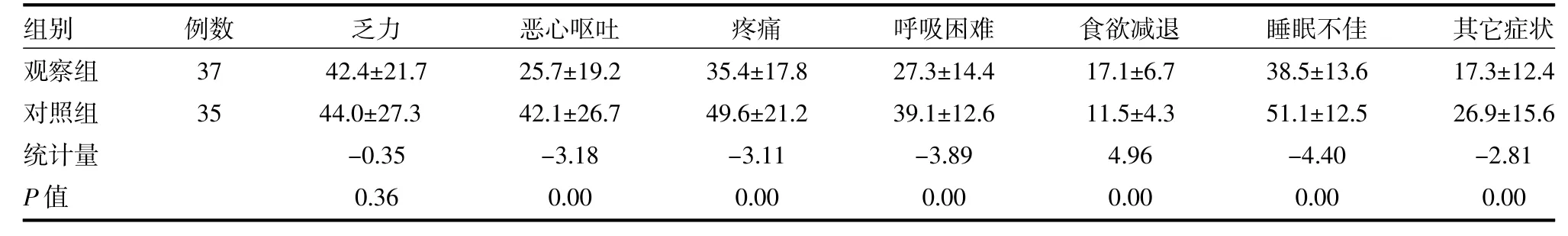
表4 两组EORTC QLQ-C30生活质量症状项目评分比较(分±s)
组别观察组对照组统计量P值例数37 35乏力42.4±21.7 44.0±27.3 -0.35 0.36恶心呕吐25.7±19.2 42.1±26.7 -3.18 0.00疼痛35.4±17.8 49.6±21.2 -3.11 0.00呼吸困难27.3±14.4 39.1±12.6 -3.89 0.00食欲减退17.1±6.7 11.5±4.3 4.96 0.00睡眠不佳38.5±13.6 51.1±12.5 -4.40 0.00其它症状17.3±12.4 26.9±15.6 -2.81 0.00
EORTC QLQ-C30评分表是针对肿瘤患者的核心量表,主要分为功能项目和症状项目,评分越高,说明在这方面的生活质量越低[11]。本研究观察组在躯体功能、角色功能、社会功能及认知功能评分及食欲减退、恶心呕吐、疼痛、呼吸困难、睡眠不佳、其他不适症状评分均低于对照组(P<0.05)。结果显示,CTOP-P化疗方案临床疗效确切,副作用较少,化疗后生活质量评分较高,可作为晚期非霍奇金淋巴瘤的化疗方案应用。
[1]李慧,王晓冬,王春森.国内吡柔比星与阿霉素为主的化疗方案治疗非霍奇金淋巴瘤疗效与安全性的Meta分析[允].中国循证医学杂志,2013,13(2):176-181.
[2]王羽.CTOP与CHOP方案治疗老年非霍奇金淋巴瘤的对比分析[J].中国实用医药,2013,8(15):76-77.
[3]许惠丽.THP为主联合化疗方案治疗老年非霍奇金淋巴瘤[J].中国实用医药,2010,5(21):125-126.
[4]杨学宁,吴一龙.实体瘤治疗疗效评价标准-RECIST[J].循证医学,2004,4(2):85-90.
[5]侯芸,王华庆,付凯,等.CTVP与CTOP方案治疗280例非霍奇金淋巴瘤临床疗效分析[J].中国肿瘤临床,2010,37(18):1065-1068.
[6]韩霞,王华庆,刘贤明,等.美罗华联合CTOP方案治疗B细胞非霍奇金淋巴瘤35例临床分析[J].中国肿瘤临床,2010,37(6):338-341.
[7]Zhai LZ,Guo CC,Cao YB,et al.Long-term results of pi-rarubicin versus doxorubicin in combination chemotherapy for aggressive non-Hodgkin’s lymphoma∶single center,15-year experience[J].Int允Hematol,2010,91(1):78-86.
[8]Tsurumi H,Yamada T,Sawada M,et al.Biweekly CHOP or THP-COP regimens in the treatment of newly diagnosed aggressive non-Hodgkin’s lymphoma.A comparison of doxorubicin and piraru-bicin:a randomized phase II study[J].允Cancer ResClin Oncol,2004,130(2):107-113.
[9]刘伟红,李琳洁,许能文,等.化疗辅助吡柔比星治疗老年恶性淋巴瘤患者50例效果分析[J].中国生化药物杂志,2014,34(2):105-106.
[10]郑冬丽.吡柔比星为主联合化疗治疗老年非霍奇金淋巴瘤临床探讨[J].中国伤残医学,2014,22(3):149-150.
[11]何茜,张川莉,吕春蓉.恶性淋巴瘤患者生活质量调查分析[J].华西医学,2009,24(3):766-768.
(收稿:2015-01-10 修回:2015-03-10)
浙江省金华广福医院肿瘤内科(金华 321000)
王捷,Tel:13819983227;E-mail:wangjie1886@126.com
