三聚氰胺-d 6的合成及氘标记化合物作为检测内标的可行性探讨
2015-05-16郭扬振任敬霞梅向东折冬梅
郭扬振,任敬霞,宁 君,梅向东,折冬梅
(中国农业科学院 植 物保护研究所,北京 100193)
随着质谱检测技术的发展,同位素稀释质谱法(IDMS)越来越多的应用于样品检测[1]。稳定同位素标记的化合物作为示踪剂进行检测可避免由于食品复杂的基质效应、前处理和质谱检测器等因素对分析方法及测定结果的影响,有效校正方法中出现的误差,显著提高方法稳定性与准确性,因此被国际物质量咨询委员会(CCQM)规定为微量、痕量和超痕量元素唯一权威测量方法[2]。
三聚氰胺(melamine)又称氰尿酰胺,其含氮量高达66.7%。在乳制品中添加三聚氰胺,可提高含氮量,冒充成高蛋白食品,从而降低成本。近年来,已有多篇文献报道采用碳-13[3]与氮-15[4]标记三聚氰胺作为内标化合物结合液相色谱质谱联用仪对样品中三聚氰胺进行检测,都取得了良好的检测效果。与其他核素标记化合物相比,氘标记化合物具有合成步骤少、价格便宜等优点,进而间接降低检测成本。然而,在合成三聚氰胺-d6的过程中发现,三聚氰胺-d6在溶液中极易发生氢同位素交换,进而影响检测结果。同时许多文献也报道氘标记化合物不适用于某些基质检测[5-7]。本文将通过化学理论层面,阐述该现象发生的原因并探讨氘标记化合物作为检测内标化合物的必要条件。
1 实验部分
1.1 主要仪器与装置
Ther mo Nicolet 6700 FT-IR型红外测定仪:美国赛默飞世尔科技公司,溴化钾压片;Br uker DPX 300 MHz型核磁共振仪:美国Bruker公 司,氘 代 DMSO 为 溶 剂;Br uker ApexⅣFT MS质谱仪:美国Br uker公司;6890/5973GC-MS气相色谱质谱仪:美国 Agilent公司。
1.2 主要材料与试剂
ND4OD:美国 Sig ma-Aldrich公司(99 ato m%D),三聚氯氰:北京百灵威科技有限公司(纯度>99%);1,4-二氧六环:上海国药集团化学试剂有限公司(纯度>99.5%);重水:北京华威锐科化工有限公司(98 ato m%D)。
1.3 实验条件
三聚氰胺-d6的合成路线示于图1。将3.12 mL氘代氨水(0.02 mol)于10 ℃左右加入0.61 g三聚氯氰(0.003 3 mol)与10 mL 1,4-二氧六环溶液中,密封反应装置,加热至140℃,反应4 h。待反应液冷却至室温后有淡黄色沉淀物生成,过滤并用重水重结晶后烘干,计算产率(以ND4OD记)。
2 结果与讨论
2.1 三聚氰胺-d 6 的合成
2.1.1 反应原料对三聚氰胺收率的影响
先后使用氨气与氨水对三聚氯氰进行取代,因氨气通入量不易控制,且产率偏低,故选择使用氨水进行反应。

图1 三聚氰胺-d 6的合成Fig.1 Synthesis of melamine-d 6
2.1.2 反应介质对三聚氰胺收率的影响
根据文献[8]报道,使用氨气对三聚氯氰中的三个氯完全取代反应温度需高于80℃。根据已有合成方法[3,8],分别选用乙腈、水、二氧六环作为反应介质,反应按1.3节进行,结果表明,只有当反应介质为二氧六环时,产物为三聚氰胺,另外两种介质主要产物都是6-氯-2,4-二氨基-1,3,5-三嗪。
2.1.3 三聚氰胺-d6的合成与表征
在上述合成工艺优化的基础上,同时结合相关研究[3,8],以氘代氨水为标记前体,二氧六环为反应溶剂,反应温度为140℃,反应时间4 h,得到三聚氰胺-d6,产品收率为30%(以ND4OD记)
产物表征:13C NMR(DMSO-D6):δ167.415(s,3C);FT-IR (KBr)c m-1:2 589.86,2 550.43,2 507.91,2 336.71(υN—D),1 533.41,1 483.47(υC—N),1 449.63(υCN,三嗪环中碳氮双键伸缩振动),842.03,811.75,575.93,449.72。图2和图3是以氘代甲醇及甲醇分别作溶剂,气相色谱质谱联用仪对三聚氰胺-d6样品进行检测得到的质谱图。可以看出,在检测过程中,三聚氰胺-d6会快速与溶剂及色谱柱中的活泼氢发生氢同位素交换。
2.2 同位素稀释质谱法(IDMS)中的应用
使用气相色谱质谱联用仪对三聚氰胺-d6相对分子质量进行测定时,发现因为发生氢同位素交换致使相对分子质量难以测量,同时也导致其无法应用于同位素稀释质谱法对样品进行检测。同位素交换是具有不同质量数的同一元素不同原子间的交换,包括不同分子间的同一元素的同位素交换和复杂分子内不同基团间同一元素的同位素交换,属于交换反应中的一种特殊形式[8]。其中,氢同位素交换速率的快慢受到化合物与基质两方面影响。

图2 三聚氰胺-d 6的质谱图(甲醇-d 4作溶剂)Fig.2 Mass spectr u m of melamine-d 6(methanol-d 4 as solvent)
交换速率与交换分子的电子壳层结构有关。含有孤对电子元素的化合物易于进行氢同位素交换;相反,对不含孤对电子元素(如C)的化合物则难以发生氢同位素间的交换[9]。
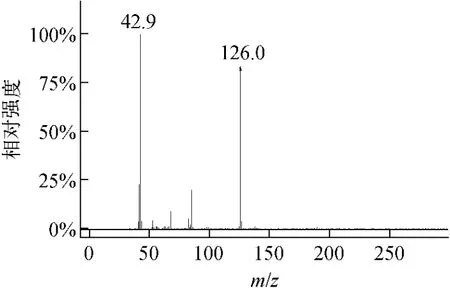
图3 三聚氰胺-d 6的质谱图(甲醇作溶剂)Fig.3 Mass spectr um of melamine-d 6(methanol as solvent)
以三聚氰胺-d6和苯-d6为例,三聚氰胺中氮元素具有孤对电子,与氢离子发生Lewis酸碱中和反应,显然这种交换不需要克服很大的势垒(见图4)。而苯中的碳原子没有孤对电子,交换的氘必须先从一个键上把氢分出来产生自由电子对,然后才能使交换完成。这必须要使C—D键断裂,故需要克服很大的势垒(见图5)。因此,倘若有合适的催化剂或有使C—D键的键能减弱的取代基存在,都能使交换反应活化能降低,从而使交换速度加快。因此,氘标记化合物中,凡是存在N—D、O—D及S—D键的化合物,都不适用于作为内标化合物。

图4 三聚氰胺-d 6的氢同位素交换机理Fig.4 Hydrogen isotope exchange mechanism of melamine-d 6
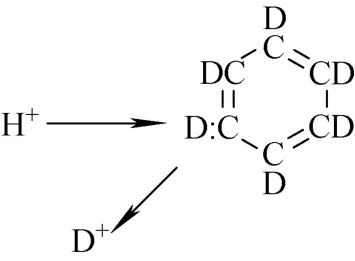
图5 苯-d 6的氢同位素交换机理Fig.5 Hydrogen isotope exchange mechanism of benzene-d 6

图6 解离机理Fig.6 Dissociation mechanism
C—H键中的氢同位素交换属于慢交换。该类交换反应的反应机理可分为解离机理和缔合机理。图6简单演示了解离机理,其中RH表示有机化合物,DA表示其他含氘化合物,交换按a或b式进行,如果RH比DA的酸性弱,交换按a式进行;反之按b式进行。在化合物中引入吸电子基团以及采用碱性介质可以显著加快这一类型交换反应的速度。有研究发现,中性溶液中甲苯与重水长时间煮沸,不发生交换,有碱存在时,特别是在酒精溶液中,交换便显著进行,因为C2H5O—比OH—为更强的碱。因此,若采用甲醇等碱性强的介质作为提取溶剂,会加快氘标记内标化合物的氢同位素交换。以苯与氘代浓硫酸交换为例形象解释了缔合机理(图7),和解离机理相反,环中存在能增高C—H键附近电子云密度的取代基以及增加氘给予体酸度有利于配合物生成从而促进交换[10]。

图7 缔合机理Fig.7 Associative mechanism
Chavez-Eng 等[5]用 GC-MS 和 HPLCMS-MS测定了[13CD3]Rof ecoxib在环己烷、乙腈和乙腈-水(50∶50)三种溶剂中[13CH3]Rofecoxib、[13CH2D]Rof ecoxib、[13CHD2]Rofecoxib及[13CD3]Rofecoxib的含量,结果表明Rofecoxib在这三种溶剂中的氢同位素交换速率由高到低依次为乙腈-水(50∶50)、乙腈、环己烷。而 Verplaetse[11]等对fentanyl-d5进行了同样的实验却并没有发现同位素交换现象。原因可能是Rofecoxib在这三种溶剂中按照解离机理发生氢同位素交换,—CN为吸电子基团,降低邻碳的电子云密度,使得C—H键能降低,易于断裂。而氧具有孤对电子,进行氢同位素交换不需要克服很大势垒,容易发生交换。因此Rofecoxib在乙腈-水(50∶50)及乙腈中较易发生同位素交换。而—SO2—与—CO—基团相比具有更强的吸电子能力,因此[13CD3]Rofecoxib中C—D键键能较低,易发生氢同位素交换(电子转移见图8,其中箭头表示转移方向)。

图8 [13 CD3]Rofecoxib、fentanyl-d 5 及acetonitrile的电子转移Fig.8 Electron transfer in[13 CD3]Rofecoxib,fentanyl-d 5 and acetonitrile
3 结论
由上可知,三聚氰胺-d6中氮原子含有孤对电子,在溶剂中易发生氢同位素交换,因此通过质谱检测难以准确测得相对分子质量,同时也导致其难以应用于同位素稀释质谱法对样品进行检测。
本研究以氘代氨水与三聚氯氰取代合成三聚氰胺-d6,合成方法简单且环保,可以考虑在日常化工合成中采用该合成方法;同时也从理论上阐述将氘标记化合物应用于稳定同位素稀释质谱法时,需要首先对其同位素稳定性进行评估。因为C—D键中的氢同位素交换属于慢交换,所以氘标记化合物不适合长期保存。同时,合成氘标记化合物需要慎重选择在化合物中引入氘的位置,尽可能远离吸电子基团,运用计算化学的手段对引入位置的C—H键的牢固程度进行评估是一个可行的办法。
[1] 稳定同位素标记有机合成法[M].北京:化学工业出版社,1986.
[2] 赵墨田.同位素稀释质谱法特点[J].质谱学报,2004,25(10):167-168.Motian Z.The characteristics of isotope dilution mass spectro metry[J].Jour nal of Chinese Mass Spectrometry Society,2004,25(10):167-168(in Chinese).
[3] Varelis P,Jeskelis R.Preparation of[13C3]-melamine and[13C3]-cyanuric acid and their application to the analysis of melamine and cyanuric acid in meat and pet food using liquid chromatogra-phy-tandem mass spectro metry[J].Food Additives and Contaminants,2008,25(10):1 208-1 215.
[4] Filigenzi M S,Puschner B,Aston L S,et al.Diagnostic deter mination of melamine and related co mpounds in kidney tissue by liquid chr omatography/tandem mass spectrometry[J].Journal of Agricultural and Food Chemistr y,2008,56(17):7 593-7 599.
[5] Chavez-Eng C M,Constanzer M L,Matuszewski B K.High-perf or mance liquid chro matographictandem mass spectrometric evaluation and determination of stable isotope labeled analogs of r ofecoxib in human plas ma samples from oral bioavailability studies[J].Jour nal of Chro matography B,2002,767(1):117-129.
[6] Mutlib A E.Application of stable isotope-labeled co mpounds in metabolis m and in metabolis m-mediated toxicity studies[J].Chemical Research in Toxicology,2008,21(9):1 672-1 689.
[7] Briscoe C J,Hage D S.Factors affecting the sta-bility of dr ugs and dr ug metabolites in biological matrices[J].Bioanalysis,2009,1(1):205-220.
[8] 张丽雅,杨维成,罗勇.13C3-三聚氰酸、15N3-三聚氰胺的合成工艺研究[J].同位素,2010,23(3):139-143.Liya Z,Weicheng Y,Yong L.Synthetic Technology of 13 C 3-cyanuric Acid and 15 N 3-melamine[J].Jour nal of Isotopes,2010,23(3):139-143(in Chinese).
[9] 张永洪.动态核磁共振研究化学交换相关的动力学性质[D].武汉:中国科学院研究生院(武汉物理与数学研究所),2002.
[10]郭正谊.稳定同位素化学[M].北京:科学出版社,1984.
[11]Ver plaetse R,Tytgat J.Develop ment and validation of a sensitive ultra perf or mance liquid chromatography tandem mass spectrometry method f or the analysis of fentanyl and its major metabolite norfentanyl in urine and whole blood in forensic context[J].Jour nal of Chr omatography B,2010,878(22):1 987-1 996.
