离子色谱法测定厄贝沙坦胶囊中叠氮化物的残留量
2015-05-03林伟豪吴婵娟
林伟豪 ,李 东 ,吴婵娟
(1.广东省深圳市坪山新区人民医院药剂科,广东 深圳 518118; 2.暨南大学第二临床医学院·深圳市人民医院临床药学研究室,广东 深圳 518020)
叠氮化钠又称叠氮钠,可经呼吸道消化道和皮肤迅速吸收,属于剧毒物质,与氰化物类似。体外研究表明,其主要抑制细胞色素氧化酶和其他酶,并能使体内氧合血红蛋白形成受阻,具有黏膜刺激、降压、中枢神经损害及强致突变作用。叠氮化钠是厄贝沙坦合成工艺最后一步中使用的物料[1],使用量比较大,在精制过程中可能无法完全除去而残留。因叠氮化物毒性较大,美国药典(USP35-NF30)、欧洲药典(EP8.0)均对厄贝沙坦中叠氮化物的限度作了严格的规定,规定不得超过10 ppm。厄贝沙坦用于高血压的治疗,在医院应用量大[2]。笔者采用离子色谱法对厄贝沙坦中叠氮化物的残留量进行测定,以达到控制厄贝沙坦胶囊中叠氮化物残留量的目的。
1 仪器与试药
Diones ICS 2000离子色谱仪(美国戴安公司),包括 AS40 Automated Sampler自动进样器、电导检测器、在线淋洗液发生器(美国戴安公司)。叠氮化钠对照品(美国 Aldrich,含量99.5%,水分0.14%);厄贝沙坦胶囊(珠海润都民彤制药有限公司,规格为每粒 0.15 g,批号为 20090601,20090602,20090603);去离子水(Milli-Q超纯水发生器)。
2 方法与结果
2.1 色谱条件
色谱柱:保护柱为 IonPac AG11-HC 柱(50 mm ×4 mm),分析柱为IonPac AS11-HC离子交换色谱柱(250 mm×4 mm);淋洗液:KOH溶液(内置淋洗液发生器),梯度洗脱,见表1;柱温:30℃;进样量:25 μL。

表1 梯度洗脱条件
2.2 溶液配制
精密称取叠氮化钠对照品适量,加水溶解并定量稀释制成每1 mL中含叠氮化物1 μg的溶液,作为对照品溶液。取厄贝沙坦胶囊(4粒)内容物研细,精密称取相当于厄贝沙坦 0.5 g的内容物,置容量瓶中,加水5 mL,用力振摇使厄贝沙坦分散均匀,超声15 min,0.45 μm的微孔滤膜滤过,滤液作为供试品溶液。
2.3 方法学考察
专属性试验:分别精密吸取对照品溶液、供试品溶液及去离子水各25 μL,按拟订色谱条件进样,色谱图见图1。在叠氮化物对照品色谱峰处,供试品溶液与溶剂中其他成分对叠氮化物峰无干扰。
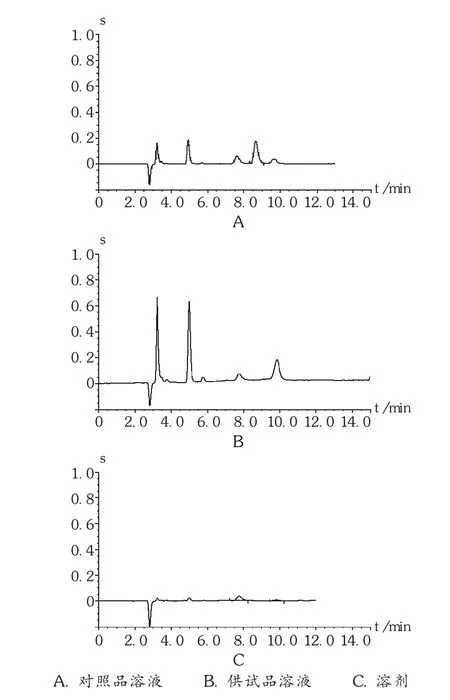
图1 离子色谱图
线性关系考察:分别精密称取叠氮化物对照品 0.008 47,0.010 91,0.012 14 g,置 100 mL 容量瓶中,加水溶解并稀释至刻度,摇匀,作为对照品贮备液A,B,C。精密量取对照品贮备液A 1 mL置100 mL容量瓶中,加水稀释至刻度,即得质量浓度为0.842 μg /mL 的线性对照品溶液;精密量取对照品贮备液 B 2,1,1 mL,分别置 10,100,200 mL容量瓶中,加水稀释至刻度,摇匀,即得质量浓度分别为 2.168,1.084,0.542 μg /mL 的线性对照品溶液;精密量取对照品贮备液 C 5,1 mL,分别置 50,100 mL容量瓶中,加水稀释至刻度,摇匀,即得质量浓度分别为1.508,1.206 μg/mL的线性对照品溶液。分别精密量取上述线性对照品溶液25 μL注入离子色谱仪,记录色谱图。以叠氮化物峰面积为(Y)对质量浓度(X)进行线性回归,得回归方程 Y=11.175 X+0.036 7, r=0.999 6(n=6)。结果表明,叠氮化物质量浓度在0.542 ~2.168 μg/mL 与峰面积呈良好的线性关系。
加样回收试验:精密称取厄贝沙坦(批号20090601)内容物9份,分别精密加入高、中、低3个水平浓度叠氮化钠对照品溶液5 mL,按供试品测定方法测定含量,计算回收率。结果见表2。

表2 叠氮化物加样回收试验结果(n=9)
精密度试验:按2.2项下操作配制对照品溶液6份,连续进样6次,记录色谱图。结果叠氮化物峰面积的 RSD为1.0%(n=6),表明仪器精密度良好。
稳定性试验:取2.2项下的同一供试品溶液,别在放置0,2,4,6,8,10,12 h时进样检测。结果叠氮化物峰面积的 RSD 为1.2%(n=7),表明供试品溶液在 12 h内稳定。
检测限及定量限试验:取2.2项下的对照品溶液,加去离子水逐级稀释,分别精密量取25 μL注入离子色谱仪,记录色谱图。结果表明,叠氮化物的检测限为 0.1 μg /mL(2.5 ng),定量限为0.5 μg /mL(12.5 ng)。2.4 样品含量测定
取 3 批样品(批号为 20090601,20090602,20090603),按外标法以峰面积计算厄贝沙坦胶囊中叠氮化物的残留量。结果均未检出叠氮化物。
3 讨论
文献[3-5]采用Dionex IonPac AS18分析柱来测定叠氮化物。本方法采用 IonPac AS11-HC,且采用了不同浓度的 OH-,对叠氮化物测定方法作了补充,证明可以通过不同类型的离子色谱柱及淋洗液浓度测定叠氮化物的残留量;且按照本方法测得的检测线/定量限低于上述方法,能准确地对叠氮化物进行痕量分析。
本方法中采用戴安公司商品化的在线淋洗液自动发生器[6],其优点是只用水和鼠标控制就能精确而在线地产生无污染(CO2)的所需浓度的淋洗液,并得到非常好的色谱重现性。另外,本方法所用淋洗液(25 μL,18 mmol/L)浓度低于美国药典(USP35-NF30)与欧洲药典(EP8.0)的规定(20 μL,100 mmol/L),在检测过程中大大降低了背景噪音,基线更平稳,提高了检测的灵敏度。
欧美药典均对厄贝沙坦中叠氮化物的限度均作了严格规定,不大于 10 ppm,按本方法测得的定量限为 0.5 mg /L(12.5 ng),远低于限度浓度,能够准确定量。经过方法学验证,本方法专属性强,线性良好,回收率、重复性、溶液稳定性均良好,灵敏度高,前处理及操作简单,可测定厄贝沙坦胶囊中叠氮化物残留量。
参考文献:
[1]岑均达,马 霞.厄贝沙坦的合成[J].中国医药工业杂志,2007,38(3):239.
[2]余德松,祝 红,胡国仕.2010年至2012年医院口服抗高血压药利用分析[J].中国药业,2014,23(3):61-63.
[3]姚超英.离子色谱法测定沙坦类药物中的叠氮酸根[J].浙江大学学报:理学版,2008,35(3):305-310.
[4]李美君,姚先珍,汪秀林,等.离子色谱法测定厄贝沙坦中叠氮化物[J].中国医药导报,2012,9(32):118-119.
[5]黄巧巧,何佳佳,钟乃飞,等.柱切换离子色谱法测定厄贝沙坦中的叠氮根离子[J].药物分析杂志,2013,33(8):1 431-1 434.
[6]牟世芳,刘克纳,丁晓静.离子色谱方法及应用[M].北京:化学工业出版社,2010:57.
