没药化学成分和药理作用研究进展
2015-04-26孙甲友付雪艳白长财
韩 璐,孙甲友,周 丽,付雪艳,3,白长财,3
(1.宁夏医科大学 药学院,宁夏 银川,750004;2.宁夏回药现代化工程技术研究中心,宁夏 银川,750004;3.宁夏回医药协同创新中心,宁夏 银川,750004)
没药化学成分和药理作用研究进展
韩 璐1,2,孙甲友1,周 丽1,2,付雪艳1,2,3,白长财1,2,3
(1.宁夏医科大学 药学院,宁夏 银川,750004;2.宁夏回药现代化工程技术研究中心,宁夏 银川,750004;3.宁夏回医药协同创新中心,宁夏 银川,750004)
没药为重要的香药之一,被广泛应用于回药香药复方、中药复方中。近年来,对没药的研究报道逐年增多,为了更好地开发和利用该药材,通过查阅国内、外文献,对其化学成分和药理作用的研究进行综述,以期为进一步开发和利用没药药材资源提供参考。
没药;挥发油;化学成分;药理作用
没药(Myrrh)为没药属(Commiphora)植物树皮渗出的油胶脂状物质,主要产于索马里和埃塞俄比亚等地区。性平,味苦,具有活血化瘀、消肿生肌的功效,临床常用于治疗跌打损伤、瘀滞疼痛等[1]。C.Myrrha也被叫做Commiphoramolmol,其他熟悉的名字包括 “Arabian myrrh” “Karam” “Morr Higazi” “murr” “guggul” “makkul” “ malmal” “mo yao”and “bola”[2]。没药曾一度能和黄金相媲美,然而没药最早是被圣经希伯来书引用作为圣油而出名,随着时间的推移才逐渐被发现并用于治疗。没药除用作香料成分外,也可用于化妆品、食品和药品[3]。
随着国家对民族医药及相关健康产业的投入不断增加,近年来,有关没药在回药、中药及其复方中的应用相关研究报道越来越多。为了更好地开发和利用该药材,通过查阅国内外文献,对其化学成分和药理作用的研究进行综述,以期能为开发和利用没药药材资源提供参考。
1 化学成分
调查不同种属及分布的没药,其化学成分的分布中挥发油占3%~8%,醇溶性树脂占25%~40%,水溶性树胶占30%~60%[4]。现代化学研究表明,没药中主要化学成分类型有单萜、倍半萜、三萜、甾体、木脂素等,而分离鉴别得到的没药成分与其来源以及提取方法有密切的关系。Assad等[5]利用GC-MS技术对多种没药挥发油进行了分析,发现挥发油成分中单萜部分因品种、产地而有较大的差异。王维等[6]从肯尼亚产地的没药挥发油中分离出26个成分,鉴定了其中的16个,证明其主要成分是单萜和倍半萜。
王勇等[7]采用气相色谱-质谱法分别对超临界CO2萃取法、索氏提取法、超临界提取法和水蒸气提取没药(橄榄科植物)所得提取物的化学成分进行比较分析,发现各提取方法所得提取物成分差异较大。除了用不同的提取方法得到的化学成分有差异外,从不同萃取剂和不同产地的没药中得到的成分也不全相同。万文珠等[8]对来源于爱伦堡没药树(BalsamodendronehrenbergianumBerg.)没药的化学成分进行了系统研究,分离鉴定了15个化合物,其中十八烷-1,2,3,4-四醇-1-鼠李糖苷(octadecane-1,2,3,4-1-rhamnoside)(1),环阿尔廷-24-烯-1,2,3-三醇(cyclolansotane-24-en-1,2,3-triol)(2),愈创木-2-甲氧-7(11),8(9)-二烯-10-烃基-6-羰基-8,12-内酯(guaia-2-methoxy-7(11),8(9)-dien-10-hydroxy-6-oxo-8,12-olide)(3),愈创木-6,7-环氧-4,10-二醇(guaia-6,7-epxoy-4,10-diol)(4),呋喃杜松-6-(1),7(8),9(10)-三烯-3-醇(furanocadina-6-(1),7(8),9(10)-triene-3-ol)(5),杜松-6(1),7(8),9(10)-三烯-11-羟基-2-羰基-8,12内酯(cadina-6-(1),7(8),9(10)-triene-11-hydroxy-2-oxo-8,12-olide)(7),吉玛-2-甲氧-1(10),7(11)-二烯-6-羰基-8,12-内酯(genmacr-2-methoxy-1(10),7(11)-dine-6-oxo-8,12-olide)(8),桉烷-1,5,11三醇(eudesma-1,5,11-triol)(9)是新化合物,愈创木-6(7)-烯-4,10-二醇(guaia-6(7)-en-4,10-diol)(6)为首次从没药中分离获得。杨国春等[9]通过硅胶柱色谱、SephadexLH-20柱色谱、开放ODS柱色谱、制备HPLC等多种色谱手段,从没药的氯仿提取物中共分离出17个化合物,其中倍半萜类化合物:杜松烷型:(4α,11α)-2-oxo-8,11-dihydroxycadina-1(6),7-9-trien-12-oic acid γ-lactone(10),(4α,11β)-2-oxo-8,11-dihydrocadina-1(6),7,9-trien-12-oic acid γ-lactone(11),9-methoxymyrrhone(12)为新化合物没药酮(myrrhone),Dihydropyrocurzerenone;而化合物愈创木烷型:orientalol E(13), alismol(14),桉叶烷型:proximadiol(15) 为首次从该属植物中分离得到。
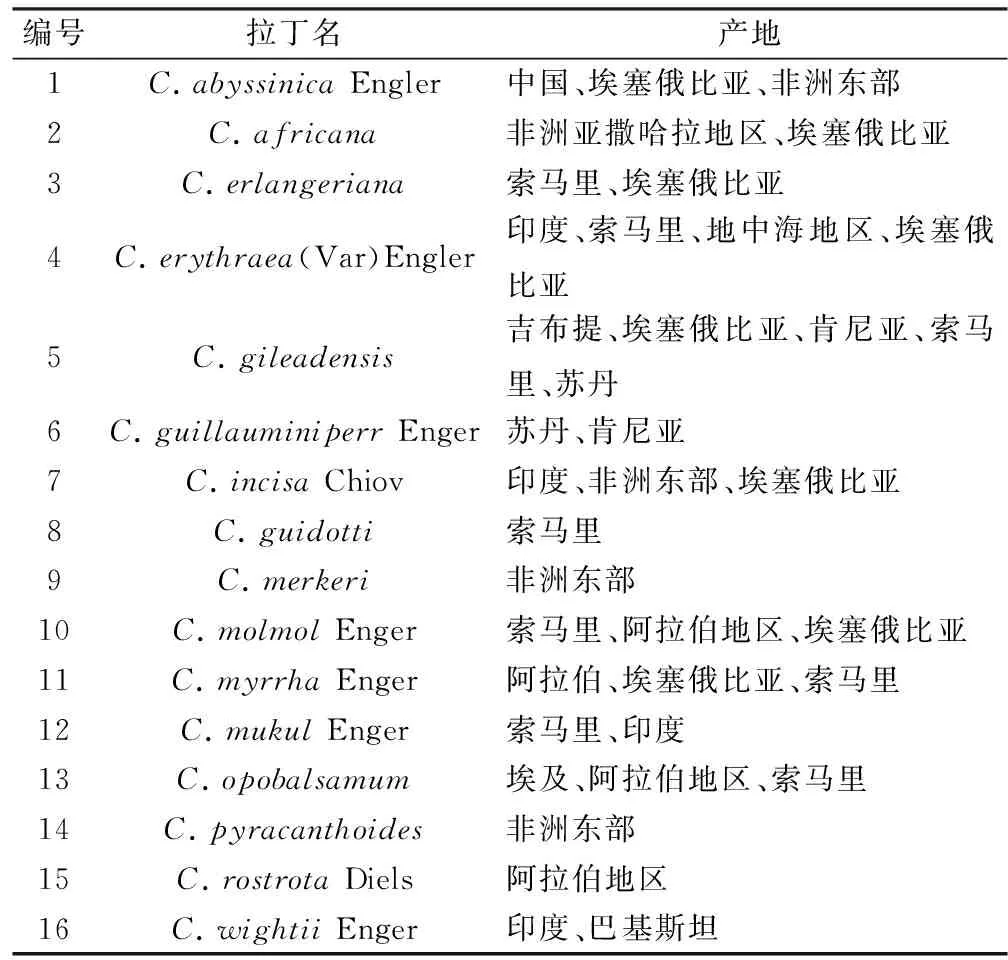
表1 没药属部分植物的主要分布地区
李蓉等[10]采用硅胶柱色谱,ODS柱色谱及制备HPLC等方法对穆库没药化学成分进行了分离纯化,从中分离得到4个化合物,分别鉴定为Epi-magnolin(16),1,7,8,10,11,12,13,14,15,17-decahydro-decahydro-17-17-(S)-1-hydroxyethyl-10,13-dimethyl-2H-eyclopenta[α]phenanthrene-3,16(16H,19H)-dione(17),1,7,8,10,11,12,13,15,16,17-decahydro-17-(2-hydroxy-6-methylheptan-2-yl)-10,13-dimethyl-2H-cyclopenta[α]penanthrene-3(6H,9H,14H)-one(18),20-methoxy-4,17(20)Z-pregnadiene-3,16-dione(19),化合物16~18从橄榄科中首次分离得到,化合物19从该植物中首次分离得到。
有学者从Commiphora sphaerocarpa石油醚组分中得到化合物(20)、(21)、(22)、2-甲氧基-呋喃二烯(23)、(1(10)E,2R,4R)-8,12-环氧吉玛-1,7,10,11-四烯-6-酮(24)、(1(10)E,4E)-8,12-环氧吉玛-1,7,10,11-四烯-6-酮(25)、(1E)-8,12-环氧吉玛-1,7,10,11-四烯-6-酮(26)、(1E)-3-甲氧基-8,12-环氧吉玛-1,7,10,11-四烯-6-酮(27)、二氢焦莪术烯(28)[11]。Commiphora molmol 乙酸乙酯组分和正己烷组分中得到化合物(29)、(30)、(31)、(32)、(33)、(34)、(35)、2-甲氧呋喃愈创木-9-烯-8酮(36)、1(10)Z,4Z-呋喃-二烯-6-酮(37)、4,5-二氢呋喃二烯-6-酮(38)、甾醇(39~41)、没药甾醇-I(42)、没药甾醇-II)(43)[21]。从Commiphora guidottii 乙酸乙酯组分中得到化合物(44)、T-杜松醇(45)、4β,5α,10β-三羟杜松烷(46)、桉树烯(47)、3-羰基-T-杜松醇(48)、6β,10β-二羟-4(15)-愈创木烯(49)、(-)-oplopanone(50)[12]。
部分化合物的结构式如图1。
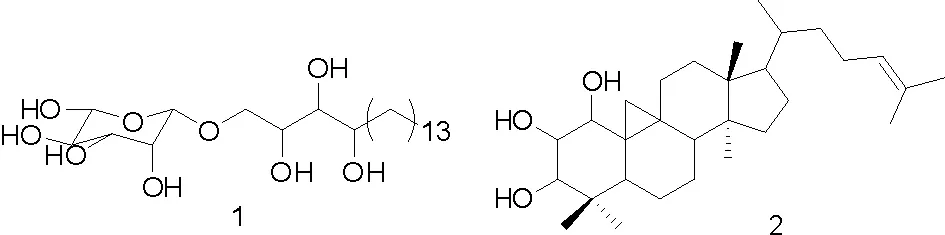
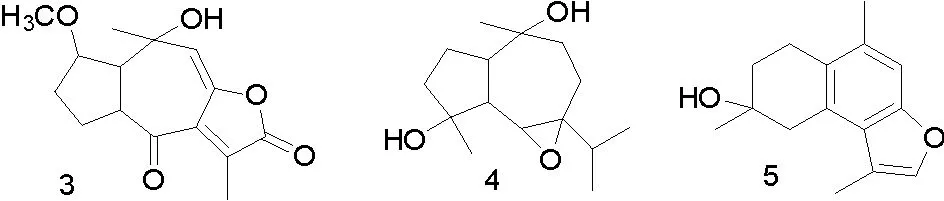
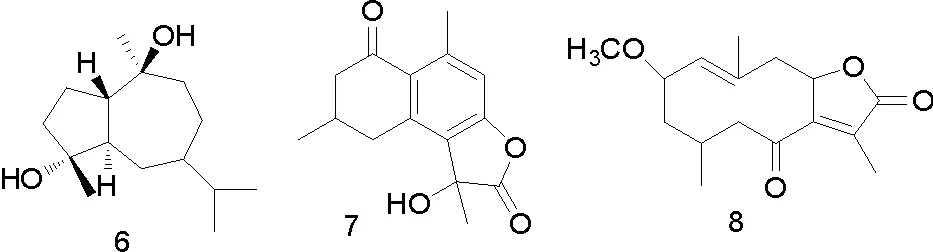
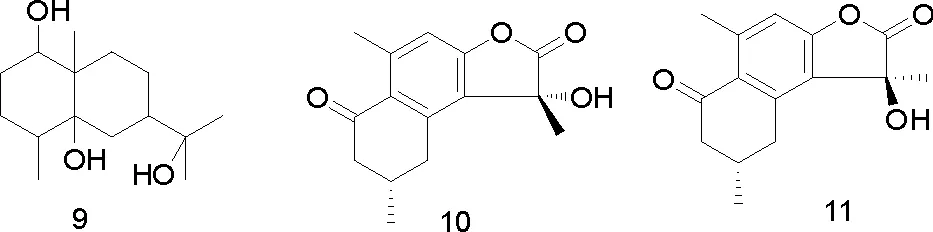
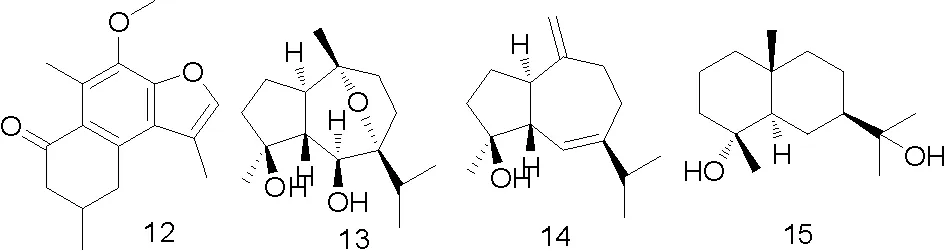
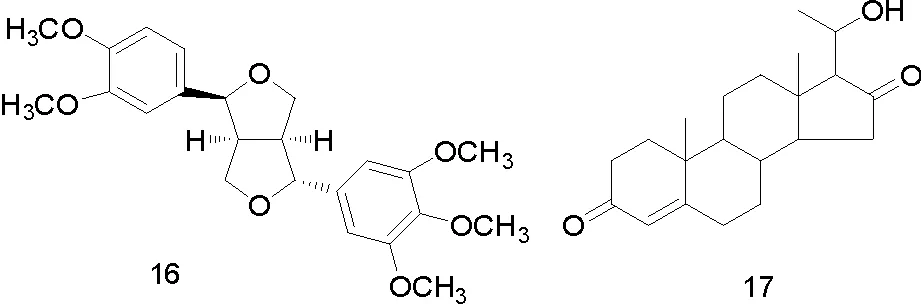
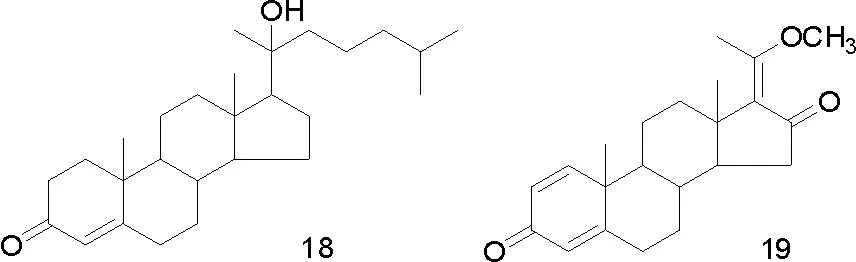

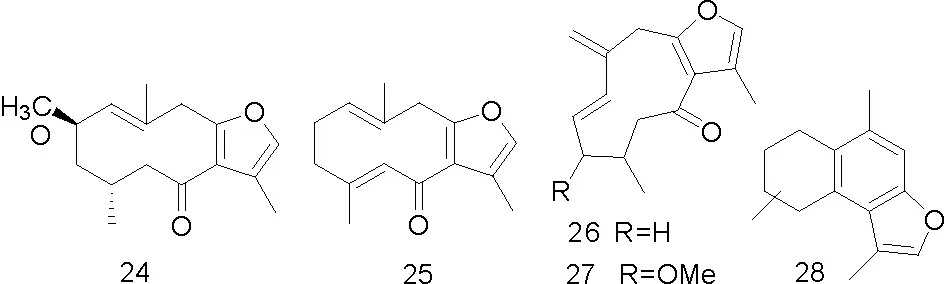
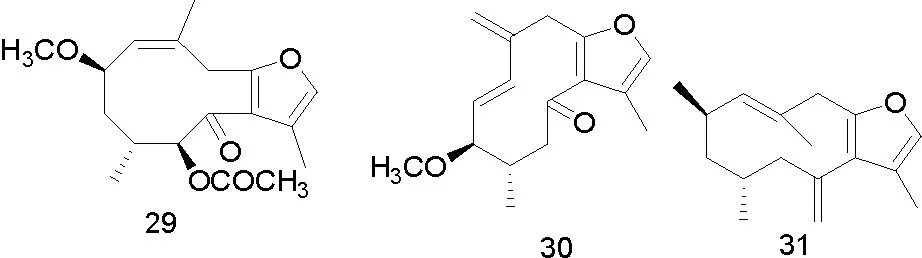
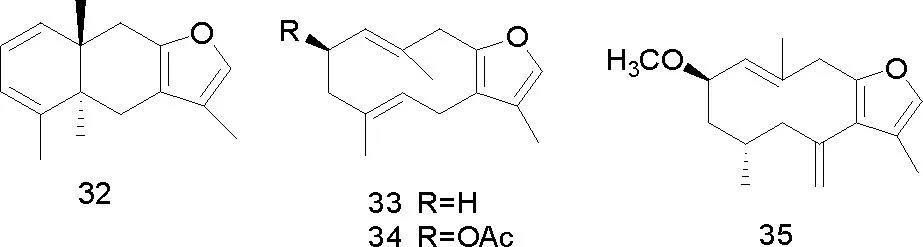
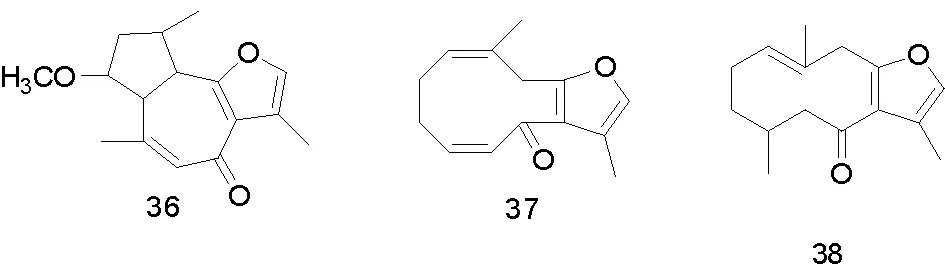
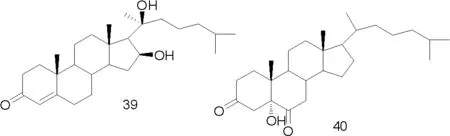

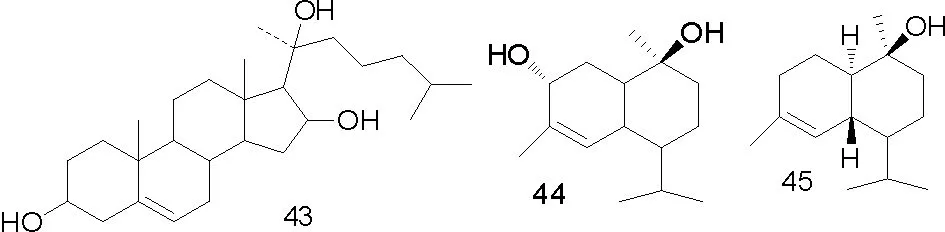
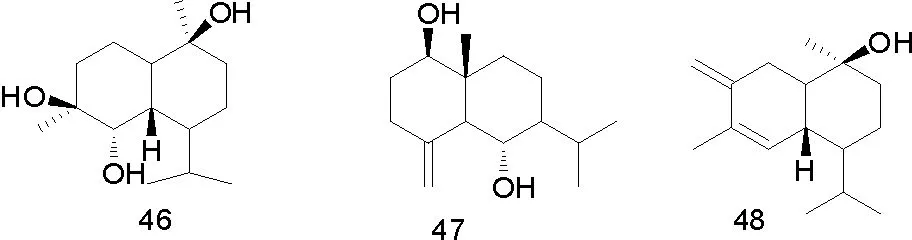
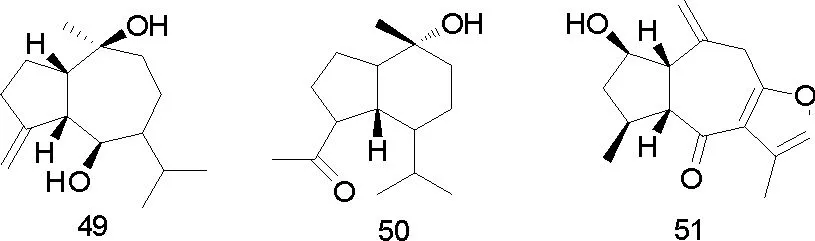
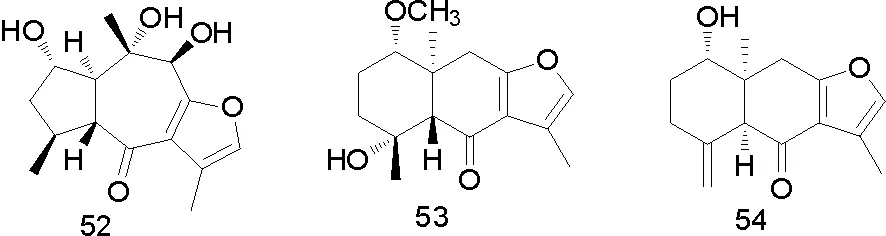
图1 从没药中分离得到的部分化合物结构
2 药理活性
2.1 抗肿瘤活性
没药对C6胶质瘤细胞、A2780细胞、SK-OV-3细胞、Shikawa细胞和A2708细胞等均表现出显著的抗肿瘤活性[13]。没药倍半萜中含有β、γ和δ-榄香烯,现代药理和临床研究表明榄香烯有很好的抗肿瘤功效。β-榄香烯已作为抗癌药物治疗各种癌症,包括胶质母细胞瘤,并且β-榄香烯对胶质母细胞瘤的抗增殖作用是通过激活p38 MAPK实现[14]。没药中的呋喃型倍半萜rel-1S,2S-epoxy-4R-furanogermacr-10(15)-en-6-one对乳腺癌细胞系MCF-7具有弱的细胞毒性(IC50为40μmol·L-1)[15]。
吉恺等[16]对没药C.opobalsamum研究中分得20多个倍半萜类化合物,并对其中含量较高的2个吉玛烷型倍半萜化合物进行抗肿瘤活性筛选。结果表明,倍半萜类化合物对三种激素非依赖性前列腺癌细胞的增殖均有显著的抑制作用,在高浓度下对大肠癌细胞的增殖有抑制作用。呋喃型没药倍半萜成分可下调抗凋亡基因Bcl-2的表达,对细胞增殖抑制明显。没药二萜成分中的Abietic acid和Dehydroabietic acid对A2780、SK-OV-3和Shikawa癌细胞具有以剂量依赖方式的显著细胞毒性。Abietic acid对A2780细胞的抗增殖作用最明显,IC50值为46.89μmol·L-1。Dehydroabietic acid能抑制SK-OV-3细胞的生长,IC50为26.93mol·L-1,而其作用机制有待研究[13]。没药三萜中的7个环木菠萝烷型三萜,对PC3和DU145人乳腺癌细胞具有中等强度的细胞毒性,IC50值为10.1~37.2μmol·L-1[17]。
2.2 保肝作用
没药提取物能保护CCl4对Wistar大鼠造成的肝损伤,其作用机制可能与没药提取物的抗氧化、清除自由基活性有关[18]。没药甾酮可显著抑制肝星状细胞生长并呈时间剂量依赖,24h最大抑制率可达(57.4±2.45)%(100μmol·L-1);50μmol·L-1和75μmol·L-1没药甾酮可使G2/M期细胞比例增多,G0/G1和S期比例下降;没药甾酮可使MDA水平下降,GSH和SOD、CAT活性升高。没药甾酮可干扰细胞周期,抑制肝星状细胞增殖;还可降低氧化应激反应从而抑制肝星状细胞活化[19]。
2.3 凝血作用
蒋海峰等[20]采体外二磷酸腺苷(ADP)诱导的血小板聚集实验观察没药提取物的抗血小板聚集活性及量效关系;采用凝血酶时间(TT)法观察没药提取物对凝血酶的影响及量效关系。得出没药的水提物、挥发油对家兔血小板聚集及凝血酶时间的影响均能产生显著效应。没药的水提液及挥发油与空白对照比较均具有明显抑制血小板聚集活性(P<0.05),且水提物活性强于相应挥发油活性,IC50为0.004 2g·mL-1;与空白对照比较没药的水提物及挥发油有非常显著的抗凝活性(P<0.001),没药水提物活性IC50为0.004 6g·mL-1。
2.4 镇痛作用
没药作为一味传统的中药,中国古代就发现其有镇痛作用,《本草衍义》曰:“没药,大概通滞血,打扑损疼痛,皆以酒化服。血滞则气壅凝,气壅凝则经络满急,经络满急,故痛且肿。凡打扑着肌肉须肿胀者,经络伤,气血不行,壅凝,故如是。”现代研究中也进一步证明了镇痛作用,Dolara等[21]发现,没药中的倍半萜成分,呋喃桉烷-1,3-二烯和莪术烯可作用于中枢神经系统阿片受体,有镇痛活性,其作用可被吗啡拮抗纳洛酮阻断。近期对没药烷吉酮的研究还发现其有治疗痛经的作用,结果表明,没药烷吉酮在4mg·kg-1、8mg·kg-1下对小鼠痛经模型具有明显镇痛作用;没药烷吉酮在有效浓度(1.2μg·mL-1、1.6μg·mL-1)下对缩宫素所致在体、离体子宫收缩均具有明显对抗作用;没药烷吉酮(1.6μg·mL-1)能同时明显抑制CaCl2、KCl、乙酰胆碱所致离体子宫的收缩[22]。
2.5 神经保护作用
Jing Xu等[23]从C.myrrha(印度)分离得到四个新倍半萜类化合物K-N(51-54),其中(51)和(54)有表现出神经保护作用,特别对人神经母细胞瘤细胞中的MMP+有诱导死亡作用,鸟嘌呤被用作乳糖操纵子的正调控。神经母细胞瘤暴露在MMP+其生存能力通过MTT实验进行检测,进行对照实验,有显著性差异(P<0.01)。
2.6 其他作用
郭文虎[24]对50只SD雄性大鼠进行实验,发现没药水提取物具有应激性溃疡的保护作用。结果表明,使用雷尼替丁、没药治疗21天后,大鼠胃黏膜炎性细胞浸润明显减少,与模型组比较差异有统计学意义(P<0.05)。在周昆等[25]的研究中,乳香没药混合物(1∶1)口服可导致Beagle犬血清TC、ALP升高,肝脏胆汁淤积,而大鼠虽然TC显著升高,但ALP无明显升高,肝脏病理改变以脂肪变性为主而无胆汁淤积,所以关于乳香没药的肝毒性还有必要进行深入研究。
3 结语
没药中主要化学成分有单萜、倍半萜、三萜、甾体以及木质素等。药理研究表明,没药具有退热、抗炎、镇痛、神经保护等多方面的药理活性,无明显毒副作用。目前没药在香料、化妆品、食品、药品以及保健品中都得到了广泛的应用[9]。
没药分布广泛,品种繁多。随着现代科技在中药材研究发面的应用,在国内外学者不懈的努力下,分离鉴定出很多新的化合物并测定了其特定的药理作用,为进一步开发和利用没药资源奠定了良好的基础。另外,从目前的研究报道看,不同来源及种属的没药其化学成分也存在一定的差异,而其药理作用是否也存在差异,还需要更加深入的研究。
没药为回药香药中的重要药材之一,在许多方剂中均有提及,而有关没药在回药香药复方中的作用、地位及其意义等方面的研究资料较为缺乏。因此,有必要加强此方面的研究,为回医香药配伍提供科学依据。
[1] 秦华珍,冼寒梅,宁小清,等.不同剂型没药对外伤致血瘀的消肿作用研究[J].广西中医学院学报,2001,4(4):91-93.
[2] OMER SA, ADAM SE, KHALID HE. Effects on rats of Commiphora myrrha extract given by different routes of administration[J].Vet Hum Toxicol,1999,41(4):193-196.
[3] MASSOUD A, SISI S EI, SALAMA, O, et al. Preliminary study of therapeutic efficacy of a new fasciolicidal drug derived from Commiphora molol(Myrrh) [J]. Am J Trop Med Hyg,2001,65(2):96-99.
[4] HAMM S, BLETON J, TCHAPLA A. Headspace solid phase microextraction for screening for the presence of resins in Egyptian archaeological samples[J]. J Sep Sci,2004,27(3),235-243.
[5] ASSAD Y O H, TORTO B, HASSANALI A, et al. Seasonal variation in the essential oil composition of Commiphora quadricincta and its effect on the maturation of immature adults of the desert locust, Schistocerrca gregaria[J].Phytochemistry,1997,44(5):833-841.
[6] 王维,朱永新,秦祥林,等.肯尼亚没药挥发油化学成分研究[J].药物分析杂志,1995,15(6),33-36.
[7] 王勇,赵艳红,陈彦,等. 超临界二氧化碳萃取没药化学成分可行性研究[J].时珍国医国药,2005,16(3):177-178.
[8] EL ASHRY E S, RASHED N, SALAMA O M, et al. Components,therapeutic value and uses of myrrh[J]. Pharmazie,2003,58(3):163-168.
[9] 杨国春.没药化学成分的研究[D].沈阳:沈阳药科大学,2009.
[10] 李蓉,李国玉,王航宇, 等.穆库没药化学成分的研究[J].中国现代中药,2012,14(9):13-17.
[11] DEKEBO A, DAGNE E, STERNER O. Furanosesquiterpenes from Commiphora sphaerocarpa and related adulterants of true myrrh[J]. Fitoterapia,2002,73(1):48-55.
[12] EDWARDS H G M, FALK M J.Fourier-transform raman spectroscopic study of frankincense and myrrh[J]. Spectrochimica Acts Part A,1997,53,2393-2401.
[13] SU SL, WANG TJ, CHEN T, et al. Cytotoxicity activity of extracts and compounds from Commiphora myrrha resin against human gynecologic cancer cells[J]. J Med Plant Res,2011,5(8):1382-1389.
[14] YAO YQ, DING X, JIA YC, et al. Anti-tumor effect of beta-elemene in glioblastoma cells depends on p38 MAPK activation[J]. Cancer Letters,2008,264(1):127-134.
[15] ZHU N, KIKUZAKI H, SHENG S, et al. Furanosesquiterpenoids of Commiphora myrrha[J]. J Nat Prod,2001,64(11):1460-1462.
[16] 吉恺,孔峰,沈涛,等.没药倍半萜成分的分离鉴定及抗肿瘤活性[J].山东大学学报:医学版,2008,46(4):343-348.
[17] SHEN T,YUAN HQ,WAN WZ,et al. Cycloartane-type triterpenoids from the resinous exudates of Commiphora opobalsamum [J]. J Nat Prod,2008,71(1):81-86.
[18] NLGOWRI SHANKAR,R MANAVALAN,DVENKAPPAYYA, et al. Hepatoprotective and antioxidant effects of Commiphora berryi(Arn)Engl bark extract against CCl4-induced oxidative damage in rats[J].Food Chem Toxicol,2008,46(9):3182-3189.
[19] 贾晓黎,石娟娟,封婷,等.没药甾酮对肝星状细胞HSC-T6增殖的影响[J].Chinese Hepatology,2013,18(8):522-525.
[20] 蒋海峰,宿树兰,欧阳臻,等.乳香、没药提取物及其配伍对血小板聚集与抗凝血酶活性的影响[J].中国实验方剂学杂志,2011,17(19):160-164.
[21] Dolara P,Luceri C,Ghelardini C ,et al.Analgestic effect of myrrh [J]. Nature, 1996, 379 (6560) :29-29
[22] 吴方方,汪鋆植,黄年玉,等.没药烷吉酮治疗痛经及机制研究[J].中国药理与临床,2013,29(5):47-49.
[23] JING XU, YUANQIANG GUO,PENG ZHAO, et al. Four new sesquiterpenes from Commiphora myrrha and their neuroprotective effects[J].Fitoterapia,2012,83(4):801-805.
[24] 郭文虎.乳香没药提取物对大鼠应激性溃疡治疗作用的研究[J].中国医药指南,2012,10(20):454-455.
[25] 周昆,谈英,柳占彪,等.乳香没药对大鼠肝脏毒性的比较研究[J].中国实验方剂学杂志,2010,16(6):221-223.
(责任编辑:魏 晓)
Advances on Chemistry and Pharmacological Research of Myrrh
Han Lu1,2,Sun Jiayou1,Zhou Li1,2,Fu Xueyan1,2,3,Bai Changcai1,2,3*
(1.Ningxia Medical University Pharmacy College, Yinchuan 750004, China;2.Ningxia Engineering & Technology Research Center for Modernization of Hui Medicine, Yinchuan 750004, China;3.Ningxia collaborative innovationcenter for Hui medicine, Yinchuan 750004, China)
As one of important aromatic drug, Myrrh have been widely used in Hui medicine, traditional Chinese medicine and so on. In recent years, studies have reported myrrh increasing year by year, in order to better development and use of the medicine, the paper access to domestic and foreign literature, reviewed its chemical constituents and pharmacological action, with a view to provide reference for the further development and utilization of the medicinal resources.
Myrrh; Essential Oil; Chemical Composition; Pharmacological Effects
2014-09-09
国家“十二五”科技支撑计划项目(2013BAI11B07)
韩璐(1982-),女,宁夏医科大学讲师,研究方向为中药、回药质量控制。
白长财(1980-),男,宁夏医科大学副教授,研究方向为民族药活性成分及质量控制。E-mail:changcaibai@163.com
R285
A
1673-2197(2015)03-0038-04
10.11954/ytctyy.201503015
