基于药物体系质量评价模式的石菖蒲质量表征关联分析研究
2015-04-21张璐李焕娟朱乃亮彭平孙道涵孙雅姝迟蕾姜艳艳石任兵
张璐 李焕娟 朱乃亮 彭平 孙道涵 孙雅姝 迟蕾 姜艳艳 石任兵
石菖蒲为天南星科多年生草本植物石菖蒲Acorus tatarinowii Schott 的干燥根茎,具芳香化湿,开窍宁神等功效,用于治疗癫痫、惊厥、健忘、老年痴呆等证。其中,2010 版《中华人民共和国药典》(一部)收录的石菖蒲含量测定方法为测定石菖蒲中总挥发油的量[1],以挥发油含量表征石菖蒲的质量。在研究石菖蒲药物中,本课题组发现石菖蒲药物成分苯丙素类与酚类相互作用与其镇静、抗抑郁药效的关联性[2-6],并建立了有效物质分离富集方法[7-8]。
在运用本课题组建立的药代动力学—药效动力学—药物成分相互作用关联分析方法(pharmacokinetics-pharmacodynamics-drug interactions,PK-PDDI)研究经方远志汤、开心散(远志、石菖蒲、茯苓、人参)以及组成单味药,抗痴呆、抗抑郁药物体系时,笔者发现石菖蒲芳香酸类与苯丙素类同为药物体系组成成分。中药化学成分的有效性与其质量性有关,即与中药化学成分的类型以及存在的量、组成比例等有关[9-11]。
本文报道运用课题组所建立的基于药物体系的中药质量评价模式[12],对石菖蒲进行质量评价与控制。即基于药物体系的石菖蒲芳香酸类(原儿茶酸、香草酸、2,4,5-三甲氧基苯甲酸之和)与苯丙素类(β-细辛醚、α-细辛醚之和)有效指标性成分的含量测定,关注有效指标性成分的含量及组成比例,并与有效性确切的基准饮片进行关联度分析比较与质量综合考量,以确定其饮片质量优良度,为石菖蒲的有效应用提供科学依据,亦为有关药物的质量保障提供支撑。
1 仪器与试药
1.1 仪器
Waters e2695 高效液相色谱仪,Empower Pro 软件系统,2998 二极管阵列检测器;METTLER-AE240型电子分析天平(北京赛多利斯仪器有限公司);KQ-500DE 型数控超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药
原儿茶酸(批号121009,纯度≥98%)、香草酸(批号120915,纯度≥98%)、α-细辛醚(批号100298-201203,纯度100%)均购自北京方程生物科技有限公司,2,4,5-三甲氧基苯甲酸(批号20130816,纯度97%)购自国药集团化学试剂有限公司,β-细辛醚(批号00011017-T9K,纯度95%)购自天津一方科技有限公司,乙腈(色谱级,Fisher Scientific 公司),甲醇(分析纯,北京化工厂),乙酸(分析纯,北京化学试剂公司);娃哈哈纯净水(杭州娃哈哈集团有限公司),其余试剂均为分析纯。
15 批石菖蒲饮片购自于北京同仁堂药材有限责任公司及北京金象大药房,经北京中医药大学生药系刘春生教授鉴定为石菖蒲Acorus tatarinowii Schott 的干燥根茎,有关样品进行编号后存放在北京中医药大学中药学院中药化学系。
2 方法与结果
2.1 色谱条件
Thermo Hypersil GOLD (C18)液相色谱柱(250 mm×4.6 mm × 5 μm),流动相乙腈(A)-0.2%乙酸水(B),洗脱梯度(0 ~5 分钟,0% ~2%A;5 ~10 分钟,2% ~5% A;10 ~11 分钟,5% ~6%A;11 ~14 分钟,6% ~8%A;14 ~17 分钟,8%A;17 ~27 分钟,8% ~10% A;27 ~40 分钟,10% ~13%A;40 ~50 分钟,13% ~15%A;50 ~52 分钟,15% ~30%A;52 ~55 分钟,30% ~45%A;55 ~60分钟,45% ~47%A;60 ~67 分钟,47%A;67 ~70 分钟,47% ~100%A),流速1.0 mL/min,柱温25℃,检测波长256 nm,进样量10 μL。
上述色谱条件下,石菖蒲对照品及饮片的HPLC 谱图见图1。采用二极管阵列检测器在190 ~400 nm 全波长扫描,结果显示5 种有效指标性成分在256 nm 波长下有最大吸收且与其他色谱峰分离度良好,故选用256 nm 为检测波长,确保待测成分均有最高的检测灵敏度。
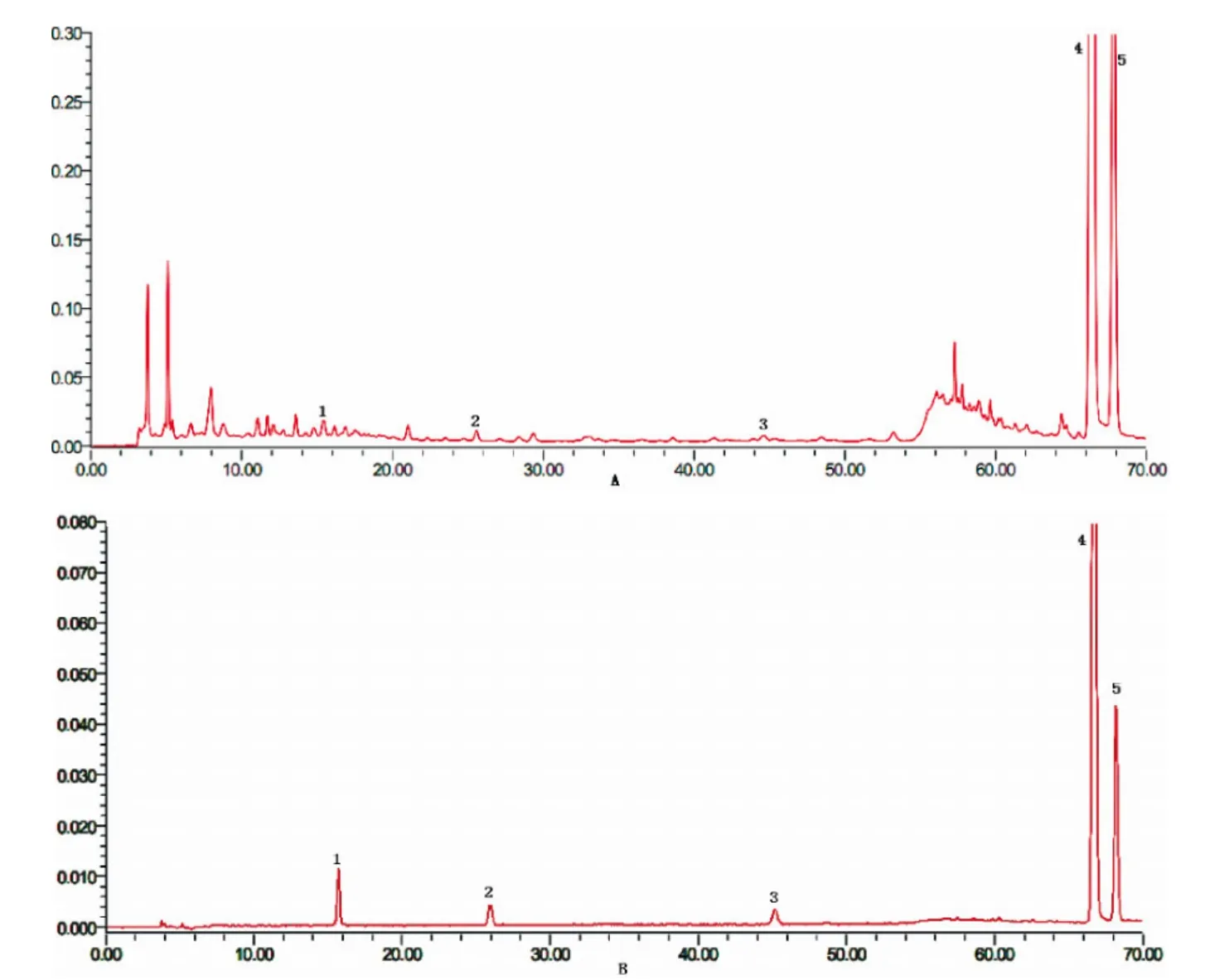
图1 石菖蒲供试品(A)及对照品(B)的HPLC 色谱图
2.2 对照品溶液的制备
分别取上述5 种对照品适量,精密称定,加入甲醇制成每1 mL 含有原儿茶酸19.9 μg、香草酸19.1 μg、2,4,5-三甲氧基苯甲酸31.2 μg、β-细辛醚652.8 μg、α-细辛醚104.6 μg 的对照品混合溶液。
2.3 供试品溶液的制备
取石菖蒲饮片粉碎,过四号筛,称取约2 g,精密称定,置于100 mL 圆底烧瓶中,精密加入50%甲醇50 mL,加热回流提取60 分钟,趁热过滤,提取3 次,合并滤液,回收溶剂至干,残渣加70%甲醇使溶解,定容至10 mL,即得。
2.4 线性关系考察
将“2.2”项下对照品混合溶液进样1 μL,4 μL,8 μL,16 μL,32 μL,48 μL,以进样量(μg)为横坐标,峰面积为纵坐标绘制标准曲线,计算回归方程及相关系数,结果见表1。
对小区边界及住宅周边进行智能监控,检测入侵、盗抢、翻墙等异常行为并自动报警,第一时间发现危险情况,保障小区/校园安全。
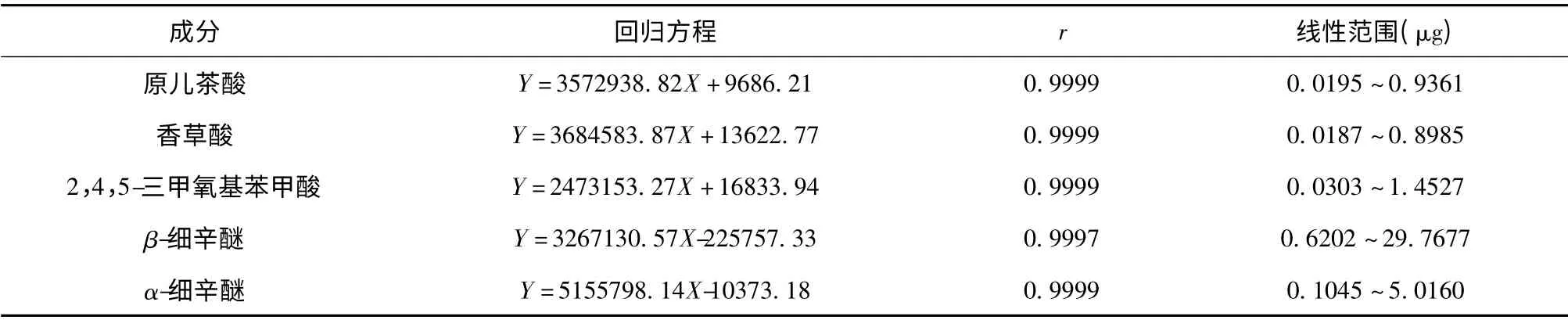
表1 5 种成分的回归方程、相关系数和线性范围(n=6)
2.5 精密度试验
取“2.3”项下同一石菖蒲样品溶液,连续进样6次,测得原儿茶酸、香草酸、2,4,5-三甲氧基苯甲酸、β-细辛醚、α-细辛醚的峰面积的RSD 分别为2.97%,2.47%,1.40%,0.68%,0.67%,精密度良好。
2.6 重复性试验
取同一石菖蒲饮片样品,按“2.3”项下方法平行制备供试品溶液6 份,测得原儿茶酸、香草酸、2,4,5-三甲氧基苯甲酸、β-细辛醚、α-细辛醚的平均含量分别为0.0026%、0.0015%、0.0016%、0.6897%、0.0901%,RSD 分别为2.83%,0.62%,1.53%,0.85%,0.55%,重复性良好。
2.7 稳定性试验
取“2.3”项下同一供试品溶液,于室温下放置,分别于0 小时,2 小时,4 小时,8 小时,12 小时,24小时进样,测得原儿茶酸、香草酸、2,4,5-三甲氧基苯甲酸、β-细辛醚、α-细辛醚的峰面积的RSD 分别为2.83%,2.04%,2.17%,0.38%,0.61%,供试品溶液在24 小时内稳定。
2.8 加样回收率试验
称取同一石菖蒲样品粉末(过四号筛)约1 g 共6 份,精密称定,加入对照品适量,按“2.3”项下方法制备供试品溶液,进样,测得原儿茶酸、香草酸、2,4,5-三甲氧基苯甲酸、β-细辛醚、α-细辛醚的加样回收率分别为99.59%、99.14%、100.15%、100.33%、100.14%,RSD 分别为2.97%、2.93%、1.72%、0.51%、1.44%,加样回收率合格,说明本方法准确、可靠,结果见表2。

表2 加样回收率试验结果
2.9 石菖蒲质量表征
2.9.1 基于有效指标性成分含量的质量表征 取15 个石菖蒲饮片样品,按“2.3”项下方法制备供试品溶液,每个平行制备3 份,照“2.1”项色谱条件进样,测定原儿茶酸、香草酸、2,4,5-三甲氧基苯甲酸、β-细辛醚、α-细辛醚的含量,对石菖蒲饮片中有效指标性成分含量进行全面表征,结果见表3。
2.9.2 基于有效指标性成分含量相对比值的质量表征 以药物体系中关键有效指标性成分香草酸的含量为基准,将15 个石菖蒲饮片样品中各有效指标性成分含量与香草酸含量的相对比值予以表征,结果见表4。
2.10 石菖蒲质量表征关联分析
2.10.1 基于与基准饮片有效指标性成分含量相对比值的质量表征的关联分析 基于“2.9.1”项下表3进行15 个石菖蒲饮片样品质量表征关联分析,如表3所示,15 个石菖蒲饮片中各有效指标性成分含量相差较大,并计算最高比值与最低比值的比,以反映各饮片中有效指标性成分含量的差异。原儿茶酸含量最大相差约1.84 倍,含量从高到低排序为:样品9>3>7>14>2>6>15>11>12>1>10>8>4>5>13;香草酸含量最大相差约2.0 倍,含量从高到低排序为:样品11>12>1>15>13>10>7>9>3>14>2>6>8>5>4;2,4,5-三甲氧基苯甲酸含量最大相差约5.2 倍,含量从高到低排序为:样品1>3>9>14>15>6>7>5>12>2>10>4>13>11>8;芳香酸类含量和最大相差约1.81倍,含量从高到底排序为:样品9>1>3>14>15>7>6>12>11>2>10>5>13>4>8;β-细辛醚含量最大相差约3.5 倍,含量从高到低排序为:样品12>1>4>11>9>6>7>15>14>10>5>13>3>2>8;α-细辛醚含量最大相差约10.8 倍,含量从高到低排序为:样品12>9>14>6>1>15>5>7>8>10>3>13>2>4>11;苯丙素类含量和最大相差约3.8 倍,含量从高到底排序为:样品12>9>6>14>1>7>4>15>11>5>10>13>3>2>8。
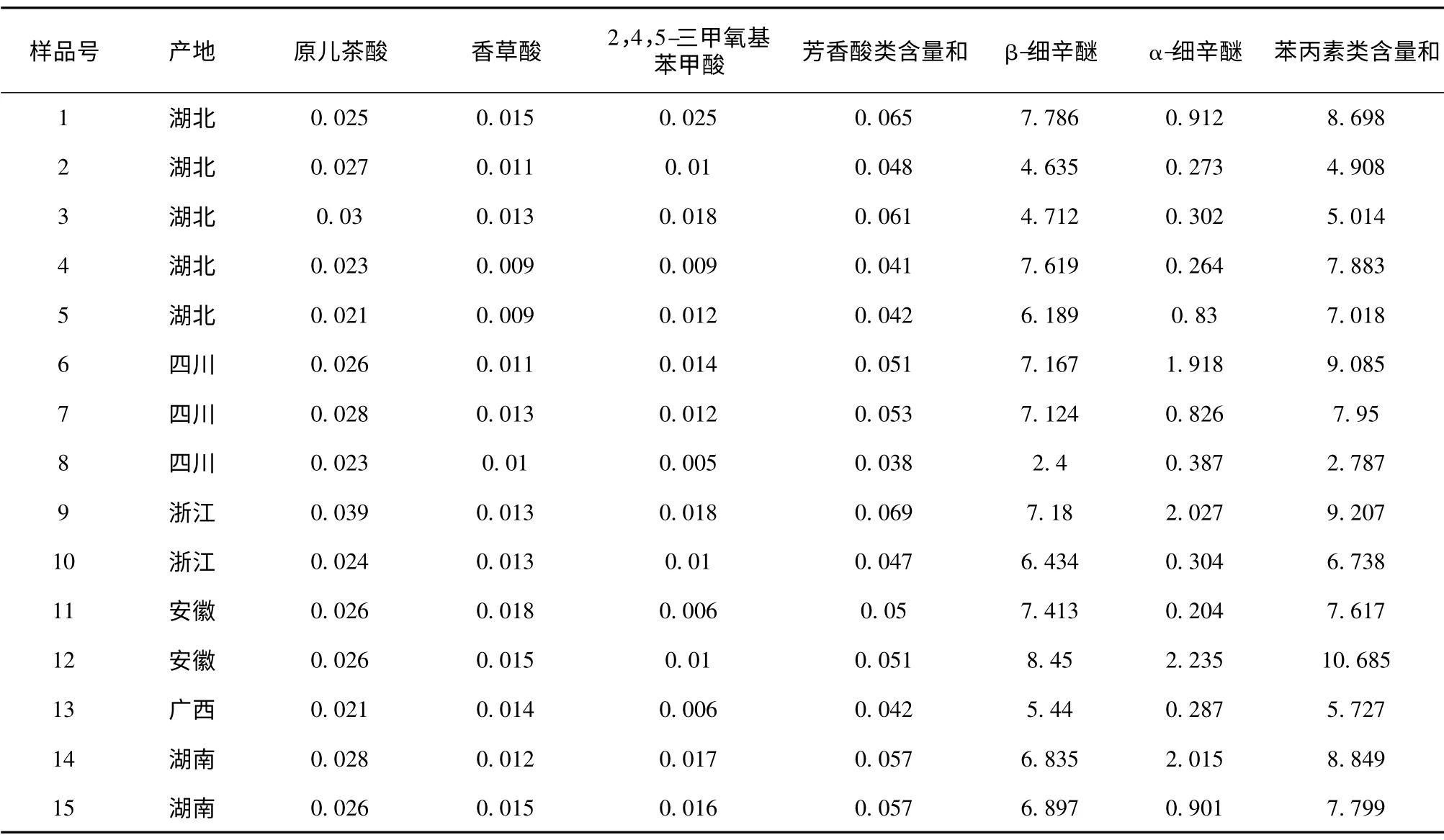
表3 基于有效指标性成分含量的15 个石菖蒲饮片样品质量表征(mg/g,n=3)
可见,在15 个石菖蒲饮片样品中有效指标性成分含量差异性:α-细辛醚(10.8 倍)>2,4,5-三甲氧基苯甲酸(5.2 倍)>苯丙素类含量和(3.8 倍)>β-细辛醚(3.5 倍)>香草酸(2 倍)>原儿茶酸(1.84倍)>芳香酸类含量和(1.81 倍);而基于原儿茶酸、香草酸、2,4,5-三甲氧基苯甲酸、芳香酸类含量和、β-细辛醚、α-细辛醚、苯丙素类含量和进行综合考量,样品1、6、9、12、14 中有效指标性成分含量总体高于有效性确切的基准饮片样品15[13],样品7 中有效指标性成分含量与样品15 接近。
2.10.2 基于与基准饮片有效指标性成分含量相对比值的比值质量表征的关联分析 将“2.9.2”项下表4以样品15 为基准,将15 个石菖蒲饮片中有效指标性成分含量相对比值与基准饮片样品15 的相对比值的比值进行关联分析得表5、图2。
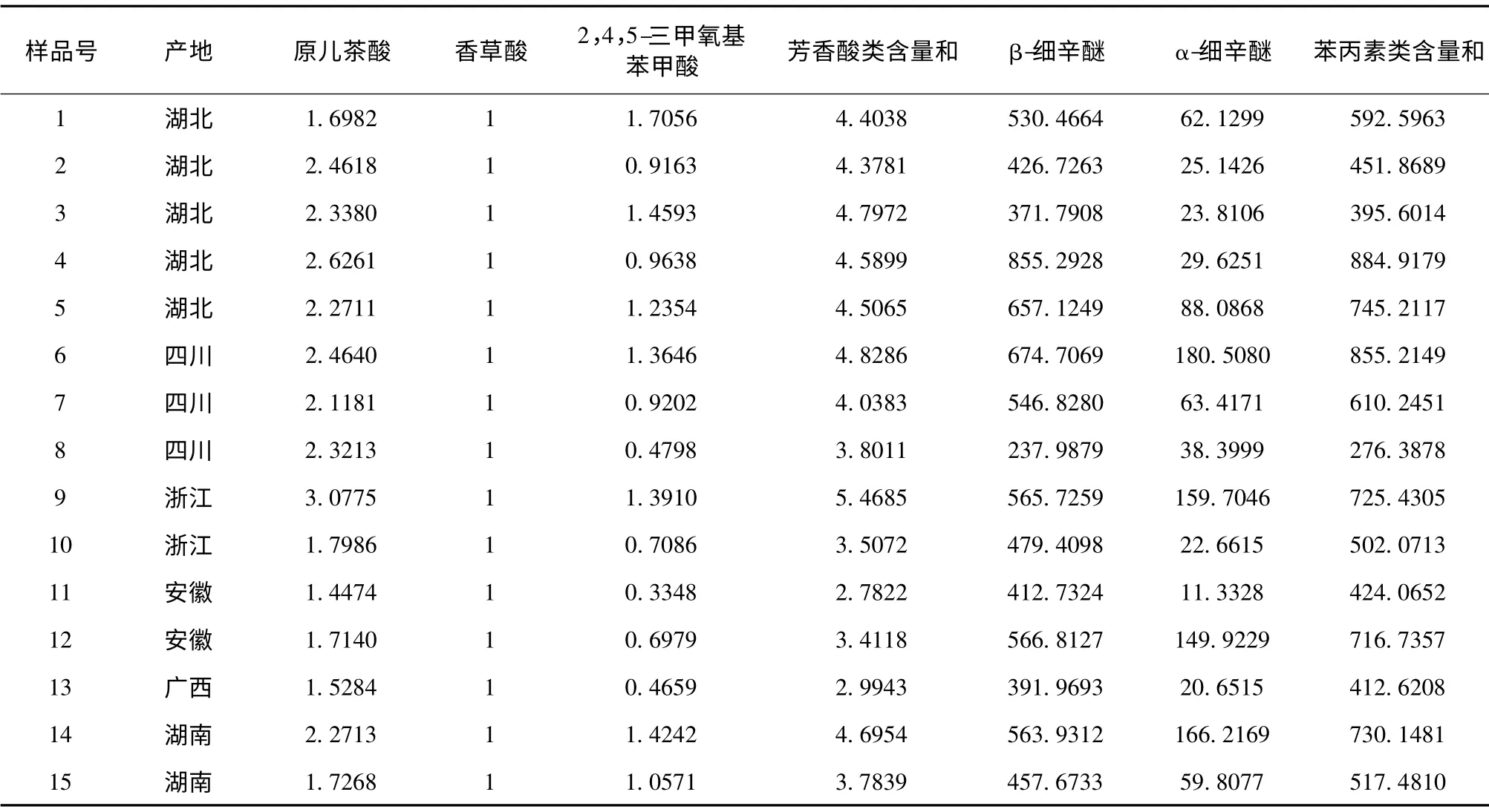
表4 基于有效指标性成分含量相对比值的15 个石菖蒲饮片样品质量表征
图2中不同颜色的矩形条代表各饮片中有效指标性成分含量相对比值与样品15 对应成分含量相对比值的比值,矩形条大小与样品15 中相同颜色的矩形条大小越相近,代表该饮片有效指标性成分含量比值与样品15 越接近,即质量表征关联密切。可以看出,样品1、5、7 与15 质量表征关联密切。以样品15 为基准,其他样品与其相对比值的比值差值的绝对值之和,即非关联系数δ;非关联系数与有效指标性成分的数目的比值,即非关联度,进而得到关联度,以反映饮片质量之间的关联性,得表5。
由表5可知,关联度由高到低排序为样品15(0/100%)>7 (0.8573/87.75%)>1 (1.1368/83.76%)>10 (1.1428/83.67%)>2 (1.4900/78.71%)>13 (1.8837/73.09%)>5 (2.0236/71.09%)>3 (2.0273/71.04%)>8 (2.1988/68.59%)>11 (2.1990/68.59%)>12 (2.5758/63.20%)>4 (2.9056/58.49%)>14 (3.3258/52.49%)>9 (3.8515/44.98%)>6 (4.1389/40.87%),即样品7、1、10 与基准样品15 质量关联性最高,而样品6、9 与基准样品15 质量关联性相差较大。
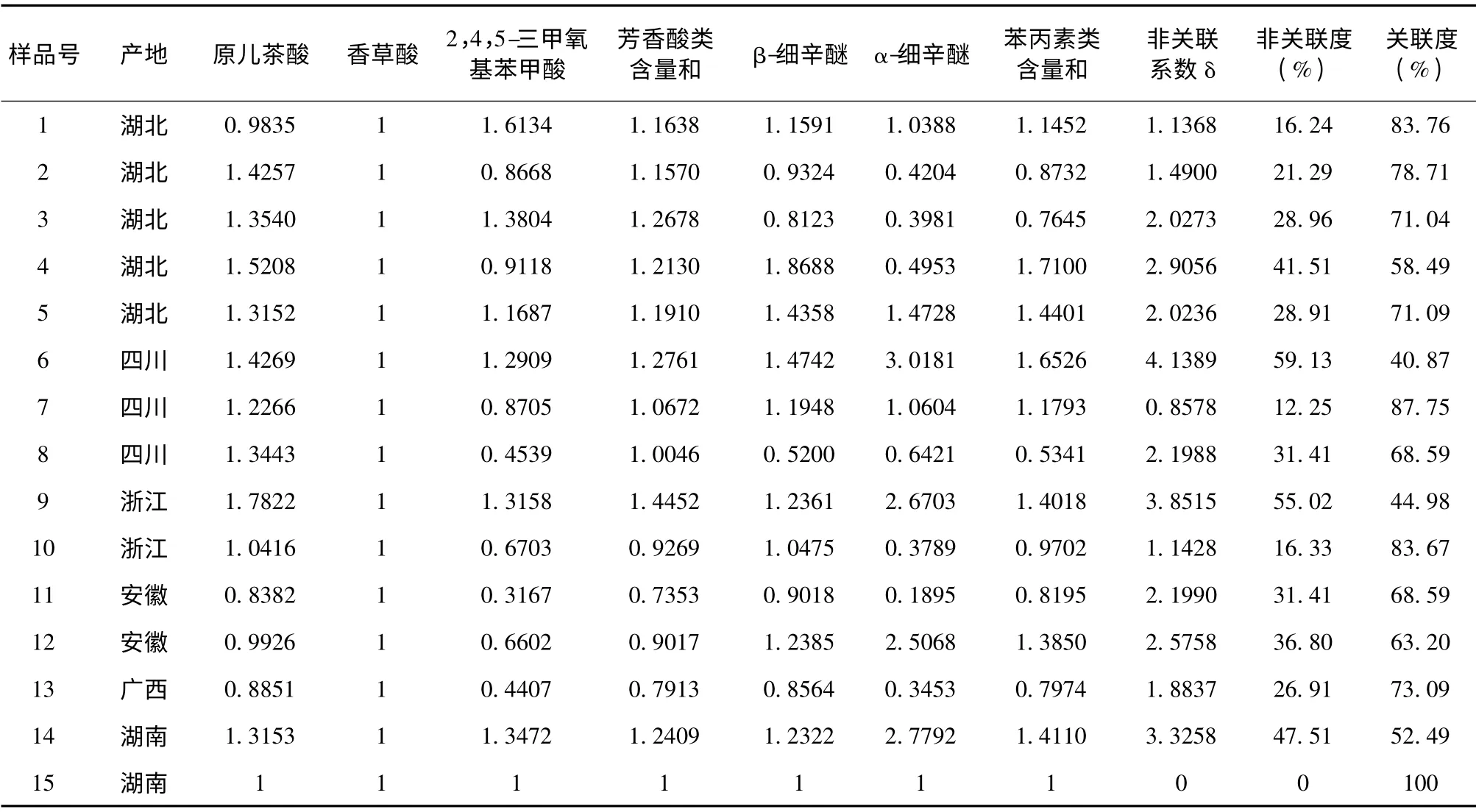
表5 15 个石菖蒲饮片样品关联度表征

图2 15 个石菖蒲饮片中各有效指标性成分含量相对比值与基准饮片样品15 对应成分含量相对比值的比值
3 结论
本文基于药物体系质量评价模式,对石菖蒲进行质量表征及关联分析研究,确定出样品1、6、9、12、14 有效指标性成分含量总体高于基准样品15,样品7 有效指标性成分含量与基准样品15 接近。其中样品7、1、10 与基准样品15 关联性最高,综合评价得出样品1 及样品7 质量优良度居前,其次为样品6、9、12、14、10。
中药饮片质量与其所含有效化学成分类型及存在的量、组成比例等有关。本文在自然药学观相关理论的指导下,基于药物体系组成成分的发现,运用有关中药质量评价模式,对15 个石菖蒲饮片样品质量进行表征,并以具有确切药效的样品15 为基准,进行质量关联度分析比较,综合精准评价出石菖蒲饮片质量的优良度。即综合考量了石菖蒲应用有效性及质量关联性,从而为石菖蒲资源筛选及其药物的原料质量控制及应用提供了依据,亦为中药药材及其饮片的质量评价提供了研究借鉴。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:85.
[2]董玉.石菖蒲有效物质基础研究[D].北京:北京中医药大学,2007.
[3]岳贵娟.降香化学表征与石菖蒲有效部位配伍药效研究[D].北京:北京中医药大学,2011.
[4]董玉,石任兵,刘斌.石菖蒲化学成分的研究(I)[J].北京中医药大学学报,2007,30(1):61-63.
[5]董玉,石任兵,刘斌.石菖蒲有效部位中一对苯丙素异构体galgravin 和veraguensin 的含量测定[J].北京中医药大学学报,2008,31(3):196-198.
[6]董玉,石任兵,刘斌.石菖蒲有效部位中α-细辛醚、β-细辛醚的含量测定[J].北京中医药大学学报,2007,30(5):340-342.
[7]石任兵.一种具有抗痴呆作用的中药提取物及其制备方法:中国,201110053682.9[P].2011-03-07.
[8]石任兵.一种抗抑郁的药物组合物及其制备方法:中国,ZL02153313.X[P].2002-11-27.
[9]石任兵,王永炎,姜艳艳,等.论中药化学发展近况[J].北京中医药大学报,2012,35(3):153-159.
[10]石任兵,王永炎.自然药学观的相关性思考[J].北京中医药大学学报,2012,35(4):221-225.
[11]梅莹莹,许舒娅,左胜,等.基于药物体系的连翘饮药物制备物质量表征分析研究[J].北京中医药大学学报,2014,37(5):338-343.
[12]左胜,孙雅姝,石任兵,等.基于药物体系的藁本质量评价研究[J].北京中医药大学学报,2014,37(7):481-485.
[13]戴莹.开心散药物体系表征研究[D].北京:北京中医药大学,2013.
