正常大鼠体内女贞子红景天苷制备物药代动力学表征研究
2015-04-21彭平赵丽敏刘斌姜艳艳冯朵孙道涵杨书娟朱乃亮石任兵
彭平 赵丽敏 刘斌 姜艳艳 冯朵 孙道涵 杨书娟 朱乃亮 石任兵
红景天苷为中药红景天特性功效成分。现代药理学研究表明,红景天苷及其苷元酪醇均具有抗炎、抗肿瘤、保护心脑血管及其它脏器等作用[1-3]。为了解决基于红景天苷的药物开发资源问题,本课题组研究建立了基于碱转化大孔吸附树脂分离富集,由女贞子制备红景天苷系列制备物的工艺方法与质量控制体系,经放大验证工艺经济稳定简便可行[4-9],从而为基于红景天苷的药物创新提供了药原支撑。目前已报道了诸多体内外红景天苷的含量测定方法,但对其代谢产物酪醇含量的同时测定方法只有超高效液相色谱-串联质谱(UPLC-MS/MS)[10-11],使得分析条件因仪器昂贵而受到一定的限制,鉴于此,笔者建立UPLC-PDA 同时测定制备物红景天苷及酪醇体内外含量的分析方法,并成功应用于制备物质量控制与药物动力学表征及其类药特性的系统研究,在研究中发现了制备物、红景天苷与酪醇以及所构建的有关药物体系体内表征特性,体现出药物体系的三大基本特性:自然性、协同性、亲和性[12-13]。研究结果为深入系统进行制备物药物研究奠定了基础,同时亦为基于红景天苷的药物创新提供研究思路与分析方法学借鉴。
笔者拟陆续系统报道有关研究结果,本文首先报道所建立的UPLC-PDA 同时测定大鼠血清中制备物红景天苷及酪醇的含量分析方法,与应用于药代动力学表征及其类药特性的研究结果。
1 仪器与材料
1.1 仪器
Waters ACQUITY 超高效液相色谱仪,PDA 检测器,Empower 工作站,自动进样;Waters ACQUITY UPLC H-CLASS T3 色谱柱(50 mm ×2.1 mm,1.8 μm),METTLER TOLEDO XS204(METTLER TOLEDO,瑞士),METTLER TOLEDO XP26(METTLER TOLEDO,瑞士),sigma 1-14 小型台式离心机(sigma,德国),Labconco ® CentriVap 离心浓缩仪(LABCONCO,美国),涡旋混合器(其林贝尔,中国),0.2 μm 微孔滤器。
1.2 药品与试剂
红景天苷对照品(北京方程生物科技有限公司,批号130426;含量99.9%)、水杨苷对照品(北京方程生物科技有限公司,生产批号121118;含量99.9%)、酪醇对照品(北京方程生物科技有限公司,批号120927;含量99.9%)、高氯酸(分析纯,天津市鑫源化工有限公司)、色谱乙腈(色谱纯,Fisher公司)、哇哈哈纯净水。
女贞子红景天苷制备物:取女贞子药材(浙江产地)70%乙醇提取,经碱转化后,大孔树脂分离富集制备而得。(批次:20130926,由课题组制备,样品经高效液相色谱法测定,红景天苷含量64.5%,酪醇含量0.2%),
1.3 实验动物
健康Sprague-Dawley(SD),雌性,大鼠,体质量200 ~220 g,由北京维通利华实验动物技术有限公司提供,许可证编号:SCXK(京)2012-0001。
2 方法
2.1 女贞子红景天苷制备物给药方案与样品采集
采用单次正常大鼠口服灌胃100 mg/kg 制备物(样品中红景天苷含量64.5%,酪醇含量0.2%),并于给药后2 分钟、5 分钟、10 分钟、15 分钟、30 分钟、45 分钟、1 小时、1.5 小时、2 小时、3 小时、4 小时、8 小时、12 小时、24 小时时间点(每时间点5 只大鼠)腹主动脉取血,每次5 mL,4000 r/min 离心10 分钟,分离血清,即为含药血清,于-80℃保存备用。
2.2 血样处理方法
取300 μL 含药血清,置于2 mL 离心管内,准确加入50 μL 质量浓度为100 μg/mL 的内标水杨苷溶液,涡旋30 秒,加0.4 mol/mL 高氯酸180 μL,涡旋30 秒,静置15 分钟,14800 r/min 高速离心15 分钟,取上清液200 μL 加1 μL 50%NaOH 调pH 到6 ~7,过0.22 μm 微孔滤器,供UPLC-PDA 检测分析。
2.3 体内分析方法建立及液相色谱条件及系统适用性
2.3.1 对照品溶液的配制 精密称取红景天苷、酪醇、水杨苷对照品各10 mg,分别置于10 mL 容量瓶中用流动相溶解并定容至10 mL,得质量浓度均为1 mg/mL的母液,用时用流动相稀释至所需浓度。
Waters ACQUITY 超高效液相色谱仪,PDA 检测器,Empower 工作站,ACQUITY UPLC H-CLASS T3色谱柱(50 mm ×2.1 mm,1.8 μm);流动相:乙腈-水(3 ︰97),流速为0.3 mL/min;柱温为25℃;进样体积为10 μL,检测波长276 nm。
血清中杂质对成分测定无干扰,且红景天苷、酪醇和水杨苷分离效果良好,具有较好的专属性,分析条件可行,色谱图见图1。

图1 空白血清和含药血清UPLC 色谱对比图
2.3.2 线性关系与灵敏度考察 取空白血清加入红景天苷和酪醇混合对照品溶液,配制成红景天苷浓度分别为1、5、10、25、50、100、200 μg/mL,酪醇浓度分别为0.5、1、5、10、25、50、100 μg/mL 的血清样品,按血样处理方法处理并测定,以红景天苷或酪醇与内标浓度比(X)为横坐标,红景天苷或酪醇与内标峰面积之比(Y)为纵坐标绘制标准曲线。红景天苷体内浓度回归方程为:Y =1.1958X-0.1421,R=0.9996(n=7),线性范围为1 ~200 μg/mL,酪醇体内浓度回归方程为:Y =2.6114X-0.0323,R =0.9996(n =7),线性范围为0.5 ~100 μg/mL。配制已知浓度的红景天苷、酪醇对照品溶液测得方法最低检测限(S/N =3)分别为0.5 μg/mL、0.25 μg/mL,最低定量限(S/N = 10)分别为1 μg/mL、0.5 μg/mL。
2.3.3 回收率与精密度考察 取空白血清加入红景天苷和酪醇混合对照品溶液配制成低、中、高浓度血清样品(红景天苷质量浓度分别为5、25、100 μg/mL,酪醇质量浓度分别为1、10、50 μg/mL)各5 份,按血清处理方法处理测定,每一浓度进行5份样本分析,连续测定3 天,根据标准曲线计算相对回收率(n=5)、绝对回收率(n =5)、日内RSD(n =5)和日间RSD(n=3),见表1。

表1 红景天苷及酪醇体内含量测定回收率与精密度考察结果
2.3.4 稳定性考察 取空白血清加入红景天苷和酪醇混合对照品溶液,配制成低、中、高浓度的血清样品(红景天苷质量浓度分别为5、25、100 μg/mL,酪醇质量浓度分别为1、10、50 μg/mL)各3 份,一份于常温(24℃)放置24 小时(测定时间为放置0、4、8、12、24 小时),一份于-20 ℃放置30 天(测定时间为放置1、8、15、22、30 天),一份于-80 ℃反复冻融5 次(测定时间为冻融次数1、2、3、4、5),于相应测定时间测定各血样中红景天苷和酪醇的浓度。结果表明红景天苷和酪醇在-20℃放置及反复冻融条件下稳定性较好,见表2。

表2 红景天苷及酪醇体内含量测定稳定性考察结果(n=5)
3 结果
3.1 血药浓度测定结果
取各组血清样品制备测定,并计算口服制备物各时间点红景天苷血药浓度,结果见表3。在制备物血药浓度检测中,于0.5 小时、0.75 小时、1 小时时间点可检测到酪醇的吸收峰,并计算血药浓度分别约为0.30 ± 0.03 μg/mL、0.32 ± 0.04 μg/mL、0.21 ±0.03 μg/mL。
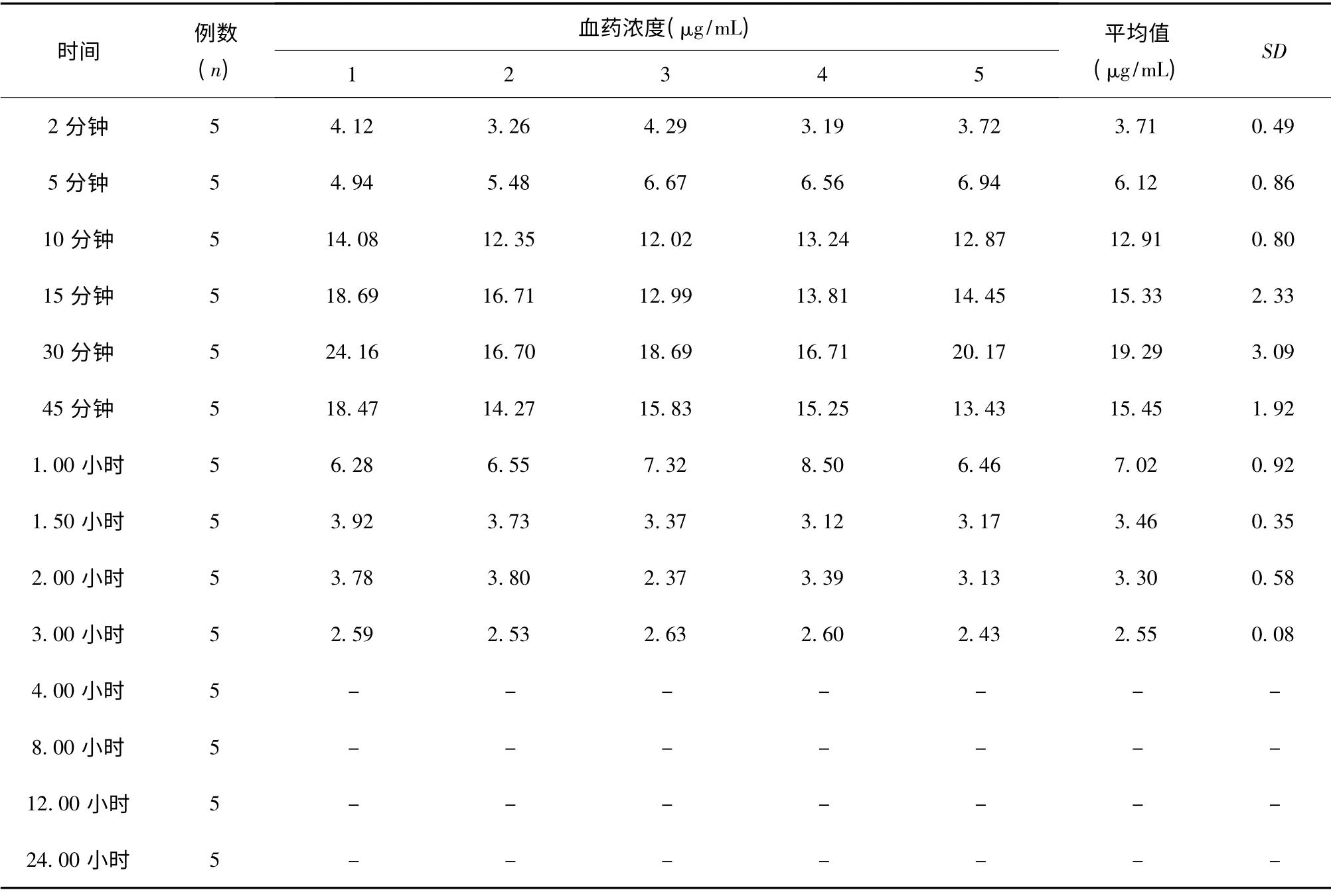
表3 红景天苷制备物给药后不同时间点红景天苷的血药浓度(μg/mL)
3.2 药代动力学表征分析
采用生物学统计软件PKSolver 计算得红景天苷制备物大鼠体内主要成分红景天苷的药代动力学参数,见表4,其体内动态变化药时曲线见图2。

表4 制备物红景天苷大鼠体内药代动力学参数

图2 制备物红景天苷大鼠体内药-时曲线
3.3 红景天苷及酪醇体内外含量相对比值分析
以红景天苷含量为参比,计算体内外制备物中成分酪醇含量与红景天苷含量比值,即体外制备物成分含量比值为:酪醇︰红景天苷;体内成分血药浓度比值为:酪醇︰红景天苷,结果见表5。

表5 体内外制备物红景天苷与酪醇动态含量比值
结果显示,以红景天苷含量为参比,酪醇与红景天苷含量比值排序为:制备物体外<体内0.5 小时<体内0.75 小时<体内1 小时;在大鼠体内酪醇与红景天苷含量比值较制备物增大了5.03 ~9.65倍,且从给药后0.5 小时到1 小时持续了0.5 小时的增量动态变化。
4 讨论
本研究建立了UPLC-PDA 同时测定大鼠血清中红景天苷及酪醇的含量分析方法,并成功应用于女贞子红景天苷制备物药代动力学表征及其类药特性研究。研究发现女贞子红景天苷制备物在正常大鼠体内类药成分主要以红景天苷原型存在,其药代动力学表征为:吸收快、生物利用度较高;而酪醇表征为体内最大血药浓度出现相对滞后,且与红景天苷的血药浓度比值较制备物成分含量比值呈明显增高,并与红景天苷具有部分共血药与协同吸收时间。因此,酪醇的体内表征及其来源是制备物中的微量酪醇在体内以原型存在?还是制备物中红景天苷由机体“有意”所为的代谢产物,而与红景天苷构成药物体系,从而对其药物属性特性产生协同性?这引起课题组的高度关注,并系统探究其原委,揭示出其药物体系基本表征特性。以制备物及其在正常大鼠体内红景天苷及酪醇含量、含量比值动态变化与药代动力学表征关联分析,揭示了女贞子红景天苷制备物类药特性,为对其进行深入创新药物研究奠定了基础,同时亦为有关药物研究提供了思考以及技术与方法学支撑。
正常状态下大鼠女贞子红景天苷制备物体内药代动力学表征研究结果发现,大鼠体内可同时存在红景天苷和酪醇成分,但酪醇成分血药浓度在正常状态下仅达到检测限,但在课题组系统研究中发现,在有关病理模型状态下大鼠体内酪醇成分血药浓度明显增高,高出最低定量限,并应用本分析方法成功研究了女贞子红景天苷制备物的有关药物体系及其药物属性与特性,有关实验结果将进一步报道。
[1]张明发,沈雅琴.红景天苷及其苷元酪醇的抗炎、抗肿瘤和免疫调节作用[J].药物评价研究,2013,36(3):228-234.
[2]张明发,沈雅琴.红景天苷及其苷元酪醇的心血管保护作用[J].中国新药杂志,2012,21:2521-2525.
[3]谢卉,朱大会.红景天苷对神经系统疾病药理作用的研究进展[J].中国中药杂志,2012,37(17):2505-2509.
[4]周文娟,石任兵.女贞子有效部位制备工艺及其质量控制方法研究[D].北京:北京中医药大学,2008.
[5]石任兵,周文娟,田恒康,等.一种从女贞子中制备高纯度红景天苷的方法:中国,CN101279992[P].2008-10-08.
[6]李娟,石任兵.基于碱转化的女贞子红景天苷部位及其单一成分的制备与质量标准研究[D].北京:北京中医药大学,2011.
[7]石任兵,姜艳艳,李娟.一种从女贞子中制备红景天苷的新方法:中国,CN102321127A[P].2012-01-18.
[8]彭晓敏,石任兵.基于碱转化的女贞子中红景天苷制备工艺及其质量标准研究[D].北京:北京中医药大学,2012.
[9]石任兵,彭平,姜艳艳,等.一种从女贞子中制备系列纯度红景天苷的方法:中国,CN103351415A[P].2013-10-16.
[10]郭娜.红景天苷及其代谢产物酪醇在大鼠体内的药物代谢动力学研究[D].哈尔滨:东北林业大学,2012.
[11]吴趋凡,李耿,符崖.LC-MS/MS 同时测定大鼠血浆中红景天苷和酪醇及其药物动力学研究[J].中药新药与临床药理,2013,(2):169-172.
[12]石任兵,王永炎.自然药学观的相关性思考[J].北京中医药大学学报,2012,35(4):221-225.
[13]石任兵,王永炎,姜艳艳,等.论中药化学发展近况[J].北京中医药大学学报,2012,35(3):3-159.
