碘乳康口服溶液微生物限度检查方法学验证
2015-04-07张广求刘文田祥学
张广求刘文田祥学
(1黄冈市中心医院药剂科,湖北 黄冈 438000;2黄冈市食品药品监督检验中心)
碘乳康口服溶液微生物限度检查方法学验证
张广求1刘文1田祥学2
(1黄冈市中心医院药剂科,湖北 黄冈 438000;2黄冈市食品药品监督检验中心)
目的:建立碘乳康口服溶液的微生物限度检查方法。方法:按《中华人民共和国药典》2010年版二部附录微生物限度检查法,进行碘乳康口服溶液的细菌、霉菌、酵母菌及控制菌检查方法验证,各进行3次独立的平行试验,分别计算各试验菌的回收率。结果:采用常规法对5种阳性对照菌株进行测定,金黄色葡萄球菌、大肠埃希菌、枯草芽孢杆菌、白色念珠菌和黑曲霉的回收率均小于70%;采用培养基稀释法(0.5 mL/皿),5种阳性对照菌株的回收率均大于70%;控制菌大肠埃希菌采用常规法可检出。结论:碘乳康口服溶液的微生物限度检查中,细菌、霉菌及酵母菌计数可采用培养基稀释法(0.5 mL/皿),大肠埃希菌检查采用常规法。
碘乳康口服溶液;微生物限度;方法学验证试验;回收率
微生物限度检查是药品安全性检查的重要组成部分,《中华人民共和国药典》2010年版规定,当建立药品的微生物限度检查方法时,应进行方法学验证[1]。碘乳康口服溶液是黄冈市中心医院的自制制剂(批准文号:鄂药制字H20110227),主要由碘、碘化钾组成,用于乳腺增生症,安全性好,临床疗效显著。由于碘具强有力的消毒防腐作用,能杀死细菌、霉菌、病毒[2],文献[3]亦证实碘注射液中的碘有抑菌作用,为保证制剂质量,本研究参考有关文献[4-6],并进行多次试验,建立了适合该制剂的微生物限度检查方法,保证了方法的科学性和检验结果的准确可靠。现报道如下。
1 仪器与试药
1.1 仪器
SZK202净化工作台(蚌埠净化设备厂);YC-875S医用净化工作台(苏州净化设备厂);高压蒸汽灭菌器(上海三申医疗器械有限公司);KWY-100型电热干燥箱(武汉市武昌实验仪器厂);DG-1多功能恒温箱(上海医疗器械修理厂);HHB11420电热恒温培养箱(湖北省黄石市医疗器械厂);XK97-A菌落计数器(江苏省姜堰市新康仪器厂);ZF-1型三用紫外分析仪(上海顾村电光仪器厂)。
1.2 试验菌株
金黄色葡萄球菌CMCC(B)26003,大肠埃希菌CMCC(B)44102,枯草芽孢杆菌CMCC(B)63501,白色念珠菌CMCC(F)98001,黑曲霉CMCC(F) 98003均为第0代冷冻保藏菌株,购自湖北省食品药品监督检验研究院。
1.3 培养基
营养琼脂培养基、改良马丁培养基、营养肉汤培养基、玫瑰红钠琼脂培养基均由北京三药科技开发公司生产;改良马丁琼脂培养基、4-甲基伞形酮葡糖苷酸培养基(MUG)均由北京奥博星生物技术有限责任公司生产;蛋白胨、胆盐乳糖培养基均由武汉市天益生化试剂有限公司生产。以上培养基的适用性检查均符合《中华人民共和国药典》2010年版规定,可用于微生物限度检查。
1.4 试药、试液、稀释液、样品
氯化钠(中盐宏博集团云梦云虹制药有限公司,批号:20130710);0.9%无菌氯化钠溶液、pH 7.0无菌氯化钠-蛋白胨缓冲液、靛基质试液(均按《中华人民共和国药典》方法配制[1]);碘乳康口服溶液(批号:141012,141121,150129,黄冈市中心医院自制)。
2 方法与结果
2.1 供试液的制备
取样品2瓶共10 mL,加pH 7.0无菌氯化钠-蛋白胨缓冲液(稀释液)至100 mL,摇匀,制成1∶10的供试液,备用。
2.2 阳性对照菌液的制备
取经35℃培养18~ 24 h的金黄色葡萄球菌、大肠埃希菌、枯草芽孢杆菌的营养肉汤培养物各1 mL,分别加0.9%无菌氯化钠溶液9 mL,按10倍稀释法稀释至含菌数为50~ 100 cfu/mL的菌悬液,作活菌计数备用。
取经25℃培养24 h的白色念珠菌改良马丁培养物1 mL,加0.9%无菌氯化钠溶液9 mL,按10倍稀释法稀释至含菌数为50~ 100 cfu/mL的菌悬液,作活菌计数备用。
取经25℃培养7 d的黑曲霉改良马丁琼脂斜面培养物,加0.9%无菌氯化钠溶液5 mL,将孢子洗脱,用管口带有薄无菌脱脂棉的无菌毛细吸管,吸取孢子悬液至无菌试管内,用0.9%无菌氯化钠溶液稀释至含孢子数为50~ 100 cfu/mL的孢子悬液,作活菌计数备用。
各菌悬液均采用平皿计数法测定活菌数,每株试验菌平行制备2个平皿,结果见表1。
验证细菌、霉菌及酵母菌计数法时,加菌量为50~ 100 cfu;验证控制菌检查法时,加菌量为10~ 100 cfu。
2.3 细菌、霉菌及酵母菌计数方法的建立和验证
2.3.1 回收率测定
2.3.1.1 试验组 ①常规法:取供试液1 mL和含50~ 100 cfu试验菌的菌悬液,注入同一平皿中,立即倾注约15 mL温度不超过45℃的溶化的营养琼脂培养基或玫瑰红钠琼脂培养基,每株试验菌平行制备2个平板,凝固后倒置,按规定温度培养,细菌培养24~ 48 h,霉菌及酵母菌培养48~72 h,观察结果,点计菌落数。②培养基稀释法:取供试液,采用0.2 mL/皿和0.5 mL/皿法,再加入各试验菌50~ 100 cfu,其余操作同常规法。
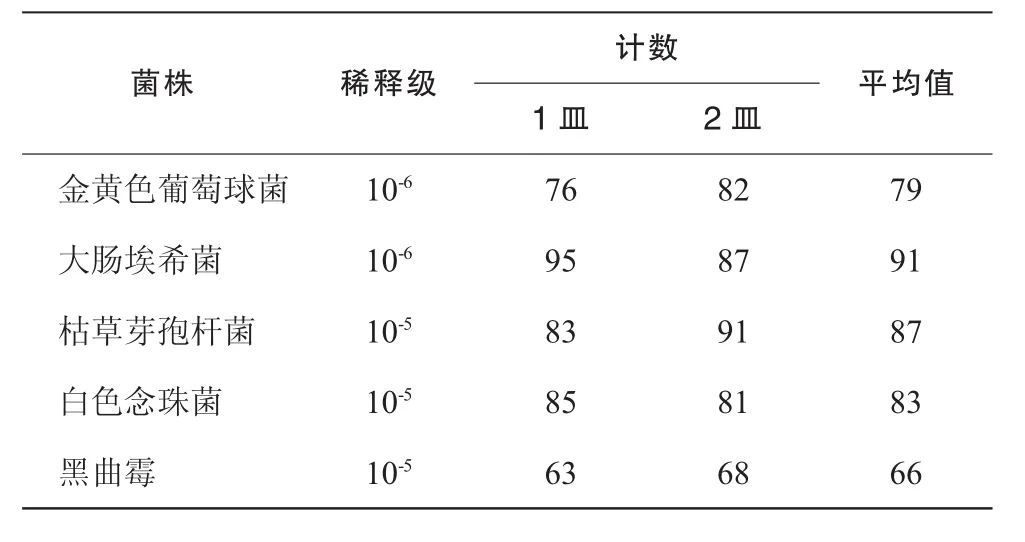
表1 细菌、霉菌及酵母菌计数结果 (cfu/mL)
2.3.1.2 菌液组 分别取各试验菌50~ 100 cfu注入平皿中,注入相应培养基,每株试验菌平行制备2个平板,培养,点计菌落数,以测定每一菌株加入的试验菌数。
2.3.1.3 样品对照组 除不加菌液外,其余操作同试验组,以测定样品的本底菌数。
2.3.1.4 稀释液对照组 除以稀释液代替供试液外,其余操作同试验组,以考察供试液制备过程中对微生物影响的程度。
2.3.1.5 回收率计算 各进行3次独立的平行试验,分别计算各试验菌每次试验的回收率。
试验组的菌回收率(%)=(试验组的平均菌落数 - 样品对照组的平均菌落数)/菌液组的平均菌落数 ×100%。
2.3.2 方法的确定
2.3.2.1 常规法 各试验菌回收率试验结果见表2。由表2可知,常规法各试验菌回收率均低于70%,即碘乳康口服溶液在该检验条件下,有不同程度的抑菌作用,不能采用常规法进行细菌、霉菌及酵母菌计数。
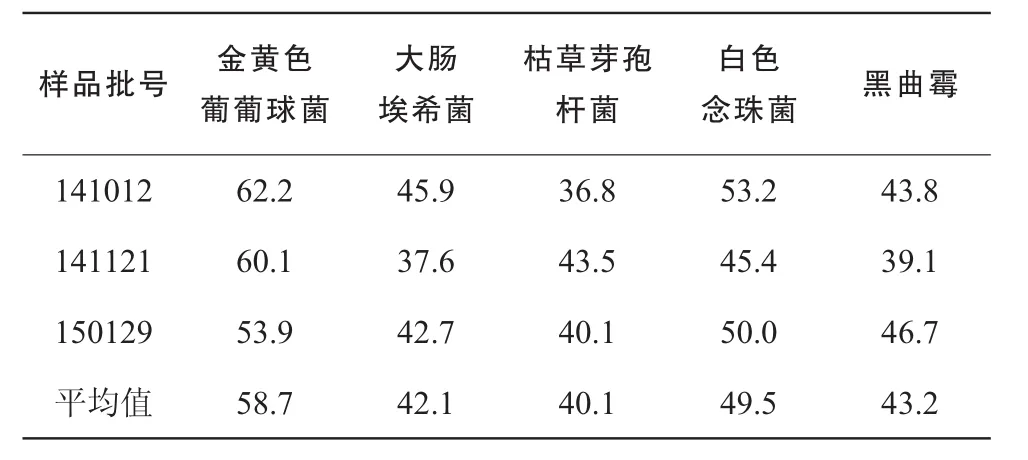
表2 常规法各试验菌回收率试验结果 (%)
2.3.2.2 培养基稀释法 0.2 mL/皿和0.5 mL/皿法各试验菌的回收率试验结果见表3。由表3可见,上述5种试验菌的菌回收率 0.2 mL/皿和0.5 mL/皿法均大于70%,且0.2 mL/皿和0.5 mL/皿法的测定结果基本一致。培养基稀释法中的0.5 mL/皿即可消除样品的抑菌活性,为减少测定误差,将0.5 mL/皿法作为样品的细菌计数方法,经方法学验证试验成立。
2.4 控制菌检查方法的验证
2.4.1 菌株选择碘乳康口服溶液为化学药口服液体制剂,按照《中华人民共和国药典》2010年版[1]附录微生物限度检查法中的有关控制菌检查方法,应检查大肠埃希菌,阴性对照菌为金黄色葡萄球菌。

表3 培养基稀释法各试验菌回收率试验结果 (%)
2.4.2 验证方法与结果取 100 mL胆盐乳糖培养基 6份,2份分别加入10 mL供试液及 1 mL 10~ 100 cfu/mL大肠埃希菌菌悬液,作为试验组;2份分别加入 10 mL供试液及 1 mL 10~100 cfu/mL金黄色葡萄球菌菌悬液,作为阴性菌对照组,以验证大肠埃希菌检查方法的专属性;2份分别加入稀释剂10 mL,作为阴性对照组,置35℃培养24 h。取上述培养物0.2 mL,接种至含MUG培养基5 mL的试管中培养,于5,24 h在366 nm波长紫外光下观察有无荧光反应。沿培养管的管壁加入靛基质试液数滴,观察液面是否呈玫瑰红色,结果见表4。

表4 控制菌检查法验证结果
试验结果显示,试验组3批样品均检出大肠埃希菌,阴性对照菌金黄色葡萄球菌均未检出。表明样品的控制菌检查方法按常规法,经方法学验证试验成立。
2.5 3批样品的微生物限度和控制菌检查
根据方法学验证试验结果,碘乳康口服溶液的微生物限度检查法可采用下列方法:细菌、霉菌及酵母菌计数可采用培养基稀释法(0.5 mL/皿),大肠埃希菌检查采用常规法。3批样品的微生物限度检查结果见表5。
3 讨论
3.1 碘乳康口服溶液有一定程度的抑菌作用,常规法无法真实反映溶液被污染的情况。采用培养基稀释法(0.5 mL/皿),碘在平皿中的浓度只有5.67×10-6g/mL,能较好地消除抑菌成分碘的干扰,试验菌株的回收率均符合要求。培养基稀释法可稀释药品中的抑菌成分,减少其对细菌、霉菌及酵母菌生长的影响,较其他方法简便、经济,但该法仅限于有弱抑菌作用的药品,不适用于含较强抑菌作用药品的微生物限度检查。笔者曾采用薄膜过滤法,也获得较理想的结果,但薄膜过滤法操作较繁琐、费时。对于抑菌作用较强的药品的微生物限度检查,薄膜过滤法是一种检出率较高、结果较准确可靠的方法[8]。
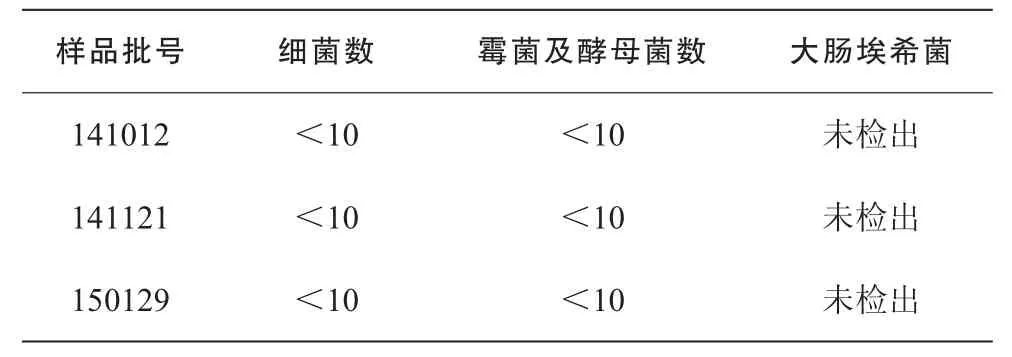
表5 3批样品微生物限度检查结果 (cfu/mL)
3.2 制备阳性对照菌液的含菌数应控制在 50~100 cfu,过多或过少时,回收率测定结果会产生较大的误差。供试液和阳性对照菌液分别注入平皿后,应立即倾入培养基混匀,试验时,最好两人配合操作。
[1] 国家药典委员会.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2010:附录107-116.
[2] 国家药典委员会.中华人民共和国药典临床用药须知(化学药和生物制品卷)[M].北京:人民卫生出版社,2005:859.
[3] 张广求.碘注射液无菌检查方法学验证[J].中国医院药学杂志,2010:30(2):165-166.
[4] 中国药品生物制品检定所.中国药品检验标准操作规程[M].北京:中国医药科技出版社,2010:351-407.
[5] 杜建红,张国庆,方晨,等.水合氯醛合剂微生物限度检查的验证[J].中国执业药师,2014:11(5):21-23.
[6] 张广求.十九味赤芍胶囊微生物限度检查方法的建立[J].医药导报,2009,28(8):1075-1076.
Methodology Validation of Microbial Limit Test for Dianrukang Oral Solution
Zhang Guangqiu1,Liu Wen1,Tian Xiangxue2(1 Pharmacy Department of Huanggang Central Hospital,Hubei Huanggang 438000,China;2 The Center for Food and Drug Control of Huanggang City)
Objective:To establish the method of microbial limit test for dianrukang oral solution.Methods:According to the method of microbial limit test set forth in the Volume II Appendix of China Pharmacopoeia(2010 edition),the test method validations were carried out for bacteria,mold,yeast and the control bacteria for dianrukang oral solution.For each test three parallel experiments were performed independently and the recovery rate of each tested organism was calculated.Results:Using the conventional method for the tests of five kinds of positive control strains,the recovery rates of Staphylococcus aureus,Escherichia coli,Bacillus subtilis,Candida albicans and Aspergillus niger were all less than 70%,using medium dilution method (0.5 mL/plate),the recovery rates of the above mentioned strains were all greater than 70%,and the control bacteria of Escherichia coli can be detected by conventional method.Conclusion:In the microbial limit test of dianrukang oral solution,culture medium dilution method (0.5 mL/plate)can be used for bacteria,mold and yeast counting and the conventional method can be used for the test of Escherichia coli.
Dianrukang Oral Solution;Microbial Limit;Methodology Validation Test;Recovery Rate
10.3969/j.issn.1672-5433.2015.08.003
2015-04-23)
张广求,男,副主任药师。研究方向:医院药学、药物分析。通讯作者E-mail:ccnpa@163.com
