对食盐水中生铁锈蚀问题的探讨
2015-04-01郑梅花张祁帆
郑梅花+张祁帆
摘要:通过实证方式,探讨了生铁在食盐水中的锈蚀问题,指出生铁的腐蚀和生锈是两个不同的概念。当生铁发生电化学腐蚀(如氧浓差腐蚀)时,生锈与腐蚀的发生部位可能并不一致,常会有水线腐蚀现象,即铁锈生成集中于水线附近,腐蚀主要发生在溶液深处。
关键词:生锈;电化学腐蚀;氧浓差腐蚀;水线腐蚀;实验探究
文章编号:1005–6629(2015)3–0040–04 中图分类号:G633.8 文献标识码:B
1 问题背景
鲁科版《化学反应原理(选修)》教材指出,钢铁中含有可充当正极材料的碳等杂质,在通常情况下暴露于潮湿空气中,表面会附上一层酸性不强的水膜,继而在表面杂质附近形成微小的原电池而腐蚀(吸氧腐蚀)。为了让学生获得感性体验,促进对电化学腐蚀原理的理解,笔者在教学时补充了盐水滴实验[1]。具体操作及现象为:将NaCl和酚酞的混合液滴在一块光亮清洁的铁板表面上,1~2min后即可看到在液滴外沿形成了清晰的红色环(a)(如图1所示)。但直接观察液滴覆盖的中心区(b)生铁被腐蚀而变暗的现象并不明显。
负极铁溶解现象不明显是否是由腐蚀时间较短所致呢?笔者将实验后的铁片继续放置,最先在a区域观察到浅褐色锈环,最后锈点布满整个液滴覆盖区域,负极(b区域)腐蚀仍不明显。对此,有学生认为可能是电解质溶液用量过少导致,继而提议通过将铁片部分浸泡于食盐水中的方式改进实验。基于这样的思考,课后笔者组织他们成立兴趣小组,一起通过实验探索、文献查阅等手段对生铁在食盐水中的锈蚀问题作了进一步探究,得到了一些意料之外的收获。
2 实验过程
实验1 截取15cm×1cm、厚度1mm的光亮生铁片,依次用Na2CO3溶液、蒸馏水洗净表面油污。选择18mm×180mm规格(以外径×长度表示)的试管,并加入约2/3试管高度的2%的食盐水。然后用细棉线将火柴梗和生铁片一端系上并使火柴梗架于试管口,按图2使铁片悬挂于试管中,其中2/3浸于溶液,并在自然通风环境中敞口、静置。1h后在水线附近(即图2中a区域)最先出现少量红褐色的锈迹。放置过夜,a区域已有大量明显铁锈,而区域b呈灰黑色、无金属光泽。3天后,锈蚀程度加剧,并有部分铁锈沉底,但b处无铁锈,露于空气中部分也仍无明显变化;取出铁片,擦去表面附着物,水线以下部分变薄(尤其以b区域附近为甚)。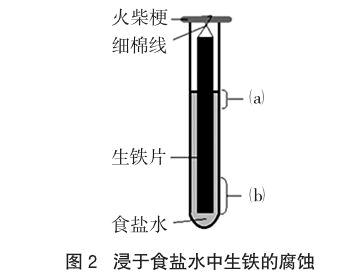
若将试管中的食盐水更换为蒸馏水,重复上述实验,结果与实验1同,但由于溶液导电性差、无Cl-促进效应等,铁片腐蚀速度要慢很多(一般需要10天以上)。
可见,无论是生铁片浸泡于食盐水还是蒸馏水中,都是水线附近锈迹斑斑,但内层铁厚度较初始却并未明显改变,而铁片在溶液深处b区域部分虽无锈迹却因严重电化学腐蚀而显著变薄,即铁片生锈位置与生铁腐蚀溶解位置不一致。
实验2 按实验1截取并洗涤两块同样大小的光亮的生铁片,其中一块作对照。将另一块平放于培养皿中,加入适量2%的食盐水浸没生铁片,然后在自然通风环境中敞口、静置。约3h后整块铁片表面上均匀出现少量红色点状锈迹,放置过夜红褐色锈斑愈加明显。7天后,取出铁片,除去表面附着物并对照,厚度变薄。
实验说明,生铁片各部位都发生明显锈蚀,锈蚀程度几乎一致,并未出现实验1中生锈和腐蚀位置不吻合的状况。
实验3 按实验1操作截取并洗涤同样大小的一块光亮生铁片。取一两通管,一端配单孔橡胶塞并插上约3cm长导管(预先充满含KCl的琼脂,作盐桥)及生铁片(露出胶塞部分上下大致相等),然后按图3组装实验装置。向两通管和烧杯中各加入适量2%食盐水至没过生铁片,将水族箱增氧泵的塑料软管插入两通管深处,通过调节阀向食盐水匀速鼓入空气。自然通风环境中敞口、静置30min,各取两通管和烧杯中食盐水少许(记为溶液A、B),分别用酚酞、K3[Fe(CN)6]溶液检验,结果见表1。继续通空气2h,取出铁片,其中浸于烧杯一端的铁片与另一端比较明显变薄,但均无铁锈。若改用增氧泵向烧杯中食盐水鼓气,重复以上操作,最终现象相同,但现象位置恰好相反。
实验表明,持续通入空气一端O2得电子生成OH-,电解质溶液显碱性,是原电池的正极区;而未通空气一端的铁片作负极,氧化腐蚀生成Fe2+。可见,电解质溶液中氧气浓度的差异会影响铁片两段的电化学腐蚀。
3 理论探讨
从热力学观点看,绝大多数的金属都具有与周围介质发生作用而转入氧化(离子)状态的倾向(即发生腐蚀)。金属腐蚀是指金属与周围环境发生化学、电化学反应和物理作用引起的变质和破坏现象,一般分为化学腐蚀与电化学腐蚀,其本质都是金属原子失去电子被氧化的过程。当金属与电解质溶液接触时,由于电化学作用而引起的腐蚀叫做电化学腐蚀,通常分为析氢腐蚀和吸氧腐蚀,宏观上也可分为原电池腐蚀、接触腐蚀、浓差腐蚀(氧浓差腐蚀)等[2]。
3.1 氧浓差腐蚀简介
氧浓差腐蚀又称差异充气腐蚀,是由金属与含氧量不同的溶液接触而形成。当金属浸入含氧的溶液中时,氧的电极电位与氧分压有关,可表示为:
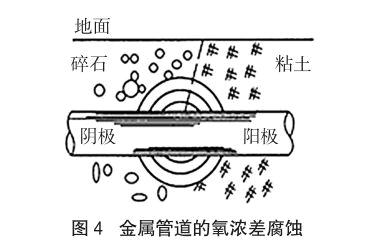
可见,如果各部位含氧量不同,存在浓差,O2浓度较小的部位处金属的电位较低,成为阳极而腐蚀;而O2浓度较大部位电位较高,成为电化学腐蚀的阴极。氧浓差腐蚀在生产生活中也常会遇到,如金属管道通过不同性质土壤时,黏土段(相较于碎石段)贫氧,易发生腐蚀,特别是在两种土壤的交接处的部位腐蚀最为严重(如图4)。此外,还有金属裂缝深处腐蚀,钉入木头的长铁钉、浸入水中的铁柱(闸)的腐蚀等等。
3.2 腐蚀和生锈是两个概念
生铁的电化学腐蚀机理与原电池原理相同,实际上是一种短路了的原电池。当它工作时,虽然也有电流产生,但其电能不能被利用,而是以热的形式散失掉,其工作的直接结果便是造成阳极铁的溶解(Fe-2e-→Fe2+),即铁发生腐蚀。生锈则是指铁锈的生成,即阳极氧化生成的Fe2+与溶液中的OH-作用生成Fe(OH)2,继而进一步被氧气氧化为Fe(OH)3,Fe(OH)3脱去一部分水生成Fe2O3·nH2O,它就是铁锈的主要成分。
可见,生铁的腐蚀和生锈是两个不同的概念[3]。当生铁发生腐蚀时不一定会生锈(如实验3),而若生锈,其发生部位与腐蚀位置可能也不一致(如实验1)。
3.3 水线附近生铁生锈最严重
部分浸于食盐水的生铁片,为什么邻近水线区域生锈最严重?文献[4]介绍,由于溶液上下氧的浓度不同,引起铁表面pH发生变化,进一步在水线附近铁的表面形成或加强了氧化膜;而c(O2)小的部分(图2中b区域)则即使原有的一点氧化膜也被溶解掉。两处铁的溶解已不再遵循同一动力学方程,引起两处阳极和阴极的电流密度不同,从而形成阳极区和阴极区,电子从c(O2)小处流向c(O2)大处,发生氧浓差腐蚀。
实验1溶液深处的铁发生阳极腐蚀生成Fe2+并向上扩散,水线附近的O2得电子不断与水作用生成OH-。OH-与从溶液深处扩散的Fe2+生成Fe(OH)2附于铁片表面,并与空气中O2继续反应转化为Fe(OH)3、铁锈。虽然水线附近的一些OH-也会向溶液深处扩散并与Fe2+生成Fe(OH)2,但溶液深处溶解氧少,难将Fe(OH)2氧化,且溶液内部处于湿润、运动状态,不利于铁锈附着,故浸入溶液中的铁片不易形成铁锈。因此,实验1生成铁锈集中于图2中a区域,腐蚀主要在b区域;而实验3未通空气(氧浓度小)一端阳极铁溶解,但因盐桥存在,Fe2+、OH-不直接接触就不生成铁锈。
至于实验2,平放于食盐水中的生铁片,各部位所处溶液深度相同、含氧量相等(或接近),无法形成典型的氧浓差电池,因而久置后的铁片表面锈斑分布均匀,无明显阴、阳极区。而盐水滴实验中,开始时液滴表面因氧的直接接触、溶解,使氧浓度较液滴中心区大,形成浓差电池而会快速出现红色环现象(生成OH-),但因水膜厚度小,短时间内水膜不同位置的氧浓度差就会消失,因此长时间放置不会出现锈、蚀部位不一致的情况。
4 教学反思
生铁的腐蚀和生锈是两个不同的电化学概念。实证表明,当生铁发生电化学腐蚀(如氧浓差腐蚀)时,生锈与腐蚀的发生部位不一定相同,常有水线腐蚀现象,即铁锈生成集中于水线附近,腐蚀主要发生在溶液深处。基于上述理解,反思我们教学中使用的部分习题,还需要同行全面审视,如题1(见附录)想当然地认为,选项A铁棒发生腐蚀时靠近底端的部分与氧气接触少,所以腐蚀程度轻;题2(2014年福建高考理综卷24题)中生成铁锈最多的区域为什么是B,而腐蚀最严重的为什么是C却不是D等,都值得我们进一步探讨、甄别。可见,教师对试题的研究不能仅浮于问题的表面,而要善于总结,勤于反思,乐于探究,积累经验。大胆质疑、小心论证,应该成为我们的惯用方式和教学常态。
附录
题1:下列与金属腐蚀有关的说法正确的是
A.图5-a中,插入海水中的铁棒,越靠近底端腐蚀越轻
B.图5-b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率增大
C.图5-c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图5-d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
参考答案:A
题2:图6是实验室研究海水对水闸不同部位腐蚀情况的剖面示意图。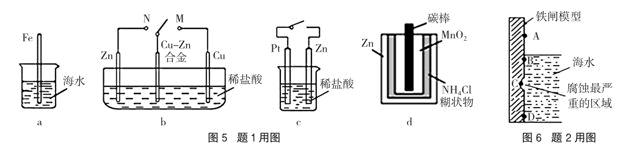
(1)该电化学腐蚀称为 ____ 。
(2)图中A、B、C、D四个区域,生成铁锈最多的是(填字母) __________ 。
参考答案:(1)吸氧腐蚀;(2)B
参考文献:
[1]王祖浩.普通高中化学课程标准实验教科书《实验化学》(选修)[M].南京:江苏教育出版社,2006:64.
[2][英] UR.艾万思著.华保定译.金属腐蚀与氧化(The Corrosion and Oxidation of Metals)[M].北京:机械工业出版社,1976:45~96.
[3]肖中荣.也说铁的腐蚀和生锈[J].中学化学教学参考,2011,(11):41~42.
[4]邹兰,李勤,魏振枢.差异充气腐蚀产生机理的探讨[J].周口师范高等专科学校学报,1999,(9):33~35.
