羟基-碳纳米管气体传感器气敏性的仿真研究*
2015-03-30房家骅谭秋林刘文怡
房家骅,谭秋林,,刘文怡,,李 超
(1.中北大学 电子测试技术国家重点实验室,山西 太原030051;2.中北大学 仪器科学与动态测试教育部重点实验室,山西 太原030051)
0 引 言
气体传感器已广泛应用于环境安全、食品安全、工厂废气的检测当中。传统的金属氧化物气体传感器已经趋于成熟[1],新气敏材料的研究成为热门课题[2]。碳纳米管作为一种纳米材料已经被广泛应用在各种领域,由于其镂空的管状结构使其具有足够大的表面积可以和气体充分接触,这些独特的物理结构使它成为新型气敏膜的理想材料之一[3~5]。已有相关文献研究表明,碳纳米管气体传感器在灵敏度和工作温度上都要优于传统的金属氧化物传感器,尤其是采用混酸对碳纳米管进行化学改性,即清除了碳纳米管在制备过程中引入的杂质,又对其进行化学切割,使团簇现象消失,长链变成短链进一步地增大表面积,并在其断口处和表面引入一些活性基团(—OH 等基团)[6,7],大大增强了碳纳米管的气敏性。
本文通过建立与实际相符的物理模型,利用密度泛函理论[8,9],以羟基修饰过的单壁碳纳米管(SWCNT—OH)与本征单壁碳纳米管(SWCNT)为研究对象,计算对比碳纳米管对气体的吸附能等数据,判断羟基的引入能否优化碳纳米管对气体的响应灵敏度,并找出它们各自的最佳吸附位置。
1 建立结构模型
构建Cl2,H2S 气体分子与SWCNT 和SWCNT—OH 的微观模型,由于整个仿真都是在周期性的体系里进行,因此,需要建立超晶胞,将需要计算的物理模型放入晶胞中,有效避免了分子模型之间的相互影响[9]。
1.1 SWCNT 与气体分子的结构模型
本次实验仿真采用研究中常用的(8,0)型碳纳米管作为研究对象,建立(1.5 nm×1.5 nm×0.852 nm)的超晶胞,如图1 所示。气体分子模型如图2 所示。
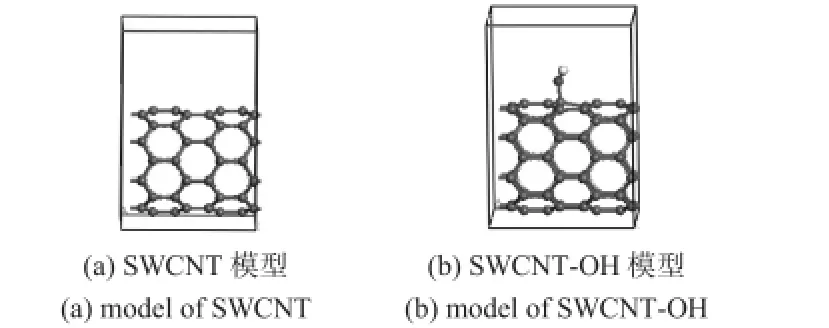
图1 碳纳米管的结构模型Fig 1 Structural model of carbon nanotube

图2 气体分子的结构模型Fig 2 Structural model of gas molecule
图1 (a)是直径为0.626 nm 的SWCNT,(b)为SWCNT—OH,—OH 中氧原子和一个碳原子以共价键结合,形成一个稳定的结构,在实际情况中会有多个羟基修饰在碳管的表面上,但是由于单根碳管是具有一定的长度(沿轴向方面延伸),并且具有周期对称性,考虑到这一点在建模的过程中可以简化为:在一个周期内,让一个羟基与一个气体分子结合,这样和在整根碳管上多个气体分子与多个羟基吸附效果是一样的。
图2(a)为H2S 气体分子的模型结构,其中优化后键长为0.136 3 nm,键角90.504°,(b)为Cl2气体分子的模型结构,优化后键长为0.199 8 nm。与实际情况相符,可用于仿真实验当中。
1.2 两种SWCNT 与Cl2,H2S 气体吸附位置构型
如图3 所示,SWCNT 在吸附气体分子时有四种构型,分别位于碳管中一个碳原子的正上方叫做顶(Top)位吸附,六边形的碳环空隙洞位,洞(Hole)位吸附,碳原子与碳原子之间的化学键位吸附也称为桥位吸附,其中桥位吸附又分为两种,一种是气体分子与化学键位平行(Parallel),另一种为气体分子与键位垂直(Vertical)。
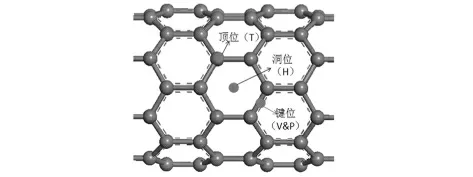
图3 SWCNT 的吸附位置Fig 3 Adsorption sites for SWCNT
如图4 所示,—OH 与气体的吸附方式有两种,一种是在氧原子顶端发生吸附(O),另一种为在氢原子顶端发生吸附(H)。

图4 SWCNT—OH 吸附位置Fig 4 Adsorption sites for SWCNT—OH
2 计算结果与分析
2.1 两种碳管态密度图分析
由图5 可知,在酸化后SWCNT—OH 的态密度图在费米能级处的峰值消失整体左移,变得更为平滑,表明其电子转移能力有所增加,并且在图5(b)中可以看出:费米能级两侧的峰值之间的DOS 并不为零,并且有一段距离,说明碳原子与氧原子之间的共价键很强,可以形成稳定的结构,在吸附气体的过程中不会轻易被破坏。

图5 态密度图Fig 5 Density of states(DOS)
2.2 两种碳管对Cl2 的吸附计算
将Cl2分子和碳管放在同一晶胞里,调整其吸附位置,直到找到最稳定的吸附位置,如图6 和图7 所示。

图6 SWCNT 与Cl2 的吸附模型Fig 6 Adsorption models of SWCNT and Cl2

图7 SWCNT—OH 与Cl2 的吸附模型Fig 7 Adsorption models for SWCNT—OH and Cl2
其中,Ea为吸附总能,E[SWCNT]为SWCNT 的总能,E[SWCNT-OH]为SWCNT—OH 的总能,E[X]为单个气体分子的能量(X 表示为某种气体),E[SWCNTS+X]为气体分子X 吸附在SWCNT 表面后整个体系所具有的能量总和,E[SWCNTS-OH+X]为气体分子X 吸附在SWCNT—OH 表面整个体系所具有的能量总和。
如表1 所示,在四种不同的吸附位置当中,ET>EV>EP>EH,T 位置的吸附能远大于其它三种位置模型(负号代表是放热反应可以自发地进行)。电荷转移量ΔQT>ΔQH>ΔQP>ΔQV,T 位置的电荷转移量为0.272×10-19C,大于其他三种吸附位形,最后从吸附距离D 上也可以看出:DT<DV<DP<DH,T 位置的吸附距离最小,说明吸附作用越大,吸附结构越稳定。由上面的数据可以得出:顶位(T)吸附时,吸附能最大,电荷转移量最多,吸附距离最小,是最佳的吸附位置。
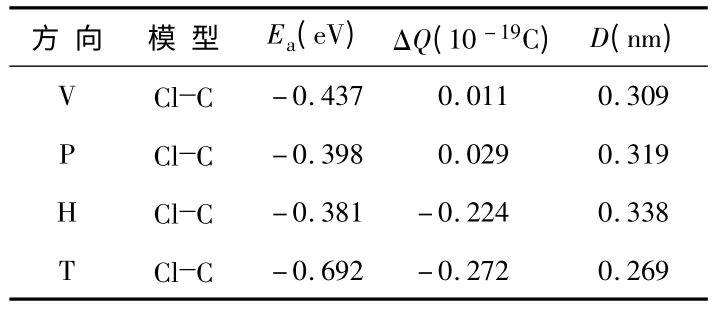
表1 SWCNT 的Cl2 吸附数据Tab 1 Cl2 adsorption data of SWCNT
(表中ΔQ 为碳纳米管与气体分子之间的电荷转移量,D 为原子之间的吸附距离。)
如表2 所示,SWCNT—OH 中,EH>EO,ΔQH>ΔQO,DH<DO,可以看出:H 位置吸附能最大,电荷转移量最多,吸附距离最小,是最佳的吸附位置。

表2 SWCNT—OH 的Cl2 吸附数据Tab 2 Cl2 adsorption data of SWCNT—OH
对比两组数据可以看出,表2 中最佳吸附位置H 中的各项数据优于表1 中最佳吸附位置T,最差吸附位置O 中的各项数据较接近表1 中最佳吸附位置T 且优于其他吸附位置,说明SWCNT—OH 对Cl2的吸附能力比SWCNT 有很大的提高。
2.3 两种碳管对H2S 的吸附计算
与吸附Cl2仿真相同,首先得到最稳定的吸附位置如图8 和图9 所示。图8 右上方小图为吸附位置的侧视图。

图8 SWCNT 与H2S 的吸附模型Fig 8 Adsorption models for SWCNT and H2S

图9 SWCNT—OH 吸附H2S 的吸附模型Fig 9 Adsorption models for SWCNT—OH and H2S
如表3 所示,五种吸附模型当中,吸附能EP>EV>ETH>ETS>EH,电荷转移量ΔQP>ΔQV>ΔQTS>ΔQTH=ΔQH,吸附距离上DTH<DP<DTS<DV<DH。因此,当H2S分子以碳环的C—C 键平行的时候(P 位置),吸附能最大,电荷转移量最高,虽然吸附距离不是最小,但与最小吸附距离DTH也较接近。因此,表3 中位置P 中碳管对H2S 的灵敏性最高,是最佳吸附位置。
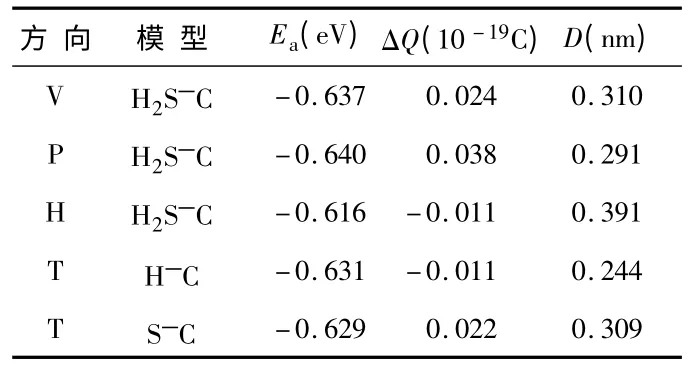
表3 SWCNT 的H2S 吸附数据Tab 3 H2S adsorption data of SWCNT
如表4 所示,吸附能EHS>EOS>EOH>EHH,电荷转移量ΔQHS>ΔQHH>ΔQOH>ΔQOS,吸附距离DOH<DHS<DHH<DOS,因此,在吸附位置H—S 中,碳管对H2S 响应灵敏,是最佳的吸附位置。

表4 SWCNT—OH 的H2S 吸附数据Tab 4 H2S adsorption data of SWCNT—OH
对比两组数据可以看出:表4 的最佳吸附位置H—S 中的各项数据要优于表3 中的最佳吸附位置P,表4 中的其他三种位置在吸附能,电荷转移量上也要优于表3 中的最佳吸附位置,说明SWCNT—OH 对H2S 的吸附能力有提高。
3 结 论
基于密度泛函理论的第一性原理研究了SWCNT—OH与本征SWCNT 对两种气体的吸附,计算结果表明:
1)酸化后的碳管羟基和碳原子以共价键的形式稳定存在,增加了碳管的电荷转移能力。碳管与被吸附气体间的电子交换更加容易,宏观体现为碳管对气体的电阻变化率高,响应灵敏。
2)SWCNT—OH 吸附能、电荷转移量大于本征SWCNT,吸附距离小于本征SWCNT—OH,因此,SWCNT 的气敏性更好,更加适用于制作气敏材料。
[1] An Wei,Wu Xiaojun,Zeng X C.Adsorption of O2,H2,CO,NH3,and NO2on ZnO nanotube:A density functional theory study[J].J Phys Chem C,2008,112(15):5747-5755.
[2] 李 昕,刘君华,朱长纯.基于碳纳米管薄膜的吸附式气体传感器的研究[J].中国科学:E 辑——工程科学、材料科学,2005,35(7):689-700.
[3] 程应武,杨 志,魏 浩,等.碳纳米管气体传感器研究进展[J].物理化学学报,2010,26(12):3127-3142.
[4] Ellison Mark D,Crotty Michael J,Koh Dukho,et al.Adsorption of NH3and NO2on single-walled carbon nanotubes[J].J Phys Chem B,2004,108(23):7938-7943.
[5] Chang H,Lee J D,Lee S M,et al.Adsorption of NH3and NO2molecules on carbon nanotubes[J].Appl Phys Lett,2001,79(23):3863-3865.
[6] 薛杉杉,隋 刚,杨小平.掺杂羧基化碳纳米管的纳米碳纤维前驱体的制备及表征[J].高等学校化学学报,2013,34(2):288-294.
[7] Elzbieta Chełmecka,Karol Pasterny,Teobald Kupka,et al.Density functional theory studies of OH-modified open-ended single-wall ZigZag carbon nanotubes(SWCNTs)[J].Journal of Molecular Structure:THEOCHEM,2010,948:93-98.
[8] 丁瑞雪.碳化硅纳米管气体吸附特性第一性原理研究[D].西安:西安电子科技大学,2010:15-25.
[9] 张晓星,代自强,孟凡生.羧基碳纳米管吸附SF6 放电分解组分的仿真计算[J].中国电机工程学报,2012,32(31):85-91.
