肤清液中苦参碱含量测定方法学研究*
2015-03-22马久太
蔡 琨 魏 迎 马久太
山东达因海洋生物制药股份有限公司(山东 264300)
肤清液中苦参碱含量测定方法学研究*
蔡 琨 魏 迎△马久太▲
山东达因海洋生物制药股份有限公司(山东 264300)
目的:建立肤清液中苦参碱的测定方法。方法:采用高效液相色谱法测定苦参碱,色谱柱采用C18柱(250mm×4.6mm,5μm),以0.018mol/L磷酸二氢钾-0.016mol/L十二烷基硫酸钠-乙腈(30:30:35)为流动相,检测波长215nm。结果:苦参碱与其它成分分离良好,线性范围为0.2575~2.5750mg,R2=0.9998,肤清液中苦参碱的含量为0.13mg/mL。结论:所采用方法准确、灵敏、专属性好,可用于肤清液中苦参碱的含量测定。
肤清液是新研发的一种纯中药复方制剂,由苦参、鸦胆子、土茯苓等八味中药组成,具有清热解毒、燥湿去毒功能,用于治疗由病毒感染引起的皮肤瘙痒、疼痛不适、女性白带量多色黄等疾病,临床效果良好。方中苦参、鸦胆子为君药,因鸦胆子成分非常复杂,暂无有效质量控制方法[1]。而苦参具有抗肿瘤、抗炎、抑制皮肤过敏等作用,临床上苦参常用于治疗寄生虫病,细菌性疾病,皮肤病,荨麻珍,湿疹,皮炎等皮肤疾病[2-3],苦参碱作为苦参中的最为重要的活性化合物[4]。本研究以苦参碱作为肤清液质量控制指标,对肤清液中的苦参碱含量测定及其方法学考察进行了系统研究,为有效控制肤清液的药品质量提供了重要依据。
1 仪器与试药 1.1 仪 器 高效液相色谱仪Waters-515),紫外-可见检测器(Waters-2487),化学工作站(Waters Empower 3.0),C18色谱柱(4.6mm×250mm,5μm)(Phenomenex Luna)。
1.2 试剂与试药 苦参碱(中国食品药品检定研究院,批号110805-201103);乙腈:色谱级;水:重蒸馏水;肤清液:批号130901、130902、130903,自制。
2 方法与结果 2.1 色谱条件与系统适用性 Waters C18色谱柱(4.6mm×250mm,5μm); 0.018mol/l磷酸二氢钾-0.016mol/l十二烷基硫酸钠-乙腈(30:30:35)为流动相;检测波长215nm;流速1.0mL/min。苦参碱理论板数不低于3000。
2.2 对照品溶液的制备 精密称取苦参碱对照品20.60mg,置20mL容量瓶中,用80%乙腈溶解,稀释至刻度,摇匀,作为苦参碱对照品溶液(浓度1.030mg/mL),4℃储存,备用。
2.3 供试品溶液的制备 精密吸取肤清液供试品溶液10mL,加10%氨水溶液调pH值9~10后,三氯甲烷萃取4次,每次20mL,合并三氯甲烷溶液,水浴蒸干,残渣加80%乙腈溶解,稀释,定容至10mL,摇匀,即得。
2.4 线性考察 精密吸取0.25、0.5、1.0、1.5、2.0、2.5mL苦参碱对照品溶液(浓度为1.030mg/mL)至10mL量瓶中,加流动相稀释至刻度,摇匀。按上述的色谱条件测定,以进样量X为横坐标,峰面积A为纵坐标,计算并得标准曲线线性回归方程为A = 30000000C+92638,R2=0.9998(n=6)。结果表明,在该色谱条件下苦参碱的线性范围是0.2575~2.5750mg,线性关系良好。
2.5 精密度考察 精密10μL苦参碱对照品溶液(浓度0.1030mg/mL),重复进样6次,并按上述色谱条件测定。结果峰面积的RSD为1.23%(n=6),保留时间RSD为0.07%,表明系统精密度良好。
2.6 溶液稳定性 取本品(批号130901)样品,按2.3项下供试品溶液制备方法制备供试品溶液,并于室温放置0、2、4、8、16h后,分别精密吸取供试品溶液10μL,测定。结果峰面积RSD为1.42%,表明稳定性良好。
2.7重复性试验 取5份样品(批号130901),按照2.3项下方法制备得供试品溶液,测定结果峰面积的RSD为1.54%(n=5),表明重复性良好。
2.8 中间精密度 同一实验室的三位不同实验人员在不同时间、不同条件下进行测定。结果不同人员测定的RSD为0.19%。
2.9 阴性试验 按照肤清液的处方、工艺,制备肤清液阴性样品,按照2.3项下方法制备得阴性样品溶液并测定。结果显示阴性溶液色谱图中无苦参碱色谱峰出现,说明阴性无干扰。
2.10 加样回收试验 取本品(批号130901)样品适量6份,精密称定,分别按80%、100%及120%比例加入苦参碱对照品溶液,按照2.3项下方法制备得供试品溶液并测定,计算回收率。结果表明本方法的加样回收率平均值98.79%, RSD为0.98%(n=6),表明本方法的准确性良好。结果详见表1。

表1 加样回收率试验结果(n=6)
2.11 样品含量测定 按照2.3项下方法制备得供试品溶液,供试品、对照品溶液分别精密吸取10μL,进样,记录峰面积,测定本品中苦参碱含量,测定结果见表2。
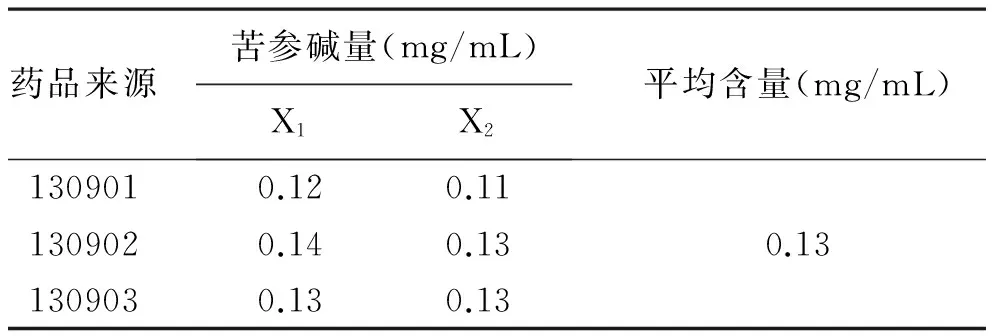
表2 含量测定结果(n=3)
3 讨 论 试验中曾参考2010年版《中国药典》一部,对苦参碱含量测定的色谱条件中流动相乙腈-无水乙醇-3%磷酸溶液(80∶10∶10)[5]进行了试验,结果表明供试品中苦参碱峰与其他杂质峰达不到基线分离。经多次研究筛选优化后以0.016mol/L磷酸二氢钾-0.016mol/L十二烷基硫酸钠-乙腈(30∶30∶35)为流动相,在此条件下苦参碱色谱峰具有较好的分离度。对于肤清液中苦参碱的提取方法,曾经对超生、回流及萃取进行了试验,结果萃取>超生>回流。在肤清液含量测定方法研究中,曾对苦参中苦参碱、氧化苦参碱都进行了研究,结果发现苦参药材中苦参碱、氧化苦参碱含量较高,而成品中氧化苦参碱特别低,与有关文献基本一致,主要原因是氧化苦参碱转化为苦参碱,提示本品在生产过程中,减低温度,减少加热时间[6]。本方法准确、灵敏、专属性好,可用于肤清液中苦参碱的含量测定。
[1] 王立军, 黄 娴, 祝静静,等.鸦胆子化学成分及肿瘤细胞毒活性研究[J].天然产物研究与开发,2013,25(6):772-777.
[2] 戴五好, 钱利武, 杨士友,等.苦参山豆根生物碱及其总碱的抑菌活性研究[J].中国实验方剂学杂志,2012,18(3):177-180.
[3] 杜思邈, 马丽强, 孙俊杰,等.苦参提取物体外抗菌实验研究[J].中医药学报,2010,8(3):74-76.
[4] 张 翅, 马 悦, 高慧敏,等.苦参化学成分研究进展[J].中国实验方剂学杂志,2014,20(4): 205-214.
[5] 国家药典委员会.中华人民共和国药典[S].一部.北京: 中国医药科技出版社,2010:188.
[6] 贾敏鸽,孙文基.苦参及其复方中苦参碱与氧化苦参碱的转化研究[J].药物分析杂志,2003,23(2):90-93.
(收稿2015-07-29;修回2015-08-25)
*国家科技重大专项项目(2011ZX09401-308-4)
色谱法,高效液相 苦参碱 碱肤清液
R282
A
10.3969/j.issn.1000-7369.2015.12.050
△咸阳职业技术学院(咸阳 712000)
▲陕西步长制药有限公司(西安 710075)
