经颈外静脉放置全植入式输液港在肿瘤化疗中的应用*
2015-03-10张宪生郭宏杰
尹 杰 张宪生 郭宏杰 佘 康 成 功
(北京大学第一医院介入血管外科,北京 100034)
·临床论著·
经颈外静脉放置全植入式输液港在肿瘤化疗中的应用*
尹 杰 张宪生**郭宏杰 佘 康 成 功
(北京大学第一医院介入血管外科,北京 100034)
目的 探讨经颈外静脉放置全植入式输液港(totally implantable venous access ports,TIVAP)作为肿瘤化疗静脉输液通路的可行性及术后并发症。 方法 对2010年1月~2013年12月96例行输液港植入术的肿瘤化疗患者进行回顾性研究,观察围手术期和远期并发症。 结果 全部病例均在术中完成输液港植入。经颈外静脉置管成功率95.8%(92/96);2例因术前曾行放疗静脉挛缩,2例血管过细无法植入导管,改行同侧颈内静脉穿刺置管。术后中位随访26个月(8~46个月),并发症发生率6.2%(6/96)。其中2例因肿瘤复发压迫造成输液港导管闭塞,1例导管移位,2例血栓形成,l例锁骨区皮肤疼痛。应用输液港装置化疗中输液顺畅,无渗漏,未发生气胸、血胸、导管相关性感染和夹闭综合征。 结论 经颈外静脉切开放置全植入式输液港是肿瘤化疗安全、快捷和有效的输液途径,可以避免气胸、血胸、夹闭综合征等严重并发症,主要并发症包括导管移位、阻塞、血栓形成。
完全植入式静脉输液港; 颈外静脉; 化疗
由于肿瘤化疗患者需要频繁进行静脉输液,许多化疗药物血管毒性较大,易引起静脉炎,直接影响化疗效果。全植入式静脉输液港(totally implantable venous access ports,TIVAP)使长期进行静脉内治疗的肿瘤患者生活质量得到了改善[1]。目前TIVAP放置的手术方式多为经颈内静脉或锁骨下静脉穿刺,气胸、血胸、导管断裂等严重并发症较多[2]。颈外静脉位置表浅,易于寻找,手术技术易学、易掌握,适合推广,但因缺乏详细、全面的技术描述,国内关于开展经颈外静脉植入输液港的报道较少[3,4]。我院2010年1月~2013年12月共96例需化疗的肿瘤患者接受经颈外静脉手术植入输液港,建立了稳定、安全、舒适的深静脉输液通路,并发症较少,并可以避免气胸、血胸、夹闭综合征等严重并发症,现报道如下。
1 临床资料与方法
1.1 一般资料
本组96例,男54例,女42例。年龄9个月~73岁,中位数57岁。18岁以上成人92例,其中乳腺癌27例,直肠癌18例,食管癌16例,结肠癌10例,肺癌8例,胃癌7例,淋巴瘤6例;小儿患者4例,年龄分别为9个月、11个月、16个月、2岁4个月,其中白血病2例,神经母细胞瘤2例。78例在输液港植入手术前已经进行至少2个疗程的化疗,其中总疗程数最多为28疗程,因外周静脉反复穿刺后输液困难、经周围静脉中心静脉置管(peripherally inserted central catheter,PICC)堵塞等原因寻求建立输液港通路。
病例选择标准:预期生存期超过1年,拟进行输液港植入,查体确认颈外静脉通畅,彩超确认中心静脉通畅。排除肿瘤晚期预期生存期低于1年,颈部曾行放疗,或有凝血功能障碍、肝肾功能不全、体质弱难以耐受手术者。
1.2 方法
采用美国巴德公司单腔标准型植入式静脉输液港(成人7F,小儿6F)。在手术室严格无菌的环境中进行,常规在C形臂X线透视下辅助完成,术前颈外静脉定位不清或迂曲的患者需在DSA引导下完成。局部麻醉(成年)或全麻(小儿)。平卧位,头偏向一侧,沿颈外静脉与胸锁乳突肌交界处做横行皮肤切口,长约1.5 cm,分开皮下组织找到颈外静脉,在静脉远端、近端下方各穿过一根丝线,远心端结扎,近心端提起,在两线之间用尖头小剪刀将静脉前壁斜行剪开一个小口,切口占其周径的1/2,成人插入导管15~17 cm,小儿为6~9 cm[回血通畅,封闭管腔并注入稀释的肝素(100 ml生理盐水加12 500 U/100 mg肝素)]。连接肝素盐水注射器,回抽静脉血及注入肝素盐水通畅,C形臂X线或DSA透视证实导管位于上腔静脉与心房交界处,结扎丝线固定导管。在泵体内注满肝素盐水待用。在同侧上胸壁锁骨下窝处做3 cm切口,向尾端游离皮瓣,皮瓣厚度0.5 cm,做出一个恰能容纳泵体的囊袋植入输液泵,将输液港导管经皮下隧道与囊袋中输液港连接,并将输液港和周围组织缝合固定,避免穿刺座翻转。可吸收线皮内缝合(图1)。
术后口服抗生素预防感染。胸片X线检查明确导管尖端位置并记录,证实导管位于上腔静脉与心房交界处,双肺无新发的气胸或积液即可开始使用(图2~4)。
如经颈外静脉术中注入肝素盐水不畅、回抽无回血,或C形臂X线或DSA透视导管未进入上腔静脉,考虑为置管未成功,在原切口位置改行颈内静脉穿刺置管。穿刺针进入点为锁骨、胸锁乳突肌胸骨端和胸锁乳突肌锁骨端构成的三角。操作者保持穿刺针与人体冠状面成60°角并向乳头方向进针。进针过程中要保持注射器负压,直到有静脉血回流。
2 结果
69例(71.9%)在普通手术室进行,27例(28.1%)因术前颈外静脉定位不清或过度迂曲在介入导管手术室借助DSA完成。92例经颈外静脉置管成功,成功率95.8%(92/96);2例因术前曾行胸部放疗静脉挛缩,2例血管过细无法植入导管,改行颈内静脉穿刺置管。15例术中透视发现导管进入颈内静脉,需在DSA引导下调整输液管(图5)。术后当天即可使用输液港输液,第1~3天开始化疗。术后次日X线胸片显示导管尖端位置理想(位于7~9后肋)。96例均获随访,中位随访26个月(8~46个月),至末次随访,96例中位带管时间22个月(4~35个月)。90例应用输液港装置化疗中输液顺畅,无渗漏,未发生气胸、血胸、夹闭综合征等严重并发症,其中2例因肿瘤进展死亡,其他病人无导管相关性感染、导管断裂等远期并发症。6例(6.2%)并发症:输液港导管闭塞2例,分别于术后7、9个月因肺癌、食管癌复发压迫导管上腔静脉处造成,因预期生存期不长未进行输液港取出术,改行外周静脉输液,保守观察,分别于发现闭塞后2、4个月因肿瘤晚期死亡;导管移位1例,因为化疗时输液不畅行X线检查发现,随即至导管室在DSA下调整导管位置,引导导管末端准确位于右心房上腔静脉入口水平,之后输液港使用通畅;血栓形成2例,为使用输液港时发现输液不畅,DSA造影显示有血栓形成,经输液港以10 ml注射器稀释肝素盐水压力性冲管、患侧上肢静脉滴注尿激酶溶栓,低分子肝素皮下注射抗凝后再通,继续使用;锁骨区皮肤疼痛l例,为手术植入港体部位炎症水肿刺激,疼痛视觉模拟评分4分,予以硫酸镁外敷,口服迈之灵改善肿胀,口服头孢克洛抗炎2周后肿胀消退,疼痛消失。
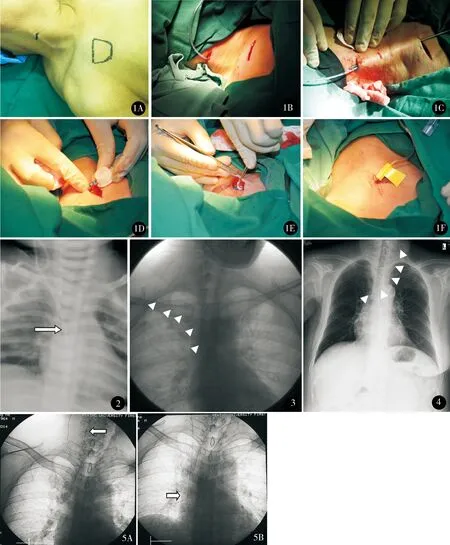
图1 经颈外静脉植入输液港手术过程 A.平卧位,头偏向一侧,术前对颈外静脉切口位置及埋港位置进行标记;B.沿颈外静脉与胸锁乳突肌交界处做横行皮肤切口,分开皮下组织找到颈外静脉,插入导管回血通畅,封闭管腔并注入稀释的肝素,C形臂X线或DSA透视证实导管位于上腔静脉与心房交界处,结扎丝线固定导管,在同侧上胸壁锁骨下窝处做3 cm切口,向尾端游离皮瓣,皮瓣厚度0.5 cm,做出一个恰能容纳泵体的囊袋植入输液泵;C.自锁骨下切口使用隧道器向颈部切口穿隧道,将输液港导管与隧道器连接后引至囊袋切口处;D.将输液港导管于锁骨下切口位置以远2 cm处剪断,套上固定锁,黑色标记处朝向头部,导管与输液港连接后将固定锁套紧;E.将输液港和周围组织缝合固定,避免港体穿刺座翻转;F.可吸收线皮内缝合,以专用Huber针穿刺输液港体,留作输液用 图2 患儿男,9个月,经右侧颈外静脉植入输液港,术后X线检查提示导管头位于上腔静脉与心房交界处(箭头位置) 图3 患者女,56岁,经右侧颈外静脉植入输液港,术后X线检查提示导管头位于上腔静脉与心房交界处(三角箭头指向导管经右侧锁骨下静脉行走方向) 图4 患者女,62岁,经左侧颈外静脉植入输液港,术后X线检查提示导管头位于上腔静脉与心房交界处(三角箭头指向导管经静脉角行走方向) 图5 经右侧颈外静脉植入输液港,因颈外静脉迂曲,导管进入颈内静脉(图A箭头位置),在DSA引导下调整导管方向顺利进入上腔静脉(图B箭头位置)
3 讨论
肿瘤患者需要接受长期静脉化疗,因而建立一个长期、可靠、相对舒适的静脉通路,对这些患者完成治疗并提高生活质量十分重要。相比外置式深静脉导管,完全植入式输液港更为安全、方便,留置时间更长[5],临床的应用越来越多,极大改善了肿瘤患者的生活质量。
3.1 经颈外静脉植入输液港的适应证及优势
输液港植入手术方法分为两类[3]:穿刺植入和切开植入。传统术式为深静脉穿刺方法,应用最多的植入位置是颈内静脉和锁骨下静脉,可根据解剖定位直接穿刺,也可在超声引导下进行,超声引导下穿刺更为准确、安全。另一种方法采取直视下游离静脉,远心端结扎,近心端植入导管并结扎固定,可选择的静脉包括颈外静脉、头静脉等。锁骨下静脉穿刺和颈内静脉低位穿刺有较高的气胸、血胸等严重并发症的发生率。在超声引导下的经颈内静脉穿刺,并发症较传统解剖定位穿刺明显降低[6,7]。
许多回顾性研究证明外科手术切开静脉置管的安全性和可行性,并且其早期并发症发生率很低[8]。Jablon等[9]回顾性比较358例患者,通过头静脉切开植入输液港是安全、快速的方法,成功率高,而头静脉方法不可行时,颈外静脉是有效、安全、合适的替代方法。从头静脉转为颈外静脉,置管成功率提高,严重并发症发生率较低。但是传统的头静脉切开置管方法失败率较高,文献报道为6%~30%[10~12]。因此,我们直接经颈外静脉切开置管,成功率达95.8%,其余4.2%通过同一切口进行同侧颈内静脉穿刺置管成功,避免另外的手术切口。
颈外静脉是颈部最大的浅静脉,由下颌后静脉的后支和耳后静脉、枕静脉等汇合而成,沿胸锁乳突肌浅面斜向下后行,在锁骨中点上方2~5 cm穿颈深筋膜注入锁骨下静脉或静脉角[13,14]。图2、4经静脉角汇入上腔静脉;图3经锁骨下静脉汇入上腔静脉。可以通过体格检查了解颈外静脉是否通畅。检查者将食指和中指并拢压在颈外静脉上,然后一手指紧压向外滑动,挤出该段静脉内血液,至一定距离放松该手指,另一手指紧压不动,看静脉是否迅速充盈。再同法松开另一手指,即看出血流方向。颈外静脉位置表浅,易于判断是否通畅,术中易于定位和寻找。拟进行输液港植入的患者进行术前查体,通过上述方法确认颈外静脉通畅、彩超确认中心静脉通畅,即适合进行经颈外静脉输液港植入。
我们选择颈外静脉切开置管的理由:严重并发症如神经损伤、误穿动脉引起的出血、气胸的发生率低,而这些并发症在传统的锁骨下静脉或颈内静脉穿刺中一旦穿刺针穿刺过深,发生率较高。本组未出现气胸、血胸、导管断裂等严重并发症。
3.2 经颈外静脉植入输液港的操作技巧
3.2.1 颈外静脉切口位置的选择 颈外静脉与胸锁乳突肌交界处选为切口位置(图1A),因为此位置表浅,周围无重要血管、神经,局部浸润麻醉后便于进行钝性分离。颈外静脉属于浅静脉,在深筋膜层上方即可找到颈外静脉,术中勿分离过深。另外,如果置管不成功,可以在此切口位置进行颈内静脉中段穿刺,避免另外的切口。
3.2.2 体位 平卧后颈外静脉充盈不明显可采用头低脚高位,或将肩部垫高1~2 cm,可使颈外静脉充盈显露,便于术中定位寻找。
3.2.3 处理静脉 在颈外静脉远端、近端下方各穿过一根丝线,远端结扎,近端打悬空结备用,将静脉前壁斜行剪开一个小口,切口占其周径的1/2,以输液港套装自带的静脉钩伸入静脉切口内,将静脉提起,减少出血并方便导管进入(图1B),X线定位导管位置准确后将远心端丝线悬空结收紧,将导管与颈外静脉结扎,可以有效防止导管移位,减少导管断裂的可能性。部分患者术中X线透视下发现,因颈外静脉迂曲,导管进入颈内静脉,在DSA引导下调整导管方向顺利进入上腔静脉(图5)。
3.2.4 输液港埋置 在同侧胸壁锁骨下窝埋置港体时应注意,游离皮瓣厚度0.5 cm。皮瓣厚度非常关键,过厚会导致穿刺困难,过浅容易出现感染、外露、炎症水肿。做出一个恰能容纳泵体的囊袋植入港体,囊袋勿过大,否则港体容易翻转、移位,将港体和周围组织缝合固定,可避免穿刺座翻转(图1E)。
3.3 经颈外静脉植入输液港的并发症的处理
3.3.1 导管堵塞 导管堵塞是输液港长期留置过程中最常见的并发症,可分为血栓性和非血栓性堵塞。非血栓性主要是机械性因素或药物沉积,占导管堵塞的42%[15]。本组2例因肿瘤复发压迫造成输液港导管闭塞,分别是同侧肺癌和食管癌复发压迫输液港导管。因此,对于胸部肿瘤如肺癌、食管癌等避免在肿瘤同侧做输液港植入,术前认真评估对侧静脉情况,在无肿瘤侧植入输液港可以避免此类并发症。血栓性堵塞又分为腔内血栓、导管顶端血栓和纤维素鞘[16,17],主要表现为导管输液缓慢、不能回抽血或者无法输液。本组2例血栓形成患者出现颈部、手臂肿胀,经输液港以10 ml注射器稀释肝素盐水压力性冲管,患侧上肢静脉滴注尿激酶溶栓,低分子肝素皮下注射抗凝。溶栓过程中密切监测凝血功能、纤维蛋白原含量。因发现较早,早期及时处理,经溶栓治疗后输液港导管得以再通,继续使用。压力性冲管以10 ml注射器较佳,因其在冲管压力和容量间能取得较好的平衡[18]。
3.3.2 导管移位 Kameyama等[19]报道导管移位发生率为0.4%~1.8%。导管沿着血管移动,最后可以停留在腔静脉、右心房或者肺动脉及其分支,极少数也可以到达颈内静脉。导管移位与上臂运动,屈颈以及咳嗽和呕吐所致的胸内压改变等有关。早期监测、定期进行X线检查对于输液港的管理十分重要,一旦发现导管移位,需要手术调整导管位置,必要时移除导管。本组1例导管移位因术后输液不畅发现,随即至导管室在DSA下调整导管位置,引导导管末端准确位于右心房上腔静脉入口水平,之后输液港使用通畅。一般如导管尖端位于第8后肋水平可认为接近上腔静脉右心房入口水平。位置相对偏浅会因血流相对慢而增加导管阻塞机会;位置过深进入心房有可能引起患者心悸等不适。
3.4 小结
经颈外静脉切开放置全植入式输液港是肿瘤化疗安全、有效、快捷的输液途径,较传统穿刺技术具有以下优点:可以直视下对颈外静脉进行操作,没有气胸、血胸、损伤大血管的风险,操作相对简单,手术风险小。颈外静脉位置表浅,易于寻找,手术技术易学、易掌握,适合推广。
1 Gallieni M,Pittiruti M,Biffi R.Vascular access in oncology patients.CA Cancer J Clin,2008,58(6):323-346.
2 Zaghal A,Khalife M,Mukherji D,et al.Update on totally implantable venous access devices.Surg Oncol,2012,21(3):207-215.
3 陈明远,夏良平,陈直华,等.植入式静脉输液港不同植入术式在恶性肿瘤患者中的应用.中山大学学报(医学科学版),2007,28(z1):145-147.
4 褚珺君,吴晔明,徐 敏.颈内、颈外静脉置管皮下埋入化疗泵在肿瘤患儿中的临床应用.中华小儿外科杂志,2001,22(1):17-18.
5 Lebeaux D,Fernandez-Hidalgo N,Chauhan A,et al.Management of infections related to totally implantable venous-access ports:challenges and perspectives.Lancet Infect Dis,2014,14(2):146-159.
6 程 琳,赵凤琴,杨德启,等.X线引导下放置植入式输液港在乳腺癌化疗中的应用.中国微创外科杂志,2011,11(7):590-592.
7 Lin CP,Wang YC,Lin FS,et al.Ultrasound-assisted percutaneous catheterization of the axillary vein for totally implantable venous access device.Eur J Surg Oncol,2011,37(5):448-451.
8 Orci LA,Meier RP,Morel P,et al.Systematic review and meta-analysis of percutaneous subclavian vein puncture versus surgical venous cutdown for the insertion of a totally implantable venous access device.Br J Surg,2014,101(2):8-16.
9 Jablon LK,Ugolini KR,Nahmias NC.Cephalic vein cut-down verses percutaneous access: a retrospective study of complications of implantable venous access devices.Am J Surg,2006,192(1):63-67.
10 Chandrasekaran A,Somasundaram J.Surgical placement of totally implantable venous access device-an institutional experience.Indian J Pediatr,2014,81(9):866-870.
11 Lin CH,Yu JC,Lee YT,et al.Conversion from cephalic vein to external jugular vein:success rate increased on totally implantable access ports with cut-down method.Surg Innov,2013,20(6):566-569.
12 Povoski SP.External jugular vein cutdown approach for chronic indwelling central venous access in cancer patients: a potentially useful alternative.World J Surg Oncol,2004,2:7.
13 陈雅玫,石新华,张 煜.超声引导下改良Seldinger技术与盲穿法行PICC在肿瘤患者中的对比研究.中国微创外科杂志,2013,13(12):1131-1133.
14 张士锋,魏 浩.颈外静脉穿刺的应用解剖学分析.中国现代药物应用,2013,7(22):228-229.
15 刘 冰,尹 杰.完全植入式静脉输液港手术方式及并发症研究进展.中华临床医师杂志(电子版),2014,8(20):3704-3708.
16 谢书勤,覃 谦,孙治平,等.TIVAP和PICC在肿瘤化疗和营养支持中的应用及并发症比较.中国肿瘤外科杂志,2013,5(3):196-198.
17 Voog E,Lazard E,Juhel L.Prophylaxis of thrombosis induced by chemotherapy or central venous catheters.Presse Med,2007,36(2 Pt 1):225-234.
18 Barbetakis N,Asteriou C,Kleontas A,et al.Totally implantable central venous access ports. Analysis of 700 cases.J Surg Oncol,2011,104(6):654-656.
19 Kameyama H,Yamazaki T,Maeda C,et al.Central venous access port devices (CVAPD) related complications in colorectal cancer patients.Gan To Kagaku Ryoho,2010,37(3):453-455.
(修回日期:2014-09-22)
(责任编辑:王惠群)
Implantation of Totally Implantable Venous Access Ports via External Jugular Vein in Chemotherapy for Cancer
YinJie,ZhangXiansheng,GuoHongjie,etal.
DepartmentofVascularandEndovascularSurgery,PekingUniversityFirstHospital,Beijing100034,China
ZhangXiansheng,E-mail:zxs66229@sina.com
Objective To explore the feasibility and complications of totally implantable venous access ports (TIVAP) implanted via external jugular vein in chemotherapy for cancers. Methods A retrospective review was conducted on 96 patients undergoing a TIVAP implantation for chemotherapy at this hospital from January 2010 to December 2013. Perioperational and long-term complications of the procedure were observed. Results The TIVAP was inserted in all the cases. The external jugular vein approach was successfully utilized in 92 cases (95.8%). In the remaining 4 cases (4.2%), the TIVAP placement was performed through ipsilateral internal jugular vein because of contractured vein due to preoperatively radiotherapy in the neck area in 2 cases and fine veins unable to implant the catheter in 2 cases. No immediate postoperative complications were detected. The patients were followed up for a median of 26 months (8-46 months).The overall complication rate was 6.2% (6/96). There were 2 cases of catheter occlusion because of tumor recurrence, 1 case of migration of the catheter, 2 cases of thrombogenesis, and 1 case of clavicular skin pain. TIVAP worked well without leakage, pneumothorax, infection, or pinch-off syndrome. Conclusions External jugular vein approach appears to be a highly successful and safe alternative route and may be considered a potentially useful primary route for TIVAP placement in cancer patients. Main complications include catheter migration, occlusion, and thrombosis.
Totally implantable venous access ports; External jugular vein; Chemotherapy
北京大学第一医院院内青年学者启动基金项目 **
R608
A
1009-6604(2015)03-0210-05
10.3969/j.issn.1009-6604.2015.03.005
2014-07-03)
**通讯作者,E-mail:zxs66229@sina.com
