HPLC法测定注射用亚锡二巯丁二钠中二巯丁二酸的含量
2015-03-06陈志明吴二明刘佳琳
汪 洋,陈志明,吴二明,王 刚,刘佳琳
江苏省原子医学研究所,卫生部核医学重点实验室,江苏省分子核医学重点实验室,无锡 214063
HPLC法测定注射用亚锡二巯丁二钠中二巯丁二酸的含量
汪 洋,陈志明,吴二明,王 刚,刘佳琳
江苏省原子医学研究所,卫生部核医学重点实验室,江苏省分子核医学重点实验室,无锡 214063
目的:以四丁基碘化胺为离子对试剂,采用离子对反相高效液相色谱法测定注射用亚锡二巯丁二钠中二巯丁二钠的含量。方法:采用SunFireTMC18色谱柱,流动相为6.5 g·L-1磷酸二氢钠溶液∶甲醇=(80∶20),流速1.0 mL·min-1,检测波长220 nm,柱温25℃。结果与结论:二巯丁二钠在1.92~17.28 μg范围内线性良好(r=0.999);平均加样回收率为98.8%,RSD为1.3%。本方法适用于注射用亚锡二巯丁二钠的质量控制。
二巯丁二钠;离子对反相高效液相色谱法;四丁基碘化胺
注射用亚锡二巯丁二钠为放射性锝[99mTc]标记配套冻干药盒,提供制备锝[99mTc]二巯丁二酸注射液,用于肾皮质诊断显像,其主要成分为二巯丁二钠及还原剂、稳定剂及pH调节剂等辅料。该药盒已在国内上市,国家标准中规定了二巯丁二钠及还原剂的标示量,但未收录两者的含量检测方法。二巯丁二钠为锝[99mTc]标记配体,还原剂氯化亚锡用于还原+7价锝[99mTc]至有标记活性的低价态,是该药盒主要的活性成分,对两者含量应加以控制。
二巯丁二钠可作为金属离子螯合剂,用于治疗重金属中毒。《中国药典》2010年版采用氧化还原滴定法测定其含量。但本文所探讨的药盒中含有还原剂,会对药典方法有干扰。现用离子对反相高效液相色谱法,对该药盒的二巯丁二钠含量进行测定。
1 仪器与试药
Waters1525二元型高效液相色谱仪;Waters2487双波长检测器;注射用亚锡二巯丁二钠冻干粉(每瓶内含二硫丁二钠2.48 mg,氯化亚锡0.4 mg)由江苏省原子医学研究所江原制药厂提供;二巯丁二酸对照品为分析纯(经二次重结晶所得,纯度99.9%)。甲醇为色谱纯;其余试剂为分析纯;水为注射用水。
2 方法与结果
2.1 色谱条件
SunFireTMC18色谱柱 (150 mm×4.6 mm,5 μm);流动相:6.5 g·L-1磷酸二氢钠溶液 (内含1.8 g·L-1四丁基碘化胺、0.9 g·L-1乙二胺四乙酸二钠)∶甲醇= 80∶20;流速:1.0 mL·min-1;检测波长:220 nm;柱温:25℃;进样量:20 μL[1]。记录色谱图至主成分峰保留时间的4倍,结果见图1。
2.2 溶液配制
对照品溶液制备:取二巯丁二酸对照品60 mg,精密称定,置25 mL量瓶中,加水适量,滴加1 mol· L-1氢氧化钠溶液,振摇使溶解,调溶液pH为4.0~4.5,加水稀释至刻度,作为对照品贮备液。精密量取对照品贮备液2 mL至10 mL量瓶中,加水稀释至刻度,即得对照品溶液。
供试品溶液制备:取本冻干品1瓶,加水溶解并全部转移至5 mL量瓶中,即得。
2.3 线性关系考察
分别精密量取二巯丁二酸对照品贮备液0.4、1.2、2.0、2.8、3.6 mL至10 mL量瓶中,加水稀释至刻度,按“2.1”色谱条件检测。
以二巯丁二钠对照峰面积为纵坐标(Y),二巯丁二酸进样量(μg)为横坐标(X)进行线性回归,求得回归方程式:Y=2.09×105X+7×103,r=0.999。结果表明,二巯丁二酸在1.92~17.28 μg范围内线性关系良好。
2.4 进样精密度试验
分别精密吸取对照品溶液及样品溶液各20 μL,连续进样6次,测定峰面积,计算RSD分别为0.6%和0.9%(n=6)。
2.5 回收率试验
分别取二巯丁二酸0.04、0.06、0.08 g,各3份,精密称定,置25 mL量瓶中,滴加1 mol·L-1氢氧化钠适量,加入抗坏血酸0.075 g,振摇使溶解,控制pH值符合制剂要求,加水稀释至刻度。分别取上述溶液2 mL置10 mL量瓶中,加水稀释至刻度。按“2.1”色谱条件的方法分别进样,计算回收率为98.8%,RSD=1.3%(n=3)。
2.6 专属性试验
精密称取本品(批号20150106-1)1瓶,分别经酸(1 mL,1 mol·L-1稀盐酸,室温放置30 min,中和,加水至5 mL)、碱(1 mL,1 mol·L-1氢氧化钠溶液,室温放置30 min,中和,加水至5 mL)、氧化(0.5 mL,30%H2O2,室温放置2 h,加水至5 mL)、水浴高温(80℃,2 h,加水至5 mL)等条件强制降解破坏,以上样品按“2.1”色谱条件检测,结果见图2,图示主峰与杂质峰分离良好,说明该法专属性较强。
2.7 注射用亚锡二巯丁二钠含量测定 见表1。
3 讨 论
本法检测药盒中二巯丁二酸含量时,其含量低于标示量。原因可能在于制备该冻干药盒过程中,在药液冷冻干燥尚未完成的阶段,药液中的二巯丁二酸离子与亚锡离子发生络合,致游离的二巯丁二酸含量下降。同时结合锝[99mTc]标记率的测定,发现尽管二巯丁二钠的含量有所下降,药盒仍能较好地用于锝[99mTc]标记。这是因为该药盒锝[99mTc]标记放射性强度不超过3700 MBq,该强度的锝[99mTc]化学量是微不足道的,理论上二巯丁二钠仅需几微克即可完成反应;但实际标记情况受多种化学、物理因素的影响,为保证锝[99mTc]标记,仍应使二巯丁二钠含量控制在合理水平上[3]。

图2 不同降解条件下注射用亚锡二巯丁二钠的液相色谱图
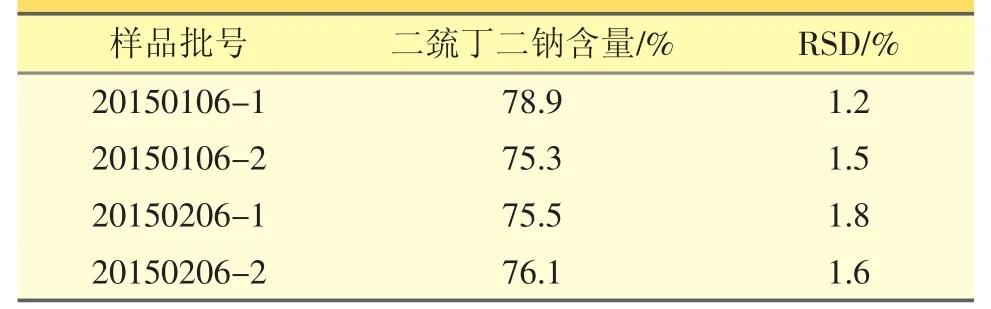
表1 注射用亚锡二巯丁二钠含量测定结果
[1] 陈红红,张惠贤,罗梅初,等.反相高效液相色谱法测定二乙烯三胺五醋酸注射液的含量[J].中国现代应用药学杂志,1998,15(6):41.
[2] 国家药典委员会.中华人民共和国药典[S].二部,北京:北京工业出版社,2010:500-3.
[3] 陈 方,周 前,李玉萍,等.电位滴定法定量测定药盒中的微量亚锡[J].中华核医学杂志,1990,10(3):157-60.
Determination of Content of Succimer in Kit for Preparation of Technetinm [99mTc]Succimer Injection by HPLC
WANG Yang,CHEN Zhi-ming,WU Er-ming,WANG Gang,LIU Jia-lin
Key Laboratory of Nuclear Medicine,Ministry of Health,Jiangsu Key Laboratory of Molecular Nuclear Medicine,Jiangsu Institute of Nuclear Medicine,Wuxi 214063
Objective:To establish a reversed-phase HPLC method for determination of succimer in the kit of sodium succimer and stannous chloride mixture for injection.Methods:Tetrabutylammonium iodide was used as the ion pair reagent.A SunFireTMC18ODS column was adopted with 6.5 g·L-1sodium dihydrogen phosphate solution-methanol(80∶20)as the mobile phase at a flow rate of 1.0 mL·min-1,and the eluate was detected at 220 nm.Results and Conclusion:The curve was linear in the range of 1.92-17.28 μg (r=0.999),the average recovery was 98.8%and RSD was 1.3%.This method can be used for the quality control of the active pharmaceutical ingredient.
Succimer;Reversed-phase HPLC;Tetrabutylammonium iodide
R927.2
A
1673-7806(2015)06-569-02
汪洋,男,副主任药师 E-mail:wangyang@jsinm.org
2015-06-05
2015-00-00
