HPLC-UV法测定人血浆及尿中多尼培南
2015-02-20秦永平梅亚君章丽毛锐南峰向瑾梁茂植余
秦永平梅亚君章 丽毛 锐南 峰向 瑾梁茂植余 勤
(1.四川大学华西医院临床药理研究室,四川 成都 610041;2.成都中医药大学药学院,四川 成都 611137)
HPLC-UV法测定人血浆及尿中多尼培南
秦永平1,梅亚君1,2,章 丽1,毛 锐1,南 峰1,向 瑾1,梁茂植1,余 勤1
(1.四川大学华西医院临床药理研究室,四川 成都 610041;2.成都中医药大学药学院,四川 成都 611137)
建立HPLC-UV法测定人血浆及尿中多尼培南(DP)的质量浓度,用于DP人体药代动力学研究。采用Ultimate XB-C18(150 mm×4.6 mm×3 μm)色谱柱,血浆及尿样测定用流动相分别为10 mmol/L醋酸钠:乙腈:三乙胺(体积比94:6:0.1,冰乙酸调pH为4.51)和8mmol/L醋酸钠:乙腈:三乙胺(体积比95.5:4.5:0.1,冰乙酸调pH值为4.99),流速均为1mL/min,检测波长为297nm。血浆样品经乙睛沉淀蛋白,再用二氯甲烷反洗后取上清液进样,以美罗培南(MRP)做内标;尿样直接用水稀释后进样,外标法定量。血药浓度在0.0625~200μg/mL范围内与峰面积线性关系良好,定量限为0.0625μg/mL,批内精密度在1.0%~6.0%之间,批间精密度在3.0%~6.7%之间,方法回收率在92.4%~104.5%之间,预处理回收率在91.2%~103.8%之间。尿药浓度在0.625~4 800 μg/mL范围内与峰面积线性关系良好,定量限为0.625μg/mL,批内精密度在0.7%~4.0%之间,批间精密度在1.1%~5.3%之间,方法回收率在94.1%~106.7%之间。该方法具有简便、灵敏、准确等特点,适用于人血浆及尿中多尼培南质量浓度的测定。
多尼培南;高效液相色谱法;血药浓度;尿药浓度
0 引 言
多尼培南是一种新的1β甲基碳青霉烯类抗生素[1],其抗菌谱广、抗菌活性强,对各种需氧、厌氧G+及G-菌均有很强的抗菌活性[2]。Sutherland C和Iked K等[3-4]分别采用固相萃取法和超滤法进行样品预处理,采用HPLC-UV法对DP的血药浓度进行测定。国内有多尼培南的临床药代动力学研究报道[5-6],但无多尼培南尿液浓度的相关测定。本实验建立了人血浆及尿液中多尼培南浓度的HPLC-UV测定方法。
1 实验部分
1.1 仪器与色谱条件
日本SHIMADZU公司2010-HPLC型高效液相色谱仪,采用Ultimate XB-C18分析柱(150 mm× 4.6mm×3μm),柱温35℃,紫外检测波长297nm。血浆和尿液样品用流动相分别为10mmol/L醋酸钠:乙腈:三乙胺(体积比94:6:0.1,冰乙酸调pH为4.51)和8mmol/L醋酸钠:乙腈:三乙胺(体积比95.5:4.5:0.1,冰乙酸调pH为4.99),流量均为1mL/min。
1.2 药品与试剂
多尼培南(Doripenem,DP)对照品(成都地奥九泓制药厂,含量:91.79%,批号:20131001);美罗培南(Meropenem,MRP)对照品(中国药品生物制品检定所,含量:87.0%,批号:30506-200702)。乙腈、甲醇、三乙胺均为色谱纯试剂;其余试剂为分析纯;实验用水由美国Millipore公司Milli-Q型超纯水器制备所得。
1.3 溶液配制
1)血浆样品测定用储备液。精密称取DP对照品21.79 mg(相当于DP20 mg)于25 mL容量瓶中,用纯水溶解并定容至刻度,即得血浆样品测定用DP储备液(800μg/mL),分装于EP管中-80℃冰箱保存。临用前,用水稀释得DP血样测定标准系列工作液。
2)尿液样品测定用储备液。称取DP对照品130.7mg(相当于DP120mg)于25mL的容量瓶中,用纯水溶解并定容至刻度,即得尿液样品测定用DP储备液(4 800 μg/mL),分装于EP管中-80℃冰箱保存。临用前,用水稀释得DP尿样测定标准系列工作液。
3)内标(IS)储备液及工作液。精密称取MRP对照品22.99 mg(相当于MRP20 mg)于50 mL的容量瓶中,用甲醇溶解并定容至刻度即得MRP储备液(400μg/mL),分装于EP管中-80℃冰箱保存。临用前,用水稀释得MRP内标工作液(40μg/mL)。
1.4 样品预处理
1)血浆样品。取待测血浆样品200μL,加入纯水50 μL、加入内标工作液50 μL,混匀,再加入乙腈600μL,充分混合后离心10min(13000r/min,8℃);倾倒上清液于圆底管,加入2mL二氯甲烷反洗,涡旋5min,离心7min(3000r/min,8℃),取20μL上清液进样。
2)尿液样品。取待测尿液样品100 μL,加入纯水900μL,混匀后离心10 min(13000r/min,8℃),取20μL上清液进样。
2 方法与结果
2.1 专属性
空白血浆(6个)、对照品、空白血浆加对照品及血浆样品色谱图见图1,DP(1)与IS(2)保留时间分别为5.3min和8.5min。结果显示:血浆中的内源性杂质对药物和内标峰均无干扰。
空白尿样(6个)、对照品、空白尿样加对照品及尿液样品色谱图见图2,DP(1)保留时间为8.3 min。结果显示:尿液中的内源性杂质对药物峰无干扰。
2.2 线性及最低定量限考察
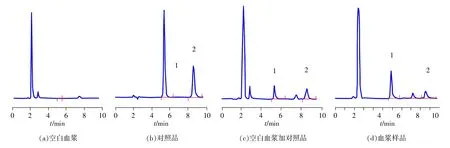
图1 血浆测定色谱图
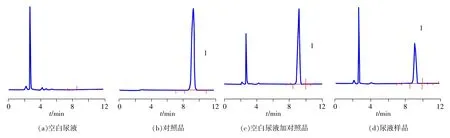
图2 尿液测定色谱图
1)血浆。分别取200μL空白血浆9份,空白管补水50μL,其余各管依次加入血样测定标准系列工作液50μL,使DP血浆质量浓度分别为0.0625,0.125,3.125,12.5,25,50,100,200μg/mL。按1.4项下1)自“加入内标工作液50μL”起操作,进样20μL。记录药物及内标色谱峰面积,以二者峰面积之比(Y)对多尼培南血浆质量浓度(X)进行加权(1/x2)线性回归,得DP的血浆标准曲线回归方程:Y=0.090 73X+ 0.006 93(r2=0.999 8),结果显示多尼培南血浆质量浓度在0.062 5~200 μg/mL范围内标准曲线线性良好。定量限为0.062 5 μg/mL,测定5次的平均值为0.057 2μg/mL,RSD为9.16%,准确度和精密度均符合相关规定。
2)尿液。取空白尿11份,每份100μL,空白管补水900μL,其余管先依次加入尿液测定标准系列工作液100 μL,使其尿药浓度分别为:0.625,1.25,5,20,100,400,800,1600,3200,4800μg/mL,再加水800μL,按1.4项下2)混匀离心处理后进样。记录药物色谱峰面积,以峰面积(Y)对尿药浓度(X)进行加权(1/x2)线性回归,得DP的尿液标准曲线回归方程:Y=2359.74X-485.866(r2=0.999 8),结果显示多尼培南尿液质量浓度在0.625~4 800 μg/mL范围内标准曲线线性良好。最低定量限为0.625μg/mL,测定5次的平均值为0.643μg/mL,RSD为2.73%,准确度和精密度均符合相关规定。
2.3 方法精密度和回收率
1)血浆样品。取用空白血浆加DP工作液配成的低(0.125 μg/mL)、中(10 μg/mL)、高(160 μg/mL)3个质量浓度血浆样品各5份,按1.4项下1)自“加入内标工作液50μL”起同法操作。以多尼培南与内标峰面积之比在当日血浆标准曲线上求出多尼培南质量浓度,于1d内连续测定5次,测得DP平均血药浓度分别为0.121,10.277,152.533 μg/mL,对应的批内精密度RSD分别为5.98%,1.03%和2.58%。血浆方法回收率分别为(97.02±5.81)%、(102.77±1.06)%和(95.33±2.46)%。于7d内测定3批,每批5次,测得DP平均血药浓度分别为0.121,10.673,158.518μg/mL,对应的批间精密度RSD分别为6.66%、2.98%和3.53%。
2)尿液样品。用空白尿液加DP工作液配成的低(1.875μg/mL)、中(3.75μg/mL)、中高(240μg/mL)、高(3 840 μg/mL)4个质量浓度的尿液样品各5份,按1.4项下2)处理进样。以多尼培南峰面积在当日血浆标准曲线上求出多尼培南质量浓度,在1 d内连续测定5次,测得DP平均尿药浓度分别为1.736,3.760,256.030,3 811.533μg/mL,对应的批内精密度RSD分别为3.99%、4.02%、0.72%和0.91%。方法回收率分别为(94.05±3.756)%、(103.09±5.612)%、(106.68±0.766)%和(99.26±0.902)%。于7d内测定3批,每批5次,测得DP平均尿药浓度分别为1.699,3.536,254.702,3 811.598μg/mL,对应的批间精密度RSD分别为4.10%、5.25%、1.13%和1.15%。
2.4 血浆预处理回收率
取用空白血浆加DP工作液配成的低(0.125 μg/mL)、中(10 μg/mL)、高(160 μg/mL)3个质量浓度血浆样品,每个浓度3份,按1.4项下1)自“加入内标工作液50μL”起同法操作,将所得药物及内标峰面积与相应浓度的工作液直接进样所得峰面积相比,得血浆样品预处理平均回收率分别为118.35%、104.53%和101.32%,内标的预处理平均回收率为96.63%。
2.5 样品稳定性考察
取用空白血浆加DP工作液配成的低(0.125 μg/mL)、中(10μg/mL)、高(160μg/mL)的3个质量浓度的血浆样品及用空白尿液加DP工作液配成的低(1.875 μg/mL)、中(3.75 μg/mL)、中高(240μg/mL)、高(3 840μg/mL)4个质量浓度的尿液样品各3份,分别考察-80℃长期放置、反复冻融、室温放置、处理后样品在进样室(8℃)放置及重复进样稳定性。结果显示,所有稳定性试验中实测值与理论值的相对偏差均小于15%。表明血浆样品在-80℃条件下保存30d,反复冻融3次,室温放置6h,进样室放置16h,重复进样1次均稳定;尿液样品在-80℃条件下保存34d,反复冻融3次,室温放置4h,进样室放置14h、重复进样2次均稳定。
2.6 尿样稀释因子考察
在尿液样品测定中,有样品质量浓度超过了标准曲线上限(4800μg/mL)的,进行4倍稀释因子的考察。取空白尿液加DP对照品配成的尿液样品(8000μg/mL)0.5mL,加入空白尿样1.5mL稀释,充分混匀后按尿液样品预处理方法处理后进样。将直接测得的质量浓度乘以4即为换算的实际质量浓度,其测定5次的平均质量浓度为7670.85μg/mL,与配制偏差为4.12%,RSD为0.85%,表明样品稀释4倍后测定结果准确可靠。
3 应 用
本文建立的方法已用于12名健康志愿者在3个周期里分别单次静脉滴注多尼培南低(0.25 g)、中(0.5g)、高(1.0g)剂量的药动学研究。其低、中、高剂量单次给药的均值药时曲线见图3;尿液中多尼培南平均累积排泄率-时间曲线见图4(低剂量12例,中剂量9例,高剂量8例)。由图可知:多尼培南血药浓度随剂量增加而相应增加,低、中、高剂量尿中24h累积排泄率在70%以上。
4 讨 论
4.1 流动相的选择
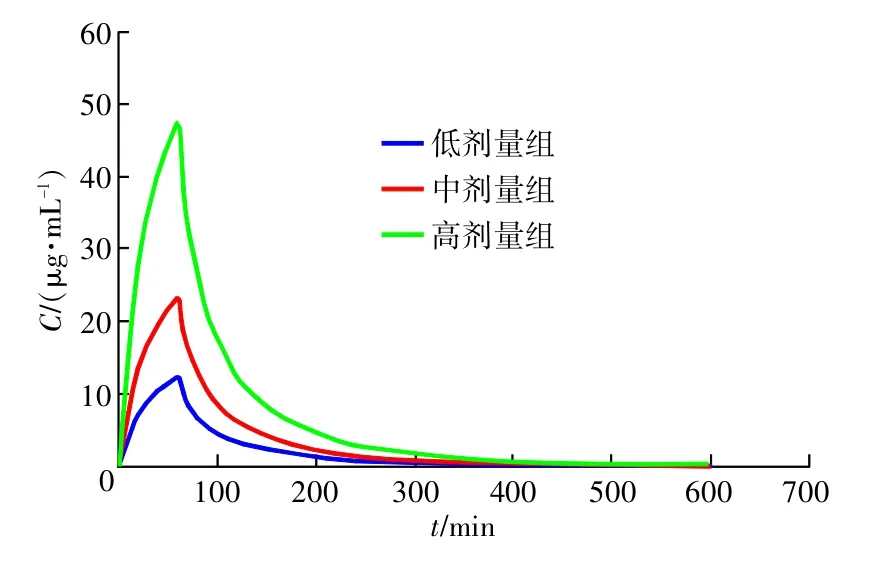
图3 12名健康受试者单次静脉注射DP后的均值药-时曲线
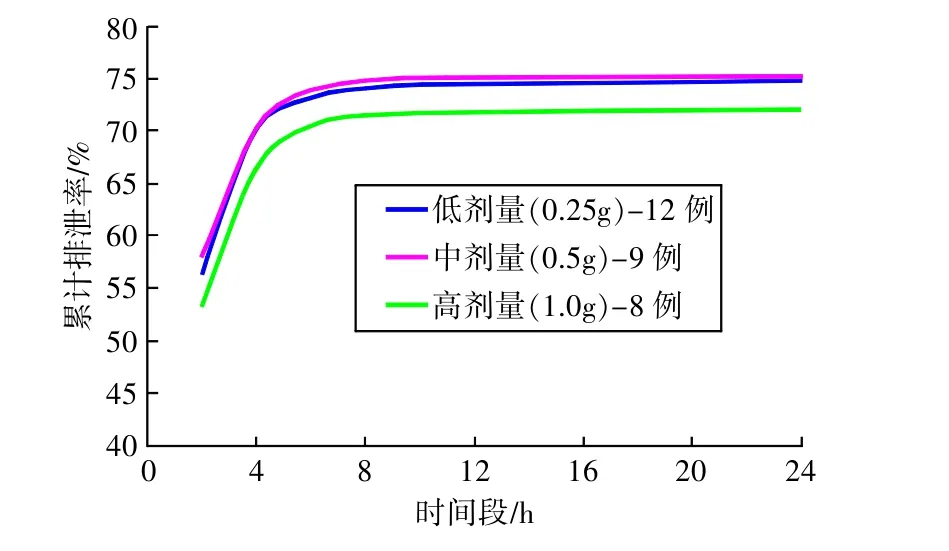
图4 12名健康受试者单次静脉注射DP后的均值尿药累积排泄率曲线
由多尼培南的化学结构可知,多尼培南属于极性较大的化合物。因此所需乙腈量较少,且乙腈量的微小改变对药物及内标的保留时间影响很大。同时,pH对血浆和尿液中的杂质出峰也有较大的影响。流动相选择时分别考察了不同乙腈比例和不同的pH值对出峰的影响,以确保药物、内标与杂质峰能完全分开,并最终选定了本文所用流动相。
4.2 样品预处理方法
DP和内标极性大,不溶于有机溶剂,无法使用液液萃取法。Sutherland C和Iked K等分别采用固相萃取法和超滤法进行样品预处理,固相萃取法和超滤法成本高,重现性较差。本文根据对同类药物样品的预处理经验[7],首先选择用乙腈沉淀蛋白,再用二氯甲烷反洗去除脂溶性杂质和沉淀蛋白的乙腈,离心取上清液直接进样,不仅操作简便、成本低,而且样品没有被稀释,测定的灵敏度高、精密度好。方法优化中考察了沉淀蛋白的乙腈用量以及反洗剂二氯甲烷的体积,确定了上述预处理方法。
4.3 尿液外标法定量
首先考虑采用血样测定方法对尿样进行测定,但由于尿液样品中杂质较多,在DP与内标处均有杂质干扰。通过调节流动相比例及pH,在DP出峰处可避开杂质干扰,但在内标MRP出峰处仍有干扰。用水直接稀释进样,预处理过程简单,操作误差可控,经方法学评价,尿液样品测定采用外标法定量完全符合生物样本测定的相关要求。
5 结束语
本文建立的HPLC-UV法测定血浆及尿液中DP质量浓度,具有样品具有仪器设备要求低、预处理简便、测定结果灵敏准确等特点,适用于DP血药浓度及尿药浓度的测定及药代动力学研究。
[1]朱雪焱.碳青霉烯类抗生素多尼培南及其临床应用[J].世界临床物,2006,27(9):537-551.
[2]Ge Y,Wikler M A,Sahm D F,et al.In vitro antimicrobial activity of doripenem,a new carbapenem[J]. Antimicrob Agents&Chemother,2004,48(4):1384-1396.
[3]Sutherland C,Nicolau DP.Development of an HPLC method for the determination of doripenem in human and mouse serum[J].J Chromatogr,2007,853(1-2):123-126.
[4]Ikeda K,Ikawa K,Morikawa N,et al.Quantification ofdoripenem in human plasma and peritoneal fluid by highperformance liquid chromatography with ultraviolet detection[J].J Chromatogr,2008,867(1):20-25.
[5]和佳鸳.注射用多利培南健康人体药动学研究[J].中国抗生素杂志,2013,38(11):866-870.
[6]唐季红.高效液相色谱-串联质谱法测定人血浆中多尼培南的浓度[J].中国新药与临床杂志,2009,28(5):380-384.
[7]章丽.HPLC-UV法测定人血浆及尿中头孢他美钠的浓度[J].中国抗生素杂志,2013,38(10):756-759.
HPLC-UV determination of doripenem in human plasma and urine
QIN Yongping1,MEI Yajun1,2,ZHANG Li1,MAO Rui1,NAN Feng1,XIANG Jin1,LIANG Maozhi1,YU Qin1
(1.Laboratoryof ClinicalPharmacologyGCPCenterof WestChinaHospital,SichuanUniversity,Chengdu610041,China;2.College of Pharmacy,Chengdu University of TCM,Chengdu 611137,China)
To establish a HPLC-UV method for determining Doripenem(DP)in human plasma and urine to perform DPhuman pharmacokinetic studies.The assay was conducted on a HPLC-UV column of Ultimate XB-C18(150mm×4.6mm×3μm).Mobile phases were 10mmol/L natrium aceticumacetonitrile-triethylamine(94:6:0.1(ν:ν:ν),pH adjusted to be 4.51 with acetic acid)and 8 mmol/L natrium aceticum-acetonitrile-triethylamine(95.5:4.5:0.1(ν:ν:ν),pH adjusted to be 4.99 with acetic acid).The above mobile phases were pumped at the rate of 1mL/min through the column,with the detection wavelength set at 297nm.Plasma samples were deproteinized with acetonitrile,which was extracted and removed with dichloromethane.Meropenem(MRP)was used as the internal standard(IS). Urine samples were diluted in distilled water and then quantified with the external reference method. The plasma concentration was in a linear relationship with the calibration curve within the range of 0.0625-200μg/mL while the quantitation limit was 0.0625μg/mL.The within-run and between-run precisions were 1.0%-6.0%and 3.0%-6.7%,respectively.The method recovery was 92.4%-104.5% and the plasma pretreatment recovery was 91.2%-103.8%.The urine concentration had a linear correlation to the calibration curve in the range of 0.625-4 800 μg/mL while the quantization limit was 0.625 μg/mL.The within-run and between-run precision were 0.7%-4.0%and 1.1%-5.3%,respectively.The method recovery was 94.1%-106.7%.This method is simple and rapid,sensitive and accurate,suitable for determining DPconcentration in human plasma and urine.
doripenem;HPLC;plasma concentration;urine concentration
A
:1674-5124(2015)05-0054-04
10.11857/j.issn.1674-5124.2015.05.014
2014-11-08;
:2015-01-05
秦永平(1963-),男,四川长宁县人,技师,硕士,主要从事体内药物分析工作。
