高效液相色谱法测定银黄口服液中黄芩苷含量及不确定度分析
2015-02-20何玲玲韦国兵胡奇军
何玲玲,韦国兵,胡奇军
(江西中医药大学药学院,江西 南昌 330004)
·论著·
高效液相色谱法测定银黄口服液中黄芩苷含量及不确定度分析
何玲玲,韦国兵,胡奇军
(江西中医药大学药学院,江西 南昌 330004)
目的建立银黄口服液中黄芩苷的定量测定方法,并对所建立方法进行不确定度评价。方法采用高效液相色谱(HPLC)法测定银黄口服液中黄芩苷含量,再根据方法学验证数据,对测定过程中引入的不确定度进行评估,由此计算合成不确定度,最终给出测量结果在95%置信区间下的扩展不确定度。结果采用本方法测定银黄口服液中黄芩苷的扩展不确定度为2.40%。结论建立的黄芩苷HPLC定量测定方法,结果准确且重现性好;建立的不确定度评定适用于HPLC法测定药物中有效成分的不确定度分析。
银黄口服液;黄芩苷;HPLC;不确定度
测量不确定度是表征合理地赋予被测量之间的分散性与测量结果相关联系的参数,是被测量客观值在某一量值范围内的一个评定,其大小决定了测量结果的实用价值[1]。不确定度越小,测量结果的质量越高,实用价值越大。《检测和校准实验室能力的通用要求》规定,检测和校准实验室都必须有对测量结果进行不确定度评定的程序,以对实验测量结果的可信度进行评定。目前,测量不确定度的理论已在国家计量基准、标准物质的研究及仪器校准、化工生产和产品检验等领域得到大力的推广应用,因此正确表达和评定测量方法的测量不确定度正逐步成为国际通行的要求[2]。
当前国内很多学者对银黄口服液中的黄芩苷开展了含量测定[3-5],但很少对其开展不确定度分析。本文根据《测量不确定度评定与表示》[6](JJF1059-1999)中有关规定对高效液相色谱法测定银黄口服液中黄芩苷含量的不确定度进行分析,找出影响其不确定度的因素并对各分量进行评估,最终给出测量结果的置信区间和置信水平,以期加强对含量测定的数据分析和测量结果的准确性和可信度的认识。
1 材料与方法
1.1 仪器与试剂
Agilent 1200高效液相色谱仪(美国Agilent公司),G1314B紫外检测器,GZX-9070 MBE恒温箱,色谱柱Kromasil 100-5C18ODS2(5μm,250 mm×4.6 mm,瑞典Kromasil公司),AB104-N电子天平(瑞士METTER公司);KQ-100型超声波清洗机(江苏昆山超声仪器有限公司)。
金银花、黄芩药材均购自江西省樟树市药材市场,黄芩苷购自中国药品生物检定所(质量分数>98%,批号:110715-201016),甲醇为色谱纯,其他为分析纯;水为双蒸馏水。
1.2 银黄口服液制备
取黄芩和金银花,参照《中国药典,2010版》(一部)[7]进行提取,分别得黄芩提取物和金银花提取物;将黄芩提取物加水适量使之溶解,用8%氢氧化钠溶液调节pH值为8.0,过滤,滤液与金银花提取物合并,用质量分数为8%的氢氧化钠溶液调节pH值到7.2,煮沸1 h,过滤,加入单糖浆适量,加水至全量,摇匀,用质量分数为8%的氢氧化钠溶液调节pH值到7.2,加水至1 000 ml,滤过,灭菌即得银黄口服液样品。
1.3 色谱条件
色谱柱Kromasil 100-5C18ODS2(5μm,250 mm× 4.6 mm)。流动相:甲醇-水-磷酸(45.0∶55.0∶0.2)。检测波长:280 nm;柱温:室温;流速:1 ml/min;理论塔板数按黄芩苷的色谱峰计算不少于2 200。
1.4 溶液制备
1.4.1 对照品溶液的制备精密称取干燥的黄芩苷对照品6.8 mg于25 ml的容量瓶中,加甲醇至刻度,超声20 min,摇匀,定容至刻度,即得到浓度为0.272 mg/mL的对照品溶液。
1.4.2 供试品溶液的制备精密吸取银黄口服液2.0 ml置于25 ml量瓶中,用甲醇稀释至刻度,超声30 min,摇匀过滤,定容至刻度,即得供试品溶液。
1.4.3 阴性样品溶液的制备取金银花按照《中国药典》(2010版,一部)[7]制备工艺制备成相应的阴性样品溶液。
1.5 方法学考察
1.5.1 线性关系考察精密吸取0.272 mg/ml的黄芩苷对照品溶液0.2、0.4、1.0、2.0、3.0和4.0 ml分别置于10.0 ml容量瓶中,加甲醇稀释至刻度,摇匀,分别得到0.00544、0.01088、0.0272、0.0544、0.0816及0.1088 mg/ml的对照品溶液。分别取以上6种对照品溶液各进样10μl,记录色谱图色谱峰面积,以进样量X(μg)为横坐标,峰面积值Y为纵坐标作线性回归,回归方程为:Y=5835.5x-79.640,r=0.9992,表明黄芩苷进样量在0.0000544 mg~0.001088 mg范围内与峰面积呈良好的线性关系。
1.5.2 精密度试验取浓度为0.272 mg/ml的对照品溶液,精密吸取对照品溶液10μl,连续进样6次,按上述色谱条件进行测定,记录峰面积,计算得黄芩苷峰面积的RSD为0.91%。
1.5.3 稳定性试验取配制好的同一供试品溶液分别在0、2、4、6、8、12和24 h进样各10μl,按上述色谱条件进行测定,记录峰面积,计算RSD值,RSD为1.2%,表明供试品溶液室温放置24 h内基本稳定,可以用于样品的重复测定。
1.5.4 重复性试验取同一批号银黄口服液样品(批号:140608)6份,精密吸取,按上述方法进行测定,测得黄芩苷含量为0.09449 mg/ml,RSD为1.3%。1.5.5回收率试验取同一批号银黄口服液样品(批号:140710)6份,再分别用移液管精密移取1 ml溶液于3只10 ml容量瓶中,进行编号。再分别用移液管量取对照品溶液(0.272 mg/ml)相当于供试品溶液质量的80%、100%及120%于上述3个容量瓶中,摇匀,按样品溶液制备项下操作,进样、记录色谱峰面积并计算回收率。见表1。
1.6 样品测定
精密量取对照品与样品溶液(批号:140608、140609及140610)各10μl,注入液相色谱仪,按上述方法测定,按照外标法根据峰面积计算样品中黄芩苷的含量,结果见表2。
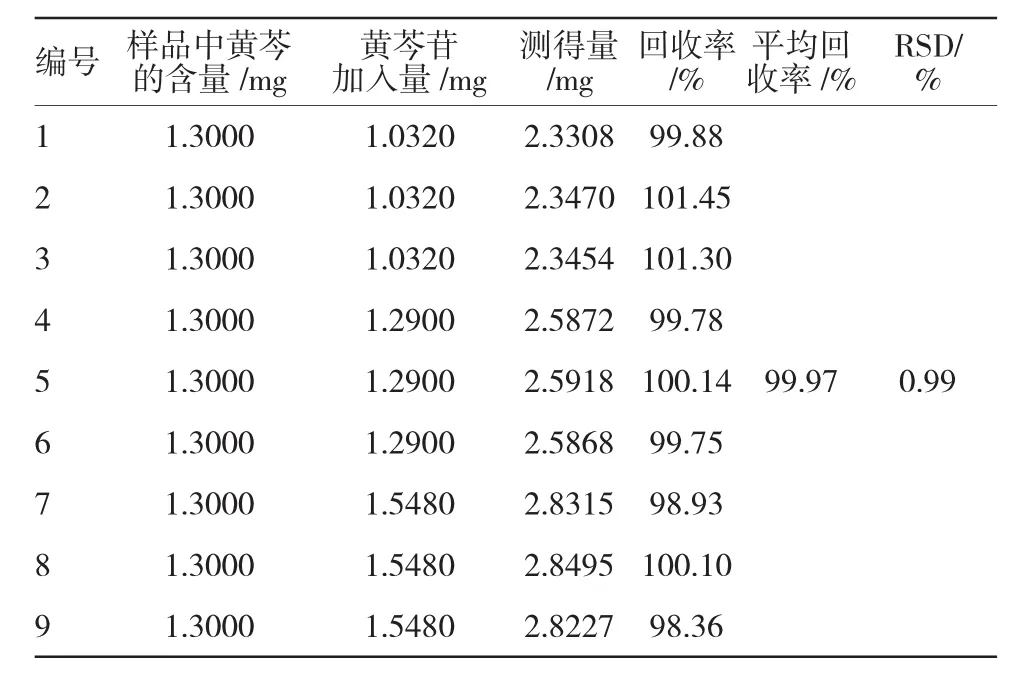
表1 回收率试验结果
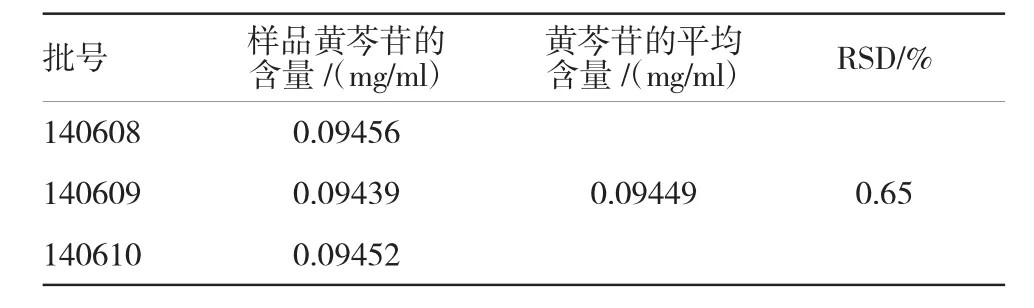
表2 样品含量测定结果(n=3)
2 不确定度评定
2.1 不确定度来源分析
不确定度分量主要来源于测量过程中样品与对照品的质量不确定度、体积引入的不确定度、样品回收率影响引入的不确定度、液相测试过程随机效应带来的不确定度。采用重复性研究数据及实验准确度的回收率试验数据,将涵盖所有样品制备与检测过程中随机效应及仪器操作、样品基质等因素的系统误差所引起的不确定度进行评定。
2.2 不确定度分量量化
2.2.1 试验方法精密度相对标准不确定度测定根据试验方法学对重复性试验数据进行验证,采用公式(1)对测定方法中精密度不确定度进行评定。
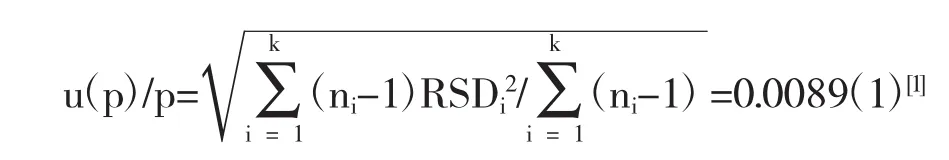
u(p)/p为相对标准不确定度,RSDi为样本i的相对标准偏差,ni为样本i的重复测定次数
2.2.2 试验方法准确度相对标准不确定度测定u(Rm)/(Rm)试验方法准确度是通过加样回收率试验测定的,回收率不确定度按照公式(2)评定。

回收率试验中对照品溶液的配制是采用的是十万分之一电子天平精密称量对照品12.9 mg定容于10 ml容量瓶中,采用2 ml移液管分别吸取0.8,1.0,1.2 ml加至样品溶液中,所有引入的不确定度u(mspike)/(mspike)包括对照品称量u(m)、对照品溶液配制u(V1)与对照品溶液的移取u(V2)共3部分所引入的不确定度。
电子天平称量允许的误差为±0.1 mg,对允许误差采用矩形分布计算示值不确定度,对标准偏差采用正态分布的计算称量重复性不确定度。国家计量检定规程规定2 ml单标移液管、10 ml量瓶的容量允许误差分别为0.01及0.02 ml,样品稀释过程中校准不确定度及量器允差按三角分布计算,采用试验中各规格量器重复吸取各标称容量蒸馏水共6次,以质量所得出的标准偏差,按正态分布计算其不确定度,对照品溶液配制的相对不确定度评定结果见表3。
2.2.3 计算对照品加入量的相对标准不确定度为
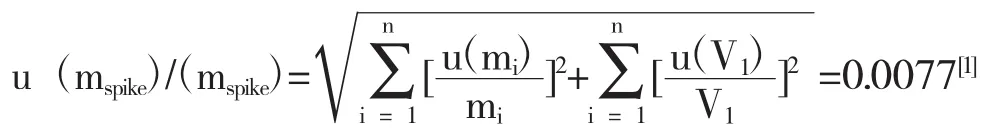
试验方法准确度不确定度u(Rm)根据公式2评定,结果Rm=99,97%,mobs=1.2896mg,量取对照品溶液相当于供试品溶液质量的80%、100%及120%进行3组试验,每组试验的方差分别为S1=0.0089 mg、S2=0.0028 mg、S3=0.0137 mg,所以合并方差Sp=0.0096 mg,u(mspike)/(mspike)=0.0077,u(Rm)/(Rm)=0.0081。
2.2.4 计算合成不确定度由上述各不确定度分量合成银黄口服液中黄芩苷定量相对不确定度为[8]:
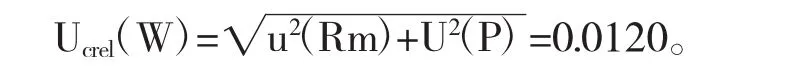
2.2.5 扩展不确定度及报告不确定度95%置信概率下取包含因子k=2,则相对扩展不确定度U95(W)=k×U=0.0240=2.40%。由实验所测银黄口服液中黄芩苷的含量W=0.09449 mg/ml,故其扩展不确定度为:U95=0.009449×0.0240=0.00023 mg/ml,本次实验所测银黄口服液中黄芩苷的含量为:W=(0.09449±0.00023)mg/ml。
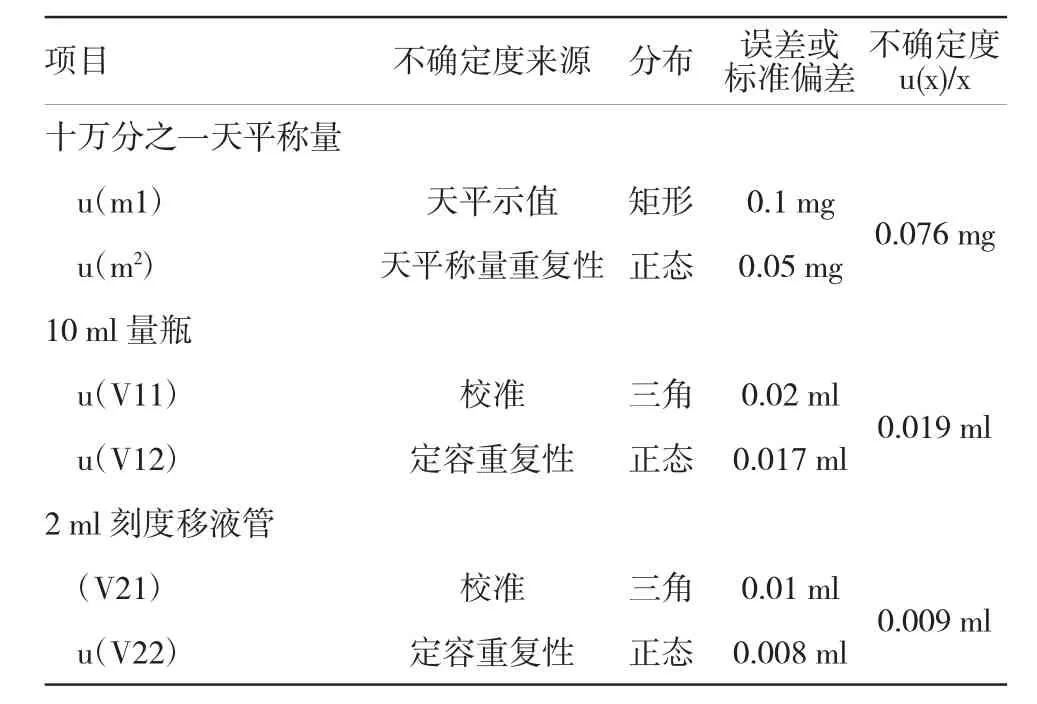
表3 对照品溶液配制的相对不确定度
3 讨论
选取银黄口服液为研究对象,建立其有效成分黄芩苷的含量测定方法,根据不确定度理论对回收率试验及方法重复性不确定度评定,并于95%可信空间下得出该法测定含量结果扩展的不确定度为(W×2.40%)mg/ml,对试验方法可信度进行定量描述,可作为银黄口服液中测定黄芩苷含量方法学验证的补充[9]。
本实验不确定度分析中,从不确定度量化及表3对照品溶液配制的不确定可以看出,本方法测定黄芩苷结果各分量的不确定度均较小,而测量银黄口服液中黄芩苷结果的不确定度主要来自测量过程中样品与对照品的质量不确定度、对照品溶液配制的不确定度、样品回收率影响引入的不确定度等,其中影响最大的来自对照品溶液配制的不确定度[10]。因此在本实验操作中为减小操作过程中因实验操作者熟练程度产生的不确定度,在实验操作过程中还需增强操作者的实验操作熟练程度,并尽量避免小容量体积溶液的配制、量取、定容,从而减少因实验操作引入的不确定度。同时在数据分析中采用方差分析以进一步判断不确定度分析中一个独立变量是否受到一个或多个变量因素的影响,从而判断结果不确定度是一个因素的作用还是多个因素的交互作用,从而较真实的反映实验操作过程对结果的影响,并避免复杂实验操作中对各个实验操作开展不确定度的分析,从而减少不确定度分析的工作量,以达到对各分量进行快速准确的不确定度分析的评估目的。
在药物分析检测评定不确定度时,应尽可能的分析产生不确定度的所有可能来源。目前,分析测试领域中多采用对每个测定步骤的分析以得出测定结果的不确定度。但由于化学分析操作相对较复杂,需附加试验后再进行B类不确定度的评定,而且其测定过程中对A类不确定度也较难评定,本实验通过实验室内部方法学验证法的数据进行评定,通过采用方法学考察的准确度与精密度试验,整体考察检测方法的不确定度,为实际生产中药物分析提供参考。
[1]国家质量技术监督局.测量不确定度评定与表示指南[M].北京:中国计量出版社,1999:34-42.
[2]中国国家标准化管理委员会.检测和校准实验室能力的通用要求(GB/T27025-2008)[S].北京:中国标准出版社,2008:1-6.
[3]朱啸风,孙钦美,刘景俊.银黄口服液中黄芩苷和绿原酸含量的测定[J].齐鲁药事,2004,23(6):25-26.
[4]桑旭峰,吴海雯,徐奇超.HPLC同时测定银黄口服液中绿原酸和黄芩苷含量[J].中成药,2005,27(1):96-98.
[5]韦国兵,胡奇军,廖夫生.HPLC法测定银黄口服液中黄芩苷含量[J].江西师范大学学报,2013,35(5):79-82.
[6]国家质量技术监督局.JJF 1059-1999测量不确定度评定与表示[S].北京:中国计量出版社,1999:1-11.
[7]国家药典委员会.中华人民共和国药典[S].一部.北京:中国医药科技出版社,2010:1082-1083.
[8]韦国兵,胡奇军,张秀秀.HPLC测定银黄颗粒中绿原酸含量及不确定度分析[J].江西中医药大学学报,2014,26(5):60-63.
[9]李卓,李湘斌.反相HPLC法测定咽喉炎合剂中黄芩苷的含量[J].中南医学科学杂志,2010,38(4):64-65.
[10]田冀媛.HPLC-MS法测定人血浆奥美拉唑的水平[J].中南医学科学杂志,2008,36(3):52-55.
Determination of Baicalin in Yinhuang Oral Liquid by HPLC and evaluation of its measurement uncertainty
Ling-ling HE,Guo-bing WEI,Qi-jun HU
(Pharmacy College,Jiangxi University of Traditional Chinese Medicine, Nanchang,Jiangxi 330004,P.R.China)
【Objective】To establish a HPLC method for the determination of Baicalin in Yinhuang Oral Liquid and carry on the Uncertainty Analysis to the HPLC method.【Methods】The HPLC method is adopted to measure the content of Baicalin,and the data is verified in terms of methodology.Then the uncertainty,which is drawn into during the process of the determination,will be evaluated.As a result,the combined uncertainty can be worked out. The uncertainty is calculated under 95%confidence interval.【Results】The uncertainty of Baicalin in Yinhuang O-ral Liquid is 2.40%by adopting this method.【Conclusion】The HPLC method established for Baicalin is accurate and reproducible,and the established uncertainty analysis can be applied to the uncertainty analysis of high performance liquid chromatography method in the determination of active ingredient in drugs.
Yinhuang Oral Liquid;Baicalin;HPLC;uncertainty
1005-8982(2015)34-0015-04
R944.5
A
2015-03-12
江西省卫生和计划生育委员会项目(No:2014A008),江西中医药大学中医药专项(No:ZX1013)
