微波协同固体超强酸催化合成香料肉桂酸环己酯
2015-02-16屈飞强任晓琼李建华吴文芳
黄 飞,屈飞强,任晓琼,李建华,吴文芳
(黄山学院 化学化工学院,安徽黄山 245041)
微波协同固体超强酸催化合成香料肉桂酸环己酯
黄 飞,屈飞强,任晓琼,李建华,吴文芳
(黄山学院 化学化工学院,安徽黄山 245041)

肉桂酸环己酯,固体超强酸,微波协同,催化合成
肉桂酸环己酯是一种无色粘稠液体,不溶于水,难溶于丙二醇,易溶于乙醇,具有特殊的鲜水果香气,广泛用于软饮料、烘烤食品、香料等领域,属于典型的常用香料和食品添加剂[1-3]。肉桂酸环己酯具有清除活性氧、抑制食品氧化、防止DNA受损伤等药理活性,可用作医药中间体及化妆品配方[4-8]。

1 材料与方法
1.1 材料与仪器
肉桂酸、环己醇、氨水、三氯化铁、氯化亚锡、对甲苯磺酸、浓硫酸、硫酸氢钠、无水硫酸镁、无水碳酸钠、氯化钠、氢氧化钠均为分析纯;四氯化钛、MCM-41中孔分子筛、聚乙二醇-400均为化学纯;La2O3纯度为99.99%。
NICOLET-380傅里叶变换红外光谱仪 美国尼高力公司;AVANCE-400MHZ核磁共振仪 德国布鲁克公司;CE-400元素分析仪 美国EAI公司;SHZ-D(III)循环水式真空泵 河南巩义市予华仪器制造有限公司;MCR-3型微波化学反应器 上海微波炉有限公司;RE-2000E旋转蒸发仪 河南巩义市予华仪器制造有限公司;马弗炉 上海仪器仪表有限公司。
1.2 实验原理


图1 肉桂酸环己酯合成原理图Fig.1 Schematic diagram for the synthesis of cyclohexyl cinnamate
1.3 实验方法

1.3.2 肉桂酸环己酯的催化合成 在装有分水器的100mL三颈烧瓶中,加入一定量的肉桂酸、环己醇和催化剂,并在分水器中加环己醇至支管口处,置于微波反应器中。设定微波反应器一定功率和一定微波时间,进行辐射回流反应。反应完成后得到淡黄色混合物,冷却至室温,分别用饱和食盐水溶液、饱和碳酸钠溶液洗涤数次,用无水硫酸镁干燥,处理后经减压蒸馏,蒸出未反应的环己醇,收集195℃/1.6kPa下的馏分得到无色肉桂酸环己酯。称量,计算产率。
产率(%)=液体产物质量/合成肉桂酸环己酯理论质量×100。
1.3.3 单因素实验 采用单因素实验分别考察催化剂种类、催化剂用量、肉桂酸与环己醇物质的量比、微波功率、微波时间等因素对催化合成肉桂酸环己酯的影响。







表1 正交实验的因素和水平表Table1 Factors and levels of orthogonal experiment
1.4 数据统计分析
根据单因素实验和正交实验,所有的实验均重复3次,利用统计分析软件正交实验助手IIv3.1和Excel软对实验结果进行统计和分析。
2 结果与讨论
2.1 单因素实验


表2 催化剂种类对肉桂酸环己酯产率的影响Table2 Effect of the type catalyst on the esterification
2.1.2 肉桂酸与环己醇物质的量比对肉桂酸环己酯产率的影响 由图2可知,肉桂酸与环己醇的酯化反应为可逆反应,增加肉桂酸与环己醇物质的量比有利于酯化反应向右进行,从而提高了肉桂酸环己酯产率。当肉桂酸与环己醇物质的量比为1∶4时,肉桂酸环己酯产率达到最高;继续增加肉桂酸与环己醇物质的量比,肉桂酸环己酯产率反而迅速下降,这可能由于肉桂酸与环己醇物质的量比过大,使得体系内肉桂酸浓度降低,从而降低了肉桂酸酯化反应速率,使肉桂酸环己酯产率迅速下降。因此肉桂酸与环己醇的最佳物质的量比为1∶4。

图2 肉桂酸与环己醇物质的量比对肉桂酸环己酯产率的影响Fig.2 Effect of the molar ratio of cinnamic acid and cyclohexanol on the esterification


图3 催化剂用量对肉桂酸环己酯产率的影响Fig.3 Effect of catalyst amount on the esterification
2.1.4 微波功率对肉桂酸环己酯产率的影响 由图4可知,肉桂酸环己酯的产率随着微波功率的升高逐渐升高,表明肉桂酸环己酯的产率与微波功率呈正比例关系,这是由于高功率微波对反应物分子内加热效率高、有效反应时间长,因此肉桂酸环己酯的产率逐渐升高。但是微波功率不是越高越好,微波功率过高可能会引起副反应发生,从而降低产物的产率[21],此外考虑到合成工艺的能耗问题,因此确定微波功率500W为肉桂酸环己酯合成的适宜条件。

图4 微波功率对肉桂酸环己酯产率的影响Fig.4 Effect of microwave power on the esterification
2.1.5 微波时间对肉桂酸环己酯产率的影响 由图5可知,微波时间对肉桂酸环己酯产率有显著影响。随着微波时间的增加,肉桂酸环己酯的产率急剧增加,说明肉桂酸环己酯的酯化反应需要一定的微波时间才能完成,当微波时间为20min,肉桂酸环己酯的产率达到最高;继续延长微波反应时间,其产率反而有所下降,说明微波时间过长,反应体系内会有水解等副反应发生,降低了肉桂酸环己酯的产率,因此微波时间不是越长越有助于肉桂酸环己酯的酯化反应。综合考虑肉桂酸环己酯的产率和微波反应的能耗,最佳微波时间为20min。

图5 微波时间对肉桂酸环己酯产率的影响Fig.5 Effect of microwave time on the esterification
2.2 催化合成肉桂酸环己酯的工艺优化


表3 合成肉桂酸环己酯正交实验表及结果Table3 Orthogonal experiment results of synthesis of cyclohexyl cinnamate
2.2.2 方差分析 方差分析,又称变异数分析或F检验,用于两个及两个以上样本均数差别的显著性检验。由表4方差分析可得出:肉桂酸与环己醇物质的量比、催化剂用量对实验结果影响非常显著;微波功率和微波时间对实验结果影响不显著。各因素对实验结果的影响显著性次序为:因素A(肉桂酸与环己醇物质的量比)>因素B(催化剂用量)>因素C(微波功率)>因素D(微波时间)。
由极差和方差分析可以得出:肉桂酸与环己醇物质的量比对肉桂酸环己酯的产率影响最大,当肉桂酸与环己醇物质的量比为1∶4时产率最高。催化剂用量对催化合成肉桂酸环己酯次于肉桂酸与环己醇物质的量比的影响,且随着肉桂酸与环己醇物质的量比的增加,肉桂酸环己酯的产率逐渐升高。微波功率和微波时间对合成肉桂酸环己酯也有影响,但影响度不显著。
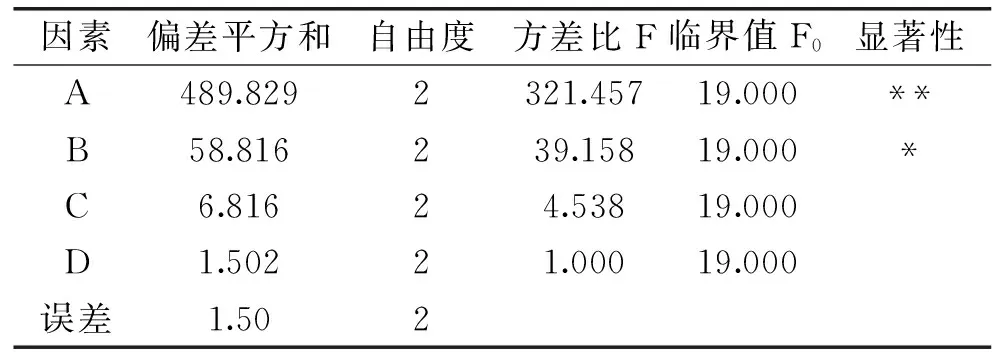
表4 肉桂酸环己酯正交实验方差分析Table4 Analysis of variance for the cyclohexyl cinnamate
注:F0.05(2,2)=19.00。
2.3 产品分析
2.3.1 元素分析 经过元素分析仪测定,肉桂酸环己酯(C15H18O2)测定值(计算值)为C 78.28%(78.26%),H 7.85%(7.83%)。
2.3.2 红外光谱图分析 反应目标产物肉桂酸环己酯为无色粘稠液体,用KBr压片法测定其红外光谱,其结果如图6所示。

图6 肉桂酸环己酯的红外光谱图Fig.6 IR spectra of cyclohexyl cinnamate
由图6可知,在2932、2856cm-1为环己基中C-H的特征吸收峰;1697cm-1为C=O的吸收峰;1637cm-1为C=C的吸收峰;1363、1179cm-1为C-O-C的吸收峰;1578,1496,1450cm-1为苯环骨架C=C的吸收峰;968cm-1为反式CH=CH的吸收峰。上述各官能团的特征吸收峰与文献中目标产物的主要官能团的吸收峰一致[11]。
2.3.3 核磁氢谱分析1H-NMR:TMS为内标,CDCl3为溶剂,δ1.22-1.91(10H,-CH2),δ3.71(1H,O-C-H),δ6.41(1H,=C-H,靠近苯环),δ7.25-7.28(5H,Ar-H),δ8.49(1H,=C-H,靠近羰基),其核磁氢谱图如图7所示。经解析可知,该产品为肉桂酸环己酯。
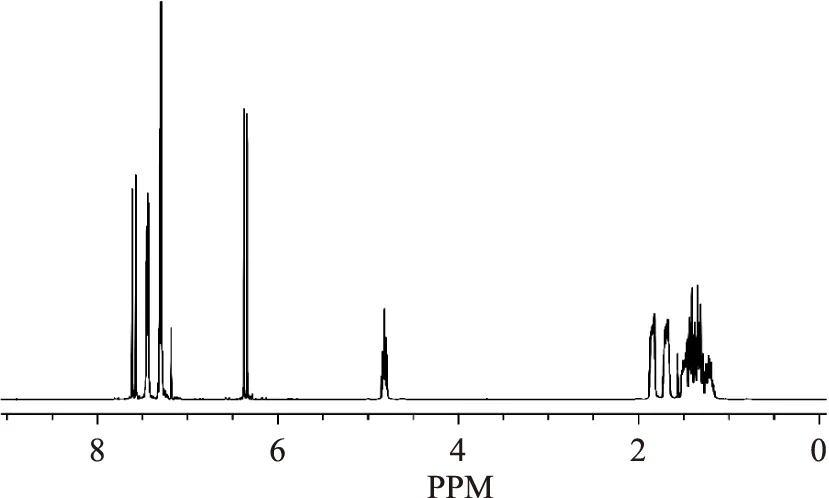
图7 肉桂酸环己酯的1H-NMR图Fig.7 1H-NMR of cyclohexyl cinnamate
3 结论

[1]许戈文,李布青.合成香料产品技术手册[M].北京:中国商业出版社,1996:369.
[2]济南市轻工业研究所编译.合成食用香料手册[M].北京:轻工业出版社,1985:644.
[3]Bhatias P,Wellington G A,Cocchiara J,et al. Fragrance material review on isoamyl cinnamate[J]. Food and Chemical Toxicology,2007,45(1):98-101.
[4]刘金,张立伟.肉桂酸衍生物抗氧化剂对·OH引发的DNA损失的防护作用[J].食品科学,2006,27(9):49-51.
[5]赵春贵,张立伟,王晖,等.肉桂酸及其衍生物抗氧化活性研究[J].食品科学,2005,26(1):218-222.
[6]Cartron E,Carbonneau M A,Fouret G,et al. Specific antioxidant activity of caffeoyl derivatives and other natural phenolic compounds:LDL protection against oxidation and decrease in the proinflammatory lysophosphatidylcholine production[J]. Journal of Natural Products,2001,64(4):
480-486.
[7]Baderschneider B,Winterhalter P. Isolation and characterization of novel benzoates,cinnamates,flavonoids,and lignans from riesling wine and screening for antioxidant activity[J]. Jouranl of Agricultural and Food Chemistry,2001,49(6):2788-2798.
[8]张立伟,赵春贵,杨频.肉桂酸衍生物清除羟基自由基活性研究[J].中国医院药学杂志,2004,24(11):662-663.
[9]俞善信,李豪雄,曾盈.氯化铁催化合成肉桂酸环己酯[J].陕西化工,1999,28(1):11-12,24.
[10]王永红,钟国伦,楼岳年,等.肉桂酸环己酯的合成研究[J].化学研究与应用,2002,14(5):552-553,574.
[11]张富捐,盛淑玲,张翔宇.对甲苯磺酸催化合成桂皮酸环己酯[J].化工时刊,2004,18(7):61-62.
[12]高艳萍.氯化亚锡催化合成肉桂酸环己酯的研究[J].化工时刊,2008,22(11):40-41,49.
[13]高艳萍.硫酸氢钠催化合成肉桂酸环己酯[J].安阳师范学院学报,2008,(2):75-77.
[14]唐晓红,李保军,李成未,等.肉桂酸环己酯的新催化合成[J].化学世界,2013,54(3):148-151.
[16]周芳,赵鑫,宫婕,等.响应面法优化微波辅助提取红皮云杉多酚工艺[J].食品工业科技,2014,35(10):275-283.
[17]曹崇江,鞠兴荣,刘晓庚.微波协同固体酸合成肉桂酸异丙酯[J].食品科学,2013,34(24):1-5.
[18]赵二劳,吴晓鹏,赵昀,等.微波-表面活性剂协同提取金莲花黄酮的研究[J].精细化工,2010,27(11):1069-1072.
[19]黎彧,黄伟乾,陶文成,等.微波辅助合成肉桂酸异丙酯的新工艺[J].精细石油化工,2008,25(1):54-56.

[21]李延,李丕高.微波辐射合成食品防腐剂富马酸单环己酯[J].食品科学,2011,32(16):375-378.
Microwave-assisted catalytic synthesis of cyclohexyl cinnamate by solid superacid catalyst
HUANG Fei,QU Fei-qiang,REN Xiao-qiong,LI Jian-hua,WU Wen-fang
(College of Chemistry and Chemical Engineering,Huangshan University,Huangshan 245041,China)

cyclohexyl cinnamate;solid superacid;microwave-assisted;catalytic synthesis
2014-08-21
黄飞(1983-),男,硕士研究生,助教,主要从事有机化学催化合成研究。
国家自然科学基金项目(21071005,21271006);国家级大学生创新创业训练计划项目(201410375003);安徽省大学生创新创业训练项目(AH201310375027);黄山学院自然科学研究项目(2012xkj006)。
TS202.3
A
:1002-0306(2015)09-0204-05
10.13386/j.issn1002-0306.2015.09.036
