银杏内酯B冻干粉针处方和冻干工艺的研究
2015-01-16袁海建安益强陈宜刚
袁海建, 安益强, 王 卉*, 陈宜刚
(1.泰州职业技术学院,江苏泰州225300;2.徐州医学院,江苏徐州221000)
银杏内酯B冻干粉针处方和冻干工艺的研究
袁海建1, 安益强2, 王 卉1*, 陈宜刚1
(1.泰州职业技术学院,江苏泰州225300;2.徐州医学院,江苏徐州221000)
目的对银杏内酯B冻干粉针剂处方和冻干工艺进行研究。方法选取助溶剂聚乙二醇400用量 (A)、增溶剂聚乙二醇-12-羟基硬脂酸酯用量 (B)和赋型剂甘露醇用量 (C)为主要考察因素,以药液中银杏内酯B、制剂溶解性为评价指标,建立L9(34)正交实验以确定最优处方;以药液共熔点、成品冻干情况和残余水分为质量评价指标,确定最优的冻干工艺。结果最优处方为A3B2C3;最优冻干工艺为预冻温度-45℃,保持4 h,升华干燥以0.1℃/min的速率升温至-15℃,保持12 h,解吸附干燥升温至30℃,保持6 h。以最优处方和冻干工艺制备的3批银杏内酯B冻干粉针样品的外观良好均一,复溶性好,含量和有关物质等指标均符合要求。结论该处方及冻干工艺的可行性和重现性较理想,可为新药的研制和申报奠定基础。
银杏内酯B;冻干粉针剂;处方筛选;冻干工艺研究
银杏内酯(ginkgolides,GG)是银杏叶提取物中主要的活性成分,对血小板活化因子 (PAF)受体有较强的拮抗作用,并具有多种显著的药理活性,在心脑血管系统疾病的治疗上效果理想,有良好的临床应用前景[1]。目前,国内已有相应银杏内酯注射液上市,受到广泛的应用[2-3],但冻干粉针尚未上市。从药物稳定性、储存和运输方面考虑,冻干粉针要优于注射液,且银杏内酯中的银杏内酯B(ginkgolide B,GB)为主要药效成分,拮抗PAF受体的作用最强[4],故本实验选用银杏内酯B进行冻干粉针处方筛选和工艺的研究,为其研制和申报奠定基础。
1 仪器与试药
Triad 2.5L冷冻干燥机(美国Labcono公司);电子天平(美国梅特勒-托利多公司);RCT basic电磁搅拌器(德国IKA公司);Q2000差示量热扫描仪 (美国TA公司);ZS90纳米粒度仪 (英国马尔文仪器有限公司);Agilent 1200型高效液相色谱仪(美国Agilent Techologies公司);C20卡尔费休水分测定仪 (美国梅特勒-托利多公司)。
银杏内酯B(南京海陵中药制药工艺技术研究有限公司,纯度≥98%);注射级聚乙二醇400(南京威尔化工有限公司);注射级甘露醇 (法国罗盖特公司);聚乙二醇-12-羟基硬脂酸酯 (德国BASF公司);注射用水 (焦作市康华药业有限公司);乳糖、葡萄糖、海藻糖为分析纯(国药集团化学试剂有限公司)。
2 方法与结果
2.1 处方研究
2.1.1 规格确定 根据目前正在进行临床三期研究的由中国人民解放军总医院开发的一类新药银杏内酯B注射液,确定其规格为40 mg/支。
2.1.2 制备方法确定 取处方量的银杏内酯B原料药溶解于一定量助溶剂和增溶剂中,另取适量赋型剂溶于注射用水中,搅拌状态下滴加到前一溶液,混匀后即得药液。后经除热源过滤、除菌过滤、灌装、冻干、压塞和轧盖,即得银杏内酯B冻干粉针制剂。
2.1.3 助溶剂选择 由于银杏内酯B在水中的溶解度极低,小于0.1 mg/mL[5],而制备冻干制剂所配的溶剂通常为水,且溶剂量不能过大,所以需要用助溶剂来增加银杏内酯B的溶解度。本实验研究发现,银杏内酯B在聚乙二醇400、丙二醇和乙醇中均有较高的溶解度,但考虑到冻干制剂的特殊性,需复溶成溶液才能进行注射给药。由于丙二醇和乙醇的沸点较低,在干燥阶段容易升华,导致难以复溶,故采用聚乙二醇400作为助溶剂,参考FDA IIG和The Handbook of Pharmaceutical Excipients数据,其用量的体积分数不超过11.25%。
2.1.4 增溶剂选择 取处方量的银杏内酯B溶于一定量聚乙二醇400中,搅拌状态下滴加处方量的注射用水,由于此时药物会大量析出,故需一定增溶剂来增加药物在水中的溶解度。目前用于注射制剂中常用的增溶剂有吐温80、聚氧乙烯氢化蓖麻油、聚乙二醇-12-羟基硬脂酸酯[6]。研究表明[7],相对于吐温80和聚氧乙烯氢化蓖麻油,聚乙二醇-12-羟基硬脂酸酯因其组胺释放少、溶血作用低、增溶能力高而受到越来越多的关注和重视,因此实验选用聚乙二醇-12-羟基硬脂酸酯作为本制剂的增溶剂,参考国外毒理研究和注射剂临床研究的规定[7-8],设定其用量的体积分数不超过10%。
取处方量的银杏内酯B原料药溶解于体积分数为10%的聚乙二醇400和体积分数为10%的聚乙二醇-12-羟基硬脂酸酯中,搅拌状态下滴加处方量的注射用水,制备得到澄清透明药液。然后将其冷藏,避光放置12 h,有关物质和溶液的澄清度无明显变化,也无固体析出,说明其稳定性良好。
2.1.5 赋型剂筛选 常用的冻干赋型剂有甘露醇、乳糖、葡萄糖、海藻糖,用量大致相当[9]。本实验选用体积分数为5%的各种赋型剂,在其他因素均相同的情况下,分别制备和冻制,结果见表1。由表可知,甘露醇为较理想的赋型剂。

表1 赋型剂筛选结果
2.1.6 处方正交筛选 根据前期研究结果,以助溶剂用量(A)、增溶剂用量 (B)和赋型剂用量 (C)为主要考察因素,以冻干前药液中银杏内酯B的含有量 (过0.22μm滤膜后进行检测)、制剂溶解性为评价指标,建立L9(34)正交试验,因素水平见表2,实验结果见表3。由表可知,以药液中银杏内酯B的含有量的直观极差分析,影响大小为A>B>C,最佳处方为A3B3C3;以制剂溶解性的直观极差分析,影响顺序为B>C>A,最佳处方为B2C2A2。
银杏内酯B采用HPLC法测定,外标法计算其含有量。色谱条件为Agilent ZORBAX SB-C18(4.6 mm×150 mm,5μm)色谱柱;流动相为乙腈-0.02%氨水 (30∶70);体积流量1.0 m L/m in;柱温30℃;检测波长225 nm;进样体积10μL。供试品溶液配制方法为取药液适量,过0.22 μm滤膜,续滤液用乙腈稀释10倍,混匀后离心,取上清液即得。对照品溶液配制方法为精密称取银杏内酯B对照品10 mg,置于10 mL量瓶中,乙腈溶解并稀释定容至刻度,混匀后即得。
另外,方差分析结果见表4。银杏内酯B的含有量表明,只有A因素有显著性差异 (P<0.05),以A3为最佳;溶解性表明,只有B因素有显著性差异 (P<0.05),以B2为最佳;C因素 (即甘露醇的用量)在两个评价指标中均无显著性差异 (P>0.05),但发现当其用量为8%时,冻干饼状物的外观更饱满,而且品质更优良,故甘露醇用量选择为8%。综上所述,确定最佳的工艺处方为A3B2C3,即聚乙二醇400用量为10%,聚乙二醇-12-羟基硬脂酸酯用量为6%,甘露醇用量为8%。

表2 因素水平
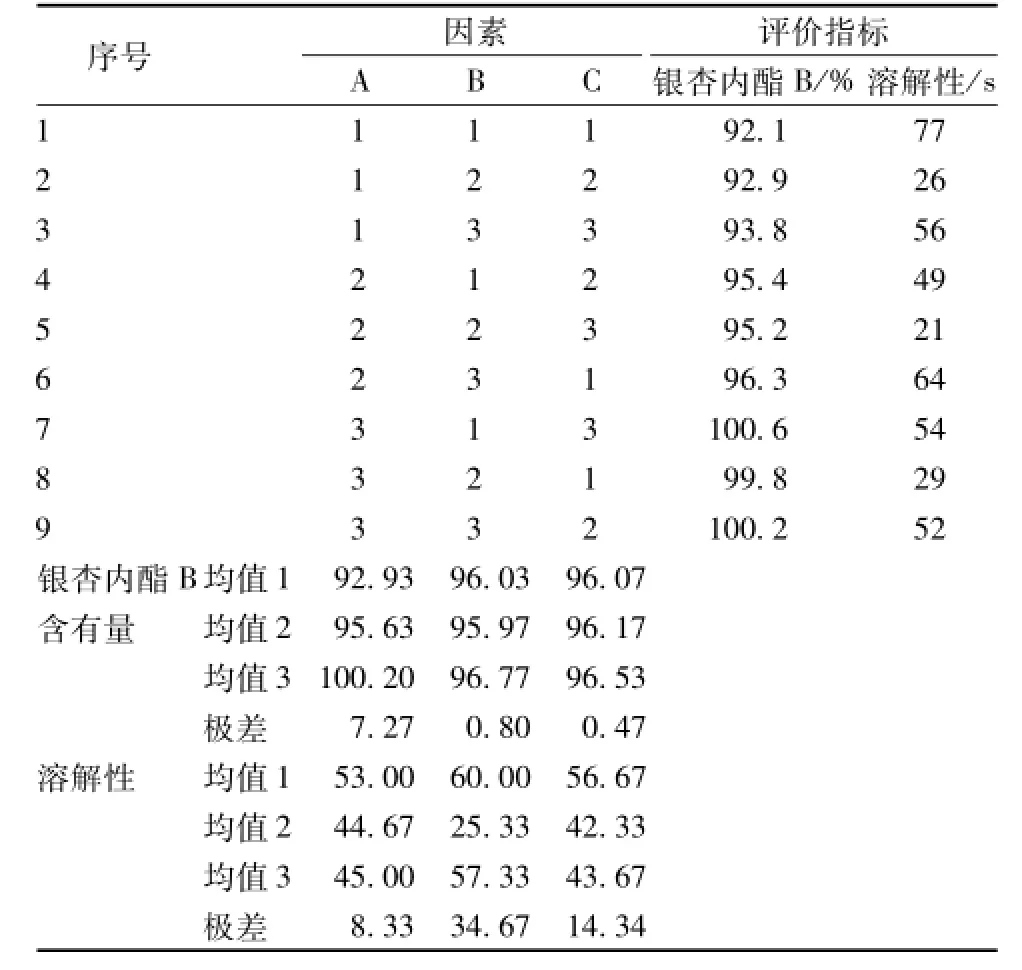
表3 正交实验结果

表4 方差分析结果
2.2 冻干工艺的研究
2.2.1 共熔点的测定 采用DSC法进行测定。取少量最优处方配制的药液于样品皿中,以空样品皿为参比,-50℃下保持10 min后开始升温,升温速率为1℃/min,结果见图1。由图可知,经 -50℃预冻的处方溶液在-14℃时开始发生熔融吸热,说明最低共熔点为-14℃,而样品溶液预冻温度应至少低于20℃ (最低共熔点)时[10],才能充分预冻,故本制剂预冻温度设定在-45℃。
2.2.2 工艺的研究 研究发现,在预冻温度-45℃,保持3 h时,样品溶液就能完全冻实。升华干燥阶段升温速率不能过高,否则会导致喷瓶,最终确定升温速率为0.1℃/min,升至-15℃,保持至少12 h,此条件下水分基本升华完全,且无喷瓶现象发生。在解吸附干燥阶段,采用25℃,保持至少6 h,此条件下样品水分能控制在3%以下。
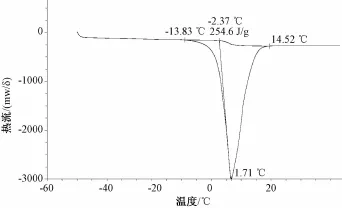
图1 共熔点测定结果
2.3 验证试验 按照最优处方,即聚乙二醇400用量10%、聚乙二醇-12-羟基硬脂酸酯用量 6%、甘露醇 50 mg/mL,根据 “2.1.2”项工艺配制银杏内酯B药液,每个西林瓶灌装4 mL药液,批量为1 000支,采用最优冻干工艺进行冻制。(1)预冻:温度-45℃,保持4 h。(2)升华干燥:以0.1℃/min升温至-15℃,保持12 h。(3)解吸附干燥:升温至30℃,保持6 h。结果发现,3批样品外观均为类白色疏松块状物,冻干前银杏内酯B含有量分别为100.2%、99.8%和100.1%,制剂溶解性分别为18 s、20 s和17 s,说明该处方符合要求,且重复性良好。另外,成品制剂的银杏内酯B含有量均在95.0%~105.0%之间,而且有关物质、无菌、内毒素均符合规定,其他各项指标也均符合冻干制剂的相关规定。
3 讨论
本研究对银杏内酯B冻干粉针的处方和工艺进行研制,取得了较理想的结果,解决了银杏内酯B注射液的一些不足,应用前景较为广泛。在本实验中,应用聚乙二醇400和聚乙二醇-12-羟基硬脂酸酯来解决银杏内酯B在水中溶解度非常差的问题,用量均在安全用量范围,而且在国内均有市售的相应注射级辅料,安全性有所保障,能满足国内临床新药的申报要求。
用水对该制剂复溶后,药液用纳米粒度仪进行粒径检测,结果见图2。由图可知,复溶后药液中微粒的粒径均在10 nm以下。由此推测,在制备过程中可能形成一个稳定的纳米胶束体系,银杏内酯B被聚乙二醇400和聚乙二醇-12-羟基硬脂酸酯体系的胶束包埋,从而增加了水溶性。
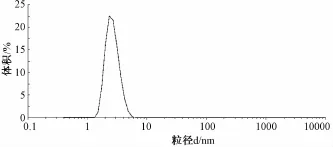
图2 复溶后药液粒径测定结果
采用该处方工艺制备的银杏内酯B冻干粉针在外观和性状方面具有较好的均一性;加入注射用水后,复溶情况良好;成品水分均低于3%,稳定性较好,易于长期保存和运输;进行加速试验后,成品各项检测指标均无明显变化。由此可知,该制剂处方工艺成熟稳定、质量可控性良好,为银杏内酯B冻干粉剂新药的研制和申报奠定了基础。
[1]郭瑞霞,李 骘,李力更,等.天然药物化学史话:银杏内酯[J].中草药,2013,44(6):641-645.
[2]柳于介,萧 伟,王振中,等.银杏内酯注射液不良反应鉴定的试验研究[J].中国药物警戒,2013,10(6):321-323.
[3]李海山,付世龙.银杏达莫注射液的临床应用及研究进展[J].中外医学研究,2012,10(12):146-147.
[4]高晋生,李囿松.银杏内酯B的药理作用研究进展[J].黑龙江中医药,2012,40(6):62-63.
[5]潘 见,吴泽宇,惠爱玲,等.银杏内酯B及其前药脂水分配系数的测定[J].时珍国医国药,2011,22(10):2397-2400.
[6]易 红,高 进,杨 华,等.几种注射用表面活性剂的质量标准及安全性概述[J].中国实验方剂学杂志,2010(1):115-119.
[7]Ahmad J,Mir SR,Kohli K,etal.Effect of oil and co-surfactant on the formation of Solutol HS 15 based colloidal drug carrier by Box-Behnken statistical design[J].Colloid Surf A-Physicochem Fng Asp,2014,453:68-77.
[8]Lin HW,Saul I,Gresia V L,et al.Fatty acid methyl esters and solutol HS 15 confer neuroprotection after focal and global cerebral ischemia[J].Transl Stroke Res,2014,5(1):109-117.
[9]李向荣.药剂学[M].杭州:浙江大学出版社,2010:85-93.
[10]钱应璞.冷冻干燥制药工程与技术[M].北京:化学工业出版社,2007:14-20.
R944
:B
:1001-1528(2015)07-1600-03
10.3969/j.issn.1001-1528.2015.07.048
2014-07-18
泰州职业技术学院 “博硕基金”项目 (TZYBS-12-7);2013年江苏省大学生创新创业训练计划项目 (201312106012Y);泰州市科技局项目 (1828666KY4)
袁海建 (1981—),男,硕士,讲师,研究方向为中药新剂型与新技术。E-mail:yuanjian8101@163.com
*通信作者:王 卉 (1974—),女,硕士,副教授,研究方向为新药药理学。
