复方四参颗粒提取和精制工艺优化
2015-01-16司爱永赵继会朴香花张永太冯年平
司爱永, 田 丰, 赵继会, 朴香花, 张永太, 冯年平*
(1.上海中医药大学,上海201203;2.上海市第一人民医院分院,上海200081)
复方四参颗粒提取和精制工艺优化
司爱永1, 田 丰2*, 赵继会1, 朴香花1, 张永太1, 冯年平1*
(1.上海中医药大学,上海201203;2.上海市第一人民医院分院,上海200081)
目的对复方四参颗粒原药材的提取和精制工艺进行优化。方法建立太子参中环肽B定量测定的HPLC方法。采用正交设计,以太子参环肽B的提取率为指标,对提取过程中的提取次数和时间,以及醇沉过程中的乙醇用量和体积分数进行考察。结果方差分析发现,提取次数对太子参环肽B提取率的影响存在显著性差异 (P<0.05),其提取率随提取次数的增加而上升。最佳提取和精制工艺为加12倍量水提取3次,每次1.5 h,提取液浓缩后加1.5倍量70%乙醇进行醇沉。按最佳工艺进行3次重复实验,结果太子参环肽B的提取率均在60%左右。结论优化后的工艺稳定性良好,采用其对复方四参颗粒原药材进行提取和精制时,主要有效成分太子参环肽B的提取率较高。
复方四参颗粒;太子参环肽B;提取率;正交实验设计
复方四参颗粒源于 “国医大师”张镜人教授的经验方——复方四参饮,作为院内制剂已有近20年的临床应用,前期临床调查了480多例心律失常患者,发现服用该药后总有效率达80%以上。其全方由太子参、南沙参、丹参、苦参、甘草、广郁金、远志 (制)、酸枣仁、莲子心九味药组成,其中太子参、南沙参为君药;丹参、苦参、甘草、广郁金为臣药;远志 (制)、莲子心、酸枣仁共为佐使药。复方四参颗粒益气养阴,扶正以治本;活血清热,祛邪以治标,具有益心气、滋心阴、和心血、宁心神之功效,主治冠心病、病毒性心肌炎等各种心脏病所引起的心律失常、临床胸闷、心悸乏力、气短等症状,而且对过早搏动,如房性早搏、室性早搏等临床疗效较好[1-3]。
为了进一步提高复方四参颗粒的质量,为其新药申报奠定基础,本实验在遵循原有提取方法的基础上,采用正交实验设计[4-7],选择君药太子参中代表性的有效成分太子参环肽B的提取率为指标,对复方四参颗粒原药材的提取和精制工艺作进一步优化[8-12]。
1 仪器与试药
1.1 仪器 Agilent 1260高效液相色谱仪(美国Agilent Technologies公司);BAS224S型微量电子分析天平(德国Sartorius公司);Minispin高速离心机(德国Eppendorf公司);SENCOR206旋转蒸发仪 (上海申生科技有限公司);JA31002电子天平 (上海精天电子仪器有限公司)。
1.2 试药 太子参 (批号140307-1,产地安徽)、南沙参(批号140218-1,产地吉林)、丹参 (批号140312-1,产地山东)、甘草 (批号 130806,产地甘肃)、苦参 (批号140209-1,产地内蒙古)、广郁金 (批号140220-1,产地广西)、远志 (制) (批号130702-1,产地山东)、酸枣仁(批号140217-1,产地山东)、莲子心 (批号140117-1,产地湖南)(上海万仕诚国药制品有限公司);太子参环肽B对照品 (中国科学院云南昆明植物研究所谭宁华课题组,纯度99%以上)。
色谱级甲醇、乙腈 (德国 Merck公司,批号P1083040、P1095114);实验用水为超纯水 (自制);分析级无水乙醇、95%乙醇 (国药集团化学试剂有限公司)。
2 方法和结果
2.1 复方四参颗粒原药材提取物中太子参环肽B测定方法的建立
2.1.1 色谱条件 Spursil C18色谱柱(250 mm×4.6 mm,5μm,Dikma);检测波长为203 nm;检测器为Agilent1260紫外检测器;体积流量为1 mL/min;柱温为30℃;进样量为20μL;流动相为乙腈和水;洗脱梯度为0~30 min,流动相中乙腈比例从5%上升至50%,之后保持恒定。
2.1.2 标准溶液的制备 精密吸取太子参环肽B对照品10.02mg,置于10 mL棕色量瓶中,甲醇定容,即得对照品贮备溶液。精密吸取对照品贮备液2.0 mL,置于50 mL棕色量瓶中,甲醇定容,即得对照品工作溶液。精密吸取对照品工作溶液0.6、1.2、2.5、5.0、7.5和10 mL,分别置于10mL量瓶中,甲醇定容,即得质量浓度为2.4~40.0 μg/mL的标准溶液。
2.1.3 供试品溶液的制备 取复方四参颗粒提取物适量,研细后精密称取10.01 g,置于圆底烧瓶中,加甲醇100 mL,水浴回流1 h,过滤后滤液减压蒸干。残渣加50 mL无水乙醇溶解,过滤后滤液减压蒸干,残渣再加入50 mL乙腈溶解,过滤后滤液减压蒸干,残渣加甲醇溶解,定容至10 mL量瓶中摇匀,即得供试品溶液。
2.1.4 阴性对照溶液的制备 取处方量药材 (太子参除外),分别加12倍量水提取3次,每次1.5 h,提取液过滤后合并,滤液浓缩至相对密度为1.15~1.20(80~85℃),再加入1.5倍量70%乙醇进行醇沉,静置40~48 h,过滤后取上清液,置于圆底烧瓶中,减压蒸干,残渣加50 mL无水乙醇溶解,过滤后滤液减压蒸干,残渣再加入50 mL乙腈溶解,过滤后滤液减压蒸干,残渣加甲醇溶解,定容至10 mL量瓶中摇匀,即得阴性对照溶液。
2.2 方法学考察
2.2.1 专属性 精密取太子参环肽B标准溶液 (20 μg/mL)、供试品溶液和阴性对照溶液各20μL,HPLC进行分析,所得图谱见图1。由图可知,阴性对照溶液对太子参环肽B的测定没有干扰,表明该方法专属性良好。

图1 专属性考察典型图谱
2.2.2 线性关系 精密吸取太子参环肽B标准溶液各20μL,HPLC进行分析,以色谱峰面积 (Y)对标准溶液的质量浓度 (X)进行线性回归,得线性回归方程Y= 70.522X+13.964,相关系数 (r)为0.999 9,提示在2.4~40.0μg/mL范围内,太子参环肽B的质量浓度与色谱峰面积线性关系良好。
2.2.3 重复性和供试品溶液稳定性 精密称取复方四参颗粒提取物适量,用于制备供试品溶液,在室温下于48 h内重复进样分析。分别记录连续测定5次及0、2、4、8、12、24、36和48 h的色谱峰面积,以所得太子参环肽B色谱峰面积的相对标准偏差 (RSD,%)为指标,考察方法的重复性和供试品溶液的稳定性,结果测得RSD分别为1.16%和1.65%,见表1。由表可知,仪器精密度和方法重复性良好,而且供试品溶液在室温下保存48 h时稳定性理想。
2.2.4 加样回收率 精密称取复方四参颗粒提取物适量,平行3份,按照 “2.1.3”项下方法制备供试品溶液,HPLC进行分析,用于测定供试品溶液中太子参环肽B的含有量。然后,再精密称取太子参环肽B对照品12.50 mg,置于10 mL量瓶中,甲醇定容,即得质量浓度为1.25 mg/mL的对照品溶液。

表1 供试品溶液稳定性考察结果
精密称取复方四参颗粒提取物适量,平行6份,每份精密加入太子参环肽B对照品溶液1.0mL,按照“2.1.3”项下方法制备加样回收率样品溶液,HPLC进行分析,计算加样回收率样品和供试品溶液中太子参环肽B含有量的差异,用于考察加样回收率,结果见表2。由表可知,太子参环肽B的加样回收率为 (98.45±1.76)%,符合规定。

表2 加样回收率试验结果
2.3 复方四参颗粒的提取和精制工艺优化
2.3.1 实验方法 采用正交实验设计,以太子参环肽B的提取率为指标,对提取过程中的提取次数和时间,以及醇沉过程中的乙醇用量和乙醇体积分数进行考察,因素水平见表3。

表3 复方四参颗粒提取精制工艺优化因素水平
2.3.2 结果和分析 实验分析结果见表4,方差分析结果见表5。由表可知,各因素对太子参环肽B提取率的影响程度为提取次数>乙醇体积分数>提取时间>乙醇用量。其中,提取次数对太子参环肽B提取率的影响具有显著性差异 (P<0.05),而其他因素无显著性差异 (P>0.05)。因此,确定最佳提取和精制工艺为加12倍量水提取3次,每次1.5 h,提取液浓缩后加1.5倍量70%乙醇(V/V)进行醇沉。
2.4 验证试验 分别称取处方量药材,平行3份,按照优化后的工艺进行提取和精制,按照 “2.1.3”项下方法制备供试品溶液,HPLC进行分析,以太子参环肽B的提取率为指标,对优化后的工艺进行考察,结果见表6。由表可知,3次实验中太子参环肽B的提取率均在60%左右,表明优化后的提取和精制工艺稳定性理想。
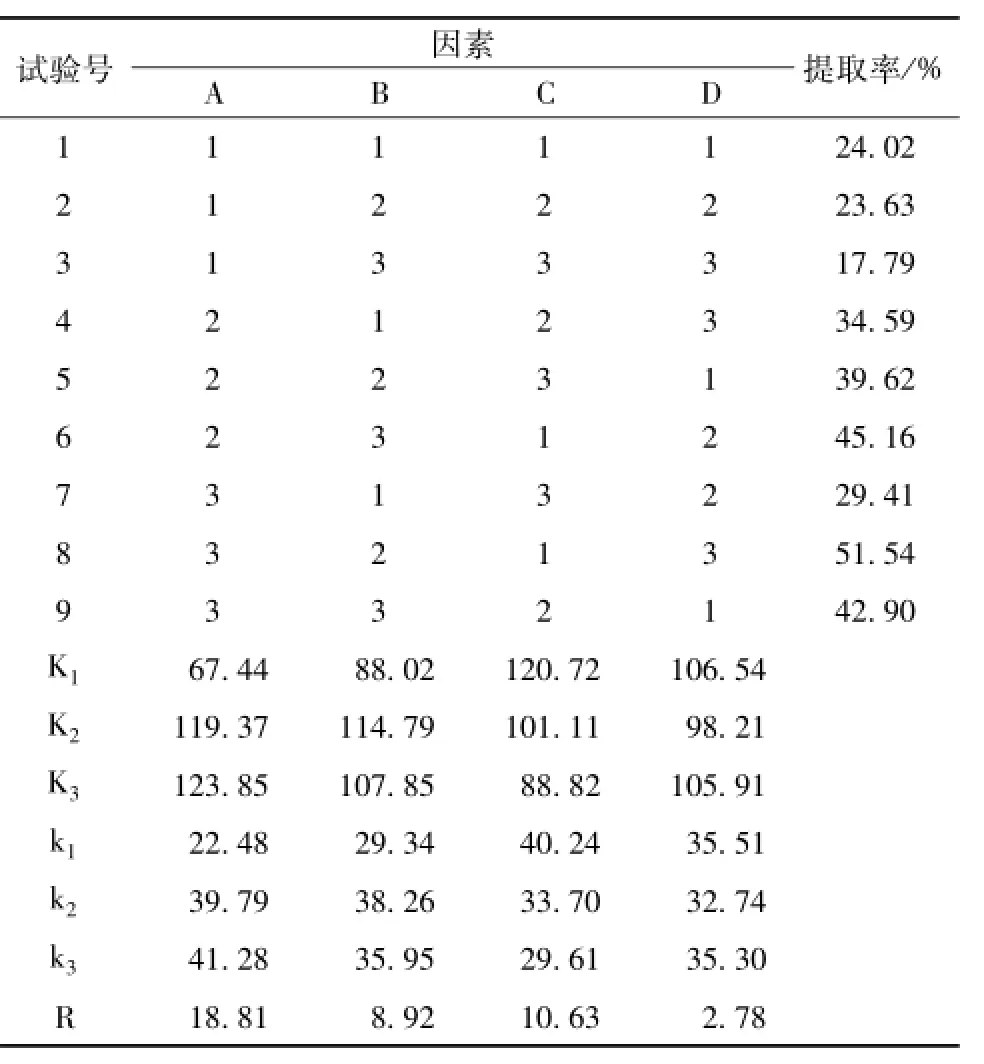
表4 复方四参提颗粒取精制工艺优化结果直观分析

表5 复方四参颗粒提取精制工艺优化结果方差分析

表6 提取和精制工艺验证试验结果(n=3)
3 讨论
复方四参颗粒由九味中药组成,成分比较复杂,并且太子参环肽B属于小分子环肽,紫外吸收较弱,属于末端吸收,各种杂质信号的响应被进一步放大,因而它是方法专属性考察验证时的重点和难点。本实验在供试品和阴性对照品处理过程中,通过应用极性不同的无水乙醇和乙腈来纯化样品,除去部分杂质,从而降低杂质对太子参环肽B测定的影响。另外,在色谱条件考察过程中,本实验以分离度为主要考察指标,通过对柱温、流动相、梯度洗脱条件、检测波长、溶剂等条件的筛选和优化,确保了该方法良好的专属性。
[1]魏强华,石蕴玉,沈博生,等.复方四参冲剂治疗病毒性心肌炎临床研究[J].中国中医药信息杂志,2001,8(2):46-47.
[2]魏强华,石蕴玉,沈博生,等.复方四参饮治疗病毒性心肌炎后心律失常的临床研究[J].中西医结合学报,2004,2(2):97-99.
[3]沈博生,郑秀春.益气养阴扶正治本,活血清热祛邪治标:张镜人复方四参饮治疗病毒性心肌炎[J].上海中医药杂志,1994(6):1-3.
[4]祁晓淼,张丽艳,彭邦梅,等.正交试验优选复方太子参颗粒处方药材的提取工艺研究[J].现代药物与临床,2013,28(5):708-711.
[5]林国钡,谢 燕,李国文,等.地黄益智颗粒水提及纯化工艺研究[J].中成药,2012,34(7):1385-1387.
[6]唐 丽,刘 跃,牟景丽,等.正交试验法优选宫炎平胶囊的提取工艺[J].中成药,2013,35(11):2528-2530.
[7]杨帝顺,虞慧华,刘继勇.正交试验法优选芩梅颗粒的提取工艺[J].中成药,2013,35(11):2538-2540.
[8]韩 超.太子参中有效成分的分离纯化、结构鉴定、及其指纹图谱研究[D].厦门:厦门大学,2006.
[9]韩 怡,巢建国,谷 巍,等.不同产地太子参环肽B含量测定[J].现代中药研究与实践,2012,26(5):69-71.
[10]韩 超,陈军辉,康海宁,等.反相高效液相色谱法测定太子参中的环肽Pesudostellarin B[J].分析试验室,2007,26(1):42-45.
[11]王 媚,宋建平,韩 乐,等.太子参环肽B含量分析及其动态研究[J].中药材,2010,33(8):1225-1227.
[12]邹立思,傅兴圣,刘训红,等.太子参药材中环肽A、B含量分析及其动态研究[J].南京中医药大学学报,2013,29(2):175-178.
R284.2
:B
:1001-1528(2015)07-1592-04
10.3969/j.issn.1001-1528.2015.07.046
2014-09-15
上海市科委生物医药领域科技支撑项目 (12401900503)
司爱永(1987—),男,硕士,研究方向为中药创新制剂。Tel:(021)51323073,E-mail:aiyongsitan@163.com
*通信作者:冯年平 (1967—),男,博士,教授,博士生导师,研究方向为中药创新制剂。Tel:(021)51322198,E-mail:npfeng@ hotmail.com田 丰,男,硕士,主管药师,研究方向为中药新药临床前研究和药物代谢基础。Tel:(021)56663031,E-mail:giantison @163.com
