丹皮酚非离子型类脂囊泡的制备
2015-01-16王建筑王欣欣毕研平郝吉福
王建筑, 王欣欣, 毕研平, 李 菲, 郝吉福
(山东泰山医学院药学院,山东泰安271016)
丹皮酚非离子型类脂囊泡的制备
王建筑, 王欣欣, 毕研平, 李 菲, 郝吉福
(山东泰山医学院药学院,山东泰安271016)
目的制备丹皮酚非离子型类脂囊泡,并考察其体外释放度。方法采用薄膜分散-超声法制备丹皮酚非离子型类脂囊泡,以包封率为指标,采用单因素考察法优选丹皮酚类脂囊泡的处方组成和制备工艺,并进行体外释放度考察。结果采用司盘-60∶胆固醇 (1∶1)为囊材,药脂比例为1∶10,40℃条件下水合60min,以频率400 Hz超声5 min,可制得丹皮酚非离子型类脂囊泡,包封率平均为78.4%,其体外释放过程与丹皮酚溶液相比较具有明显缓释作用。结论该方法适合于制备丹皮酚非离子型类脂囊泡。
丹皮酚;类脂囊泡;薄膜分散-超声法;体外释放。
丹皮酚 (paeonol)又名牡丹酚,是中药牡丹皮和徐长卿的主要活性成分,具有祛风、镇痛、抗炎、抗过敏、活血、抗病毒和抑制变态反应等药理作用[1-4],能够抑制细胞内O2-自由基的产生,使皮肤中色素还原退色,消瘀化斑,对色斑、肌肉痛、皮肤瘙痒、牛皮癣、带状疱疹、湿疹具有较好的防治效果[4-5]。除此之外,还具有较强的抗癌活性。它能通过影响肿瘤细胞基因表达等机制抑制肿瘤细胞增殖,诱导肿瘤细胞分化和凋亡,对肿瘤细胞产生杀伤作用。目前对于丹皮酚的制剂研究大多以载体的形式进行包裹,如脂质体,微囊,微球,自微乳等[6-9]。
非离子表面活性剂囊泡(Non-ionic surfactant based vesicles,简称niosomes),又称类脂囊泡,是非离子型表面活性剂和胆固醇在亲水介质中能够自组装形成的具有闭合双分子层膜结构的封闭体系[10-13],其结构类似于脂质体,但制备类脂囊泡时的材料中不含磷脂,可以避免磷脂在使用贮存中的的氧化降解,且类脂囊泡兼具有脂质体结构的缓释、高效、低毒及良好的生物相容性和可降解性,
可根据实际用途设计其结构,因此类脂囊泡技术已经成为化学、药学和生命科学研究领域中的热点之一[14-16]。本研究将丹皮酚制成非离子型类脂囊泡,可将不溶于水的且稳定性差的丹皮酚包裹于其中,考察类脂囊泡对丹皮酚的包封作用及其体外释放作用的影响。
1 仪器与试剂
1.1 仪器 S-54紫外分光光度计 (上海精密科学仪器有限公司);旋转式蒸发仪RE-52A(上海亚荣生化仪器厂);SIGMA 3K30型超速冷冻离心机;超声波细胞粉碎机 (宁波新芝生物科技股份有限公司);MD34型透析袋 (截留分子质量8 000~14 000)。
1.2 材料和试剂 丹皮酚 (泰安中荟植物生化有限公司);司盘-20(Span20);司盘-40(Span40);司盘-60(Span60);司盘-80(Span80)(国药集团化学试剂有限公司);胆固醇 (上海长城生化制药厂);其余所用试剂均为分析纯 (市售)。
2 方法与结果
2.1 包封率的测定
2.1.1 丹皮酚标准曲线的制备 精确称取适量丹皮酚用适量甲醇溶解后制成质量浓度为20μg/mL的贮备液。精密量取上述贮备液适量,分别加甲醇稀释成1、2、4、6、8μg/m L的丹皮酚溶液。以甲醇为空白对照,于波长275 nm处测定各溶液的吸光度,以吸光度A为纵坐标,丹皮酚质量浓度C(μg/mL)为横坐标进行线性回归,得线性回归方程为A=89.707C+0.009 8(r=0.999 9,n=5),结果表明,丹皮酚在1~8μg/mL的质量浓度范围内与吸光度有良好的线性关系。
2.1.2 精密度试验 取同一份丹皮酚类脂囊泡,照 “2.1.4”项下方法测定包封率,共测5次,计算日内精密度RSD为0.9% (n=5)。另取一份丹皮酚类脂囊泡,连续5 d,每天在同一时间测定包封率,计算日间精密度RSD为1.7% (n=5),表明本方法精密度良好。
2.1.3 回收率试验 精密量取质量浓度为6 μg/mL的对照品溶液2、4、6 mL,各置于10mL量瓶中,分别加入空白类脂囊泡2 m L,用甲醇定容至刻度,摇匀,进样测定峰面积。结果表明,丹皮酚的平均回收率为97.36%,RSD为2.34%(n=3)。
2.1.4 包封率测定方法 取制备好的丹皮酚类脂囊泡液摇匀,精密量取0.1 mL,适当稀释后加甲醇破乳溶解,高速离心后测定类脂囊泡中总的药物量m总。
取制备好囊泡混悬液1.0 mL置于离心管中,以转速20 000 r/min高速离心15 min,取其上清液,用甲醇稀释后,测吸光度A,计算游离药物的量m游。
包封率:EE=[(m总-m游)/m总]×100%
2.2 丹皮酚非离子型类脂囊泡的制备和优化
2.2.1 丹皮酚类脂囊泡的制备 采用薄膜分散-超声法制备丹皮酚类脂囊泡。首先称取处方量的囊泡载体材料 (司盘、胆固醇)和药物丹皮酚,加入适量二氯甲烷使其溶解,然后置于旋转蒸发仪上40℃减压蒸发至于瓶壁形成均匀薄膜为止,向烧瓶中加入适量pH 7.4磷酸盐缓冲液,控温并搅拌水合一定时间形成混悬液,然后将此混悬液冰浴下探头超声使之分散均匀,并依次通过 0.80、0.45μm微孔滤膜即得丹皮酚类脂囊泡。
2.2.2 囊材筛选 按“2.2.1”项下方法制备丹皮酚类脂囊泡时,囊泡材料 (司盘-胆固醇为1∶1)总质量浓度为10 mg/m L,加入药物质量浓度为1 mg/m L,40℃下加入磷酸盐缓冲液水合30 min,完成后采用300 W探头超声10 min,考察不同种类司盘作为囊材时对载药类脂囊泡包封率的影响,结果见表1,以Span60制备的囊泡包封率最高,且制备的囊泡外观呈均一且有蓝色乳光的混悬液,所以选择Span60作为囊材进行下一步研究。
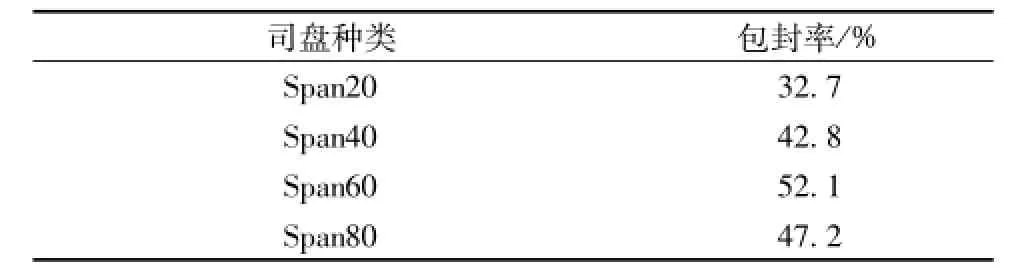
表1 司盘种类对丹皮酚类脂囊泡包封率的影响Tab.1 Effect of SpanX on the entrapment efficiency of paeonol niosom es
2.2.3 Span60与胆固醇比例的选择 改变类脂囊泡载体材料Span60与胆固醇比例 (3∶1、2∶1、1∶1、1∶2、1∶3),以药脂比为1∶5采用相同的制备工艺制备囊泡,考察不同的囊材比例对载药类脂囊泡包封率的影响,结果见表2,当Span60∶胆固醇为1∶1时,囊泡的包封率较高,所以确定处方中囊材与胆固醇比例1∶1。
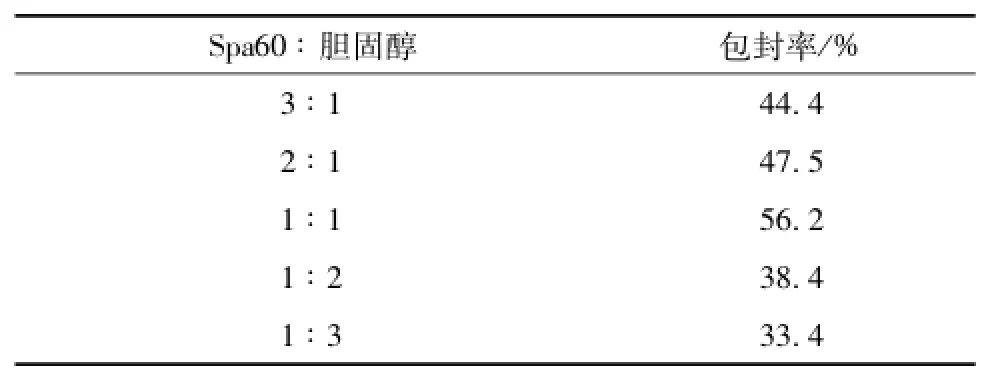
表2 司盘60和胆固醇比例对丹皮酚类脂囊泡包封率的影响Tab.2 Effect of Span60—cholesterol ratio on the entrapment efficiency of paeonol niosomes
2.2.4 类脂囊泡药脂比例对包封率的影响:分别采用不同的药脂比例 (1∶5、1∶10、1∶20、1∶40),以相同的制备工艺制备类脂囊泡,考察药脂比例的变化对丹皮酚类脂囊泡包封率的影响,结果见表3,当药脂比例1∶10时,囊泡的包封率最佳。

表3 不同药脂比例对丹皮酚类脂囊泡包封率的影响Tab.3 Effect of drug-lipid ratio on the entrapment efficiency of paeonol niosomes
2.2.5 水合时间的确定 采用上述优化的处方组成制备丹皮酚类脂囊泡,加入水合介质后,40℃水浴下分别考察不同的水合时间 (30、60、90 min)对载药类脂囊泡包封率的影响,结果包封率分别为63.6%、70.3%、71.0%,表明水合时间越长,包封率越高,但水合时间超过60 min后,时间延长对包封率影响不明显,故确定水合时间为60 min。
2.2.6 水合温度的确定 以优化的处方组成制备载药类脂囊泡,加入水合介质后,分别以不同的水合温度 (30、40、50℃)水合60 min,考察水合温度对载药类脂囊泡包封率的影响,结果包封率分别为65.2%、71.5%、71.7%,因此,确定最终水合温度为40℃。
2.2.7 超声工艺的影响 制备载药类脂囊泡水合过程完成后,分别采用不同功率进行探头超声不同时间,结果发现:超声过程中超声功率和超声时间对载药类脂囊泡包封率无显著影响,可能超声过程改变的只是类脂囊泡的粒径,因此确定超声工艺为以400 W的功率探头超声5 min。
2.3 处方验证 通过以上考察最终确定丹皮酚类脂囊泡处方组成和制备工艺为以Span60-胆固醇(比例为1∶1)为囊材,药脂比例1∶10,加入磷酸盐缓冲液以40℃水合60 min,完成后以400 W的功率探头超声5 min,平行制备3次,结果表明得到的丹皮酚类脂囊泡为带有蓝色乳光均一的白色混悬液,平均包封率为76.9%,RSD为3.3%。
2.4 显微观察形态 将制备好的类脂囊泡 (未经微孔滤膜过滤和超声处理)置于显微镜下观察,由图1可见,囊泡外观呈完整圆形或椭圆形。
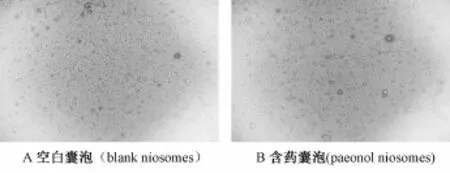
图1 丹皮酚类脂囊泡的显微形态 (x 400)Fig.1 M icro-morphology of paeonol niosomes(x400)
2.5 丹皮酚类脂囊泡的体外释放度测定 分别精密吸取丹皮酚溶液(0.1 mg丹皮酚溶解在10 m L甲醇中)和丹皮酚类脂囊泡各0.5 mL置面积大小相同的透析袋中,并将其固定于溶出仪的搅拌浆上,以pH 7.4的磷酸盐缓冲溶液200 m L为释放介质,在 (37±0.5)℃的恒温下进行体外释放性能测定 (转速50 r/min)。分别于不同时间点取样为2 mL,同时补充等量同温的释放介质,样品经0.2 μm微孔滤膜过滤后,取体外释放试验所得的样品溶液,以甲醇为空白在274 nm出测定吸光度。计算其中丹皮酚的浓度,并计算体外释放度,其体外释放曲线见图2。
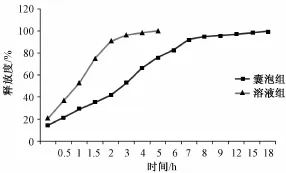
图2 丹皮酚类脂囊泡体外释放曲线Fig.2 Cu rves for paeonol niosom es in vitro release
由图2可以看出,溶液在1 h时释放即达50%以上,5 h时释放度即接近100%,而类脂囊泡1 h时只有 30%左右的释放,18 h时释放度接近100%,因此类脂囊泡明显具有缓释作用,且释药机制符合Higuchi方程。
3 讨论
制备非离子型类脂囊泡常用的囊材有司盘、吐温、卖泽及卞泽。由于丹皮酚为脂溶性药物,所以本实验采用脂溶性的司盘作为囊材,以期取得到较高的包封率。
非离子表面活性剂囊泡的制备方法主要有注入法、薄膜分散法、超声分散法、高压乳化法和反向蒸发法。其中注入法制得的囊泡粒径较大,高压乳化法和反向蒸发法适用于水溶性药物,而丹皮酚为脂溶性的药物,所以本实验采用薄膜分散法制备类脂囊泡,且该法制得的囊泡粒径较小且均匀。
如果制备过程中用span-60,水合温度应保持在span-60的相变温度 (53℃)以上,低于此温度则形成的非离子囊泡膜流动性较大,导致包封率降低。由于丹皮酚的熔点在50℃左右,所以水合温度不宜高于53℃,否则包封率比较低。类脂囊泡的结构与脂质体类似,成囊时需有表面活性剂和稳定膜结构的胆固醇。
在测定类脂囊泡包封率时,首先需要将包封的药物与游离药物进行分离,分离方法的优劣直接影响到包封率的测定结果。本实验中采用的是高速离心法。首先精密量取丹皮酚甲醇溶液适量,加至空白囊泡中,分别取该溶液1.5 mL,按20 000 r/min高速离心15min,平行做5份,测定上清液中丹皮酚的药物含有量,计算回收率。结果表明,丹皮酚-空白囊泡混合液通过高速离心法分离,加入的丹皮酚回收率均在95%以上,表明空白囊泡对游离丹皮酚基本无吸附。此法可以用于类脂囊泡混悬液中游离药物的分离。
本实验采用薄膜分散法制备丹皮酚非离子型类脂囊泡,以包封率为指标筛选,经优化后的处方组成和制备工艺制备得丹皮酚类脂囊泡包封率为76.9%,体外释放度实验表明丹皮酚经类脂囊泡包裹后,具有明显的缓释作用。并且利用非离子表面活性剂囊泡包裹药物可以减少药物在达到有效部位前被破坏、延长药物的中半衰期、从而延长药物的作用时间以及降低毒副作用的特点。
[1]胡春弟,张 杰.丹皮酚的药理及合成研究进展[J].化学与生物工程,2009,26(8):16-18.
[2]刘爱敏,武海军,杨玉梅.丹皮酚的镇痛作用[J].包头医学院学报,2004,20(2):99-100.
[3]刘春云,武廷章.凤丹丹皮酚抗菌作用的研究[J].生物学杂志,2000,17(3):23-24.
[4]邢国胜,房德敏,周咏梅.丹皮酚的制备及药理作用研究进展[J].中草药,2006,37(11):附2-7.
[5]解士海,陈志强.丹皮酚在体外对人黑素细胞酪氨酸酶活性及黑色素生成的影响[J].中华皮肤科学杂志,2006,39(11):639-641.
[6]贾献慧,唐文照,闫 军.丹皮酚脂质体的研制及其体外释放研究[J].中成药,2011,33(2):255-258.
[7]姜素芳,州艳琴.丹皮酚微囊的制备及质量评价[J].中国医院药学杂志,2009,29(21):1872-1874.
[8]姜素芳,张雪萍,周学军.丹皮酚的自微乳的制备与评价[J].中成药,2012,34(5):835-838.
[9]张海龙.丹皮酚聚乳酸羟基乙酸微球的制备及体外释药考察[J].中国药房,2013,24(19):1765-1767.
[10]Ning Meiying,Guo Yingzhi,Pan Huaizhong,et al.Niosomes with sorbitan monoester as a carrier for vaginal delivery of insulin:studies in rats[J].Drug Delivery,2006,12(6):399-407.
[11]Vyas S P,Singh R P,Jain S,et al.Non-ionic surfactant based vesicles(niosomes)for non-invasive topical genetic immunization against hepatitis B[J].Int J Pharm,2005,296(1-2):80-86.
[12]李静雅,苗凤茹,朱 丹,等.马钱子总碱囊泡凝胶经皮给药后在大鼠组织中的分布研究[J].中草药,2012,43(2):327-331.
[13]胡 杰,吴珍珍,胡克菲,等.马钱子总碱囊泡的制备与评价[J].中国中药杂志,2011,36(14):1955-1998.
[14]廖正根,韩锡镇,李 翔,等.三七总皂苷符合纳米囊泡的理化性质及对大鼠心肌缺血的保护作用[J].中国药学杂志,2013,48(6):899-903.
[15]刘 丹,胡海洋,陈大为,等.芹菜素囊泡的制备及理化性质考察[J].沈阳药科大学学报,2009,26(6):423-427.
[16]陈洪轩,徐志杰,肖衍宇.蛇床子素非离子囊泡的制备和质量评价[J].中国医药工业杂志,2011,42(1):33-37.
Preparation of paeonol niosomes
WANG Jian-zhu, WANG Xin-xin, BIYan-ping, LIFei, HAO Ji-fu
(Department of Pharmacology,Taishan Medical College,Taian 271016,China)
paeonol;niosomes;film ultrasonic dispersion;in-vitro release
R969.1
:A
:1001-1528(2015)07-1467-04
10.3969/j.issn.1001-1528.2015.07.016
2014-08-18
泰安市科技发展计划 (201440774-16)
王建筑(1981—),男,硕士,讲师,研究方向为药物新剂型与新技术。Tel:13668681261,E-mail:jzwang@tsmc.edu.cn
