消乳增胶囊的小鼠急性毒性和大鼠长期毒性研究
2015-01-13封聚强张志宏
葛 斌, 贾 海, 封聚强, 张志宏, 王 辉, 高 湘
(甘肃省人民医院,甘肃兰州730000)
消乳增胶囊的小鼠急性毒性和大鼠长期毒性研究
葛 斌, 贾 海, 封聚强, 张志宏, 王 辉, 高 湘*
(甘肃省人民医院,甘肃兰州730000)
目的对我院消乳增胶囊的急性毒性及长期毒性进行评价研究。方法对KM小鼠以高剂量组45.5 g生药/kg,中剂量组22.8 g生药/kg,低剂量组11.4 g生药/kg进行半数致死量 (LD50)试验。以原液91.3 g生药/kg进行最大耐受量 (MTD)试验、以原液91.3 g生药/kg,一日两次进行最大给药量试验,观察15 d测定出现毒性反应的剂量。Wistar大鼠灌胃分别给予18.2 g生药/kg,9.1 g生药/kg,4.55 g生药/kg,分别予给药第6周、第12周,停药3周各期分别处理一批大鼠进行长期毒性试验。结果未测定出LD50、MTD。最大给药量试验中仍未出现死亡。试验结束进行大体解剖发现小鼠全消化道外观与空白组相比颜色呈亮蓝绿色,并对之进行病理切片进一步检查。病理切片显示未见病理性改变。长毒试验对大鼠质量及脏器指数各组无统计学差异。血液学检查各组未见统计学差异。生化指标,试验初期低剂量组与空白组比较,碱性磷酸酶有所降低 (P<0.05),葡萄糖高于空白组 (P<0.05),后两期差异消失。大体解剖显示高剂量组1例大鼠肝脏出现出血点和点状突起。病理切片出现高剂量组大鼠肝细胞坏死、肝纤维化,肾上腺有充血,肺有出血。结论消乳增胶囊在临床剂量40倍以下有较好的安全性。
消乳增胶囊;急性毒性;长期毒性
消乳增胶囊是我院研制开发的中药制剂,在治疗乳痈、乳腺增生症方面发挥了重要作用。该胶囊在我院临床应用超过10年,因疗效确切,毒副作用小,成为我院的特色中药制剂。现用消乳增胶囊,因原工艺条件限制,处方中部分药材未经提取而直接入药,引起服用后胃部出现不适感;同时,经多年临床应用,患者自觉该药 “止痛”起效慢。因此原处方中增加一味元胡药材,同时将之前部分药材水提,部分药材粉碎入药改为部分药材水提,部分药材醇提,合并提取物后成为本研究制剂。为完善该制剂的安全性评价资料,对急性毒性及长期毒性进行研究,为该药在临床更好地服务于患者提供有效的参考。
1 材料与方法
1.1 动物 健康雌性SPF级KM小鼠40只,体质量(20±2)g,健康雌性SPF级Wistar大鼠120只,体质量(200±20)g,由甘肃省中医学院动物试验中心提供,实验动物质量合格证号:SCXK(甘)2011-0001。动物购买后适应性饲养7 d后开始试验。
1.2 药物 消乳增胶囊为甘肃省人民医院自制制剂,由苦参、当归、香附、白芍、川楝子等18味中药组成。由甘肃省人民医院制剂中心提供,批号为20131001,批准文号甘药制字H04000801。该药处方为甘肃省人民医院协定处方。临床日剂量为16粒,按成人70 kg计算相当于0.22 g生药/kg。试验时混悬液最大质量浓度为3.65 g生药/mL。对最大质量浓度混悬液进行适当稀释备用。
1.3 主要仪器 Olympus 5400全自动生化分析仪;Mindray BC-5390血液分析仪。
1.4 小鼠急性毒性试验[1-3]根据 《中药、天然药物急性毒性研究技术指导原则》进行急性毒性试验研究。小鼠灌胃体积为0.25 mL/10 g。对KM小鼠以高剂量组45.5 g生药/kg(相当于人临床服用量kg体质量200倍),中剂量组进行22.8 g生药/kg(相当于人临床服用量kg体质量100倍),低剂量组11.4 g生药/kg(相当于人临床服用量kg体质量50倍)进行半数致死量 (LD50)试验。以原液91.3 g生药/kg(相当于人临床服用量kg体质量400倍)进行最大耐受量 (MTD)试验、以原液91.3 g生药/kg,1日2次 (相当于人临床服用量日剂量kg体质量800倍)进行最大给药量试验,确定出现毒性反应的剂量。空白组给同等容积的蒸馏水。观察指标为外观,毛发,行为,活动,粪便,分泌物,食量,饮水量等变化及有无死亡。
1.5 大鼠长期毒性试验[1,4-6]
1.5.1 分组 取雌性W istar大鼠120只随机分成4组,每组30只。高剂量组18.2 g生药/kg(相当于人临床服用量kg体质量80倍),中剂量组9.1 g生药/kg(相当于人临床服用量kg体质量40倍),低剂量组4.55 g生药/kg(相当于人临床服用量kg体质量20倍)进行长期毒性试验。空白组给予同等剂量的蒸馏水。
1.5.2 给药及观察检测 试验期间密切观察大鼠一般状况。消乳增胶囊临床使用疗程为2~3周,最长不超过1个月,根据技术指导原则长毒连续给药观察时间定为12周。给药第6周、第12周末次给药12~24 h,每组随机选10只大鼠,采用腹主动脉采血5mL分别送检做血液学指标及血液生化指标。停药观察3周做可逆性观察。病理组织学检查药物对脏器的影响。
1.5.3 数据处理 本实验计量资料用均数±标准差 (x± s)表示。多组间比较,方差齐的用方差分析,方差不齐的用非参数检验,两两比较用t检验,全部数据用SPSS 17.0统计软件协助处理。
2 结果
2.1 消乳增对小鼠的急性毒性 由于实验中未能测出LD50及MTD,于是最终以最大给药量结果进行分析。给药后动物少动,约1 h后恢复正常,连续观察15 d,动物未见异常,也无死亡。处死动物后,肉眼观察心、肝、脾、肺、肾、胃、肠道等脏器。发现与空白组相比,最大给药量组小鼠消化道均呈现亮蓝绿色,取两组小鼠消化道做病理切片未见病理性改变。此时小鼠的累积给药量即最大给药量达到183 g生药/kg,相当于70 kg体质量的成人临床每日用量的800倍,相当于临床等效剂量的91倍,见表1。给药后连续观察15 d期间对小鼠体质量进行比较,各组比较未见统计学差异,P>0.05,见表2。
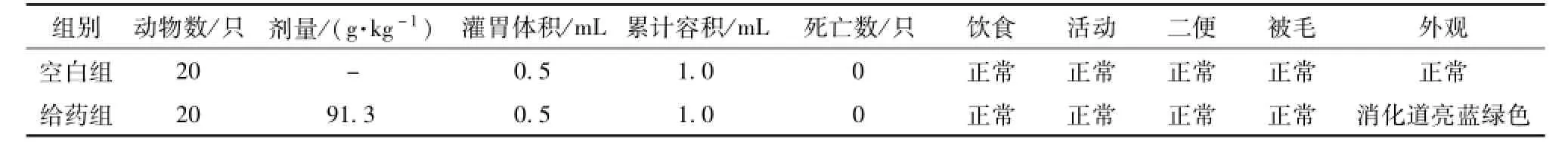
表1 小鼠最大给药量结果

表2 给药后小鼠体质量增长变化 (x±s,n=10)
2.2 消乳增胶囊对大鼠的长期毒性2.2.1 对大鼠一般情况及体质量的影响 大鼠灌胃给药消乳增6周、12周和停药恢复性观察3周,消乳增对大鼠的外观体征、毛色、行为活动、粪便性状均无明显影响,试验期间未出现动物死亡。由表3可以看出,消乳增对各组大鼠体质量增长变化未出现统计学差异,P>0.05。
2.2.2 对大鼠血液学指标的影响 由表4~5可以看出,消乳增对大鼠各试验阶段血常规的影响各组指标间比较均未出现显著性差异,P>0.05。
2.2.3 对大鼠血液生化指标的影响 由表6~7可以看出,消乳增对大鼠血液生化学指标,各组指标间比较均未出现显著性差异。
2.2.4 对大鼠脏器指数的影响 由表8~9可以看出消乳增对大鼠脏器指数不同试验阶段影响没有统计学差异,P>0.05。
2.2.5 对大鼠脏器病理影响 在长毒各期大鼠解剖中发现1例高剂量组大鼠肝脏表面出现出血点和点状隆起,其他各组大鼠并未出现类似表现。长毒对各组大鼠包括心、肝、脾、肺、肾、肾上腺、胸腺、卵巢、子宫、脑、胃、十二指肠、空肠、回肠、直肠共15个脏器进行病理切片,查找出现病理学改变的脏器。病理切片显示有病理学改变的只在高剂量组出现,病变部位主要集中在肝脏、肾上腺及肺脏。由图1可以看出肝脏出现纤维化、坏死及出血表现,肾上腺轻度充血,肺有大量出血表现。

表4 消乳增对大鼠给药12周血常规的影响 (x±s,n=10)

表5 消乳增对大鼠停药3周血常规的影响 (x±s,n=10)
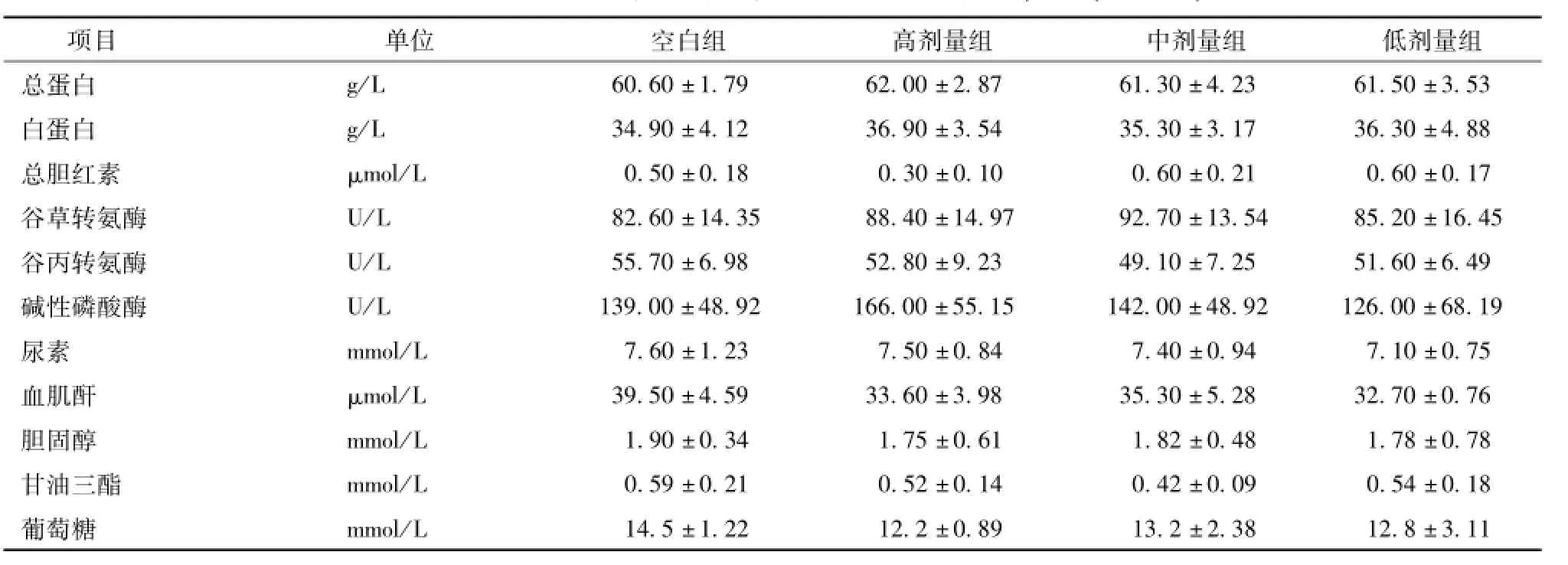
表6 消乳增对大鼠给药12周血液生化学指标的影响 (x±s,n=10)
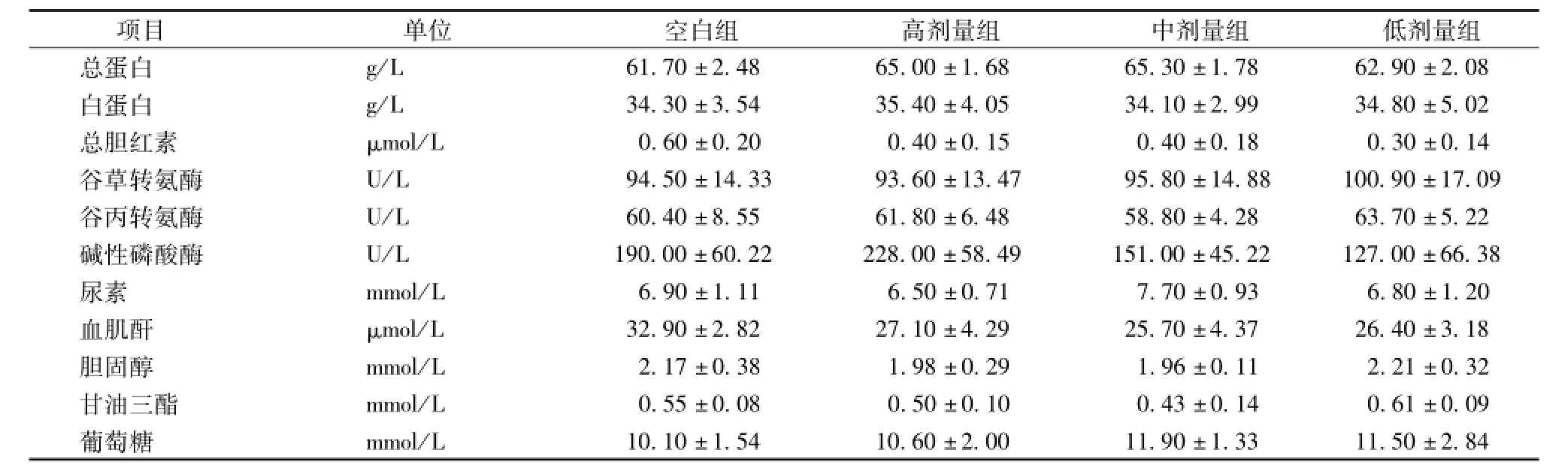
表7 消乳增对大鼠停药3周血液生化学指标的影响 (x±s,n=10)

表8 消乳增对大鼠给药12周脏器指数的影响 (x±s,n=10)
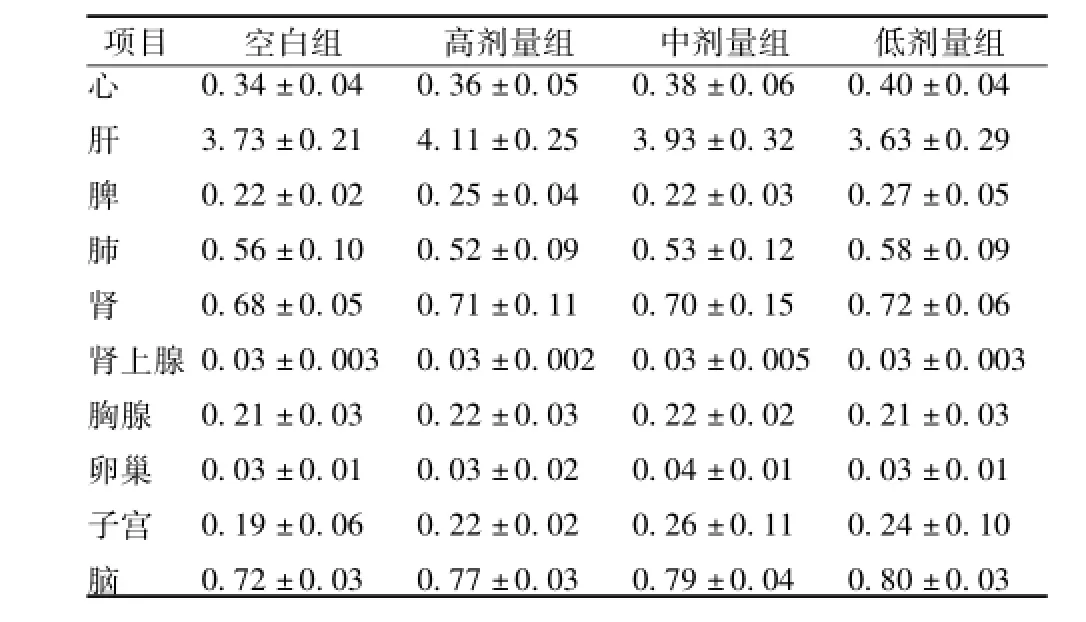
表9 消乳增对大鼠停药3周脏器指数的影响 (x±s,n= 10)
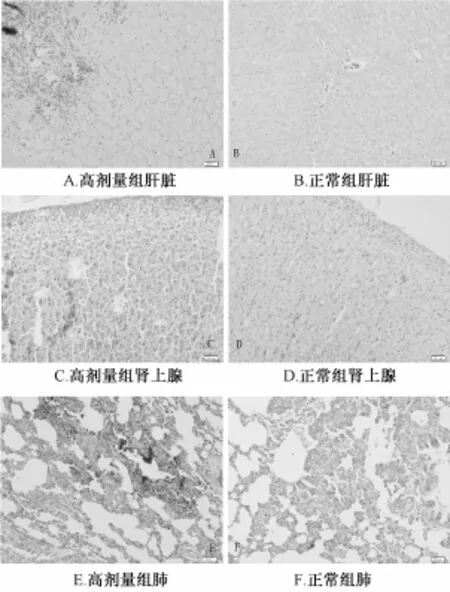
图1 大鼠病理阳性结果及对照 (HE染色,10×20倍)
3 讨论
由于之前预试验无法测出LD50、最大耐受量,所以考察最大给药量对小鼠的急性毒性反应。由于在临床多年使用经验判断,该药能够安全、有效地治疗乳腺增生。在急性毒性试验中未显示出明显毒性反应。在观察期结束后进行大体解剖发现给药组消化道出现亮蓝绿色异常,于是进行病理切片进一步考察有无病理改变。病理切片显示未见病理改变。分析消化道颜色改变原因可能为给药组消化道药物与内容物相互作用产生颜色所致,与药物作用于肠道微生物或致消化道胆绿素增加有关。该药在急性毒性试验中未出现毒性反应,尽管由于种属差别,但结合临床实际经验及该试验显示出该药是安全的。
由试验结果可以看出,消乳增对大鼠体质量及各脏器指数的影响并未出现统计学差异,说明对饲料的消耗并不会影响大鼠正常生长、发育,从这一点来看,消乳增对大鼠消化系统是安全的。
在血液学检测时常常只注意红细胞计数而忽视网织红细胞的检查。事实上,红细胞计数无论在反映溶血还是反映红系造血抑制上都不灵敏,特别是对试验周期不长的长期毒性试验上来说红系的变化单靠红细胞计数不易被发现,因为红细胞寿命很长,平均120 d。在此期限内,骨髓红系造血即使受抑,外周血液也表现不出来。在溶血的情况下,机体可以从储存库中将红细胞动员出来,使外周血红细胞也不致明显下降。但血液网织红细胞计数却是一个很敏感的指标,其计数下降提示红系造血障碍;增高提示溶血现象[7]。因此从本实验结果可以看出消乳增对血液系统没有明显影响,各剂量组,各试验阶段均未出现明确的影响,说明该药对大鼠血液系统是安全的。血液生化指标中,本实验中碱性磷酸酶低剂量组与空白组比有所降低,但不能说明消乳增对肝功有影响。第一期数据显示葡萄糖与空白组比较,低剂量组有升高,差异有统计学意义,说明消乳增对葡萄糖的代谢有一定影响,葡萄糖升高可能与对甲状腺、肾上腺和垂体功能的影响有关,由于实验所限,并未进一步阐明机理。但之后的实验对葡萄糖的影响并未出现有统计学差异,说明消乳增对大鼠血糖无长期影响。
实验中消乳增高剂量组为临床常用剂量的80倍,在该剂量组个别大鼠出现肝细胞坏死,肾上腺充血及肺出血的表现,而空白组只有一例肺出血,尽管是个别动物出现也不能完全肯定该药在80倍临床剂量下是安全的。中、低剂量组并未出现病理改变,说明该药在中、低剂量下即临床剂量的40倍、20倍时是安全的。
至于对肝细胞的损害,经分析认为,消乳增方中有一味药是川楝子。川楝子(Toosendan Fructus)为临床常用药,《中国药典》2010年版[8]所载川楝子为楝科植物川楝的干燥成熟果实,性味苦寒,有小毒,归肝、小肠、膀胱经,具有疏肝泄热,行气止痛,杀虫等功效,临床用于治疗胸胁、脘腹胀痛,疝气痛,虫积腹痛。有关川楝子毒性的记载首见于 《名医别录》。有多篇报道川楝子的毒性主要在肝脏,通过炎症反应加重肝细胞的损伤,最后导致肝损伤。所以这也可以部分解释高剂量组会对肝脏有一定毒性,导致纤维化及坏死等。尽管川楝子入药为炮制品,毒性有所降低,但高剂量长期使用对肝毒性的研究有待于进一步深入探索。
[1]卫生部药政管理局.中药新药研究指南 (药学、药理学、毒理学)[M].1994:202-209.
[2]中药、天然药物急性毒性研究技术指导原则课题研究组.中药、天然药物急性毒性研究技术指导原则:第二稿[M].北京:国家食品药品监管局,2004:1-9.
[3]陈 奇.中药药理研究方法学[M].北京:人民卫生出版社,2006:112-119.
[4]中药、天然药物长期毒性研究技术指导原则课题研究组.中药、天然药物长期毒性研究技术指导原则[M].北京:国家食品药品监管局,2005:1-12.
[5]李建荣,黄芳华.中药新药长期毒性实验设计及常见问题分析[J].中国新药杂志,2004,13(9):769-772.
[6]李仪奎.中药药理实验方法学[M].2版.上海:上海科学技术出版社,2006:1008-1018.
[7]胡 雷.药物非临床研究与临床试验质量管理实务全书[M].北京:当代中国音像出版社,2003:353-354.
[8]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:39-40.
R285.5
:B
:1001-1528(2015)05-1107-05
10.3969/j.issn.1001-1528.2015.05.042
2014-06-15
甘肃省自然科学研究基金计划 (1107RJZA130)
葛 斌(1965—),男,硕士生导师,从事中药安全性评价研究。E-mail:gjy0630@163.com
*通信作者:高 湘 E-mail:1071359340@qq.com
日期:2014-12-24
网络出版地址:http://www.cnki.net/kcms/detail/31.1368.R.20141224.1554.001.htMl
