丹参水提物一步制备丹参素乙酯的研究
2015-01-09钱三立李冰玉吴君怡张真中杨春杰邹云增
钱三立,李冰玉,吴君怡,张真中,杨春杰,邹云增*
1复旦大学附属中山医院,上海 200032;2 上海市中医医院,上海 200071
丹参来源于唇形科鼠尾草属植物Salvia miltiorrhiza 的干燥根及根茎。丹参水溶性组分,包括丹参素、丹酚酸B、紫草酸、迷迭香酸等,是丹参主要的活性化合物[1]。丹参素是丹参中重要的水溶性活性组分,其他水溶性化合物都可以看作是丹参素的衍生物或者聚合物。丹参素具有抗炎、抗肿瘤、抗氧化、保肝的药理活性,可用于心脑血管疾病、肝病、糖尿病并发症、肾病、神经系统疾病的治疗[2-4]。
众多研究报道了丹参素衍生物的制备方法[5],期望能够找到活性更强、口服利用率更高的化合物。由于酚羟基是丹参素抗氧化作用的活性基团,其结构修饰主要集中在其醇羟基和羧基上进行,羧基酯化反应是其中重要的一种。丹参素在大鼠体内的代谢产物丹参素异丙酯,即3-(3,4-二羟苯基)-2-羟基丙酸异丙酯,在体外实验中证明具有扩张血管的作用[6]。崔庆彬等研究了丹参素醇羟基结构修饰对其活性的影响,结果显示醇羟基的修饰,不能明显增加丹参素的活性[7]。
丹参素在丹参中含量较低,常规的制备方法是采用碱处理丹参水提取物,使丹参的丹参素聚合物(如丹酚酸B、紫草酸等)在碱性条件下水解,得到丹参素粗品,后者经过进一步纯化制得丹参素纯品。然而,丹参素在碱性条件下不稳定,并且纯化得到的丹参素进行结构修饰后,需要再一次纯化其产物,这无疑大大增加了生产成本。丹参中主要水溶性成分丹酚酸B、紫草酸和迷迭香酸,是丹参素多聚体,在丹参中含量较高。如果能够开发一条工艺,将丹参素多聚体的解聚和衍生化合并一步完成,直接制备丹参素的衍生物,将显著降低其生产成本。本研究探讨了用丹参水提取物一步制备成丹参素乙酯的工艺,具有生产应用前景。
1 材料与方法
1.1 药材与试剂
丹参药材,产自山东临沂,购自安徽亳州药材市场,经过上海医药工业研究院王曙光博士鉴定确证。乙醇、盐酸、氢氧化钠、乙酸乙酯、硫酸,皆为分析纯,购自国药集团化学试剂厂。色谱级乙腈、甲醇为美国天地(Tedia)品牌。1,1-二苯基-2-三硝基苯肼[1,1-Diphenyl-2-picrylhydrazyl radical;2,2-Diphenyl-1-(2,4,6-trinitrophenyl)hydrazyl),DPPH],购自Sigma。丹参提取物对照品丹酚酸B(批号:13091231)、紫草酸(批号:12082915)、迷迭香酸(批号:14011215)、丹参素(批号:13121106)购自上海同田生物技术有限公司。
1.2 丹参提取物的制备
丹参药材加入10 倍量70%乙醇,80 ℃提取两次,每次1 h,提取液过滤合并,旋转蒸发仪回收乙醇,剩余部分调节至pH 7,两倍体积的乙酸乙酯萃取两次,去除其中的脂溶性成分丹参酮。剩余水相,调节至pH 2,两倍体积的乙酸乙酯萃取两次,乙酸乙酯相浓缩至干,得到的浸膏即为水提取物,可以直接作为合成用原料(其中丹酚酸B、紫草酸、迷迭香酸三者含量应该不低于85%,以上述三者计算的收率应该不低于90%)。
1.3 丹参素乙酯制备
10 g 丹参水提取物溶解在200 mL 无水乙醇中,加入浓硫酸200 μL,水浴加热,保持乙醇回流,HPLC 检测反应进程,6 h 后终止反应。
调节反应液至pH 2,浓缩回收乙醇,剩余部分,加入200 mL 水溶解,调节至pH 6,过大孔吸附树脂“微球1 号”,水洗脱,分步收集50 mL/瓶,HPLC 检测。产物纯度超过80% 的样品合并,浓缩至200 mL,调节pH 6,再次过树脂,最终得到纯度超过98%的样品,冷冻干燥,用于下一步的光谱学分析,结构鉴定。由于丹参素乙酯水溶性较强,该纯化过程收率较低,约30%左右。
1.4 DPPH 自由基清除试验
丹参素、丹参素乙酯清除自由基能力实验,通过稳定自由基DPPH 来检测[8]。取96 孔板,每孔加入10 μL DPPH(无水乙醇溶液,1mM),89.6 μL 无水乙醇和0.4 μL 丹参素(或丹参素乙酯),混匀后置于黑暗中静置30 min,517 nm 处检测吸光值。自由基清除能力,以IC50来计算,表示清除半数自由基所需要的丹参素(或丹参素乙酯)的浓度。
1.5 HPLC 分析方法
丹参水溶性组分的提取、丹参素乙酯的制备、纯化等,都通过HPLC 检测。HPLC 采用安捷伦HP1200 液相色谱仪,配备四元泵、自动进样器、DAD检测器。流动相为1.7%甲酸∶乙腈∶水=75∶23∶2,流速1 mL/min,检测波长286 nm。采用C18液相色谱柱,柱温25 ℃,进样体积10 μL。
2 结果与讨论
2.1 产物的分离纯化及结构鉴定
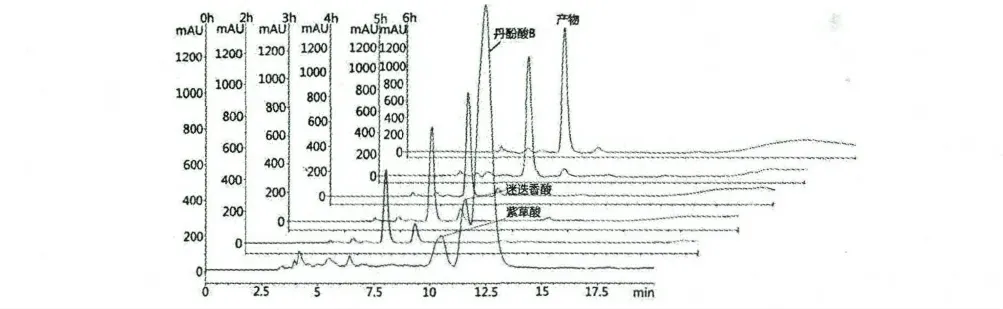
图1 丹参提取物一步法制备丹参素乙酯反应过程的HPLC 图谱Fig.1 HPLC chromatograms of S.miltiorrhiza extract in the transformation to ethyl 3-(3,4-dihydroxyphenyl)-2-hydroxypropanoate
如图1 所示,随着时间的延长,HPLC 保留时间6.5 min 处出现产物并逐渐增加。紫外吸收图谱表明,该产物具有和丹参素相似的吸收峰,显示该化合物可能是丹参素的衍生物。ESI-MS 显示其分子量为226,等同于丹参素乙酯化产物的分子量。由于该反应体系采用乙醇作为溶剂,可以猜测该化合物可能是丹参素乙酯(3-(3,4-二羟苯基)-2-羟基丙酸乙酯)。NMR 结果验证了该化合物的结构(图2)。
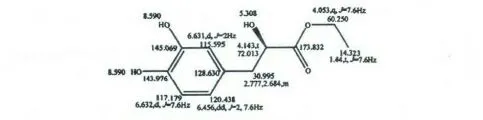
图2 丹参素乙酯的NMR 数据Fig.2 NMR data of ethyl 3-(3,4-dihydroxyphenyl)-2-hydroxypropanoate
2.2 丹参提取物一步法直接制备丹参素乙酯
随着反应时间的延长,丹参素乙酯含量逐渐增加,反应体系中丹酚酸B、紫草酸、迷迭香酸含量逐渐降低,显示丹参素乙酯可能来源于它们。同时生成保留时间7.5 min 的产物(原紫草酸,prolithospermic acid,参考文献的方法制备[9]),来源于丹酚酸B在酸性条件下的水解。原紫草酸在该条件下不稳定,逐渐进一步降解生成其他物质。
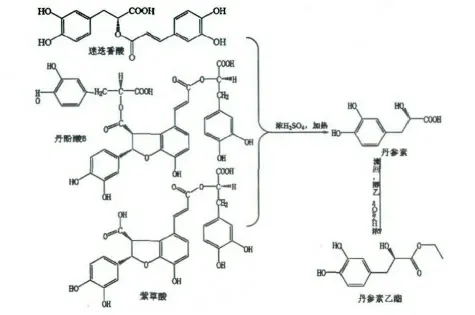
图3 反应路线图Fig.3 Chemical reaction routes
整个体系反应过程如图3 所示,丹参水溶性组分中丹酚酸B、紫草酸、迷迭香酸在浓硫酸的催化下发生水解,生成丹参素,后者在乙醇体系内发生酯化丹参素乙酯。由于羧酸和醇的酯化反应一般采用相似的反应条件,可以预见若采用其它醇类化合物,亦会发生类似的酯化反应,得到相关醇的酯化产物。采用类似的方法,可以直接由丹参水溶性提取物,制备各种丹参素酯化产物。相比传统的首先提纯丹参素然后酯化反应的方法,本工艺采用硫酸做催化剂,并且省略了丹参素纯化的过程。由于丹参素在酸性条件下更加稳定,本方法得率更高,为我们提供了一种制备丹参素酯化产物的新方法。
2.3 丹参主要化合物及丹参素乙酯清除自由基试验
自由基主要包括超氧阴离子自由基、羟基自由基、脂氧自由基、羧自由基等,是机体氧化反应产生的物质,具有强氧化性,可以对机体健康细胞产生巨大的损害,引起慢性疾病及衰老症状[10,11]。丹参水溶性组分,包括丹参素、丹酚酸B 等,具有非常强的清除自由基的能力。化合物抗氧化活性的大小,常用其清除自由基能力的大小来检测。DPPH 是一种稳定自由基,其溶液在517 nm 波长下有较大吸收,当该自由基被其它化合物所清除时在该波长下吸收减弱,因此常采用它来测定化合物对自由基的清除能力[8]。
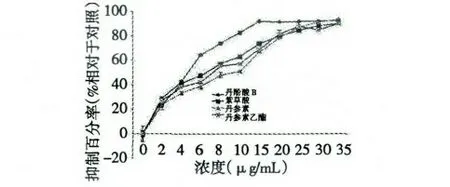
图4 丹酚酸B、紫草酸、丹参素和丹参素乙酯对自由基的清除能力对比Fig.4 DPPH scavenging ability of salvianolic acid B,lithospermic acid,danshensu and ethyl 3-(3,4-dihydroxyphenyl)-2-hydroxypropanoate
图4 显示丹参主要水溶性化合物丹酚酸B、紫草酸、丹参素和丹参素乙酯自由基清除能力,他们的IC50分别为:5.15、6.40、10.25、9.68 μg/mL。丹酚酸B、紫草酸的自由基清除能力强于丹参素,丹参素被乙酯化后,其自由基清除能力略有增加,差异达到显著水平(P<0.01)。
乙酯化后,丹参素的自由基清除能力增加,同时乙酯化后导致丹参素脂水分配系数的改变,使其更容易透过细胞膜进入体内,从而可以明显增加其口服吸收率。
丹参素是丹参中主要的活性组分之一,虽然其活性低于丹酚酸B,但由于其分子量更小,且更容易被纯化,使其化合物的结构修饰成为一个研究热点。
由于通过化学合成的丹参素是光学混旋体,目前丹参素的大量制备方法仍然以丹参水提取物水解为主。本研究将丹参水提取物的水解和衍生化在一个体系内通过一步反应完成,同时水解催化采用浓硫酸而非碱,水解后的产物进一步酯化得到了丹参素衍生物,从而保证了水解反应进行完全,且反应原料和产物未接触强碱从而降低了副反应,增加了反应的收率(以丹酚酸B 计算,本反应总收率超过40%)。可以预见,本实验采用的思路,可以推广至其他丹参素酯化物的制备,为我们提供了一种简单、高效、低成本的制备方法。
3 结论
本实验介绍了一种通过丹参水提物直接制备丹参素乙酯的方法。同已有的报道相比,本研究省略了丹参素制备、纯化的过程,直接将丹参水提物水解成丹参素和丹参素的酯化反应合并到一步反应进行,使反应过程变得更加简单。由于酯化反应具有类似的反应条件,因此丹参素其他酯化衍生物的制备,也可以借鉴本研究使用的方法。
1 Lu Y,Foo LY.Polyphenolics of Salvia--a review.Phytochemistry,2002,59:117-140.
2 Cao Y,Chai JG,Chen YC,et al.Beneficial effects of danshensu,an active component of Salvia miltiorrhiza,on homocysteine metabolism via the trans-sulphuration pathway in rats.Br J Pharmacol,2009,157:482-490.
3 Chang JY,Chang CY,Kuo CC,et al.Salvinal,a novel microtubule inhibitor isolated from Salvia miltiorrhizae Bunge(Danshen),with antimitotic activity in multidrug-sensitiveand-resistant human tumor cells.Mol Pharmacol,2004,65:77-84.
4 Zhang XX (张晓晓),Zhang S (张硕),Huang XY (黄晓燕),et al.Anti-lipoperoxidation of several organic polyphenol acids in vitro.Nat Prod Res Dev,2014,26:398-402.
5 Wang TF (王庭芳),Zheng LP (郑莉萍),Zhang N (张宁),et al.Progress on Danshensu derivatives.J Pharm Pract,2011,29:83-90.
6 Zhang QZ (张群正),Dong Y (董岩),Nan YF(南叶飞),et al.Synthesis of β-(3,4-Dihydroxyphenyl)-α-hydroxy propionic acid esters.Chin J Org Chem,2009,29:1466-1469.
7 Cui QB (崔庆彬),Shan LC (单璐琛),Zhu H (朱华),et al.synthesis and preliminary evaluation of Danshensu derivatives modified at hydroxyl group.J Int Pharm Res,2013,40:795-800.
8 Kan S,Cheung WM,Zhou Y,et al.Enhancement of doxorubicin cytotoxicity by tanshinone IIA in HepG2 human hepatoma cells.Planta Med,2014,80:70-76.
9 Kan SD,Lin HM,Li JA,et al.Biotransformation of salvianolic acid B by Fusarium oxysporum f.sp cucumerinum and its two degradation routes.Nat Prod Commun,2012,7:885-888.
10 Esmaeili MA,Sonboli A.Antioxidant,free radical scavenging activities of Salvia brachyantha and its protective effect against oxidative cardiac cell injury.Food Chem Toxicol,2010,48:846-853.
11 Wu WG,Qiu FZ.A new method of superoxide free radical determination in ischemia and reperfusion injury of rat liver.J Tongji Med Univ,1995,15:151-153.
