CuO/ZnO/CeO2-ZrO2催化甲醇水蒸气重整制氢性能
2015-01-07祁文旭何依隆刘道胜潘立卫王树东
祁文旭,张 娜,何依隆,张 磊,,刘道胜,吴 限,潘立卫,王树东
1.辽宁石油化工大学化学化工与环境学部,辽宁 抚顺 113001;
2.中国科学院大连化学物理研究所,辽宁 大连116023;
3.抚顺职业技术学院,辽宁 抚顺 113122
CuO/ZnO/CeO2-ZrO2催化甲醇水蒸气重整制氢性能
祁文旭1,张 娜3,何依隆1,张 磊1,2,刘道胜1,吴 限1,潘立卫2,王树东2
1.辽宁石油化工大学化学化工与环境学部,辽宁 抚顺 113001;
2.中国科学院大连化学物理研究所,辽宁 大连116023;
3.抚顺职业技术学院,辽宁 抚顺 113122
以液体燃料甲醇分布式现场重整制氢系统开发为研究目的,根据非对称耦合的思想,将CuO/ZnO/CeO2-ZrO2甲醇水蒸气重整催化剂和Pt/Al2O3催化燃烧催化剂应用于套筒式小型制氢反应器中,实现了甲醇水蒸气重整反应和燃烧反应的耦合。实验考察了CuO/ZnO/CeO2-ZrO2催化剂在套筒式小型制氢反应器中的性能。结果表明:在套筒式小型制氢反应器内,CuO/ZnO/CeO2-ZrO2催化剂的甲醇水蒸气重整活性比商业CuO/ZnO/Al2O3催化剂高出30%左右;并且多次开停车和改变反应条件,均未对催化剂和反应器产生明显影响,150 h内催化剂和反应器稳定性良好。当反应温度为230~260 ℃,甲醇气体空速为300~1200 h-1,水醇物质的量比(S/M)为1.2时,最大氢产率达162.8 L/h,可为百瓦级质子交换膜燃料电池提供氢源。
甲醇水蒸气重整 制氢催化剂 氢-燃料电池
随着电子科技的进步,无线电通讯设备和便携式电子产品不断涌现并迅速发展,对电池的需求量逐年上升,同时对电池的性能也提出了更高的要求[1]。但目前普遍采用的镍镉、镍氢和锂电池等由于其制造技术基本成熟、性能发展空间较小,且存在环境污染等问题,已经越来越难以满足电子产品发展的要求。因此,电子产品市场急需一种容量高、环境友好的新型电池来取代目前广泛使用的电池。近些年,许多研究者发现[2-5],将小型的制氢系统与微型燃料电池联合起来设计出的微型氢-燃料电池就是一种符合上述要求的新型电池,具有较好的工业前景。但氢-燃料电池是一个复杂的能源系统,降低成本、延长使用寿命和提高运行可靠性是其面临的主要问题。目前各国在相继进行示范的同时将重点转向基础研究,希望通过研究氢能与燃料电池技术中的基础性问题,寻求实现氢能与燃料电池产业化的办法。其中,氢源技术已成为燃料电池走向市场的瓶颈之一,用醇类、烃类、汽油等化石原料进行小规模便携式制氢是氢-燃料电池成功走向应用所面临的一个核心问题。
液体燃料甲醇由于具有制氢转化条件(温度、压力、容积、质量)相对温和、不含硫、低毒、制氢过程相对容易实现等特点成为这些富氢燃料中的首选。甲醇重整包括甲醇水蒸气重整[6-10]、甲醇部分氧化重整[11,12]和甲醇自热重整[13-18],其中甲醇水蒸气重整反应(CH3OH+H2O→CO2+3H2,ΔH298为49.5 kJ/mol)条件温和,尾气中含氢量高、CO含量低,有利于实现系统集成,因此甲醇水蒸气重整制氢催化剂和反应器的开发成为了近些年的研究热点[19]。目前,应用于甲醇水蒸气重整制氢的反应器主要有管式反应器(套管式和列管式)[20]、板式反应器[21]和微通道反应器[22]三种类型,其中管式反应器因其结构简单,添加或更换催化剂容易,并且催化剂不容易磨损而广泛受到关注。穆昕等[23]对甲醇重整套筒反应器进行了研究,结果发现套筒反应器具有启动时间短、能量效率高、单位体积产氢率高等优点,该种反应器足以为小功率燃料电池提供电源。
鉴于以上对套筒反应器的阐述,根据非对称耦合的思想,将自主研发的CuO/ZnO/CeO2-ZrO2甲醇水蒸气重整催化剂和Pt/Al2O3催化燃烧催化剂应用于自主开发的套筒式小型制氢反应器中[24],着重对CuO/ZnO/CeO2-ZrO2甲醇水蒸气重整催化剂在实际反应体系下的性能进行研究。
1 实验部分
催化剂的制备和组成如参考文献[9,10]。对比催化剂选用兰州中科凯迪公司生产的商业CuO/ZnO/Al2O3催化剂。
催化剂的评价在套筒式小型制氢反应器内进行,反应器采用不锈钢材质,外观为套筒式,内部由两个不锈钢圆筒组成,外观结构尺寸为∅53 mm×86 mm。反应器包括燃烧腔和重整腔:内腔为燃烧腔,填装自制的Pt/Al2O3颗粒催化剂约17.5 mL,进行催化燃烧反应;外腔为重整腔,填装自制的CuO/ZnO/CeO2-ZrO2颗粒催化剂(或商业CuO/ZnO/Al2O3颗粒催化剂)约45 mL,进行重整反应。反应器依靠氢气或液态甲醇的催化燃烧启动水蒸气重整,燃烧物料和重整物料采用逆流流动方式。反应中预先配置好一定比例的甲醇水溶液,经气化后,由分布器进入到重整腔内,在重整腔内的催化剂上进行甲醇水蒸气重整反应。尾气经冷凝,干燥脱水后供给燃料电池使用。在重整腔的催化床层设置K型热偶,通过温度控制器测量床层温度的变化情况。
制氢工艺流程图如图1所示。开始实验时,先向燃烧腔内通入适量的空气和氢气(或甲醇),空气过量30%左右,进行催化燃烧反应。当重整腔达到一定温度时,通过微量泵(美国LabAlliance)通入预先配好的甲醇水溶液,开始甲醇水蒸气重整反应,并且通过调整微量泵进料量改变甲醇气体空速。通过调节燃烧腔内空气和氢气(或甲醇)的比例及进料量把重整腔检测到的最高点温度控制在一定范围(230~260 ℃),并以重整腔最高点温度作为重整温度,系统稳定运行。重整尾气通过冷凝器和干燥管将未参与反应的甲醇和水分离出来;重整干气用气相色谱仪(Aglient-7890D)在线分析。
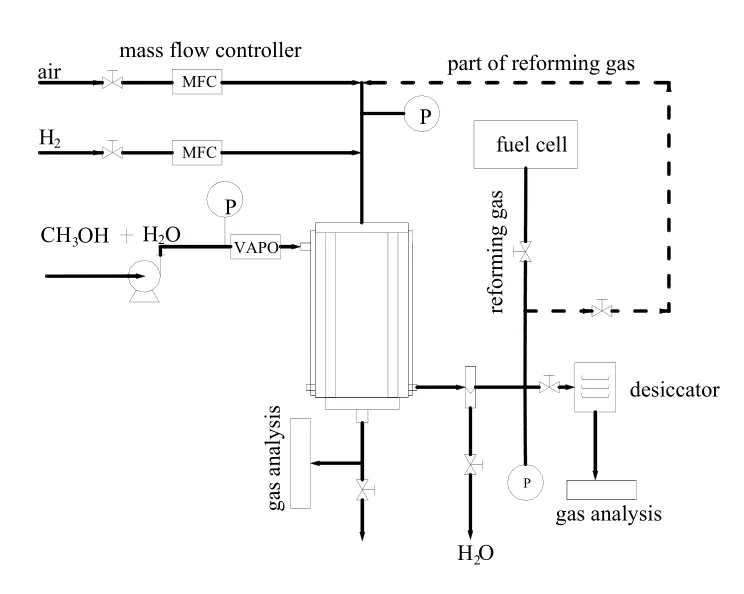
图1 制氢工艺流程Fig.1 The process of hydrogen production
2 结果与讨论
2.1 启动与停车
自制的Pt/Al2O3催化剂具有良好的低温催化活性,在室温甚至更低温度通入氢气便可点火成功,着火后即可快速加热至所需的操作温度,整个反应器系统启动容易、迅速。在室温条件下,通入过量的空气与H2启动催化燃烧反应。图2为套筒反应器的启动情况。由图可见,当H2流量为300,400,500 mL/min时,在60 min内重整腔内的平均升温速率分别为2.5,3.4,4.2 ℃/min。当氢流量为500 mL/min以上时,启动可在1 h内完成。若进一步加大H2流量,启动时间可进一步缩短。
停车时,先停止燃烧腔燃料,保留少量空气吹扫,以防止燃烧产生的水凝结在催化剂表面,影响下次点火。而后按照比例逐步减小重整腔的甲醇水溶液,不能瞬间切断甲醇水溶液,否则重整腔中残留的甲醇比例瞬间增大,引起完全燃烧反应,局部温度过高将会导致催化剂烧结失活。当温度降至200 ℃左右时,可将甲醇水溶液全部停止,用少量N2吹扫。一般来说,停车过程只需30 min。

图2 套筒反应器启动情况Fig.2 Temperature profiles during the start-up process
2.2 套筒式重整制氢反应器中的温度分布
在套筒反应器内,为了避免床层中出现燃烧“热点”和重整“冷点”,有必要对反应过程中的温度分布进行考察。结合集成反应器的结构特点,在重整腔轴向和径向分别设置了四根热偶以检测重整腔催化剂床层不同位置的温度,热偶的布置如图3所示。由于套筒反应器耦合了强吸热和强放热反应,温度分布不均。因此,采用非等间距的热偶布置方式,尽可能保证测量值全面反映反应器内温度变化情况。
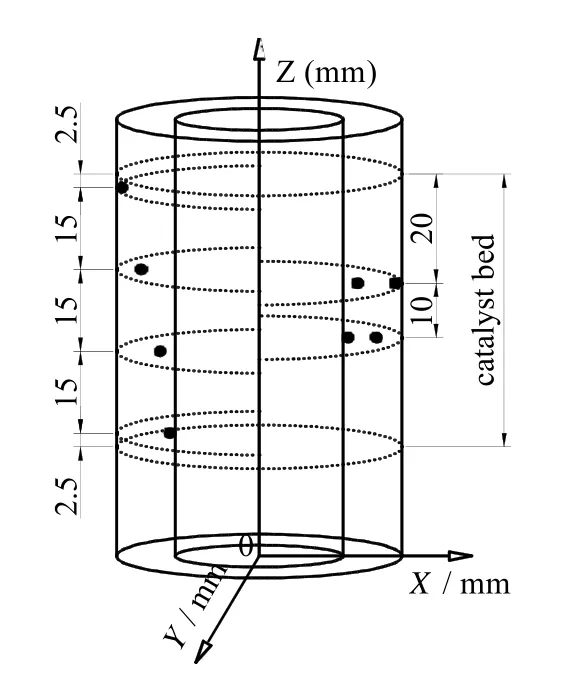
图3 重整腔中热偶分布Fig.3 The thermocouple distribution in reforming chamber
图4为不同甲醇气体空速下重整腔催化床层最高温度为260 ℃时所测到的床层轴向温度分布情况。燃烧腔内催化燃烧反应主要发生在燃烧腔的入口,释放出大量的热,导致燃烧催化床层的“热点”在燃烧腔入口处。重整腔内随甲醇气体空速的增大,轴向温差逐渐加大,导致重整床层的“冷点”出现在重整腔入口处。重整腔轴向温度随着燃烧物料流动方向由高到低变化,最大温差可达93 ℃
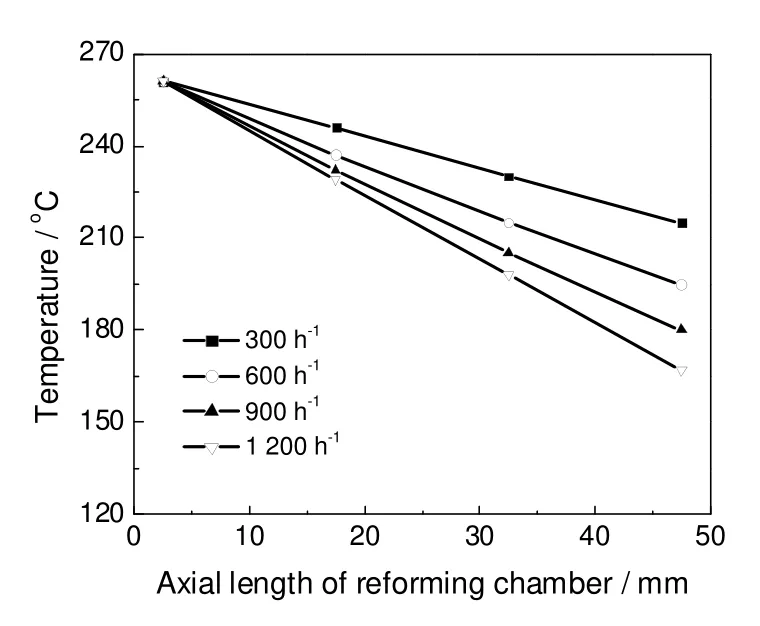
图4 重整腔内床层轴向温度分布Fig.4 The axial temperature distribution in reforming chamber
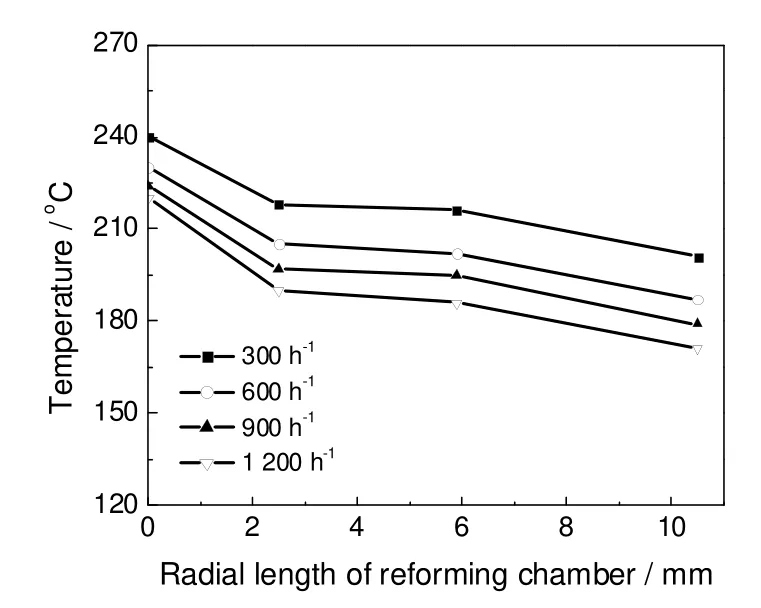
图5 重整腔内床层径向温度分布Fig.5 The radial temperature distribution in reforming chamber
图5为不同甲醇气体空速下重整腔催化床层最高温度为260 ℃时所测到的床层径向温度分布情况。由图可知,重整腔径向温度由内到外逐渐降低。径向最大温差为49 ℃,这是因为重整反应的热源在反应器中心,随着远离热源中心,径向温度降低。
2.3 催化剂活性比较
图6为对自制的CuO/ZnO/CeO2-ZrO2催化剂与商业CuO/ZnO/Al2O3催化剂性能的比较,由图可以看出,在套筒反应器内,商业CuO/ZnO/Al2O3催化剂的活性较比CuO/ZnO/CeO2-ZrO2催化剂低30%左右,说明自制的CuO/ZnO/CeO2-ZrO2催化剂具有良好的催化活性。
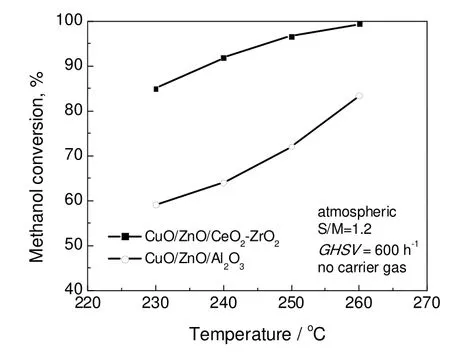
图6 套筒反应器内催化剂活性的比较Fig.6 Comparison of the activity of CuZnCeZr and CuZnAl catalysts in reforming chamber
2.4 甲醇水蒸气重整制氢反应的性能
在石英管固定床反应器内,甲醇气体空速越低,甲醇的停留时间越长,转化率越高[10],但由于实际情况需要,较低的甲醇气体空速,难以提供足够的氢产量,因此还需要结合实际情况对甲醇气体空速进行考察,为不同需求的燃料电池提供氢源。另外,由于套筒反应器内,温度场分布不均,很难控制整个反应器内的温度都维持在最佳状态,因此对重整腔内反应温度对甲醇水蒸气重整反应的性能影响需做进一步考察。
图7为重整温度和甲醇气体空速对甲醇转化率的影响。从图中可以看出,重整温度对甲醇转化率有明显的作用,固定空速时,随着反应温度的升高,甲醇转化率增加,尤其在高空速下,提升温度对提高甲醇转化率有较大的促进作用。由于甲醇气体空速的增大导致甲醇与催化剂的接触时间减少,进而甲醇转化率降低,当反应温度为230 ℃,甲醇气体空速为1 200 h-1时,甲醇转化率最低,仅为77.5%。当反应温度为260 ℃,甲醇气体空速为300 h-1时,甲醇转化率最高,基本全部转化。
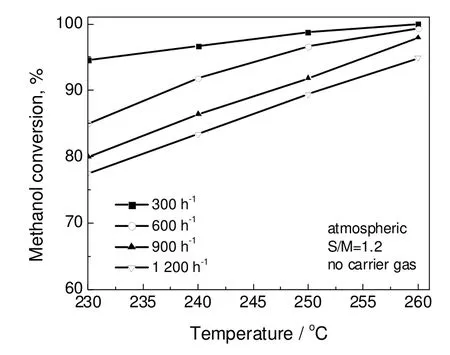
图7 不同温度和空速下的甲醇转化率Fig.7 Methanol conversion under different reforming temperatures andGHSVs
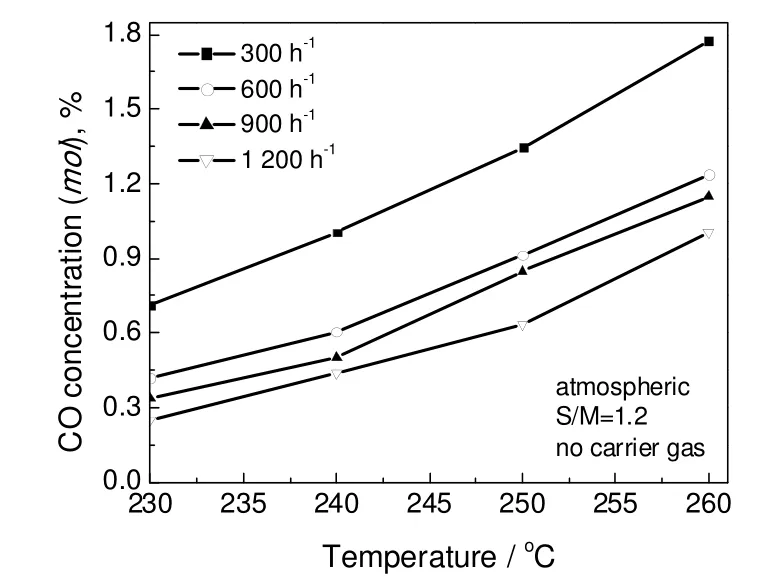
图8 不同温度和空速下重整尾气中CO含量Fig.8 CO concentration in products under different reforming temperatures andGHSVs
图8为重整温度和甲醇气体空速对重整尾气中CO含量的影响。从图中可以看出,随反应温度的增加,重整尾气中CO含量急剧增加;随甲醇气体空速的降低,重整尾气中CO含量增加,尤其在空速由600 h-1降低到300 h-1时,重整尾气中CO含量增加明显。在所选实验条件下,重整尾气中最低CO含量为0.24%,最高为1.7%。目前,对于重整尾气中CO的形成主要存在两种机理[25,26]:一种为逆水气变换反应而来,另一种为甲醇直接分解而来。第一种机理认为,重整尾气中CO含量随空速的增加而减小。相反的,后一种机理认为,重整尾气中CO含量不受空速的影响。由图8可以看出,重整尾气的CO含量随空速的增加而减少,因此意味着在230~260 ℃时,重整尾气中的CO应主要由逆水气变换反应而生成。
图9为重整温度和甲醇气体空速对燃烧氢气量的影响。从图中可以看出,燃烧氢气量随重整温度的升高而线性增加,这是因为提高重整温度,需燃烧腔提供更多的热量来供给。甲醇气体空速的增加,同样也需要燃烧腔提供更多的热量,因此燃烧的氢气量也随着需要增加。
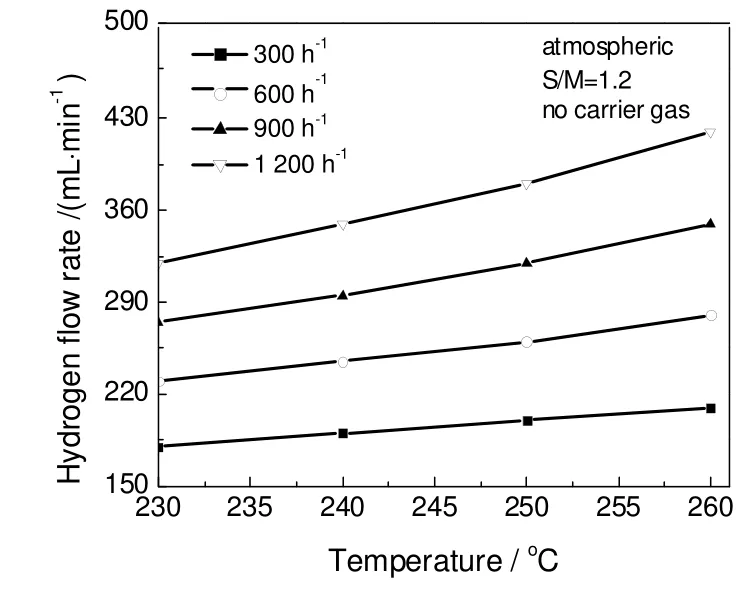
图9 重整温度和甲醇气体空速对燃烧H2流量的影响Fig.9 Effect of reforming temperature and methanolGHSVon hydrogen flow rate for combustion
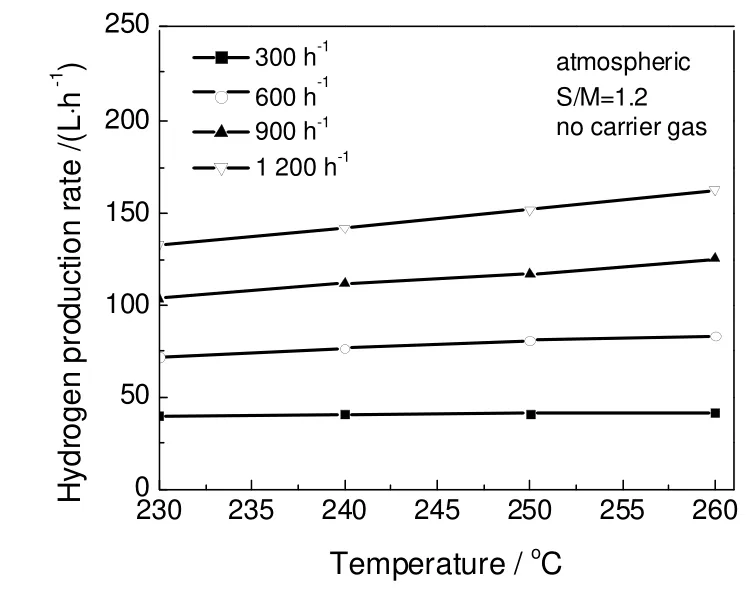
图10 重整温度和甲醇气体空速对氢产率的影响Fig.10 Effect of reforming temperature and methanolGHSVon hydrogen production rate
图10为重整温度和甲醇气体空速对氢产率的影响。从图中可以看出,在低空速下,氢产率和理论发电量随温度的变化不明显,在高空速下,氢产率和理论发电量随重整温度的升高略有增加。当反应温度为230~260 ℃,甲醇气体空速为300~1200 h-1,水醇比1.2时,最大氢产率为162.8 L/h。
2.5 催化剂稳定性实验
催化剂的使用寿命是决定其成本的重要因素,其既取决于催化剂的物理结构,又与催化剂的机械强度密切相关,还受到反复开、停车冲击的影响。考虑微型制氢反应器的应用环境,一般在负荷和操作条件不断变化的情况下运行。因此,有必要考察催化剂在非稳态下的稳定性。图11(a)和11(b)反映了不同条件间歇操作下的催化剂稳定性,具体条件:常压,反应温度为230~260 ℃,甲醇气体空速为300~1 200 h-1,水醇比1.2。在150多小时的间断运行中,由于在不同操作条件下催化剂活性不同,表现出甲醇转化率在75%~100%波动。条件的改变对重整气组成的影响不大,其中H2含量基本维持在74%以上,CO含量在2%以下。测试中对于多次的开车、停车、条件改变,CuO/ZnO/CeO2-ZrO2催化剂都表现出了良好的性能,150 h内性能稳定。
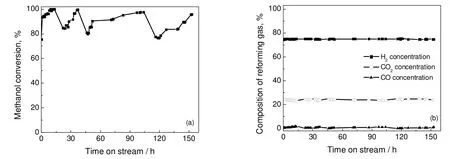
图11 稳定性实验Fig.11 Stability of the reactor for different operation conditions
3 结 论
根据非对称耦合的思想,将自主研发的CuO/ZnO/CeO2-ZrO2催化重整催化剂和Pt/Al2O3催化燃烧催化剂应用于套筒式小型制氢反应器中,实现了催化重整反应和催化燃烧反应的热量耦合。通过对CuO/ZnO/CeO2-ZrO2催化剂和套筒反应器的性能研究表明,反应器在室温下即可启动,启动时间小于60 min。反应器重整腔内轴向温差比径向温差大,最大温差可达93 ℃。CuO/ZnO/CeO2-ZrO2甲醇水蒸气重整催化剂在实际反应体系下催化性能良好,最高转化率可达100%,最大氢产率可达162.8 L/h,可为百瓦级燃料电池提供氢源。在150 h的稳定性实验中,催化剂和反应器都表现出良好的性能,无明显的失活现象,多次开停车,并未对催化剂和反应器产生明显影响。
[1] Koeneman P B, Busch-Vishniac I J, Wood K L. Feasibility of micro power supplies for MEMS [J]. Journal of Microelecrtomechchanical Systems, 1998, 6(4):355- 362.
[2] Pan L W, Ni C J, Zhang X B, et al. Study on a compact methanol reformer for a miniature fuel cell [J]. International Journal of Hydrogen Energy, 2011, 36(1):319-325.
[3] 苏石龙, 张 磊, 张 艳, 等. 千瓦级PEMFC甲醇水蒸气重整制氢过程热力学模拟 [J]. 石油化工高等学校校报, 2015, 28(2):19-25. Su Shilong, Zhang Lei, Zhang Yan, et al. Thermodynamic simulation for hydrogen production in the methanol steam reforming system of kilowatt PEMFC [J]. Journal of Petrochemical Universities, 2015, 28(2):19-25.
[4] 谢东来, 汪 祺, 费广平. 一种新型制氢反应器气体流动特性的实验研究 [J]. 化学反应工程与工艺, 2011, 27(1):6-9. Xie Donglai, Wang Qi, Fei Guangping. Gas mixing in a novel fluidized bed reactor cold model with intensive membrane panals [J]. Chemical Reaction Engineering and Technology, 2011, 27(1):6-9.
[5] 陈恒志, 郭正奎. 天然气制氢反应器的研究进展 [J]. 化工进展, 2012, 31(1):10-18. Chen Hengzhi, Guo Zhengkui. Research development in reactors for hydrogen production from methane [J]. Chemical Industry and Engineering Progress, 2012, 31(1): 10-18.
[6] Fukunaga T, Ryumon N, Ichikuni N, et al. Characterization of CuMn- spinel catalyst for methanol steam reforming [J]. Catalysis Communications, 2009, 10(14):1800-1803.
[7] Huang G, Liaw B J, Jhang C J, et al. Steam reforming of methanol over CuO/ZnO/CeO2/ZrO2/Al2O3catalysts [J]. Applied Catalysis A:General, 2009, 358(1):7-12.
[8] 张 磊, 潘立卫, 倪长军, 等. 沉淀温度对CuO/ZnO/CeO2/ZrO2甲醇水蒸气重整制氢催化剂性能的影响 [J]. 催化学报, 2012, 33(12):1958-1964. Zhang Lei, Pan Leiwei, Ni Changjun, et al. Effect of precipitation temperature on the performance of CuO/ZnO/CeO2/ZrO2catalyst for methanol steam reforming [J]. Chinese Journal of Catalysis, 2012, 33(12):1958-1964.
[9] 张 磊, 潘立卫, 倪长军, 等. 甲醇水蒸气重整制氢反应条件的优化 [J]. 燃料化学学报, 2013, 41(1):116-122. Zhang Lei, Pan Liwei, Ni Changjun, et al. Optimization of methanol steam reforming for hydrogen [J]. Journal of Fuel Chemistry and Technology, 2013, 41(1):116-122.
[10] Zhang Lei, Pan Leiwei, Ni Changjun, et al. Effect of precipitation aging time on the performance of CuO/ZnO/CeO2-ZrO2for methanol steam reforming [J]. Journal of Fuel Chemistry and Technology, 2013, 41(7):883-888.
[11] Agrell J, Germani G, Jaras S G, et al. Production of hydrogen by partial oxidation of methanol over ZnO-supported palladium catalysts prepared by microemulsion technique [J]. Applied Catalysis A:General, 2003, 242(2):233-245.
[12] Cubeiro M L, Fierro J L G. Selective production of hydrogen by partial oxdiation of methanol over ZnO-supported palladium catalysts[J]. Journal Catalysis, 1998, 179(1):150-162.
[13] Wang C W, Liu N, Pan L W, et al. Measurement of concentration profiles over ZnO-Cr2O3/CeO2- ZrO2monolithic catalyst in oxidative steam reforming of methanol [J]. Fuel Processing Technology, 2007, 88(1):65-71.
[14] Liu N, Yuan Z S, Wang S D, et al. Characterization and performance of a ZnO-ZnCr2O4/CeO2-ZrO2monolithic catalyst for hydrogen production by methanol auto-thermal reforming process [J]. International Journal of Hydrogen Energy, 2008, 33(6):1643- 1651.
[15] Liu N, Yuan Z S, Wang C W, et al. The role of CeO2-ZrO2as support in the ZnO-ZnCr2O4catalysts for autothermal reforming of methanol [J]. Fuel Processing Technology, 2008, 89(6):574-581.
[16] Chen G W, Yuan Q, Li S L. Microchannel reactor for methanol autothermal reforming [J]. Chinese Journal of Catalysis, 2002, 23(6):491-492.
[17] Patel S, Pant K K. Selective production of hydrogen via oxidative steam reforming of methanol using Cu-Zn-Ce-Al oxide catalysts [J]. Chemical Engineering Science, 2007, 62(18):5436-5443.
[18] Patel S, Pant K K. Hydrogen production by oxidative steam reforming of methanol using ceria promoted copper-alumina catalysts [J]. Fuel Processing Technology, 2007, 88(8):825-832.
[19] Zhang L, Pan L W, Ni C J, et al. CeO2-ZrO2-promoted CuO/ZnO catalyst for methanol steam reforming [J]. International Journal of Hydrogen Energy, 2013, 38(11):4397-4406.
[20] Mu X, Pan L W, Liu N, et al. Autothermal reforming of methanol in a mini-reactor for a miniature fuel cell [J]. International Journal of Hydrogen Energy, 2007, 32(15):3327-3334.
[21] 潘立卫, 王树东. 板翅式反应器中甲醇水蒸汽重整制氢的研究 [J]. 化工学报, 2005,56(3):468-473. Pan Liwei, Wang Shudong. Methanol steam reforming in plate-fin reactor for fuel cell system [J]. Journal of Chemical Industry and Engineering, 2005, 56(3):468-473.
[22] Holladay J D, Wang Y, Jones E. Review of developments in portable hydrogen production using microreactor technology [J]. Chemical Reviews, 2004, 104(10):4767-4790.
[23] 穆 昕. 重整氢气燃料电池中微型制氢反应器的研究 [D]. 大连: 中国科学院大连化学物理研究所, 2008.
[24] 米 杰, 孙国兵, 潘立卫, 等. 小型重整制氢反应器的性能 [J]. 化工进展, 2012, 31(9):1903-1907. Mi Jie, Sun Guobing, Pan Leiwei, et al. Investigation of mini-reformer for hydrogen production [J]. Chemical Industry and Engineering Progress, 2012, 31(9):1903-1907.
[25] Breen J P, Ross J R H. Methanol reforming for fuel-cell applications: development of zirconia- containing Cu-Zn-Al catalysts [J]. Catalysis Today, 1999, 51(3-4):521-533.
[26] Purnama H, Ressler T, Jentoft R E, et al. CO formation/selectivity for steam reforming of methanol with a commercial CuO/ZnO/Al2O3[J]. Applied Catalysis A:General, 2004, 259(1):83-94.
Performance of CuO/ZnO/CeO2-ZrO2Catalyst for Methanol Steam Reforming
Qi Wenxu1, Zhang Na3, He Yilong1, Zhang Lei1,2, Liu Daosheng1, Wu Xian1, Pan Liwei2, Wang Shudong2
1. College of Chemistry, Chemical Engineering and Environmental Engineering, Liaoning Shihua University, Fushun 113001, China;
2. Dalian Institute of Chemical Physics, Chinese Academy of Sciences, Dalian 116023, China;
3. Department of Chemical Engineering, Fushun Vocational Technology Institute, Fushun 113122, China
The aim of this work was to develop the system of distributed hydrogen production from methanol steam reforming (MSR). According to the idea of the asymmetric coupling, the CuO/ZnO/CeO2-ZrO2catalyst for methanol steam reforming and the Pt/Al2O3catalyst for catalytic combustion were used in a sleeve of mini reactor for hydrogen production and the coupling of methanol steam reforming reaction and combustion reaction was realized. The performances of CuO/ZnO/CeO2-ZrO2catalyst were investigated in the sleeve of mini reactor. The results showed that the activity of CuO/ZnO/CeO2-ZrO2catalyst was about 30% higher than that of CuO/ZnO/Al2O3catalyst in this reactor. No significant impact on the performances of catalyst and reactor was observed after the reaction condition was changed and the program of the reactor was switched on and off for many times. The CuO/ZnO/CeO2-ZrO2catalyst had excellent reforming performances with no deactivation during 150 h stability test. When the reaction temperature was 230-260 ℃, the methanol gas hourly space velocity was 300-1 200 h-1,and the molar ratio of steam to methanol was 1.2, the highest hydrogen yield can be up to 162.8 L/h, and the hydrogen production process was supplied for proton exchange membrane fuel cell on hectowatt scale.
methanol steam reforming; hydrogen-production catalyst; hydrogen-fuel cell
O643.32
A
1001—7631 ( 2015 ) 05—0393—07
2015-03-12;
: 2015-05-21。
祁文旭(1994—),男,本科生;张 磊(1983—),男,讲师,通讯联系人。E-mail:lnpuzhanglei@163.com。
国家自然科学基金(21376237);辽宁省教育厅科学研究一般项目(L2014157)。
