右美托咪定在颅脑损伤患者术后24 h内持续镇静的有效性及安全性
2015-01-05蒋世双苟小红冉昆足
唐 泽,陶 武,王 念,李 丹,蒋世双,苟小红,冉昆足
(重庆医科大学附属永川医院重症医学科,重庆永川 402160)
右美托咪定在颅脑损伤患者术后24 h内持续镇静的有效性及安全性
唐 泽,陶 武△,王 念,李 丹,蒋世双,苟小红,冉昆足
(重庆医科大学附属永川医院重症医学科,重庆永川 402160)
目的 探讨右美托咪定(Dex)对颅脑损伤(TBI)患者术后24 h内持续镇静的有效性及安全性。方法选取2013年4月至2014年4月在该院重症医学科住院治疗的TBI术后患者60例,采用随机数字表的方法将患者分为对照组和观察组,每组各30例。对照组仅接受常规治疗,观察组在此基础上持续泵入Dex,观察比较两组患者术后4、12、24 h 3个时间点的心率(HR)、平均动脉压(MAP)、呼吸频率(R)及血氧饱和度(SpO2)、氧分压(PO2)及血二氧化碳分压(PCO2)水平的变化。结果观察组患者平均HR、R及MAP水平分别为(84.9±15.2)、(20.5±2.0)次/分及(98.0±8.5)mm Hg,显著低于对照组的(89.3±15.0)、(23.1±2.2)次/分及(97.0±1.2)mm Hg,差异均有统计学意义(P<0.05);两组患者的平均SpO2比较,差异无统计学意义(P>0.05)。观察组患者在应用Dex后,R、SpO2、动脉PO2及PCO2随着时间的变化,差异无统计学意义(P>0.05)。结论Dex能改善TBI患者术后的应激反应,无呼吸抑制作用,且不影响对意识的评估。
右美托咪定;颅脑损伤;镇静;有效性;安全性
颅脑损伤(traumatic brain injury,TBI)是临床上一种常见的意外损伤,据流行病学统计,在全身外伤所致各种机体损伤中,TBI的发生率及死残率分居前2位,且有逐年上升的趋势[1]。而这类患者又常会发生躁动、焦虑甚至谵妄等创伤后应激障碍,特别是在ICU期间表现尤为明显,从而使人机对抗、意外拔管等并发症的发生率明显增加,严重影响其预后[2]。因此,对TBI患者进行适度的镇痛镇静治疗具有重要的临床意义。然而,由于担心镇痛镇静药物会对患者意识评估及神经功能远期恢复情况造成不利影响,临床上尚存不少争议[3]。而右美托咪定(dexmedetomidine,Dex)作为一种高效的选择性α2肾上腺素受体激动剂,不仅具有良好的镇静效应,而且不影响对患者意识的判断,被认为在TBI中具有广泛的应用前景。但是,其综合临床收益尚不明确,仍需进一步研究[4]。本研究对其在TBI术后24 h内持续镇静的有效性及安全性进行初步探索,现报道如下。
1 资料与方法
1.1一般资料 选取2013年4月至2014年4月本院重症医学科住院治疗的TBI术后患者60例,纳入标准:(1)术前格拉斯哥昏迷评分(glasgow coma scale,GCS)评分6~15分,双瞳孔对光反射存在;(2)收缩压大于100 mm Hg,无心房心室传导阻滞患者;(3)无严重肝肾功能异常;(4)无精神障碍性疾病;(5)对试验药物无过敏;(6)除外继发性颅内出血、尿潴留及呼吸道不畅等其他因素导致躁动的患者;(7)除外有慢性阻塞性肺疾病等严重基础肺部疾病的患者,以及氧合指数小于300的患者;(8)患者均有使用镇痛镇静药物的指征,如焦虑、躁动或诉疼痛不适,术后未清醒有血压升高和(或)心率(HR)增快者。根据患者就诊顺序编号,用随机数字表的方法将60例患者分为对照组和观察组。60例均经本院医学伦理委员会批准,并征得患者及其家属书面同意。观察组30例:其中男20例,女10例;平均年龄(39.3±10.1)岁,平均体质量(56.5±5.3)kg;入科时急性生理与慢性健康(APACHEⅡ)评分(18.3±3.0)分,GCS评分为(6.5±3.1)分。致伤原因构成:车祸伤12例,高处坠落伤8例,打击伤4例,摔伤6例;颅脑损伤构成:外伤性脑内血肿13例,外伤性蛛网膜下腔出血7例,急性硬膜下血肿伴脑挫裂伤5例,急性硬膜下血肿4例,脑挫裂伤1例。观察组30例:其中男18例,女12例,平均年龄(38.8±12.0)岁,平均体质量(55.7±5.5)kg,入科时APACHEⅡ评分(18.5±2.8)分,GCS评分为(6.3±3.0)分,致伤原因构成:车祸伤10例,高处坠落伤9例,打击伤6例,摔伤5例;颅脑损伤构成:外伤性脑内血肿10例,外伤性蛛网膜下腔出血8例,急性硬膜下血肿伴脑挫裂伤6例,急性硬膜下血肿4例,脑挫裂伤2例。所有患者入院时均经头颅CT或MRI证实。两组患者在性别、年龄、体质量、APACHEⅡ、致伤原因及疾病构成等比较,差异无统计学意义(P<0.05),具有可比性。
1.2方法
1.2.1给药方案 60例患者均利用芬太尼持续泵入镇痛,并根据累积疼痛评分结果调整其剂量。观察组经外周静脉微量泵入盐酸Dex注射液(江苏恒瑞医药股份有限公司,规格:2 mL:200 μg)200 μg加至0.9%的氯化钠溶液50 mL,配成4 μg/mL,缓慢给予负荷剂量1 μg/kg(输注时间大于10 min)之后微量泵以0.2~0.7 μg·kg-1·h-1速度输注维持24 h。并根据镇静和躁动评分(SAS)细则调整泵入速度,将SAS评分维持在2~4分,尽量使患者处于随时能被唤醒的状态。而对照组患者仅进行常规的术后治疗,包括止血、预防应激性溃疡、降低颅内压、营养脑神经及维持水电解质平衡。
1.2.2观察指标 观察并比较两组患者术后4、12、24 h 3个时间点的HR、平均动脉压(MAP)、呼吸频率(R)及血氧饱和度(SpO2)、氧分压(PO2)及血二氧化碳分压(PCO2)。

2 结 果
2.1两组患者平均HR、R、SpO2及MAP水平比较 观察组患者平均HR、R、及MAP水平显著低于对照组,差异有统计学意义(P<0.05);而两组患者的平均SpO2比较,差异无统计学意义(P>0.05),见表1。
2.2观察组患者动脉血气分析指标在各时间点的动态变化情况 观察组患者在应用Dex后,R、SpO2、PO2、PCO2随着时间的变化,差异无统计学意义(P>0.05),见表2。
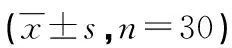
表1 两组患者HR、R等水平比较
a:P<0.05,与观察组比较。
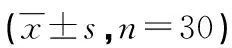
表2 观察组患者各指标随时间变化情况
2.3两组患者不良反应发生情况比较 观察组患者在用药过程中,有6例患者在给予负荷剂量的Dex后出现血压下降,MAP<65 mm Hg,当经积极补液及抬高双下肢后约5 min恢复正常;有3例患者出现HR下降低于60次/分的情况,但经短暂停药处理后恢复正常。对照组无不良反应发生。
3 讨 论
ICU作为重症患者救治的场所,各种噪音及有创操作、昼夜通明的灯光等刺激因素常会导致患者出现疼痛、躁动甚至谵妄,严重影响其预后。而镇静镇痛治疗通过使患者处于类似“休眠”状态,可降低患者机体代谢率及氧耗,可减少上述不良刺激及降低交感神经的兴奋性,从而使各种病理因素对机体造成的进一步损伤得到减轻,故镇静镇痛治疗已成为重症患者临床治疗过程中的重要组成部分[5]。而TBI患者也常伴有疼痛、躁动甚至外伤性谵妄等临床表现,若未能及时控制,不仅会增加患者的痛苦,加重脑水肿及继发性脑出血等并发症的发生,甚至会加速患者死亡[6]。因此,这类患者也有进行镇痛镇静治疗的必要[3]。然而,相对其他重症患者而言,TBI患者具有特殊性,其意识障碍水平、血压变化情况与颅内伤情变化有着极强的相关性,而传统的镇静药物,如咪达唑仑、丙泊酚等,常具有明显的呼吸抑制作用,且可能会对意识评估造成影响,又缺乏高级别的循证医学证据,临床应用受到极大的限制。因此,寻找一种既能减轻患者疼痛、躁动及谵妄等并发症的发生,又不影响对患者意识评估的药物就显得尤为重要,具有重要的临床意义。
Dex作为一种高效的选择性α2肾上腺素受体激动剂,不仅有镇静、弱镇痛作用,而且无呼吸抑制、不影响对患者意识的判定,同时具有抑制交感神经的兴奋及抗凋亡等众多神经保护功能,使其在颅脑创伤患者镇静中可能具有不俗的应用前景[4]。Yokota等[7]进行的一项回顾性研究也显示,Dex能够安全有效的应用于神经外科领域。国内郝江等[8]的一项前瞻性研究表明,Dex在中度颅脑损伤患者的疗效肯定,无明显的呼吸抑制,其减轻或消除焦虑和躁动症状有效率为85.71%,但血压及HR的下降幅度为14%~25%。然而,该研究并未设置对照组,从而使其效益下降。本研究采用随机对照的方法,观察了Dex在TBI患者术后24 h内持续镇静的有效性及安全性。结果表明,两组患者平均SpO2分别为(96.7±0.6)%、(97.0±1.2)%,差异无统计学意义(P>0.05)。而本研究对观察组患者进行动态观察时,发现其R、SpO2、PO2、PCO2水平在各时间点比较,差异无统计学意义(P>0.05)。说明Dex对TBI患者而言,无呼吸抑制作用。这与既往研究的结果相一致[8-9]。同时,本研究还观察到平均HR、R及MAP水平分显著低于对照组,且差异有统计学意义(P<0.05);而两组患者的GCS评分差异无统计学意义(P>0.05)。说明Dex不仅能稳定患者的血流动力学,而且对意识的评估无影响。本研究推测原因可能归因于Dex独特的药理作用[4,10],Dex与蓝斑核内α2肾上腺素受体突触前膜、后膜的受体相结合,抑制去甲肾上腺素的释放,同时抑制大脑皮质的觉醒反应,同时保留了患者唤醒系统的功能,且无明显蓄积作用,从而达到镇静的目的。本研究有6例患者在给予负荷剂量的Dex后出现血压下降,MAP<65 mm Hg,有3例患者出现心动过缓。而朱睿瑶等[6]在研究过程中发现,有3例患者应用负荷剂量的Dex后出现了短暂性的高血压。研究证实,Dex对患者血流动力学的影响取决于其对外周还是中枢的α2的受体占主导作用。若为前者,则因血管平滑肌上的α2肾上腺素受体被激活,使得患者外周血管收缩,而导致一过性高血压;若后者占优势,则患者中枢脑干蓝斑核副交感神经的冲动信号输出会增加,交感神经的活动减少,从而降低其血压和HR[4]。
综上所述,Dex能改善颅脑损伤患者术后的应激反应,无呼吸抑制作用,且不影响对意识的评估,适用于颅脑外伤患者的短期镇静。但是,由于其可能对患者的血流动力学造成不良影响,在如何选择合适的患者或者是否需要应用负荷剂量等方面仍需进一步研究。
[1]左永明,蒲云学.191例创伤性颅脑损伤流行病学特征分析[J].贵阳医学院学报,2011,36(2):181-183.
[2]邱海波.重症患者的镇痛和镇静:以疾病为导向[J].中华内科杂志,2013,52(4):279-280.
[3]中国医师协会神经外科医师分会神经重症专家委员会.重症脑损伤患者镇痛镇静专家共识[J].中华危重病急救医学,2013,25(7):387-393.
[4]王海燕,季君慧,王学敏.右旋托咪定在创伤性脑损伤中应用的研究进展[J].国际麻醉学与复苏杂志,2012,33(8):569-573.
[5]Barr J,Fraser GL,Puntillo K,et al.Clinical practice guidelines for the management of pain,agitation,and delirium in adult patients in the intensive care unit[J].Crit Care Med,2013,41(1):263-306.
[6]朱睿瑶,冯丽芝,张迪,等.丙泊酚与右美托咪啶用于 ICU 中颅脑外伤患者镇静效果观察[J].现代中西医结合杂志,2014,23(14):1563-1565.
[7]Yokota H,Yokoyama K,Noguchi H,et al.Post-operative dexmedetomidine-based sedation after uneventful intracranial surgery for unruptured cerebral aneurysm:comparison with propofol-based sedation[J].Neurocrit Care,2011,14(2):182-187.
[8]郝江,罗积慎,何毅,等.右美托咪啶在颅脑创伤镇静镇痛中的应用[J].中华急诊医学杂志,2011,20(12):1255-1258.
[9]马冬璞.右美托嘧啶在颅脑外伤患者镇静中的应用[J].中国实用神经疾病杂志,2013,16(21):85-86.
[10]Tawfeeq NA,Halawani MM,A-Faridi K,et al.Traumatic brain injury:neuroprotective anaesthetic techniques,an update[J].Injury,2009,40(4):S75-S85.
验交流·
10.3969/j.issn.1671-8348.2015.11.032
重庆市永川区科技计划项目(YCSTC2012BE5008);重庆市医学会重症医学专委会临床医学科研专项基金。
唐泽(1975-),主治医师,大学本科,主要从事急危重症研究。
△通讯作者,Tel:18983855955;E-mail:1642039059@qq.com。
R651.1
B
1671-8348(2015)11-1533-02
2014-09-28
2015-01-25)
