离子色谱法测定伊班膦酸钠中的亚磷酸和磷酸根离子
2014-12-24张锦梅田海峰张习志
张锦梅,田海峰,张习志
(青岛盛瀚色谱技术有限公司,山东青岛 266101)
伊班膦酸钠(Ibandronate sodium,IB)是第三代双磷酸盐类药物,由德国Boehringer Mannheim公司开发,于1996年在德国上市,临床主要用于治疗伴有或者不伴有骨转移的恶性肿瘤引起的高钙血症和治疗绝经后妇女的骨质疏松症[1–2]。李谢对伊班膦酸钠合成工艺的改进作了报道[3]。伊班膦酸钠制备的方法主要有两条合成路线[4–6],在伊班膦酸钠合成过程中,使用的PCl3和亚磷酸可能引入到成品中。双膦酸类药物作用的靶向细胞主要是破骨细胞、成骨细胞、巨噬细胞、肿瘤细胞、内皮细胞[7]。随着临床应用的增多,有必要建立一种便捷、灵敏的检测方法,对药品质量检测提供技术支持。已有人对伊班膦酸钠中的杂质阴离子进行研究[8–9],但是未有对伊班膦酸钠中磷酸和亚磷酸同时检测作过研究。目前,检测该类物质中H2PO3–,H2PO4–离子的方法主要有示差法、氧化还原滴定法[10]、电位滴定法[11]、离子色谱法[9]等。其中,离子色谱法因其快速、准确、选择性好,以及可同时测定多组分的优点被广为应用[12]。
笔者采用离子色谱–抑制电导法测定伊班膦酸钠中的H2PO3–,H2PO4–离子,通过优化选择色谱条件方式的对比,建立了最佳的色谱条件。样品用超纯水溶解后,过0.22 μm滤膜,进样后可在15 min内分析完样品。
1 实验部分
1.1 主要仪器与试剂
离子色谱仪:CIC–300型,青岛盛瀚色谱技术有限公司;
高效液相泵:UC–3281型,北京优联光电技术有限公司;
超声波清洗器:HS10260D型,北京华运安特科技有限责任公司;
工作站:HW–2000型,上海千谱软件有限公司;
Na2CO3:分析纯,上海山浦化工有限公司;
NaHCO3:优级纯,天津科密欧化学试剂有限公司;
磷酸二氢钾:工作基准试剂,上海山浦化工有限公司;
亚磷酸:分析纯,上海亭新化工有限公司;
H2PO3–,H2PO4–标准溶液:质量浓度均为1 000 mg/L,用H3PO3、KH2PO4分别配制H2PO3–、H2PO4–标准液,用时根据需要稀释成系列标准溶液,淋洗液用分析纯Na2CO3和优级纯NaHCO3配制;
实验用水为电阻率18.2 MΩ·cm的二次去离子水。
1.2 样品处理
称取一定量的伊班膦酸钠样品约0.1 g,加入超纯水振荡溶解,转移到100 mL容量瓶中,并用超纯水定容至标线,摇匀,备用。样品经过0.22 μm离子色谱专用滤膜后直接进样。
1.3 色谱条件
离子色谱柱:SH–AC–1阴离子交换柱(150 mm×4.0 mm,青岛盛瀚色谱技术有限公司)和SH–AC–1阴离子保护柱(50 mm×4.0 mm,青岛盛瀚色谱技术有限公司);淋洗液:3.6 mmol/L Na2CO3–4.5 mmol/L NaHCO3混合液,等度淋洗,流量为1.5 mL/min;柱温:45℃;进样体积:20 μL;电流:70 mA。
1.4 标准溶液的配制
称取磷酸二氢钾0.140 2 g于100 mL容量瓶中,以超纯水定容至标线,在4℃下避光保存备用。称取亚磷酸0.100 0 g于100 mL容量瓶中,以超纯水定容至标线,在4℃下避光保存备用。配制10 mg/L H2PO3–与20 mg/L H2PO4–离子混合标准溶液,逐级稀释2,4,8,10,20倍配制成系列混合标准工作溶液。
2 结果与讨论
2.1 色谱柱的选择
离子交换分离是基于流动相与固定相上的离子交换集团之间发生的离子交换过程。对高极化度和疏水性较强的离子,分离机理中还包括非离子交换的吸附过程。一般离子交换功能基为季铵基的数值用作阴离子分离。本实验采用表面氨基化聚乙烯醇的聚合物树脂(SH–AC–3)型色谱柱与表面氨基化的其它类型聚合物树脂柱(SH–AC–1)型色谱柱。用SH–AC–3型色谱柱在3.6 mmol/L Na2CO3溶液,流量0.7 mL/min,柱温40℃条件下分析,亚磷酸和磷酸的分离度为1.1,出峰时间约为25 min。采用SH–AC–1型色谱柱,以3.6 mmol/L Na2CO3–4.5 mmol/L NaHCO3混合液作为淋洗液,流量为1.5 mL/min,室温条件下分析,亚磷酸和磷酸的分离度为3.9,出峰时间约为4.8 min。综合考虑定量的准确性和效率,选用SH–AC–1型色谱柱。
2.2 淋洗液及其流量的选择
单纯使用碳酸盐/碳酸氢盐型淋洗液时,测定的噪音大,并且检测灵敏度低,笔者选用内置SHY–2自再生阴离子抑制器,在线使通过的淋洗液转变为碳酸,降低了背景电导,提高了灵敏度。选择SH–AC–1型 阴离子交换柱,3.6 mmol/L Na2CO3–4.5 mmol/L NaHCO3混合液为淋洗液可以同时检测多种阴离子,分离度达到2.0以上,且可以得到较好的保留时间重现性。对淋洗液流量分别为1.0,1.5,2.0 mL/min进行比较,结果表明,流量过低时,检测灵敏度高,但所需时间较长;流量过高时,所需时间短,但柱压升高。因此实验选用的淋洗液流量为1.5 mL/min,离子分离效果好,峰型尖锐,对称性好。
综上所述,实验选择以3.6 mmol/L Na2CO3–4.5 mmol/L NaHCO3混合液为淋洗液,流量为1.5 mL/min。
2.3 线性关系和检出限
配 制5.0 mg/L H2PO3–和10.0 mg/L H2PO4–混合标准溶液,逐级稀释2,4,8,10,20倍系列混合标准工作溶液,其中H2PO3–的质量浓度分别为2.50,1.25,0.63,0.50,0.25 mg/L; H2PO4–的质量浓度分别为5.00,2.50,1.25,1.00,0.50 mg/L。在1.3色谱条件下测定系列混合标准溶液,以离子的质量浓度x为横坐标,对应的色谱峰面积y为纵坐标作标准曲线,得方法的线性方程和检出限列于表1。

表1 离子浓度与峰面积的线性关系和检出限
2.4 精密度试验
分别取处理好的样品溶液按1.3色谱条件连续进样测定6次,测定结果见表2。由表2可知,H2PO3–,H2PO4–测定结果的相对标准偏差分别为2.5%,3.6%,说明该方法具有良好的精密度。
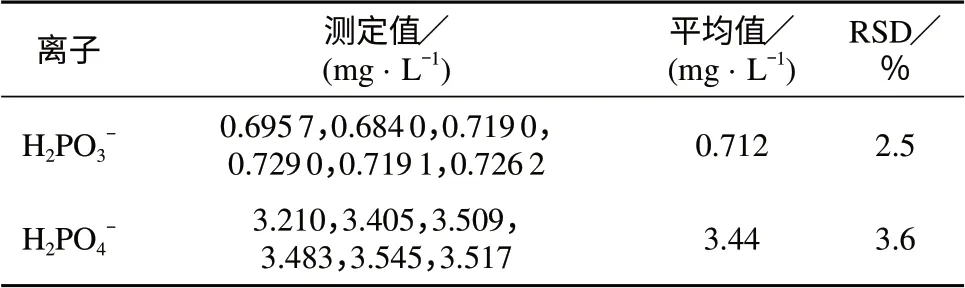
表2 样品精密度试验结果
2.5 加标回收试验
在样品中添加3种不同浓度的H2PO3–,H2PO4–阴离子的混标溶液,加标后连续测定5次取平均值,加标回收试验结果见表3。图1为伊班膦酸钠样品的加标离子色谱图(H2PO3–,H2PO4–离子加标量分别为1.20,2.6 mg/L)。
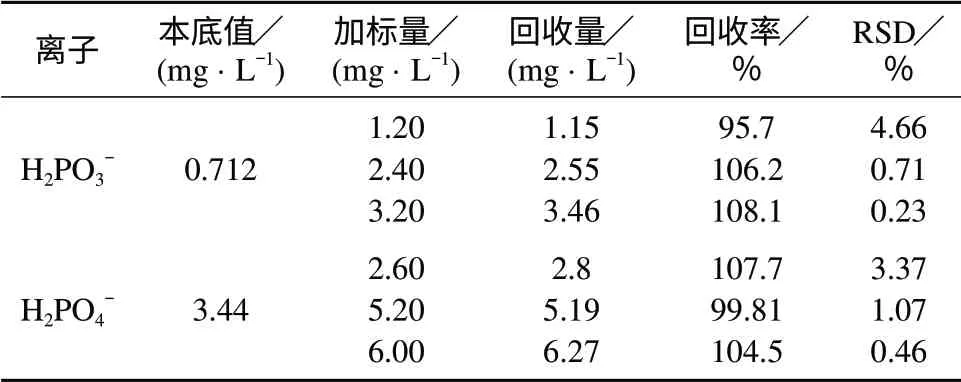
表3 回收试验结果
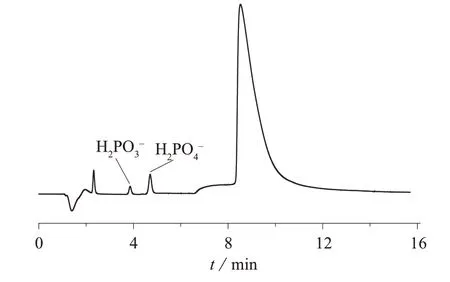
图1 伊班膦酸钠样品的加标离子色谱图
2.6 实际样品的测定
根据美国药典,伊班膦酸钠中杂质限量控制是亚磷酸、磷酸的含量均不得超过0.5%。按实验方法测得试样中亚磷酸含量为0.067%,磷酸含量为0.334%,说明供试样品为合格产品。
3 结语
采用离子色谱抑制电导法测定伊班膦酸钠中亚磷酸和磷酸残留量。该方法具有操作简单、快速,测定结果准确可靠等优点,具有很好的实用价值,这对测定双膦酸类药物中杂质离子亚磷酸和磷酸的测定有一定的借鉴作用。
[1]苏国强,朱崇泉,边军,等.骨吸收抑制剂氨基二膦酸类化合物及其钠盐的合成[J].中国药物化学杂志,2000(1): 49–50.
[2]徐春江,卢海波,谢梅,等.伊班膦酸钠的药理作用及其临床应用进展[J].中国药业,2009,18(15): 87–88.
[3]李谢,易超,徐琳,等.伊班膦酸钠合成工艺的改进[J].安徽医药,2012,16(8): 1 074–1 075.
[4]黄毅,彭国强,熊俊宇,等.一种化合物伊班膦酸钠的制备方法: 中国,201010216876.1 [P]. 2010–07–05.
[5]王卓义,李德富,黄安民,等.一种合成伊班膦酸钠的方法: 中国,201110065239.3 [P]. 2011–03–17.
[6]Mark R J. Kinetics of reversible endothermic elimination reactions: b-amino carboxylic ester and amides[J].J Org Chem,1986,51(6): 833–837.
[7]李继红.伊班膦酸钠的药理作用和临床用药分析[J].现代医药卫生,2010,26(22): 3 500–3 501.
[8]王雷,焦霞,朱岩.离子色谱法测定伊班膦酸钠及其杂质含量[J].分析化学,2008,36(3): 419.
[9]胡晓敏,宋周虎,张培敏,等.离子色谱–抑制电导法检测同时测定伊班膦酸和有关物质磷酸根离子[J].卫生职业教育,2007,25(16): 113–114.
[10]莫庆奎,卢军,袁静.亚磷酸的含量测定方法探析[J].化工技术与开发,2009,38(3): 33–34.
[11]董慧茹,张传宇,董本东,等.离电位滴定–主成分分析法同时测定磷酸与亚磷酸[J].北京化工大学学报:自然科学版,1996,36(3): 419.
[12]牟世芬,刘克纳,丁晓静.离子色谱方法及应用[M].2版.北京:化学工业出版社,2010: 158–201.
