轻度认知障碍转化阿尔兹海默病影像预测研究
2014-12-05杨文璐刘凤侠张小慢
杨文璐,刘凤侠,张小慢
(上海海事大学信息工程学院,上海 201306)
阿尔兹海默病(Alzheimer's disease,简称AD)是一种以进行性认知功能障碍和记忆损害为特征的神经系统退行性疾病[1],是目前为止最常见的一种老年痴呆疾病.截至2050年,全世界将有2 660万阿尔兹海默病患者,平均85人中将有一个患有AD[2].由于AD的临床诊断多数在中晚期,此时的治疗效果不佳,故研究的注意力开始转向 AD的早期诊断和早期干预.轻度认知障碍(mild cognitive impairment,简称MCI)是介于正常衰老和痴呆之间的一种中间状态,转化为痴呆的危险性很高.研究表明,MCI患者每年以10% ~15%的速率转化为AD,6年后转化为AD的几率高达80%[3-4].因此,MCI阶段可能是进行AD预防性治疗最重要和最合适的阶段.对MCI进行深入研究,有可能发现和筛选出AD的高危人群,提供一个最佳的治疗时期,从而预防或延缓痴呆的发生.
神经影像学技术为探讨MCI及AD患者的大脑结构和功能的改变提供了重要的诊断方法,对MCI的早期诊断、风险预测、鉴别是否转化为AD具有重要的作用.通过纵向核磁共振成像(magnetic resonance imaging,简称MRI)扫描发现,MCI患者大脑结构异常要比临床量表得分变化出现得早[5].Misra等[6]已经证明转化为AD的MCI患者与AD患者具有相似的大脑病变结构特征,随访时间内未转化的MCI患者与正常衰老人群具有相似的大脑结构特征.因此,作者利用MCI患者与AD以及正常衰老人群大脑结构特征之间的联系,对MCI向AD转化进行预测.
1 材料与方法
1.1 材 料
实验使用的研究对象均来自美国ADNI(Alzheimer's disease neuroimaging initiative)中心数据库[7].ADNI中心通过美国与加拿大的50多个机构招募了800多名年龄在55~90岁受试者进行MRI影像的跟踪采集.该文中的主要研究对象是基线AD、正常对照(healthy controls,简称HC)和MCI的结构核磁共振影像.依据临床痴呆等级量表(clinical dementia rating scale,简称CDR)将MCI样本界定为两类:一类是CDR值在基线之后的任何时刻转化为1或者2的MCI样本,记为MCI-C;另一类是CDR值在随访时间内一直保持不变的MCI样本,记为MCI-NC.为了获取AD与HC组间具有显著性差异的特征和排除噪声干扰,筛选了基线CDR值为1的AD样本以及在随访时间内CDR值一直保持为0的HC样本.最终确定的研究样本信息统计如表1所示.
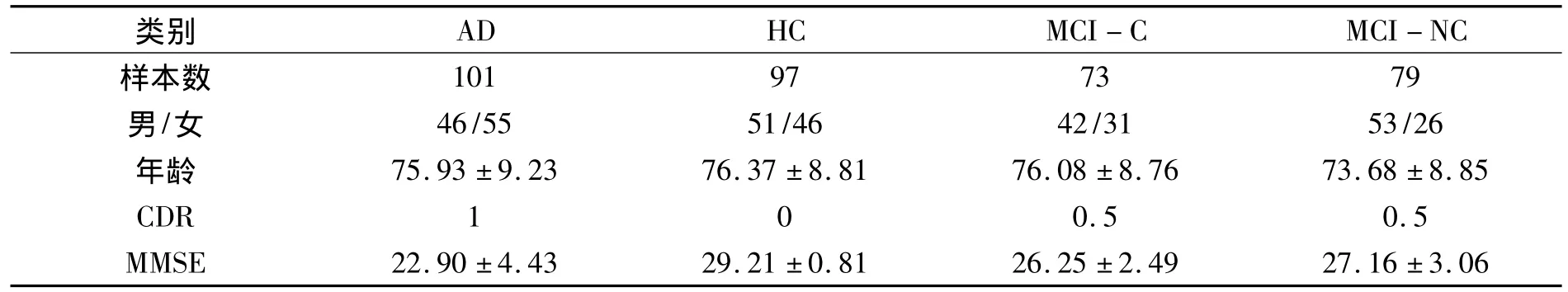
表1 样本信息统计Tab.1 Characteristics of the data set
1.2 影像预处理
由于不同受试者之间大脑形状、大小差异等原因,使得采集到的核磁共振影像本身就存在一定的差异.因此,为了后期实验需要,该研究用统计参数图(statistical parametric mapping,简称SPM)软件[8]对所有核磁共振影像预处理.首先,对所有的MRI影像进行标准化,标准化原理是将源影像的脑组织的空间位置与模板中相应的脑组织的空间位置对齐,将MRI影像归一化到蒙特利尔神经学研究所(Montreal Neurological Institute,简称MNI)的T1模板;其次,执行影像分割,从全脑影像中分离出大脑灰质,所有灰质的大小为78×95×68体素,每个体素的大小是2 mm×2 mm×2 mm.
1.3 方 法
所有影像预处理之后,首先,采取独立成分分析(independent component analysis,简称ICA)对AD与HC组的灰质影像进行组间特征提取;其次,执行感兴趣体素分析,获取AD与HC组间差异特征信息,并将MCI样本在AD与HC的特征空间上进行表达;最后,采取基于支持向量机(support vector machine,简称SVM)的分类预测.
1.3.1 ICA 模型
ICA是近年来发展起来的一种强有力的数据分析工具,广泛应用于生物医学信号处理、图像特征提取、人脸识别等领域.ICA是将给定的参数矩阵分解为相互独立的一系列独立成分.其基本的数学模型形式为

模型中X是观察随机变量,独立成分si是隐藏变量,不能被直接观察到,混合系数ai也是未知的.独立成分分析的过程就是把混合系数和独立成分同时估计出来.在ICA求解之前,先对数据进行白化处理,这样可以使得各个分量之间是不相关的,便于进行解混计算.ICA数据处理过程如图1所示,A是混合系数矩阵,W是白化矩阵,U为正交矩阵,s(t)是原始信号,x(t)是混合信号,z(t)是白化处理后的信号,y(t)是经过解混后的信号.
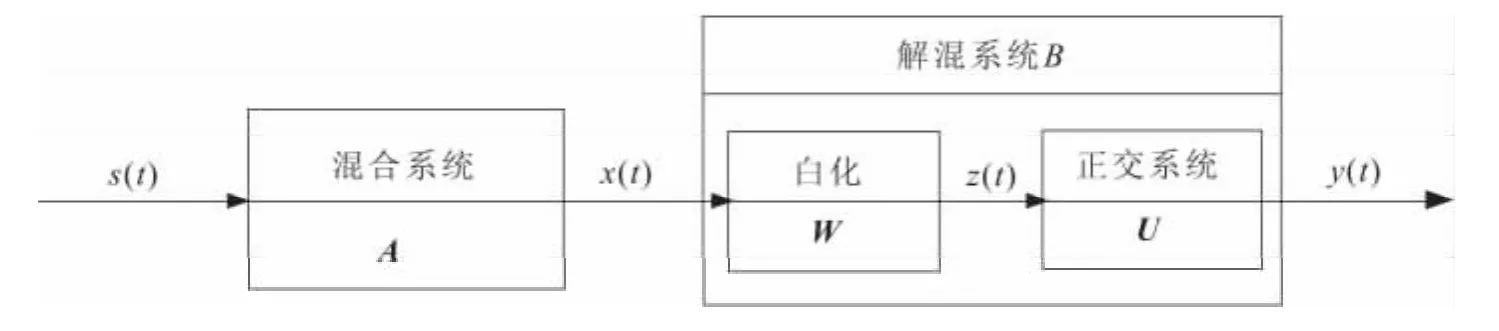
图1 ICA数据处理过程Fig.1 Data processed by ICA
针对核磁共振影像独立成分分析的模型,可进行如图2所示的图形化描述,X是N×M的观测数据矩阵,N代表了研究对象的个数,M代表了每幅MRI影像的体素数,K代表分解后独立成分的个数.X被分解为A和S,矩阵A称为混合系数矩阵,每一行元素代表每个对象所包含的所有独立成分的信息,每一列代表单个独立成分包含的所有对象的信息.矩阵S是K×M的源矩阵,Si(i=1,2,…,K)代表各个独立成分.
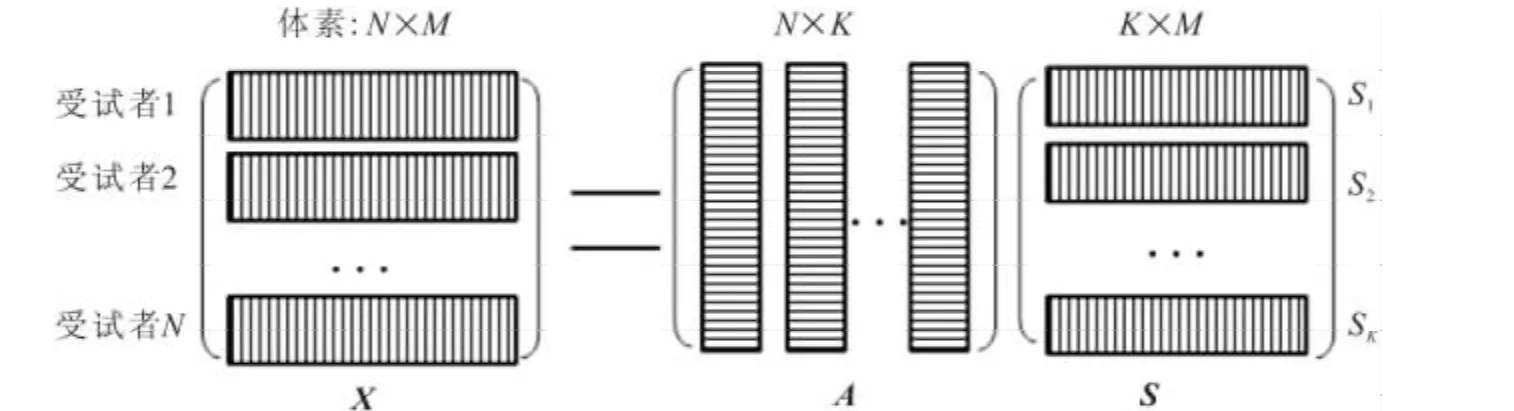
图2 磁共振影像独立成分分析模型图Fig.2 The model of ICA
目前用于核磁共振影像处理的独立成分分析算法主要有信息极大化算法和不动点算法(FastICA).作者采用的是基于负熵的不动点算法,该算法利用了牛顿迭代法原理,计算效率较高.对于任意概率分布的p(x)和具有相同协方差矩阵的高斯分布pG(x),定义负熵

基于负熵的牛顿迭代公式为
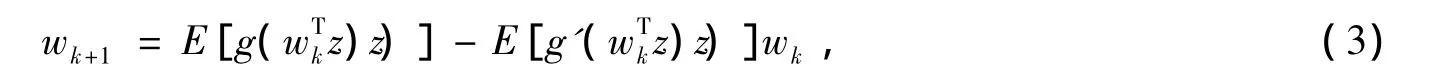
其中:E代表求均值;w是解混系数;z=wx是白化后的数据;k代表第k个独立成分;g函数为奇函数,一般可选
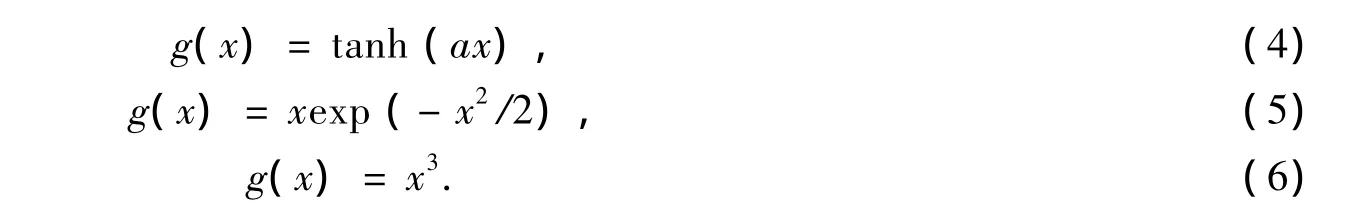
基于负熵提取多个分量的FastICA算法流程如下:
(1)观测数据X去均值,进行白化得Z;
(2)m为待提取独立成分数目,令初值p=1;
(3)任选 wp,1的初值,使 wp,1的2-范数为1,k=1;
(6)归一化:wp,k+1=wp,k+1/||wp,k+1||;
(8)若p<m,p=p+1,返回步骤(3),否则迭代结束;
1.3.2 感兴趣体素分析
对于得到的独立成分信息,有必要进行深入分析.因为每个独立成分都对应于标准大脑空间的某一空间区域,如果这些区域分别映射到每幅核磁共振影像,每幅核磁共振影像都能找到每个独立成分在其图像中对应的空间区域.对于不同的核磁共振影像,各独立成分区域内部的体素携带了各核磁共振影像的个性特征.因而,可以对各个独立成分对应区域内部的体素进行感兴趣体素提取.同时,对所有核磁共振影像每个独立成分对应区域内的体素值进行平均值与方差的计算,根据计算结果设定相应的体素值的分布区间,并对每幅核磁共振影像相应区域内满足该体素值分布空间的体素个数进行统计,所有核磁共振影像统计结果共同构成用于分类的特征信息.
1.3.3 分类预测
作者采用SVM进行两类MCI样本分类,它是一种基于结构风险最小化理论的学习算法[9],推广能力强,在解决小样本问题中表现出许多特有的优势[10].SVM的基本思想是:用核函数将输入的向量映射到高维特征空间F中,再在F中构造一个最大间隔的最优超平面,将两类样本点正确分离,并取得最大分类间隔.对于两分类问题,设(xi,yi):i=1,2,…,xi∈Rd代表训练集合的特征向量,yi∈{1,-1}是其对应的类别,对于非线性分类模型有
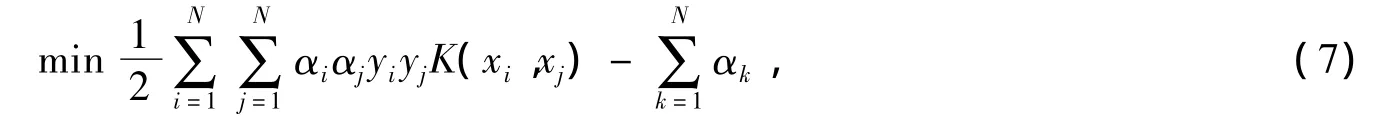
使得

判别函数为

如果y≥0,则判定x属于MCI-C,类别为1;如果y<0,则判定x属于MCI-NC,类别为-1.式(10)中K(xi,x)为核函数,选择不同的核函数可以构造出不同的SVM分类器.文中使用的是高斯径向基核函数
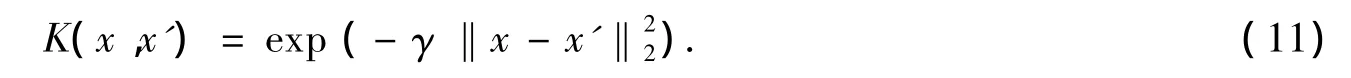
核参数γ和误差惩罚因子C是影响SVM性能的主要参数.γ的取值影响数据变换后在特征空间里的分布,C决定了SVM的收敛速度及泛化能力.所以,实验中通过调节SVM中的各种性能参数获取最佳的预测效果.
2 实验结果
2.1 ICA独立成分提取
作者采用FastICA算法提取了AD与HC组样本的70个独立成分,并通过感兴趣体素分析获取了AD、HC以及MCI的特征信息.因为矩阵S携带体素与独立成分之间的相关信息,因此,可以利用S提取得到这些独立成分的可视化结果,可视化的过程是将源矩阵的每一行重新转换到一幅三维图像.以其中一个独立成分为例,它的可视化效果如图3所示.
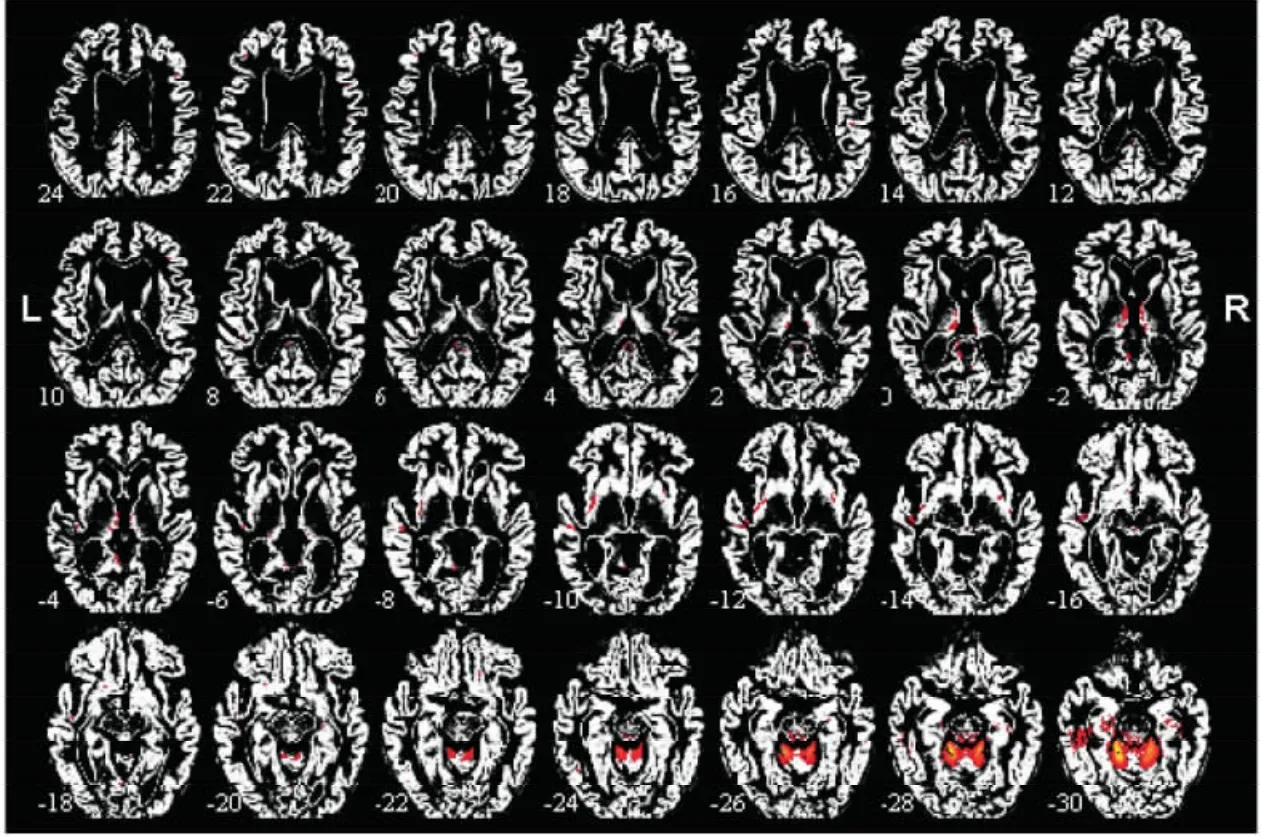
图3 独立成分的可视化Fig.3 The visualization of independent components
2.2 分类预测
将AD与HC的特征信息作为训练数据,MCI特征信息作为测试数据.由于每个独立成分的信息对分类的贡献率是未知的,某些独立成分甚至会影响预测结果.因此,为了找出最大分类准确率下的特征数目,采用主成分分析(principal components analysis,简称PCA)方法寻找最大主成分个数,PCA可以对数据进行压缩,将高维数据压缩成低维数据并且保留数据的能量.实验时,从第1个样本特征集开始,依次递增,统计出不同主成分下的预测准确率、灵敏度、特异度,如图4所示.准确率(Accuracy)、灵敏度(Sensitivity)和特异度(Specificity)的计算如式(12)~(14)
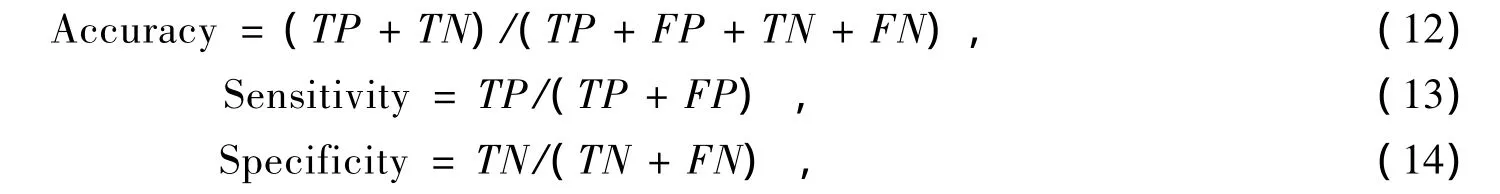
其中:TP表示正确分类得到的标签为+1的正样本个数;TN表示正确分类得到的标签为-1的负样本个数;FP表示误将标签为-1的样本统计为标签为+1的样本个数;FN表示误将标签为+1的样本统计为标签为-1的样本个数.
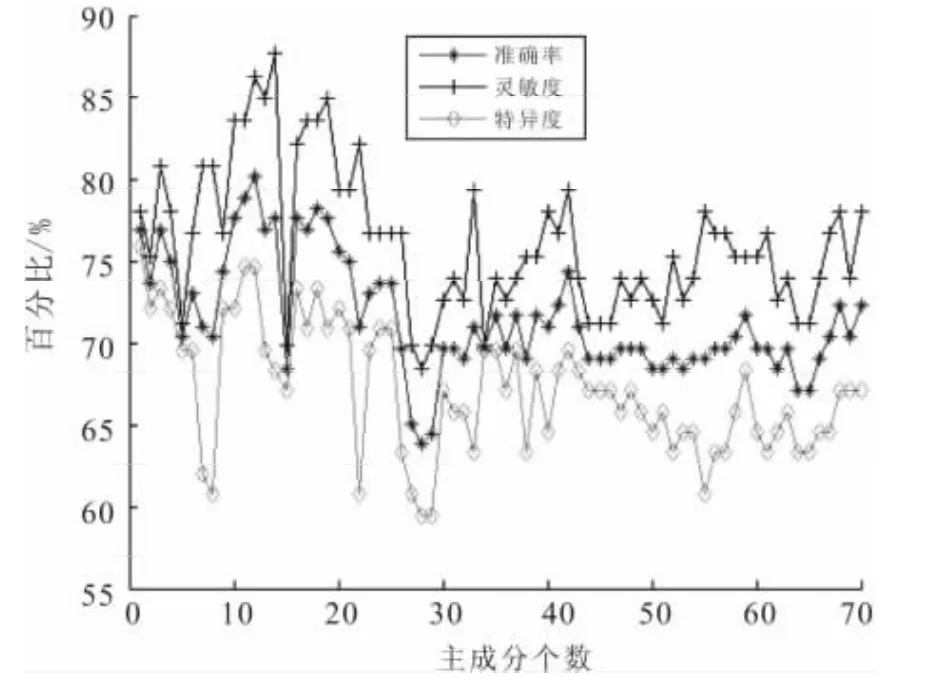
图4 MCI转化预测百分比Fig.4 The prediction results of MCI
对分类结果统计分析得到预测平均准确率、平均灵敏度分别为71.52% 和76.24%,同时,从图4可以看出,最大主成分个数为12时预测准确率、灵敏度、特异度同时达到最大值,分别为80.26%、86.30%和74.68%.该分类模型的预测灵敏度比较高,灵敏度代表有病检测能力,该研究中灵敏度代表发现MCI转化为AD的倾向.所以,利用AD与正常对照组的差异特征信息能够比较准确地对MCI患者进行转化预测.
3 讨论
MCI患者有可能向AD发生转化,也有可能一直保持为MCI状态或者恢复健康状态.文中作者利用MCI患者与AD和正常衰老人群的大脑结构特征之间的联系,采取FastICA算法、感兴趣体素提取和SVM相结合的方法对MCI进行转化预测,预测准确率、灵敏度和特异度分别达到了80.26%、86.30%和74.68%.Cui等[11]也是从美国ADNI中心数据库获取研究数据,采用FreeSurfer软件分割出MRI影像的解剖学结构并获取323个特征信息,采取SVM分类器,将AD与正常对照组的特征信息作为训练数据,将56例MCIc样本和87例MCInc样本的特征信息作为测试数据,分类准确率、灵敏度和特异度分别为62.24%、57.14%和65.52%.与之相比,该文中的研究方法所获得的预测准确率、灵敏度和特异度更高,效果更好.
在选取研究样本时,界定MCI-C和MCI-NC是根据ADNI中心随访时间内MCI受试者的CDR值是否发生变化来确定的,说明此时MCI-C已经表现出了AD的一些临床特性,而该文中的研究对象是基线时间点MCI的MRI影像,验证了MCI患者的影像异常的确早于临床特征异常表现,也表明从影像角度进行深入研究能够提前发现MCI患者是否向AD发生了转化,对AD的早期诊断和干预具有重要意义.
[1]赵亮,王东青,朱颖,等.阿尔兹海默病患者海马形态、体积变化的影像学特征研究[J].中华行为医学与脑科学杂志,2010,19(3):200-203.
[2]Brookmeyer R,Johnson E,Ziegler-Graham K,et al.Forecasting the global burden of Alzheimer's disease[J].Alzheimer's and Dementia,2007,3(3):186-191.
[3]Ewers M,Buerger K,Teipel S J,et al.Multicenter assessment of CSF-phosphorylated tau for the prediction of conversion of MCI[J].Neurology,2007,69(24):2205-2212.
[4]Golob E J,Irimajiri R,Starr A.Auditory cortical activity in amnestic mild cognitive impairment relationship to subtype and conversion to dementia[J].Brain,2007,130(3):740-752.
[5]Davatzikos C,Fan Y,Wu X Y,et al.Detection of prodromal Alzheimer's disease via pattern classification of magnetic resonance imaging[J].Neurobiology of Aging,2008,29(4):514-523.
[6]Misra C,Fan Y,Davatzikos C.Baseline and longitudinal patterns of brain atrophy in MCI patients,and their use in prediction of short-term conversion to AD:Results from ADNI[J].NeurImage,2009,44(4):1415-1422.
[7]Jack C R,Bernstein M A,Fox N C,et al.The Alzheimer's disease neuroimaging initiative(ADNI):MRI methods[J].Journal of Magnetic Resonance Imaging,2008,27(4):685-691.
[8]Yakushev I,Hammers A,Fellgiebel A,et al.SPM-based count normalization provides excellent discrimination of mild Alzheimer's disease and amnestic mild cognitive impairment from healthy aging[J].NeuroImage,2009,44(1):43-50.
[9]杨志民,刘广利.不确定性支持向量机算法及应用[M].北京:科学出版社,2012:54-68.
[10]Magnin B,Mesrob L,Kinkingnehun S,et al.Support vector machine-based classification of Alzheimer's disease from whole-brain anatomical MRI[J].Neuroradiology,2009,51(2):73-83.
[11]Cui Y,Liu B,Luo S H,et al.Identification of conversion from mild cognitive impairment to Alzheimer's disease using multivariate predictors[J].PLoS ONE,2011,6(7):e21896.
